(S)-N-metilnaltrexona, proceso para su síntesis y su uso farmacéutico.
Un compuesto de la configuración S con respecto al nitrógeno de la Fórmula I:**Fórmula**
que tiene al menos 75% pureza, en donde X es un contraión.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2006/020232.
Solicitante: PROGENICS PHARMACEUTICALS, INC..
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 777 OLD SAW MILL RIVER ROAD TARRYTOWN, NY 10591 ESTADOS UNIDOS DE AMERICA.
Inventor/es: WAGONER,HOWARD, SANGHVI,SUKETU P, BOYD,THOMAS A, VERBICKY,CHRISTOPHER, ANDRUSKI,STEPHEN.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/485 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › Derivados del morfinano, p. ej. morfina, codeína.
- A61P1/12 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 1/00 Medicamentos para el tratamiento de trastornos del tracto alimentario o del aparato digestivo. › Antidiarreicos.
- A61P25/04 A61P […] › A61P 25/00 Medicamentos para el tratamiento de trastornos del sistema nervioso. › Analgésicos que actúan sobre el sistema nervioso central, p.ej. opioides.
- C07D489/08 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 489/00 Compuestos heterocíclicos que contienen sistemas cíclicos 4 aH-8,9 c-imino-etano-fenantro [4, 5-b, c, d] furano, p. ej. derivados de 4,5-epoxi morfinano de fórmula:. › Atomo de oxígeno.
PDF original: ES-2429159_T3.pdf
Fragmento de la descripción:
(S) -N-metilnaltrexona, proceso para su síntesis y su uso farmacéutico.
CAMPO DE LA INVENCIÓN
Esta invención se relaciona con la (S) -N-metilnaltrexona (S-MNTX) , métodos de síntesis estereoselectivos para la preparación de S-MNTX, preparaciones farmacéuticas que comprenden S-MNTX y sus usos terapéuticos.
ANTECEDENTES DE LA INVENCIÓN
La metilnaltrexona (MNTX) es un derivado cuaternario del antagonista opioide puro, naltrexona. Existe como una sal. Los nombres usados para la sal de bromuro de MNTX en la literatura incluyen: bromuro de metilnaltrexona; bromuro de N-Metilnaltrexona; metobromuro de naltrexona; metil bromuro de naltrexona; MRZ 2663BR. La MNTX se reportó primero a mediados de los años 70 por Goldberg y col. como se describe en la patente de Estados Unidos núm. 4, 176, 186. Se cree que la adición del grupo metilo al anillo de nitrógeno forma un compuesto cargado con mayor polaridad y menor liposolubilidad que la naltrexona. Esta característica de MNTX evita que cruce la barrera hematoencefálica en humanos. Como consecuencia, MNTX ejerce sus efectos en la periferia en lugar de en el sistema nervioso central, con la ventaja de que no contrarresta los efectos analgésicos de los opioides en el sistema nervioso central.
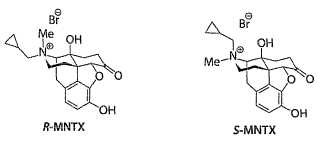
La MNTX es una molécula quiral y el nitrógeno cuaternario puede estar en la configuración R o S. (Ver la Figura 1.) Se desconoce si los diferentes estereoisómeros de MNTX exhiben diferentes propiedades biológicas y químicas. Todas las funciones informadas de MNTX descritas en la literatura indican que MNTX es un antagonista opioide periférico. Algunas de estas funciones antagonistas se describen en las patentes de Estados Unidos 4, 176, 186, 4, 719, 215, 4, 861, 781, 5, 102, 887, 5, 972, 954, 6, 274, 591, 6, 559, 158, y 6, 608, 075, y en las solicitudes de patente de Estados Unidos con núms. de serie 10/163, 482 (2003/0022909A1) , 10/821, 811 (20040266806) , 10/821, 813 (20040259899) y 10/821, 809 (20050004155) . Estos usos incluyen la reducción de los efectos secundarios de los opioides sin reducir el efecto analgésico de los opioides. Estos efectos secundarios incluyen náuseas, emesis, disforia, prurito, retención urinaria, hipomotilidad intestinal, estreñimiento, hipomotilidad gástrica, vaciado gástrico retrasado y supresión inmune. La materia describe que MNTX no sólo reduce los efectos secundarios derivados del tratamiento analgésico opioide sino que además reduce los efectos secundarios mediados por los opioides endógenos solos o junto con el tratamiento con opioides exógenos. Estos efectos secundarios incluyen la inhibición de la motilidad gastrointestinal, disfunción gastrointestinal postoperatoria, estreñimiento idiopático y otras de estas afecciones que incluyen, pero sin limitarse a, las mencionadas anteriormente. Sin embargo, no está claro a partir de la materia si la MNTX usada en estos estudios era una mezcla de los estereoisómeros R y S o un solo estereoisómero.
La materia sugiere que los estereoisómeros de un compuesto aislados a veces pueden tener propiedades físicas y funcionales opuestas, aunque es impredecible si este es el caso en cualquier circunstancia particular. El dextrometoríano es un supresor de la tos, mientras que su enantiómero, levometoríano, es un potente narcótico. El R, R-metilfenidato es un fármaco para tratar el trastorno de hiperactividad con déficit de atención (ADHD) , mientras que su enantiómero, S, S-metilfenidato es un antidepresivo. La S-fluoxetina es activo contra la migraña, mientras que su enantiómero, R-fluoxetina se usa para tratar la depresión. El enantiómero S del citalopram es el isómero terapéuticamente activo para el tratamiento de la depresión. El enantiómero R es inactivo. El enantiómero S del omeprazol es más potente para el tratamiento de la acidez que el enantiómero R.
Bianchetti y col., 1983 Life Science 33 (Sup I) :415-418 estudiaron tres pares de diastereoisómeros del antagonista narcótico cuaternario y sus aminas terciarias parentales, levallorían, nalorfina, y naloxona, para ver cómo afectaba la configuración sobre el nitrógeno quiral la actividad in vitro e in vivo. Se encontró que la actividad varió considerablemente en dependencia de cómo se prepararon los derivados cuaternarios. En cada serie, sólo el diastereómero obtenido por metilación de la amina terciaria N-alilo-sustituida (referida como "diastereómero Nmetilo") fue potente en el desplazamiento de la 3H-naltrexona de las membranas de cerebro de ratas, y actuó como un antagonista de la morfina en el íleon de conejillo de indias. Por el contrario, los diastereoisómeros obtenidos por la reacción de las aminas terciarias N-metilo-sustituidas con haluro de alilo (referido como "diastereoisómeros Nalilo") no desplazó la 3H-naltrexona y tuvo actividad antagonista insignificante y ligera acción agonista en el íleon de conejillo de indias. Los hallazgos in vivo generalmente fueron consistentes con los in vitro. Así sólo los "diastereoisómeros N-metilo" pero no los "N-alilo" inhibieron el estreñimiento inducido por la morfina en ratas y se comportaron como antagonistas. El autor declaró que los materiales preparados parecían ser puros por análisis de resonancia magnética nuclear 1H y 13C (NMR) , pero estos métodos no son exactos. El autor cita una referencia de la literatura para la asignación de la configuración R al "diastereómero N-metilo" de nalorfina. No se propone asignación para los diastereoisómeros levaloríano y naloxona. Sería aventurado extrapolar la configuración para estos diastereoisómeros (R.J. Kobylecki y col., J. Med. Chem. 25, 1278-1280, 1982) .
La patente de Estados Unidosnúm. 4, 176, 186 de Goldberg y col., y más recientemente el documento WO
2004/043964 A2de Cantrell y col. describe un protocolo para la síntesis de MNTX. Ambos describen una síntesis de MNTX por cuaternización de un alcaloide morfinano terciario N-sustituido con un agente de metilación. Tanto Goldberg y col. y Cantrell y col. guardan silencio con respecto a cómo se produjo el estereoisómero (s) por la síntesis. Los autores se mantuvieron cautelosamente en silencio sobre la estereoquímica porque la estereoquímica no se pudo determinar en base a la materia anterior. La cadena lateral ciclopropilmetilo en la naltrexona es diferente de las cadenas laterales de la materia anterior y puede haber afectado el resultado estereoquímico en la síntesis de MNTX, como puede con otros parámetros de la reacción tales como la temperatura y la presión. Basado en el método de síntesis descrito en cada uno, se conoce si la MNTX que se produjo así era R, S o una mezcla de ambos.
Iorio Maria y otros, European Journal of Medicinal Chemistr y , vol. 19, núm. 4, 1984, páginas 301-303 describe las propiedades como agonista/antagonista del narcótico de diastereoisómeros cuaternarios derivados de oximorfona y naloxona. El documento no describe la metilnaltrexona ni predice sus propiedades.
Funke Carel W y col., Journal of the Chemical Society, Perkin Transactions 2, 1986, páginas 735-738 describe estudios de resonancia nuclear de protones y 13C de sales cuaternarias de naloxona y oximorfona. Otra vez, el documento no describe la metilnaltrexona ni predice sus propiedades.
Kobylecki RJ, Journal of Medicinal Chemistr y , American Chemical Society, vol. 25, núm. 11, 1982, páginas 12781280 describe N-metilnalorfina y considera el efecto de los sustituyentes de nitrógeno ecuatoriales y axiales en el antagonismo opioide.
Ambos Yuan Chun-su, Journal of Supportive Oncology, vol. 2, núm. 2, Marzo 2004 (2004-03) , páginas 111-117 y De Ponti, Current Opinion in Investigational Drugs, vol. 3, núm. 4, abril 2002, páginas 614-620 describen la metilnaltrexona y sus propiedades antagonistas opioides.
La S-MNTX en forma pura, y un método para preparar la S-MNTX pura no se han descrito en la literatura. Los investigadores habrían sido incapaces de caracterizar y distinguir definitivamente el estereoisómero (s) obtenido por la síntesis de Goldberg y col. o Cantrell y col. en ausencia de S-MNTX como un estándar.
SUMARIO DE LA INVENCIÓN
La S-MNTX ahora se ha producido con alta pureza, lo que permite la caracterización de su tiempo de retención relativo en cromatografía contra el de (R) -N-metilnaltrexona (R-MNTX) . Se ha encontrado que la S-MNTX tiene actividad diferente de la actividad de MNTX informada en la literatura.
La presente invención proporciona S-MNTX de alta pureza, cristales de S-MNTX de alta pureza e intermedios de los mismos, métodos nuevos de hacer S-MNTX de alta pureza, métodos para analizar S-MNTX en una mezcla de R-MNTX y S-MNTX, métodos de distinguir R-MNTX de S-MNTX, métodos de cuantificar S-MNTX, productos farmacéuticos que contienen... [Seguir leyendo]
Reivindicaciones:
1. Un compuesto de la configuración S con respecto al nitrógeno de la Fórmula I:
que tiene al menos 75% pureza, en donde X es un contraión.
2. El compuesto de la reivindicación 1, en donde el contraión es un haluro, sulfato, fosfato, nitrato, o especies 10 orgánicas cargadas aniónicas, preferentemente el contraión es un haluro, que es opcionalmente:
(a) bromuro; o,
(b) yoduro.
(a) 90%; o,
(b) 95%.
5. El compuesto de las reivindicaciones 1-4, en donde el compuesto está en forma de un cristal.
6. Una composición que comprende MNTX, en donde la MNTX presente en la composición es mayor que 75% 25 en la configuración S con respecto al nitrógeno.
7. Una composición que comprende MNTX de la reivindicación 6, en donde la MNTX presente en la composición es mayor que :
(a) aproximadamente 90%;
(b) aproximadamente 95%;
(c) aproximadamente 98%; o,
(d) mayor que 99% 35 en la configuración S con respecto al nitrógeno.
8. La composición de la reivindicación 6 o la reivindicación 7, en donde la MNTX tiene un contraión que es un haluro, sulfato, fosfato, nitrato, o especies orgánicas cargadas aniónicas, preferentemente el contraión es un haluro, que es opcionalmente:
(a) yoduro; o,
(b) bromuro.
9. La composición de cualquiera de las reivindicaciones 6, 7 u 8, en donde la composición es:
(a) una solución; o,
(b) un sólido.
10. Una composición de cualquiera de las reivindicaciones 6 a 8, en donde la composición es una composición 50 farmacéutica que además comprende un portador farmacéuticamente aceptable.
11. La composición farmacéutica de la reivindicación 10, que además comprende un agente terapéutico distinto de la MNTX.
12. La composición farmacéutica de la reivindicación 11, en donde el agente terapéutico es:
(a) un opioide o agonista opioide, que es opcionalmente alfentanil, anileridina, asimadolina, bremazocina, burprenorfina, butoríanol, codeína, dezocina, diacetilmorfina (heroína) , dihidrocodeína, difenoxilato, fedotozina, fentanilo, funaltrexamina, hidrocodona, hidromorfona, levalorían, acetato de
levometadilol, levoríanol, loperamida, meperidina (petidina) , metadona, morfina, morfina-6-glucuronida, nalbufina, nalorfina, opio, oxicodona, oximorfona, pentazocina, propiram, propoxifeno, remifentanil, sufentanil, tilidina, trimebutina, tramadol, o cualquier combinación de estos;
(b) un opioide o agonista opioide el cual sustancialmente no tiene actividad sobre el sistema nervioso central (CNS) ;
(c) un no opioide, agonista opioide, o un antagonista opioide;
(d) un agente antiviral, agente antibiótico, un agente antimicótico, un agente antibacteriano, un agente antiséptico, un agente antiprotozoo, un agente anti-parasítico, un agente antiinflamatorio, un agente vasoconstrictor, un agente anestésico local, un agente anti-diarreico, un agente anti-hiperalgesia, o cualquier combinación de estos;
(e) un agente anti-diarreico que es loperamida, análogos de loperamida, N-óxidos de loperamida y análogos, metabolitos y profármacos de los mismos, didenoxilato, cisaprida, antiácidos, hidróxido de aluminio, silicato alumínico de magnesio, carbonato magnésico, hidróxido magnésico, carbonato cálcico, policarbofilo, simeticona, hiosciamina, atropina, furazolidona, difenoxina, octreotide, lansoprazol, caolín, pectina, carbón activado, sulfaguanidina, succinilsulfatiazol, ftalilsulfatiazol, aluminato de bismuto, subcarbonato de bismuto, subcitrato de bismuto, citrato de bismuto dicitrato, bismutato tripotásico, tartrato de bismuto, subsalicilato de bismuto, subnitrato de bismuto y subgalato de bismuto, tintura de opio (paregórico) , medicamentos a base de hierbas, agentes anti-diarreicos derivados de plantas o combinaciones de los mismos;
(f) un agente antiinflamatorio que es un fármaco antiinflamatorio no esteroidal (NSAID) , un inhibidor del factor de necrosis tumoral, basiliximab, daclizumab, infliximab, micofenolato, mofetil, azotioprina, tacrolimus, esteroides, sulfasalazina, olsalazina, mesalamina, o cualquier combinación de estos;
(g) un agente anti-viral;
(h) un agente anti-bacterial; o,
(i) un agente anti-hiperalgesia.
13. La composición farmacéutica de la reivindicación 10, en donde la composición es:
(a) entéricamente recubierta;
(b) en una formulación de liberación controlada o liberación sostenida;
(c) una solución;
(d) una formulación tópica;
(e) liofilizada; o,
(f) un supositorio.
14. Un inhalador que contiene la composición farmacéutica de la reivindicación 10.
15. Un dispositivo aerosol nasal que contiene la composición farmacéutica de la reivindicación 10.
16. Un método para sintetizar una sal de un compuesto de la reivindicación 1 que comprende combinar (yodometil) ciclopropano con oximorfona en un primer solvente para producir una sal yodada de S-MNTX.
17. El método de la reivindicación 16 que además comprende, transferir la sal yodada de S-MNTX a un segundo solvente; e intercambiar el yoduro por un contraión distinto del yoduro.
18. El método de la reivindicación 16 que además comprende, transferir la sal yodada de S-MNTX a un segundo solvente, e intercambiar el yoduro por bromuro para producir una sal de bromo de S-MNTX.
19. El método de la reivindicación 16, en donde el primer solvente comprende N-metilpirrolidona.
20. El método de la reivindicación 18, en donde el segundo solvente comprende al menos acetato de isopropilo
o dioxano.
21. El método de la reivindicación 18, en donde el primer solvente es N- metilpirrolidona y el segundo solvente es acetato de isopropilo o dioxano, opcionalmente la combinación de (yodometil) ciclopropano con oximorfona en un primer solvente para producir una sal yodada de S-MNTX se lleva a cabo bajo una temperatura de reacción controlada entre 65° y 75°C, en donde el intercambio de yoduro por bromuro para producir una sal de bromo de S-MNTX se lleva a cabo a temperatura ambiente.
22. El método de la reivindicación 16, que además comprende purificar la sal de S-MNTX por cromatografía, recristalización, o una combinación de estos.
23. El método de la reivindicación 18, que además comprende purificar la sal de S-MNTX por cromatografía, recristalización, o una combinación de estos, opcionalmente la purificación es por múltiples recristalizaciones.
24. El método de la reivindicación 16 o 19, en donde el método se lleva a cabo bajo una temperatura de reacción controlada entre 65° y 75°C.
25. Un compuesto de cualquiera de las reivindicaciones 1 a 5, o una composición de cualquiera de las reivindicaciones 6 a 10 para usar en un método
(a) para inhibir la diarrea, en donde la composición se administra a un sujeto y preferentemente se administra además un agente anti-diarrea que no es S-MNTX, opcionalmente un opioide o un agonista opioide;
(b) reducir un volumen de descarga de una ileostomía o colostomía en un sujeto;
(c) reducir una velocidad de descarga de una ileostomía o colostomía en un sujeto;
(d) para inhibir la motilidad gastrointestinal, en donde la composición se administra a un sujeto, un opioide o un agonista opioide es además opcionalmente administrado;
(e) para tratar el síndrome del intestino irritable, en donde la composición se administra en una cantidad eficaz para mejorar al menos un síntoma del síndrome del intestino irritable.
26. Un compuesto de cualquiera de las reivindicaciones 1 a 5, o una composición de cualquiera de las reivindicaciones 6 a 10 para usar en un método para inhibir el dolor, en donde la composición se administra a un sujeto.
27. El compuesto o composición para usar como se reivindica en la reivindicación 26, en donde un agente terapéutico que no sea S-MNTX se adminsitra también, el cual es opcionalmente:
(a) un opioide; y/o,
(b) un agente antiviral, un agente antibiótico, un agente antimicótico, un agente antibacteriano, un agente antiséptico, un agente antiprotozoo, un agente anti-parasítico, un agente antiinflamatorio, un agente vasoconstrictor, un agente anestésico local, un agente anti-diarreico o un agente antihiperalgesia.
28. El compuesto o composición para usar como se reivindica en la reivindicación 26, en donde el dolor es hiperalgesia periférica.
29. El compuesto o composición para usar como se reivindica en la reivindicación 26, en donde la composición farmacéutica se administra:
(a) localmente en un sitio del dolor;
(b) intra-articularmente;
(c) sistémicamente;
(d) tópicamente; o,
(e) en el ojo.
30. Un compuesto de cualquiera de las reivindicaciones 1 a 5, o una composición de cualquiera de las reivindicaciones 6 a 10, para usar en un método para inhibir la inflamación, en donde la composición se administra a un sujeto.
31. El compuesto o composición para usar como se reivindica en la reivindicación 30 en donde se administra también un agente terapéutico que no sea S-MNTX, que es opcionalmente un agente antiinflamatorio.
32. El compuesto o composición para usar como se reivindica en la reivindicación 30 para administrarse:
(a) localmente en un sitio de la inflamación;
(b) sistémicamente; o
(c) tópicamente.
33. Un compuesto de cualquiera de las reivindicaciones 1 a 5, o una composición de cualquiera de las reivindicaciones 6 a 10 para usar en un método para inhibir la producción del factor de necrosis tumoral (TNF) en un sujeto.
34. Un kit que comprende un empaque que contiene un contenedor sellado que comprende la composición farmacéutica de la reivindicación 10 e instrucciones para su uso.
35. El kit de acuerdo con la reivindicación 34, que además comprende un agente terapéutico que no sea S-MNTX, en donde el agente terapéutico es preferentemente un opioide o agonista opioide, y opcionalmente el opioide o agonista opioide:
(a) sustancialmente no tiene actividad CNS; y/o,
(b) es un agente antiviral, agente antibiótico, un agente antimicótico, un agente antibacteriano, un agente antiséptico, un agente antiprotozoo, un agente anti-parasítico, un agente antiinflamatorio, un agente vasoconstrictor, un agente anestésico local, un agente anti-diarreico, o un agente antihiperalgesia, o cualquier combinación de estos.
36. El kit de acuerdo con la reivindicación 35, en donde el agente terapéutico es un antagonista opioide periférico, que es opcionalmente:
(a) R-MNTX; o,
(b) una piperidina N-alquilcarboxilato, un derivado cuaternario de noroximorfona, un derivado alcaloide del opio, o un benzomoríano cuaternario.
37. Un compuesto como se define en cualquiera de las reivindicaciones 1 a 5 para usar en un método para regular la función gastrointestinal en donde dicho compuesto, y un antagonista opioide mu periférico, se administran a un sujeto.
38. Un compuesto para usar como se reivindica en la reivindicación 37 en donde el antagonista opioide mu periférico es:
(a) R-MNTX; o
(b) una piperidina N-alquilcarboxilato, un derivado cuaternario de noroximorfona, un derivado alcaloide del opio, o un benzomoríano cuaternario.
39. Un empaque que contiene una composición que comprende S-MNTX, en donde la composición está libre de R-MNTX detectable por HPLC, y marcada en o contenida dentro del empaque indicando que la composición está libre de R-MNTX detectable, y en donde la composición es opcionalmente una composición farmacéutica.
Patentes similares o relacionadas:
Regímenes de dosificación de buprenorfina, del 1 de Julio de 2020, de Indivior UK Limited: Buprenorfina para su uso en un método para tratar el trastorno por uso de opioides en un ser humano que lo necesite, que comprende las etapas […]
 Forma de dosificación llena de líquido, disuasoria del abuso y de liberación inmediata, del 24 de Junio de 2020, de Pharmaceutical Manufacturing Research Services, Inc: Una cápsula disuasoria del abuso de liberación inmediata, que comprende:
(a) un principio activo susceptible de abuso;
(b) un primer polietilenglicol (PEG) […]
Forma de dosificación llena de líquido, disuasoria del abuso y de liberación inmediata, del 24 de Junio de 2020, de Pharmaceutical Manufacturing Research Services, Inc: Una cápsula disuasoria del abuso de liberación inmediata, que comprende:
(a) un principio activo susceptible de abuso;
(b) un primer polietilenglicol (PEG) […]
Gránulos de dispersión rápida, comprimidos de desintegración oral y métodos, del 3 de Junio de 2020, de Adare Pharmaceuticals, Inc: Microgránulos de dispersión rápida, farmacéuticamente aceptables, que tienen una mediana del tamaño de partícula en el rango de 100 μm a 300 […]
Pulverizador de buprenorfina sublingual, del 22 de Abril de 2020, de Fresh Cut Development, LLC: Una formulación de pulverización sublingual que comprende una cantidad efectiva de buprenorfina, o una sal farmacéuticamente aceptable de la misma, […]
Dispositivos de administración transdérmica resistentes al abuso y composiciones que comprenden un agonista de opioides y un derivado N-óxido no administrado por vía transdérmica de un antagonista de opioide para el tratamiento del dolor, del 22 de Abril de 2020, de EURO-CELTIQUE S.A.: Un dispositivo de administración transdérmica que comprende una composición farmacéutica, en el que dicha composición comprende un derivado […]
Formulación farmacéutica a base de ibuprofeno y codeína que tiene estabilidad mejorada, del 15 de Abril de 2020, de FARMASIERRA MANUFACTURING S.L: Formulación farmacéutica a base de ibuprofeno y codeínade estabilidad mejorada. La invención consiste en una nueva formulación farmacéuticaen forma […]
Parche transdérmico de oximorfona, del 8 de Abril de 2020, de Buzzz Pharmaceuticals Limited: Un parche transdérmico que tiene una capa que contiene el fármaco que comprende oximorfona o una sal farmacéuticamente aceptable de la misma, […]
Composiciones de buprenorfina y antagonistas del receptor de opioides mu, del 1 de Abril de 2020, de Alkermes Pharma Ireland Limited: Una composición que comprende buprenorfina y un antagonista del receptor opioide μ, en donde la composición está caracterizada por un Índice […]