Procedimiento para purificar 5-amino-N, N''-bis(2,3-dihidroxipropil)-isoftalamida, un intermedio en la preparación de agentes de contraste de rayos X no iónicos.
Un procedimiento para eliminar las impurezas de monometiléster de ABA y de dímero de ABA contenidas en unasolución acuosa de 5-amino-N,
N'-bis(2,3-dihidroxipropil)-isoftalamida (ABA) o clorhidrato de ABA hidrolizando dichasimpurezas en dicha solución acuosa a un pH entre 12 y 13 mediante la adición de una solución acuosa de hidróxidosódico
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E09176517.
Solicitante: GE HEALTHCARE AS.
Nacionalidad solicitante: Noruega.
Dirección: Nycoveien 1-2 P.O. Box 4220 Nydalen 0401 Oslo NORUEGA.
Inventor/es: HOMESTAD, OLE MAGNE, HAALAND,TORFINN.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07C231/24 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07C COMPUESTOS ACICLICOS O CARBOCICLICOS (compuestos macromoleculares C08; producción de compuestos orgánicos por electrolisiso electroforesis C25B 3/00, C25B 7/00). › C07C 231/00 Preparación de amidas de ácidos carboxílicos. › Separación; Purificación.
- C07C237/32 C07C […] › C07C 237/00 Amidas de ácidos carboxílicos, estando sustituida la estructura carbonada de la parte ácida por grupos amino. › con el átomo de nitrógeno del grupo carboxamido unido a un átomo de carbono acíclico de un radical hidrocarbonado sustituido por átomos de oxígeno.
PDF original: ES-2397246_T3.pdf
Fragmento de la descripción:
Procedimiento para purificar 5-amino-N, N'-bis (2, 3-dihidroxipropil) -isoftalamida, un intermedio en la preparación de agentes de contraste de rayos X no iónicos
Campo técnico
La presente invención se refiere, en general, a la preparación de agentes de contraste de rayos X no iónicos. Se refiere adicionalmente a un procedimiento para mejorar la pureza de 5-amino-N, N'-bis (2, 3-dihidroxipropil) isoftalamida (o ABA) , un intermedio en la preparación industrial de agentes de contraste de rayos X no iónicos. En particular, se refiere a un procedimiento para retirar significativamente monometiléster de ABA y dímero de ABA de ABA antes de su yodación.
Antecedentes de la invención Los agentes de contraste de rayos X no iónicos constituyen una clase muy importante de compuestos farmacéuticos producidos en grandes cantidades. 5-[N- (2, 3-dihidroxipropil) -acetamido]-N, N'-bis (2, 3-dihidroxipropil) -2, 4, 6-triyodoisoftalamida ("iohexol") , N, N'-bis (2, 3-dihidroxipropil) -5-[ (2-hidroxiacetil) - (2-hidroxietil) amino]-2, 4, 6-triyodo-benceno1, 3-dicarboxamida ("ioversol") , y 1, 3-bis (acetamido) -N, N'-bis[3, 5-bis (2, 3-dihidroxipropil-aminocarbonil) -2, 4, 6
triyodofenil]-2-hidroxipropano ("iodixanol") son importantes ejemplos de tales compuestos. Contienen uno o dos anillos de benceno triyodados.
La producción industrial de iohexol, ioversol, e iodixanol implica una síntesis química multietapa. La sustancia farmacéutica final debe satisfacer las estrictas normas de pureza establecidas por las agencias reguladoras. Aunque la pureza es de suma importancia, también es importante reducir el coste de producción optimizando cada etapa de síntesis. Incluso una pequeña mejora en el diseño de la reacción puede conducir a un ahorro significativo en una producción a gran escala.
La presente mejora se refiere a 5-amino-N, N'-bis (2, 3-dihidroxipropil) -isoftalamida (conocida también como bisamida del ácido aminoisoftálico, bisamida AIPA o ABA) . ABA es un intermedio común en la preparación industrial de iodixanol e iohexol. Por ejemplo, una de las etapas de síntesis típicas en la preparación de iodixanol es la yodación de ABA usando cloruro de yodo para convertir ABA en 5-amino-N, N'-bis (2, 3-dihidroxipropil) -2, 4, 6-triyodoisoftalamida (Compuesto B) . Véase el Esquema 1; véanse también las Patentes de Estados Unidos Nº 6.441.235 y 6.274.762. La presente invención se refiere a retirar cantidades sustanciales de impurezas en ABA antes de su reacción de yodación.
El documento US 2002/095053 desvela la preparación de 5-amino-isoftalamidas. El documento US- B1-6 274 762 desvela la preparación de compuestos de tri-yodo benceno. El documento US 2004/082811 desvela la preparación de 5-amino-1, 3-benceno-dicarboxamidas N, N-sustituidas, por ejemplo, iopamidol e iohexol.
El documento US 6.441.235 desvela un procedimiento de conversión de 5-NIPA bisamida (5-nitro-N, N'-bis (R) isoftalamida) en ABA (5-amino-N, N'-bis (2, 3-dihidroxipropil) -isoftalamida) . Específicamente, ABA puede aislarse en forma de base libre retirando por filtración el catalizador y retirando el disolvente por evaporación o destilación; o en forma de una sal de adición de ácidos mediante la adición de un ácido fuerte orgánico o inorgánico a la solución de producto, con lo que la sal de adición de ácidos respectiva se separa en una forma cristalina de la solución.
El documento RE38.856E desvela un procedimiento de tratamiento del Compuesto B (5-amino-N, N'-bis (2, 3dihidroxipropil) -2, 4, 6-triyodoisoftalamida) . Específicamente, el documento RE38.856E desvela que el medio de reacción (por ejemplo, de ABA al Compuesto B) "normalmente se neutraliza con una base tal como hidróxido sódico antes del aislamiento de los compuestos triyodados". (Col. 2, 11, 7-9.)
Ninguno de los documentos desvela la eliminación de impurezas de ABA antes de la yodación.
Sumario de la invención La presente invención proporciona un procedimiento para eliminar dos impurezas comunes en ABA, monometiléster de ABA y dímero de ABA, antes de la reacción de yodación de ABA en una síntesis a escala industrial de iohexol, ioversol, e iodixanol. Específicamente, el procedimiento se refiere a hidrolizar ABA a un pH entre 12 y 13 en medio acuoso para convertir el monometiléster de ABA en monoácido de ABA. Después del presente procedimiento, ABA está sustancialmente libre de monometiléster de ABA y dímero de ABA, lo que simplifica en gran medida los procedimientos de purificación posteriores.
Descripción detallada de la invención ABA puede estar en su forma libre o como un clorhidrato como el material de partida para la yodación en la síntesis de iodixanol e iohexol. Tres impurezas comunes de ABA son monometiléster de ABA, dímero de ABA y monoácido de ABA, como se muestra a continuación:
Estas impurezas pueden yodarse junto con el propio ABA. Entre ellas, el monoácido de ABA yodado es relativamente fácil de retirar en las etapas de purificación posteriores. Pero se ha descubierto que el monometiléster
de ABA triyodado y el dímero de ABA yodado son extremadamente difíciles de retirar en etapas de purificación posteriores. Por ejemplo, el monometiléster de ABA triyodado es notablemente estable prácticamente a todos los pH, y es difícil de retirar en las etapas de cristalización posteriores.
Debido a que iohexol, ioversol, e iodixanol tienen todos estrictas especificaciones reguladoras con respecto al perfil de impurezas, es importante limitar la cantidad de impurezas yodadas relacionadas a un mínimo. Se requieren 30 etapas de purificación extensivas (incluyendo recristalización) en las fases posteriores de la síntesis si los niveles iniciales de monometiléster de ABA y dímero de ABA no son reducidos. Sin embargo, etapas de purificación adicionales aumentarían el coste de producción o reducirían el rendimiento de producción debido a la pérdida de intermedios, o sustancia farmacéutica final, como resultado de los nuevos procedimientos de purificación en las fases posteriores de la síntesis.
Se ha descubierto que el nivel de monometiléster de ABA puede reducirse de una manera eficaz por hidrólisis básica. La hidrólisis se realiza en un medio de reacción acuoso, que incluye un medio que contiene una mezcla de agua y otro disolvente. El producto de reacción de la hidrólisis es monoácido de ABA, que puede retirarse fácilmente en la cristalización tanto de ABA como de los productos triyodados posteriores. Además, el dímero de ABA se retira simultáneamente de ABA en el mismo procedimiento de hidrólisis. Debido a la retirada temprana de estas impurezas de ABA, mejoran los rendimientos de todas las demás etapas posteriores. Por ejemplo, la pureza del Compuesto B y, por lo tanto, del Compuesto A aumenta y, a su vez, la dimerización del Compuesto A a iodixanol resulta más eficaz.
Por lo tanto, la presente invención se refiere a un procedimiento para eliminar las impurezas de monometiléster de ABA y de dímero de ABA contenidas en una solución acuosa de 5-amino-N, N'-bis (2, 3-dihidroxipropil) -isoftalamida (ABA) o clorhidrato de ABA hidrolizando dichas impurezas en dicha solución acuosa a un pH entre 12 y 13 mediante la adición de una solución acuosa de hidróxido sódico.
La hidrólisis de la presente invención se realiza a un pH de 12 a 13. Se ha descubierto que este intervalo de pH da una velocidad de hidrólisis adecuada y, al mismo tiempo, evita la hidrólisis de las cadenas secundarias de amida en ABA. La reacción puede completarse en menos de 1 hora, preferentemente en menos de 15-20 minutos o incluso en un minuto. La reacción normalmente se realiza a temperatura ambiente, por ejemplo 20-25 ºC. Los niveles de monometiléster de ABA y dímero de ABA pueden llegar a cero después de la reacción. Normalmente, el monometiléster de ABA puede reducirse del 0, 4 a 0, 7 % a menos del 0, 04 %, como se observa por HPLC, y el dímero de ABA del 0, 1 % a menos del 0, 01 %. La cantidad de monoácido de ABA aumenta normalmente del 0, 2-0, 3 % al 0, 6-0, 8 % en la reacción en base al análisis por HPLC.
Ejemplos
EJEMPLO 1
A una solución acuosa de ABA (200 ml, 38, 8 % p/p) a pH 2, 0 se le añadió una solución acuosa de hidróxido sódico (50 % p/p, 11 ml) durante 20 minutos a temperatura ambiente. Se observó un pH de 13, 0. Un análisis por HPLC inmediato mostró que la cantidad de monometiléster de ABA se había reducido del 0, 34 al 0, 09 %. La cantidad de dímero de ABA no había cambiado. Después de 10 minutos a pH 13, 0 HPLC mostró que el monometiléster de ABA se había reducido adicionalmente al 0, 00 % y el dímero de ABA del 0, 04 al 0, 02 %. El ajuste de pH a 3, 0 mediante ácido clorhídrico... [Seguir leyendo]
Reivindicaciones:
1. Un procedimiento para eliminar las impurezas de monometiléster de ABA y de dímero de ABA contenidas en una solución acuosa de 5-amino-N, N'-bis (2, 3-dihidroxipropil) -isoftalamida (ABA) o clorhidrato de ABA hidrolizando dichas impurezas en dicha solución acuosa a un pH entre 12 y 13 mediante la adición de una solución acuosa de hidróxido sódico.
Patentes similares o relacionadas:
Compuestos opioides de carboxamido, del 4 de Junio de 2014, de JANSSEN PHARMACEUTICA NV: Un compuesto de la Fórmula (I)**Fórmula** donde: R1 y R2 se seleccionan independientemente del grupo consistente en hidrógeno, C1-4 alquilo y alquildiil donde R1 y R2 se […]
Compuestos para el tratamiento de trastornos metabólicos, del 9 de Octubre de 2013, de WELLSTAT THERAPEUTICS CORPORATION: Un agente biológicamente activo, en donde el agente es un compuesto de la fórmula:**Fórmula** en donde n es 1 ó 2; q es 0 ó 1; t es 0 ó 1; R5 es alquilo que […]
Moduladores de receptores de cannabinoides, del 22 de Agosto de 2013, de UCL BUSINESS PLC: Compuesto de fórmula I, o una sal farmacéuticamente aceptable del mismo, **Fórmula** en la que: Z es NR1R2 en el que cada uno de R1 y R2 es […]
Agentes de contraste, del 22 de Febrero de 2013, de GE HEALTHCARE AS: Compuestos de la fórmula (I) en la que cada R1 son iguales o diferentes y denotan los restos de CH2-O-CH2-R3; R2 denota R1 o uno de los restos de alquilo C1-C4, CH2O(alquilo […]
 Derivado de benciloxipropilamina, del 22 de Febrero de 2013, de NIPPON ZOKI PHARMACEUTICAL CO., LTD.: Un compuesto, que es un derivado de benciloxipropilamina de fórmula (I) o una sal o hidrato farmacéuticamenteaceptable del mismo:
en la que
R1a […]
Derivado de benciloxipropilamina, del 22 de Febrero de 2013, de NIPPON ZOKI PHARMACEUTICAL CO., LTD.: Un compuesto, que es un derivado de benciloxipropilamina de fórmula (I) o una sal o hidrato farmacéuticamenteaceptable del mismo:
en la que
R1a […]
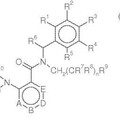 Derivados de antranilamida/2-amino-heteroareno-carboxamida, del 27 de Junio de 2012, de F. HOFFMANN-LA ROCHE AG: Un compuesto de la fórmula I **Fórmula**
en la que
R1, R2, R4 y R5 son con independencia hidrógeno, alquilo C1-C6, alcoxi C1-C6 o halógeno;
R3 […]
Derivados de antranilamida/2-amino-heteroareno-carboxamida, del 27 de Junio de 2012, de F. HOFFMANN-LA ROCHE AG: Un compuesto de la fórmula I **Fórmula**
en la que
R1, R2, R4 y R5 son con independencia hidrógeno, alquilo C1-C6, alcoxi C1-C6 o halógeno;
R3 […]
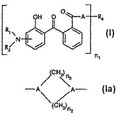 Derivados de la hidroxifenil benzofenona amino sustituidos, del 11 de Abril de 2012, de BASF SE: Compuesto de la fórmula
en forma micronizada que tiene un tamaño de partícula de 0.02 a 2 micrómetros, en donde
R1 y R2 independientemente uno del otro […]
Derivados de la hidroxifenil benzofenona amino sustituidos, del 11 de Abril de 2012, de BASF SE: Compuesto de la fórmula
en forma micronizada que tiene un tamaño de partícula de 0.02 a 2 micrómetros, en donde
R1 y R2 independientemente uno del otro […]
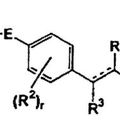 DERIVADOS DE ACIDO CRBOXILICO Y COMPOSICIONES FARMACEUTICAS QUE CONTIENEN LOS MISMOS COMO INGREDIENTE ACTIVO, del 16 de Abril de 2009, de ONO PHARMACEUTICAL CO., LTD.: Un agonista de EDG-1 que comprende, como ingrediente activo, un derivado de ácido carboxílico representado por la Fórmula (I) ** ver fórmula** en la cual R 1 es alquilo […]
DERIVADOS DE ACIDO CRBOXILICO Y COMPOSICIONES FARMACEUTICAS QUE CONTIENEN LOS MISMOS COMO INGREDIENTE ACTIVO, del 16 de Abril de 2009, de ONO PHARMACEUTICAL CO., LTD.: Un agonista de EDG-1 que comprende, como ingrediente activo, un derivado de ácido carboxílico representado por la Fórmula (I) ** ver fórmula** en la cual R 1 es alquilo […]