Novedosos compuestos inmunoadyuvantes basados en flagelina y uso de los mismos.
Un compuesto inmunoadyuvante que comprende:
a) un péptido del extremo N-terminal que tiene al menos el 90 % de identidad de aminoácidos con la secuencia de aminoácidos que comienza en el residuo de aminoácido localizado en la posición 1 de SEC ID Nº 1 y que termina en un residuo de aminoácido seleccionado del grupo que consiste en uno cualquiera de los residuos de 5 aminoácidos localizados en las posiciones 99 a 173 de SEC ID Nº 1;
y
b) un péptido del extremo C-terminal que tiene al menos el 90 % de identidad de aminoácidos con la secuencia de aminoácidos que comienza en un residuo de aminoácido seleccionado del grupo que consiste en uno cualquiera de los residuos de aminoácidos localizados en las posiciones 401 a 406 de SEC ID Nº 1 y que termina en el residuo de aminoácido localizado en la posición 494 de SEC ID Nº 1, en el que:
- dicho péptido del extremo N-terminal está directamente ligado a dicho péptido del extremo C, o
- dicho péptido del extremo N-terminal y dicho péptido del extremo C-terminal están directamente ligados, el uno con el otro, mediante una cadena espaciadora, en el que la cadena espaciadora consiste en 1-20 aminoácidos ligados por enlaces peptídicos, en el que los aminoácidos están seleccionados de los aminoácidos naturales y en el que el compuesto no es SEC ID Nº: 15, 628, 630, 632, 634, 713, 715, 717, 15 719 ó 721 del documento WO 2009/128950.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2009/057836.
Solicitante: INSERM (INSTITUT NATIONAL DE LA SANTE ET DE LA RECHERCHE MEDICALE).
Nacionalidad solicitante: Francia.
Dirección: 101, RUE DE TOLBIAC 75013 PARIS FRANCIA.
Inventor/es: SIRARD,JEAN-CLAUDE.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K39/39 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 39/00 Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53). › caracterizados por los aditivos inmunoestimulantes, p. ej. por los adyuvantes químicos.
- C07K14/255 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › Salmonella (G).
- C12N15/11 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Fragmentos de ADN o de ARN; sus formas modificadas (ADN o ARN no empleado en tecnología de recombinación C07H 21/00).
PDF original: ES-2445798_T3.pdf
Fragmento de la descripción:
Novedosos compuestos inmunoadyuvantes basados en flagelina y uso de los mismos Campo de la invención La presente invención se refiere a la inducción y/o estimulación de la respuesta inmunitaria en un individuo o un animal.
Se refiere en particular a nuevos compuestos inmunoadyuvantes útiles para composiciones inmunogénicas y de vacuna.
Antecedentes de la invención El desarrollo de vacunas seguras y eficaces sigue siendo un objetivo importante en la salud pública mundial.
En particular, las vacunas llamadas “mucosas” han emergido como una posible y atractiva alternativa a vacunas inyectables.
La administración por la mucosa tiene muchos atributos potencialmente deseables. Quizás el motivo más persuasivo para desarrollar técnicas de administración de vacunas por la mucosa sea el desarrollo de una defensa de inmunidad de primera línea, generando inmunidad local en el sitio mucoso de entrada para muchos patógenos invasores.
Además, algunos investigadores han informado que existe un sistema inmunitario mucoso común, por lo que la inmunidad mucosa inducida en un sitio puede conducir a inmunidad en un sitio mucoso distal (McGhee, J. R. y col. The mucosal immune system: from fundamental concepts to vaccine development. Vaccine 1992, 10:75-88) .
Además, la administración de un antígeno mediante un sitio mucoso tiene la posibilidad de generar también una respuesta inmunitaria sistémica.
Esto sugiere que pueden lograrse beneficios significativos por la administración de vacunas de una forma no invasiva, por ejemplo, intranasalmente u otra vía mucosa, para provocar inmunidad a una amplia gama de patógenos que pueden entrar en diferentes sitios mucosos.
La mayoría de las vacunas de nuestros días (vacunas mucosas u otras) están compuestas de dos componentes principales: (i) el antígeno diana de interés terapéutico y (ii) compuesto (s) inmunoadyuvante (s) que estimulan y/o inducen inmunogenicidad contra dicho antígeno.
La naturaleza de los inmunoadyuvantes conocidos varía enormemente, pero incluye en particular aceites minerales, extractos bacterianos, organismos vivos y atenuados, y suspensiones de metales de hidróxido de aluminio.
Aunque los adyuvantes proporcionan respuestas inmunitarias potenciadas, su uso también puede provocar efectos secundarios adversos, en función en particular de su vía administrada. Por tanto, los números de adyuvantes que están aprobados y son eficaces en seres humanos siguen siendo relativamente limitados.
Los avances en el campo de la inmunidad innata han proporcionado un mejor entendimiento de tanto los mecanismos celulares como moleculares que gobiernan la regulación de la respuesta inmunitaria del huésped.
Este mejor conocimiento del sistema inmunitario ha permitido la investigación y desarrollo de nuevos posibles inmunoadyuvantes útiles.
En particular, los receptores similares a toll (TLR) son fundamentales en la inducción coordinada de inmunidad innata y adaptativa en mamíferos. Como los TLR son expresados por una amplia variedad de tipos de células, pueden estimular la inmunidad por todo el organismo.
Tras la infección por microorganismos patógenos, los TLR reconocen motivos conservados denominados patrones moleculares asociados a microbios (MAMP) . La interacción de TLR induce un programa de expresión génica dedicado a tanto la eliminación innata de como la inmunidad adquirida a microorganismos patógenos. Por ejemplo, los TLR inducen la producción de quimiocinas que, a su vez, atraen específicamente los neutrófilos polimorfonucleares (PMN) directamente implicados en la eliminación microbiana innata. Además, los TLR promueven la secreción de mediadores inmunes pleiotrópicos (tales como TNFa) y la maduración funcional de células dendríticas (CD) que se especializan en presentación de antígeno a linfocitos.
Por consiguiente, los agonistas de TLR no solo estimulan respuestas inmunitarias pro-inflamatorias “ampliamente específicas”, sino que también potencian la respuesta inmunitaria adaptativa a antígenos, y así se considera que son inmunoadyuvantes.
A pesar de estos efectos posiblemente beneficiosos, la toxicidad sistémica de MAMP ha dado lugar a esfuerzos para desarrollar derivados que inclinen la actividad de MAMP hacia la adyuvancia. De hecho, moléculas manipuladas con propiedades únicas es un reto importante en la manipulación de respuestas inmunitarias.
Las flagelinas bacterianas (los principales componentes del flagelo en muchos patógenos bacterianos) son agonistas únicos específicos para la activación de TLR5.
La flagelina FliC de Salmonella enterica serovar Typhimurium (S. typhimurium) es el paradigma de estudios sobre la estructura-función de flagelo, inmunidad y señalización de TLR5.
Es una proteína de 494 aminoácidos con dos dominios distintos. Las regiones “conservadas” en el extremo amino y carboxi forman un dominio que es esencial para la activación de TLR5.
El dominio central de la flagelina FliC comprende aminoácidos no obligatorios para la señalización de TLR5. Se designa una región “hipervariable”, ya que las secuencias primarias varían enormemente en composición y tamaño de una especie bacteriana a otra. A diferencia, se sabe que la región hipervariable es esencial para la antigenicidad de la flagelina.
Se ha mostrado que la inyección intravenosa (i.v.) de flagelinas promueve una respuesta sistémica, caracterizada por la producción de mediadores pro-inflamatorios (tales como TNFa o IL-6) y activación de CD.
Además, las flagelinas desencadenan mecanismos de defensa innatos y adaptativos específicos de mucosa. Por ejemplo, líneas celulares epiteliales y mucosa de pulmón regulan por incremento la producción de quimiocinas como CXCL8 (IL-8) y CCL20 que, a su vez, reclutan PMN y CD mucosos, respectivamente.
Diversos autores también han informado de que las flagelinas son potentes inmunoadyuvantes sistémicos y mucosos que provocan (i) respuestas de anticuerpos en suero y/o secretoras y (ii) respuestas de células Th1 y Th2 a tanto las propias flagelinas como a antígenos co-administrados.
Debido a sus potentes actividades de inmunoadyuvante sistémico y mucoso, las flagelinas pueden ser particularmente interesantes para el desarrollo de vacuna, y en particular de tipo de vacuna mucosa. Tal uso se ha propuesto en el documento WO-A-2004 022092.
Sin embargo, la mayoría de dichos adyuvantes tipo flagelina no son completamente adecuados para tal aplicación de vacuna, y en particular para dicha estrategia de vacuna mucosa.
De hecho, los adyuvantes de flagelina conocidos muestran efectos secundarios importantes, y en particular actividad antigénica intrínseca y propiedades pro-inflamatorias sistémicas cuando se administran in vivo.
Además, la mayoría de los inmunoadyuvantes tipo flagelina conocidos necesitan estar físicamente ligados al antígeno diana, con el fin de provocar una potente respuesta inmunitaria cuando se administran in vivo. Este requisito obliga a complejas manipulaciones adicionales para obtener un enlace flagelina-antígeno adecuado, y la sustancia inmunogénica útil final.
Por tanto, existe la necesidad de nuevos compuestos que puedan usarse como adyuvantes inmunológicos, en particular para inducir y/o para potenciar la respuesta inmunitaria mucosa contra un antígeno, en particular sin desencadenar ningún efecto secundario de inflamación sistémica significativo.
Estos nuevos compuestos deben también ser capaces de desencadenar ventajosamente una respuesta inmunitaria por una simple mezcla con el antígeno diana.
La presente invención propone entonces nuevos compuestos inmunoadyuvantes que satisfacen esta necesidad, y que pueden ser particularmente útiles para la producción de composiciones inmunogénicas y de vacuna (en particular de tipo mucoso) .
Sumario de la invención Se ha encontrado, según la invención, novedosos compuestos de péptido derivados de flagelina que se originan a partir de Salmonella enterica serovar Typhimurium de tipo SEC ID Nº 1, que presentan una actividad adyuvante in vivo como se ilustra en los ejemplos en la presente memoria.
También se ha mostrado según la presente invención que estos novedosos compuestos adyuvantes presentan en particular propiedades de adyuvante mucoso, sin ejercer efectos pro-inflamatorios sistémicos significativos.
Dichos nuevos compuestos derivados de flagelina de la invención son así particularmente útiles como sustancias inmunoadyuvantes, ventajosamente para inducir y/o para potenciar una respuesta inmunitaria mucosa.
Así, la presente invención se refiere... [Seguir leyendo]
Reivindicaciones:
1. Un compuesto inmunoadyuvante que comprende:
a) un péptido del extremo N-terminal que tiene al menos el 90 % de identidad de aminoácidos con la secuencia de aminoácidos que comienza en el residuo de aminoácido localizado en la posición 1 de SEC ID Nº 1 y que termina en un residuo de aminoácido seleccionado del grupo que consiste en uno cualquiera de los residuos de aminoácidos localizados en las posiciones 99 a 173 de SEC ID Nº 1; y
b) un péptido del extremo C-terminal que tiene al menos el 90 % de identidad de aminoácidos con la secuencia de aminoácidos que comienza en un residuo de aminoácido seleccionado del grupo que consiste en uno cualquiera de los residuos de aminoácidos localizados en las posiciones 401 a 406 de SEC ID Nº 1 y que termina en el residuo de aminoácido localizado en la posición 494 de SEC ID Nº 1, en el que:
- dicho péptido del extremo N-terminal está directamente ligado a dicho péptido del extremo C, o
- dicho péptido del extremo N-terminal y dicho péptido del extremo C-terminal están directamente ligados, el uno con el otro, mediante una cadena espaciadora, en el que la cadena espaciadora consiste en 1-20 aminoácidos ligados por enlaces peptídicos, en el que los aminoácidos están seleccionados de los 20 aminoácidos naturales y en el que el compuesto no es SEC ID Nº: 15, 628, 630, 632, 634, 713, 715, 717, 719 ó 721 del documento WO 2009/128950.
2. Un compuesto inmunoadyuvante que comprende:
a) un péptido del extremo N-terminal que tiene al menos el 90 % de identidad de aminoácidos con la secuencia de aminoácidos que comienza en el residuo de aminoácido localizado en la posición 1 de SEC ID Nº 1 y que termina en un residuo de aminoácido seleccionado del grupo que consiste en uno cualquiera de los residuos de aminoácidos localizados en las posiciones 99 a 173 de SEC ID Nº 1; y
b) un péptido del extremo C-terminal que tiene al menos el 90 % de identidad de aminoácidos con la secuencia de aminoácidos que comienza en un residuo de aminoácido seleccionado del grupo que consiste en uno cualquiera de los residuos de aminoácidos localizados en las posiciones 401 a 406 de SEC ID Nº 1 y que termina en el residuo de aminoácido localizado en la posición 494 de SEC ID Nº 1, en el que:
- dicho péptido del extremo N-terminal está directamente ligado a dicho péptido del extremo C, o
- dicho péptido del extremo N-terminal y dicho péptido del extremo C-terminal están directamente ligados, el uno con el otro, mediante una cadena espaciadora, en el que la cadena espaciadora consiste en 1-20 aminoácidos ligados por enlaces peptídicos, en el que los aminoácidos están seleccionados de los 20 aminoácidos naturales
en el que dicho péptido del extremo N-terminal está seleccionado del grupo que consiste en las secuencias de aminoácidos 1-99, 1-137, 1-160 y 1-173 de SEC ID Nº 1.
3. Un compuesto inmunoadyuvante que comprende:
a) un péptido del extremo N-terminal que tiene al menos el 90 % de identidad de aminoácidos con la secuencia de aminoácidos que comienza en el residuo de aminoácido localizado en la posición 1 de SEC ID Nº 1 y que termina en un residuo de aminoácido seleccionado del grupo que consiste en uno cualquiera de los residuos de aminoácidos localizados en las posiciones 99 a 173 de SEC ID Nº 1; y
b) un péptido del extremo C-terminal que tiene al menos el 90 % de identidad de aminoácidos con la secuencia de aminoácidos que comienza en un residuo de aminoácido seleccionado del grupo que consiste en uno cualquiera de los residuos de aminoácidos localizados en las posiciones 401 a 406 de SEC ID Nº 1 y que termina en el residuo de aminoácido localizado en la posición 494 de SEC ID Nº 1, en el que:
- dicho péptido del extremo N-terminal está directamente ligado a dicho péptido del extremo C, o
- dicho péptido del extremo N-terminal y dicho péptido del extremo C-terminal están directamente ligados, el uno con el otro, mediante una cadena espaciadora, en el que la cadena espaciadora consiste en 1-20 aminoácidos ligados por enlaces peptídicos, en el que los aminoácidos están seleccionados de los 20 aminoácidos naturales
en el que dicho péptido del extremo C-terminal está seleccionado del grupo que consiste en las secuencias de aminoácido.
40. 494 .
40. 494 de SEC ID Nº 1.
4. El compuesto inmunoadyuvante según cualquiera de las reivindicaciones 2 ó 3, en el que dichos péptidos del extremo N-terminal y del extremo C-terminal consisten en las secuencias de aminoácidos 1-173 .
40. 494 de SEC ID Nº 1, respectivamente.
5. El compuesto inmunoadyuvante según cualquiera de las reivindicaciones 2-3, en el que dichos péptidos del extremo N-terminal y del extremo C-terminal consisten en las secuencias de aminoácidos 1-160 .
40. 494 de SEC ID Nº 1, respectivamente.
6. El compuesto inmunoadyuvante según cualquiera de las reivindicaciones 2-3, en el que dichos péptidos del extremo N-terminal y del extremo C-terminal consisten en las secuencias de aminoácidos 1-137 .
40. 494 de SEC ID Nº 1, respectivamente.
7. El compuesto inmunoadyuvante según una cualquiera de las reivindicaciones 2 a 6, en el que dicho péptido del extremo N-terminal y dicho péptido del extremo C-terminal están directamente ligados, el uno con el otro, mediante una cadena espaciadora intermedia que consiste en una secuencia de péptidos NH2-Gly-Ala-Ala-Gly-COOH.
8. Un compuesto inmunoadyuvante que comprende:
a) un péptido del extremo N-terminal que tiene al menos el 90 % de identidad de aminoácidos con la secuencia de aminoácidos que comienza en el residuo de aminoácido localizado en la posición 1 de SEC ID Nº 1 y que termina en un residuo de aminoácido seleccionado del grupo que consiste en uno cualquiera de los residuos de aminoácidos localizados en las posiciones 99 a 173 de SEC ID Nº 1; y
b) un péptido del extremo C-terminal que tiene al menos el 90 % de identidad de aminoácidos con la secuencia de aminoácidos que comienza en un residuo de aminoácido seleccionado del grupo que consiste en uno cualquiera de los residuos de aminoácidos localizados en las posiciones 401 a 406 de SEC ID Nº 1 y que termina en el residuo de aminoácido localizado en la posición 494 de SEC ID Nº 1, en el que:
- dicho péptido del extremo N-terminal está directamente ligado a dicho péptido del extremo C, o
- dicho péptido del extremo N-terminal y dicho péptido del extremo C-terminal están directamente ligados, el uno con el otro, mediante una cadena espaciadora, en el que la cadena espaciadora consiste en 1-20 aminoácidos ligados por enlaces peptídicos, en el que los aminoácidos están seleccionados de los 20 aminoácidos naturales
en el que el residuo de aminoácido asparagina localizado en la posición 488 de SEC ID Nº 1 está sustituido con una serina.
9. Un compuesto inmunoadyuvante según cualquier reivindicación precedente en el que dicho compuesto comprende un residuo de metionina adicional en el extremo N-terminal.
10. Una composición farmacéutica que comprende un compuesto inmunoadyuvante según una cualquiera de las reivindicaciones 1 a 9, junto con uno o más excipientes farmacéuticamente aceptables.
11. Una composición inmunogénica que comprende un compuesto inmunoadyuvante según una cualquiera de las reivindicaciones 1 a 9, junto con uno o más antígenos.
12. Una composición de vacuna que comprende un compuesto inmunoadyuvante según una cualquiera de las reivindicaciones 1 a 9, junto con uno o más antígenos.
13. La composición inmunogénica según la reivindicación 11 o la composición de vacuna según la reivindicación 12, en la que dicho compuesto inmunoadyuvante no está ligado covalentemente a dichos uno o más antígenos.
14. El compuesto inmunoadyuvante según una cualquiera de las reivindicaciones 1 a 9, para su uso como un medicamento.
15. El uso de un compuesto inmunoadyuvante según una cualquiera de las reivindicaciones 1 a 9, para fabricar una composición farmacéutica.
16. Un ácido nucleico que codifica el compuesto inmunoadyuvante según una cualquiera de las reivindicaciones 1 a 9.
17. Un vector recombinante que comprende, insertado en el mismo, el ácido nucleico de la reivindicación 16, el ácido nucleico codificando un compuesto inmunoadyuvante que comprende:
a) un péptido del extremo N-terminal que tiene al menos el 90 % de identidad de aminoácidos con la secuencia de aminoácidos que comienza en el residuo de aminoácido localizado en la posición 1 de SEC ID Nº 1 y que termina en un residuo de aminoácido seleccionado del grupo que consiste en uno cualquiera de los residuos de aminoácidos localizados en las posiciones 99 a 173 de SEC ID Nº 1; y
b) un péptido del extremo C-terminal que tiene al menos el 90 % de identidad de aminoácidos con la secuencia de aminoácidos que comienza en un residuo de aminoácido seleccionado del grupo que consiste en uno cualquiera de los residuos de aminoácidos localizados en las posiciones 401 a 406 de SEC ID Nº 1 y que termina en el residuo de aminoácido localizado en la posición 494 de SEC ID Nº 1, en el que:
- dicho péptido del extremo N-terminal está directamente ligado a dicho péptido del extremo C, o
- dicho péptido del extremo N-terminal y dicho péptido del extremo C-terminal están directamente ligados, el uno con el otro, mediante una cadena espaciadora, en el que la cadena espaciadora consiste en 1-20 aminoácidos ligados por enlaces peptídicos, en el que los aminoácidos están seleccionados de los 20 aminoácidos naturales.
18. Una célula huésped transfectada o transformada con el vector recombinante de la reivindicación 17 o con un ácido nucleico que codifica un compuesto inmunoadyuvante que comprende:
a) un péptido del extremo N-terminal que tiene al menos el 90 % de identidad de aminoácidos con la secuencia de aminoácidos que comienza en el residuo de aminoácido localizado en la posición 1 de SEC ID Nº 1 y que termina en un residuo de aminoácido seleccionado del grupo que consiste en uno cualquiera de los residuos de aminoácidos localizados en las posiciones 99 a 173 de SEC ID Nº 1; y
b) un péptido del extremo C-terminal que tiene al menos el 90 % de identidad de aminoácidos con la secuencia de aminoácidos que comienza en un residuo de aminoácido seleccionado del grupo que consiste en uno cualquiera de los residuos de aminoácidos localizados en las posiciones 401 a 406 de SEC ID Nº 1 y que termina en el residuo de aminoácido localizado en la posición 494 de SEC ID Nº 1, en el que:
- dicho péptido del extremo N-terminal está directamente ligado a dicho péptido del extremo C, o
- dicho péptido del extremo N-terminal y dicho péptido del extremo C-terminal están directamente ligados, el uno con el otro, mediante una cadena espaciadora, en el que la cadena espaciadora consiste en 1-20 aminoácidos ligados por enlaces peptídicos, en el que los aminoácidos están seleccionados de los 20 aminoácidos naturales.
Patentes similares o relacionadas:
Vacunas de Salmonella no tifoidea, del 23 de Noviembre de 2016, de GSK Vaccines Institute for Global Health S.r.l: Un polipéptido inmunogénico que comprende o consiste en: (i) un polipéptido que es una OmpD de Salmonella no tifoidea, o un fragmento inmunogénico de la misma que tiene […]
Mutantes por deleción de la flagelina y métodos para su uso, del 22 de Junio de 2016, de VAXINNATE CORPORATION: Una secuencia de aminoácidos que tiene al menos 80,0% de identidad con la secuencia de aminoácidos contigua como se expone en SEQ ID NO: 29 (R3), […]
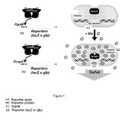 POLIPÉPTIDO MUTADO, CEPA DE BACTERIAS QUE LO COMPRENDE Y MÉTODOS PARA DETECTAR DIFERENTES CATIONES METÁLICOS SIMULTÁNEAMENTE, del 18 de Septiembre de 2014, de CONSEJO NACIONAL DE INVESTIGACIONES CIENTIFICAS Y TECNICAS (CONICET) (33.3%): Polipéptido mutado, cepas que lo comprende y métodos para detectar cationes metálicos, por ejemplo Au, Cu, Ag, Hg, Pb, Cd, Co y Zn, en muestras de manera simultánea, en […]
POLIPÉPTIDO MUTADO, CEPA DE BACTERIAS QUE LO COMPRENDE Y MÉTODOS PARA DETECTAR DIFERENTES CATIONES METÁLICOS SIMULTÁNEAMENTE, del 18 de Septiembre de 2014, de CONSEJO NACIONAL DE INVESTIGACIONES CIENTIFICAS Y TECNICAS (CONICET) (33.3%): Polipéptido mutado, cepas que lo comprende y métodos para detectar cationes metálicos, por ejemplo Au, Cu, Ag, Hg, Pb, Cd, Co y Zn, en muestras de manera simultánea, en […]
Nueva cepa de Salmonella enterica s. Typhimurium, su uso y un procedimiento para obtener un vector de vacuna terapéutico, del 22 de Noviembre de 2013, de UNIWERSYTET JAGIELLONSKI: Una cepa de Samonella enterica serovariedad Typhimurium VNP/sipB depositada en la Polish Collection of Microorganisms con el n.º de referencia B/00024.
 Toxinas bacterianas ADP-ribosilantes, del 25 de Abril de 2012, de NOVARTIS VACCINES AND DIAGNOSTICS S.R.L.: Una proteína que consiste en una secuencia de aminoácidos de SEC ID Nº: 1, excepto que la secuencia de aminoácidos contiene entre una y veinte mutaciones, en la que cada mutación […]
Toxinas bacterianas ADP-ribosilantes, del 25 de Abril de 2012, de NOVARTIS VACCINES AND DIAGNOSTICS S.R.L.: Una proteína que consiste en una secuencia de aminoácidos de SEC ID Nº: 1, excepto que la secuencia de aminoácidos contiene entre una y veinte mutaciones, en la que cada mutación […]
MUTANTES DE SPI2 DE SALMONELLA ATENUADA COMO PORTADORES DE ANTÍGENOS, del 13 de Abril de 2011, de EMERGENT PRODUCT DEVELOPMENT UK LIMITED: Célula de Salmonella atenuada que comprende el locus génico SPI2, en la que por lo menos un gen del locus SPI2 está inactivado, en la que dicha inactivación produce una […]
OLIGONUCLEOTIDOS PARA LA DETECCION DE SALMONELLA., del 1 de Diciembre de 2005, de INSTITUT PASTEUR INSTITUT NATIONAL DE LA SANTE ET DE LA RECHERCHE MEDICALE (INSERM): LA INVENCION SE REFIERE A NUEVOS MEDIOS, QUE COMPRENDEN SECUENCIAS DE NUCLEOTIDOS, PARA LA DETECCION, PARTICULARMENTE TRAS LA AMPLIFICACION, DEL ADN O DEL ADNC DE […]
 OLIGONUCLEÓTIDOS PARA LA DETECCIÓN DE SALMONELLA, del 3 de Junio de 2011, de INSTITUT PASTEUR INSTITUT NATIONAL DE LA SANTE ET DE LA RECHERCHE MEDICALE (INSERM): Par de cebadores oligonucleotídicos caracterizado porque consiste en dos oligonucleótidos de por lo menos 9 nucleótidos que hibridan en condiciones astringentes con la […]
OLIGONUCLEÓTIDOS PARA LA DETECCIÓN DE SALMONELLA, del 3 de Junio de 2011, de INSTITUT PASTEUR INSTITUT NATIONAL DE LA SANTE ET DE LA RECHERCHE MEDICALE (INSERM): Par de cebadores oligonucleotídicos caracterizado porque consiste en dos oligonucleótidos de por lo menos 9 nucleótidos que hibridan en condiciones astringentes con la […]