Monitorización del difosfato de adenosina.
Molécula fijadora de ADP que comprende un polipéptido, en donde dicho polipéptido comprende una secuencia de aminoácidos que corresponde a al menos los aminoácidos 11 a 310 de SEQ ID n.
º 1, en donde dicho polipéptido comprende una sustitución respecto a la SEQ ID n.º 1 en el aminoácido C287, y en donde dicho polipéptido comprende un resto de cisteína adicional para la conexión de al menos un resto indicador, y en donde dicho polipéptido tiene una identidad de secuencia de al menos el 68% con la SEQ ID n.º 1 en los restos de aminoácidos presentes en dicho polipéptido que corresponden a los mostrados en la columna III de la tabla A.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/GB2009/002208.
Solicitante: MEDICAL RESEARCH COUNCIL.
Nacionalidad solicitante: Reino Unido.
Dirección: 2nd Floor, David Phillips BuildingPolaris House, North Star Avenue Swindon, SN2 1FL REINO UNIDO.
Inventor/es: WEBB,Martin,Ronald, KUNZELMANN,SIMONE.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07K14/245 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › Escherichia (G).
- G01N33/573 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › para enzimas o isoenzimas.
PDF original: ES-2394156_T3.pdf
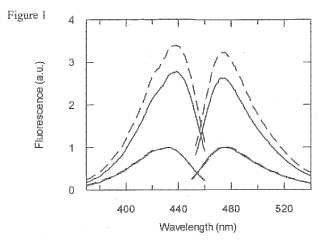
Fragmento de la descripción:
Monitorización del difosfato de adenosina
Campo de la invención La invención está en el campo de la monitorización del difosfato de adenosina (ADP) . En particular, la invención se refiere a moléculas fijadoras de ADP que comprenden polipéptidos de la proteína bacteriana ParM y uno o más fluoróforos.
Antecedentes de la invención La conversión del trifosfato de adenosina (ATP) en ADP es un proceso central en todos los organismos vivos y está catalizado por un gran número de enzimas diferentes. La energía generada por la hidrólisis del ATP puede impulsar procesos metabólicos, dirigir el transporte, generar fuerza y el movimiento, así como la transducción de señales y la regulación. Las cinasas transfieren el fosfato terminal del ATP, con la generación de ADP como producto, y fosforilan una amplia gama de sustratos, desde intermedios metabólicos a proteínas, con lo que controlan su actividad. Por consiguiente, los ensayos para monitorizar la concentración de ADP tienen aplicaciones amplias en la investigación bioquímica y biomédica, que oscila desde el conocimiento detallado del acoplamiento mecanoquímico en las proteínas motoras al escrutinio de inhibidores de ATPasas y de cinasas.
A pesar de la importancia de la detección del ADP en los sistemas biológicos, hasta la fecha se dispone sólo de unos pocos procedimientos para monitorizar la concentración de ADP. El que se aplica con más frecuencia es un ensayo enzimático acoplado que utiliza la piruvato cinasa y la lactato deshidrogenasa, que acopla la generación de ADP a la oxidación de NADH y una disminución concomitante de la fluorescencia o de la absorbancia. Aunque se utiliza con frecuencia para estudiar la cinética en equilibrio estacionario de las ATPasas y de las cinasas, esta estrategia generalmente no es la idónea para los estudios mecanísticos basados en cinéticas transitorias porque no proporciona una respuesta rápida ni es muy sensible, que son los inconvenientes de este sistema. También resulta problemático el hecho de que en el ensayo tengan que estar presentes varios componentes, pues le añade complejidad y lo encarece, en especial en las aplicaciones de alto rendimiento. Algunos compuestos pueden interferir con uno de los componentes del ensayo y/o con la detección UV. Al contar con un gran número de componentes, los riesgos de tales problemas de interferencia son, en consecuencia, grandes.
Recientemente se ha modificado el ensayo para generar fluorescencia al acoplar la reacción de la piruvato cinasa con la piruvato oxidasa y la peroxidasa de rábano picante (1) . El rojo de Amplex® se convierte en resorrufina gracias a la peroxidasa, lo que hace incrementar la fluorescencia a 590 nm. La detección de la fluorescencia a una longitud de onda larga proporciona mejoras, tanto por realzar la sensibilidad como por distinguir entre la señal óptica y la absorbancia de muchos compuestos. Sin embargo, este ensayo no soslaya el problema de la interferencia con alguno de los muchos componentes del ensayo. Además, el ensayo es todavía un ensayo enzimático acoplado que impone requisitos al sistema para que puedan tener lugar las diferentes actividades enzimáticas requeridas, e implica la presencia numerosos compuestos interdependientes en el ensayo, que siguen siendo fuente de problemas incluso con esta versión mejorada.
Con el fin de desarrollar ensayos de alto rendimiento para cinasas, se han descrito dos detectores específicos de ADP, que se basan en el reconocimiento del ADP mediante moléculas de ARN (2) . El primero se basa en un aptámero de ARN que se fija selectivamente al ADP y se puede utilizar para monitorizar la generación de ADP en un ensayo de proximidad de centelleo (radiométrico) . Aunque este procedimiento puede utilizarse para mediciones en tiempo real, se trata de nuevo de un sistema con varios componentes y complejo, e implica el centelleo radiométrico, que es peligroso y caro. El segundo detector crea una lectura de fluorescencia basada en la autoescisión, dependiente de ADP, de una ribozima marcada con fluorescencia. Este procedimiento no puede utilizase para mediciones en tiempo real, lo cual es un obstáculo.
Un procedimiento alternativo es aprovecharse de la interacción muy específica de una proteína fijadora con la molécula diana. Al conectar un fluoróforo a una posición adecuada en la proteína, el reconocimiento del ligando se puede acoplar a una señal óptica. Se ha descrito que una serie de biomoléculas, tales como azúcares, aminoácidos, iones metálicos y fosfato, pueden formar parte de tales biosensores fluorescentes proteicos (3-7) . Una ventaja de este tipo de detector es que el cambio de señal puede ser muy rápido y verse sólo limitado por la velocidad de la fijación del ligando o del cambio conformacional asociado. Además, para la detección sólo se necesita un único componente, la proteína marcada, por lo que también se clasifican como biosensores sin reactivos. Tal biosensor para ADP ya había sido desarrollado con anterioridad, basándose en una nucleósido difosfato cinasa marcada con el colorante de cumarina IDCC (8) . El biosensor responde a la proporción de concentración de ADP/ATP y, por lo tanto, puede detectar un intervalo amplio de concentraciones de ADP, desde submicromolares a milimolares. Sin embargo, la fluorescencia disminuye con el ADP y esto es desfavorable. Además, la disminución de la fluorescencia al fijarse el ADP hace que la sensibilidad sea baja, en particular cuando se miden velocidades iniciales, lo cual es un problema. Además, la intensidad de la fluorescencia no es linealmente dependiente de la concentración de ADP, lo cual es un inconveniente de este sistema.
La presente invención busca solventar el (los) problema (s) asociado (s) con la técnica anterior.
Compendio de la invención En la técnica se conocen proteínas que detectan fosfatos. Típicamente, la técnica anterior se ha centrado en la fijación del fosfato inorgánico (Pi) . Para este fin, las proteínas detectoras de la técnica anterior se han basado en proteínas fijadoras de fosfato.
Los presentes inventores han tomado una estrategia muy diferente. Han tomado sorprendentemente una proteína del campo del reparto de plásmidos bacterianos y la han modificado genéticamente para utilizarla como detector de ADP. Esto ha requerido una gran dedicación técnica, ya que la proteína en la cual se basan las proteínas detectoras de ADP de la invención (ParM) tiene actividad ATPasa intrínseca, y se sabe que se le fijan nucleótidos de guanina así como ADP. A pesar de la aparente falta de idoneidad de esta proteína para el uso como una molécula detectora de ADP, los inventores han creado con éxito un detector robusto, sin reactivos, para el ADP.
La invención da a conocer numerosos beneficios técnicos. Estos incluyen evitar los detectores basados en ácidos nucleicos, tales como las ribozimas. Aún más, al centrarse en el ADP en vez de en el fosfato inorgánico (Pi) , se ensaya una molécula de mayor relevancia biológica. Además, al monitorizar el ADP en vez de la Pi, las moléculas de la invención encuentran aplicación en un abanico de ensayos que de hecho no generan Pi. Un ejemplo importante es, por supuesto, la aplicación a la monitorización de ensayos de cinasas, en los que el fosfato seincorpora en el sustrato diana en vez de ser liberado como Pi. Éstas y otras ventajas de la invención se discuten con más detalle más adelante.
En un aspecto, la invención se refiere a una molécula fijadora de ADP que comprende un polipéptido, y dicho polipéptido comprende una secuencia de aminoácidos que corresponde a al menos los aminoácidos 11 a 310 de la SEQ ID n.º 1, en donde dicho polipéptido comprende una sustitución respecto a la SEQ ID n.º 1 en el aminoácido C287, y en donde dicho polipéptido comprende otro resto de cisteína para la conexión de al menos un resto indicador, y en donde dicho polipéptido tiene al menos una identidad de secuencia del 68% con la SEQ ID n.º 1 en los restos aminoacídicos presentes en dicho polipéptido que corresponden a los mostrados en la columna III de la tabla A. Convenientemente, dicho polipéptido puede comprender una o más sustituciones respecto a la SEQ ID n.º 1 en uno o más restos de aminoácidos seleccionados entre D6, G8, S9, T10, K13, N69, T101, E148, D170, G172, G173, T174, T175, D177, D223, I227, E284 o Q308.
En otro aspecto, la invención se refiere a una molécula fijadora de ADP como la descrita más arriba, en donde dicho polipéptido comprende una sustitución o sustituciones seleccionadas entre:
(i) I27C; o
(ii) D63C y K216C; o
(iii) D63C y D224C.
En otro aspecto, la invención da a conocer una molécula fijadora de ADP que comprende un polipéptido,... [Seguir leyendo]
Reivindicaciones:
1. Molécula fijadora de ADP que comprende un polipéptido, en donde dicho polipéptido comprende una secuencia de aminoácidos que corresponde a al menos los aminoácidos 11 a 310 de SEQ ID n.º 1, en donde dicho polipéptido comprende una sustitución respecto a la SEQ ID n.º 1 en el aminoácido C287, y en donde dicho polipéptido comprende un resto de cisteína adicional para la conexión de al menos un resto indicador, y en donde dicho polipéptido tiene una identidad de secuencia de al menos el 68% con la SEQ ID n.º 1 en los restos de aminoácidos presentes en dicho polipéptido que corresponden a los mostrados en la columna III de la tabla A.
2. Molécula fijadora de ADP de acuerdo con la reivindicación 1, en donde dicho polipéptido comprende una o más sustituciones respecto a la SEQ ID n.º 1 en uno o más restos de aminoácidos seleccionados entre D6, G8, S9, T10, K13, N69, T101, E148, D170, G172, G173, T174, T175, D177, D223, I227, E284 o Q308.
3. Molécula fijadora de ADP de acuerdo con la reivindicación 1 o la reivindicación 2, en donde dicho polipéptido comprende una sustitución o sustituciones seleccionadas entre:
(i) I27C; o
(ii) D63C y K216C; o
(iii) D63C y D224C.
4. Molécula fijadora de ADP de acuerdo con la reivindicación 3, en donde dicho polipéptido comprende una sustitución o sustituciones adicionales seleccionadas entre:
(iv) T175N; o
(v) T174A y T175A; o
(vi) T174A y T175N; o
(vii) T175L.
5. Molécula fijadora de ADP de acuerdo con la reivindicación 4, en donde dicho polipéptido comprende una sustitución o sustituciones adicionales seleccionadas entre:
(iv) T175N; o
(v) T174A y T175A; o
(vi) T174A y T175N.
6. Molécula fijadora de ADP de acuerdo con una cualquiera de las reivindicaciones anteriores, en donde dicho polipéptido comprende una sustitución adicional de K33A.
7. Molécula fijadora de ADP de acuerdo con una cualquiera de las reivindicaciones anteriores, que además comprende al menos un fluoróforo conectado a ésta, en donde dicho fluoróforo está conectado a una posición en el polipéptido de tal forma que el cambio conformacional del polipéptido tras la fijación del ADP ocasiona un cambio correspondiente en la fluorescencia de dicho fluoróforo.
8. Molécula fijadora de ADP de acuerdo con la reivindicación 7, en donde el o cada fluoróforo está conectado al polipéptido a través de un resto de aminoácido que corresponde a uno o más de I27C, D63C, K216C o D224C.
9. Molécula fijadora de ADP de acuerdo con una cualquiera de las reivindicaciones anteriores, en donde dicha molécula comprende adicionalmente al menos un resto N-[2- (1-maleimidil) etil]-7-dietilaminocumarin-3-carboxamida (MDCC) conectado a ésta.
10. Molécula fijadora de ADP de acuerdo con una cualquiera de las reivindicaciones anteriores, en donde dicha molécula comprende adicionalmente al menos dos restos 5-yodoacetamidotetrametilrodamina (5-IATR) conectados a ésta.
11. Molécula fijadora de ADP de acuerdo con una cualquiera de las reivindicaciones 1 a 10, en donde dicha molécula comprende la secuencia de aminoácidos de SEQ ID n.º 5.
12. Molécula fijadora de ADP de acuerdo con una cualquiera de las reivindicaciones 1 a 10, en donde dicha molécula comprende la secuencia de aminoácidos de SEQ ID n.º 6 o SEQ ID n.º 7.
13. Ácido nucleico que tiene una secuencia de nucleótidos que codifica la porción polipeptídica de una molécula fijadora de ADP de acuerdo con una cualquiera de las reivindicaciones 1 a 12.
14. Procedimiento para monitorizar los cambios de la concentración de ADP de una muestra, que comprende poner en contacto dicha muestra con una molécula fijadora de ADP de acuerdo con una cualquiera de las reivindicaciones 1 a 12 y determinar los cambios de conformación de dicha molécula fijadora de ADP, en donde los cambios de conformación de dicha molécula fijadora de ADP indican cambios de la concentración de ADP en dicha muestra.
15. Procedimiento de acuerdo con la reivindicación 14, en donde la conformación de dicha molécula fijadora de ADP se monitoriza mediante la medición de cambios de fluorescencia de un fluoróforo comprendido por dicha molécula fijadora de ADP.
Patentes similares o relacionadas:
PTPRS y proteoglicanos en enfermedad autoinmune, del 15 de Julio de 2020, de LA JOLLA INSTITUTE FOR ALLERGY AND IMMUNOLOGY: Una proteína recombinante no enzimática que comprende una secuencia de aminoácidos de un dominio extracelular de PTPRS, donde la proteína comprende tanto el dominio 1 (Ig1) […]
Deshidrogenasa y toxina de Clostridium difficile como un biomarcador, del 18 de Diciembre de 2019, de TECHLAB, INC.: Un método para medir una cantidad de C. difficile en una muestra fecal, el método que comprende: medir cuantitativamente un nivel de lactoferrina, […]
Ensayos de actividad de endopeptidasa redirigida basados en inmunología, del 2 de Octubre de 2019, de ALLERGAN, INC.: Método para detectar actividad endopeptidasa redirigida, comprendiendo el método las etapas de: a) tratar una célula de una línea celular establecida […]
Uso de neuregulina-4 para el tratamiento de la enfermedad inflamatoria intestinal y la enterocolitis necrotizante, del 3 de Julio de 2019, de Children's Hospital Los Angeles: Composicion que comprende Neuregulina-4 o un equivalente farmaceutico, analogo, derivado o una sal de la misma para usar en el tratamiento de la enfermedad […]
Composiciones y métodos relacionados con la argininosuccinato sintetasa, del 5 de Junio de 2019, de Bioregency, Inc: Una cantidad terapéuticamente eficaz de argininosuccinato sintetasa para uso en un método para tratar la exposición de un sujeto a una endotoxina bacteriana.
Composiciones y procedimientos que comprenden variantes de splicing de histidil-tarn sintetasa que tienen actividades biológicas no canónicas, del 15 de Mayo de 2019, de Pangu Biopharma Limited: Una composición para uso en el tratamiento del cáncer que comprende un vehículo fisiológicamente aceptable y un anticuerpo o fragmento de unión a antígenos del mismo […]
Método para la prueba de disolución de composiciones sólidas que contienen enzimas digestivas, del 8 de Mayo de 2019, de Allergan Pharmaceuticals International Limited: Un proceso para medir una cantidad de enzimas digestivas liberadas de una composición sólida de pancrelipasa en un medio de disolución que comprende utilizar espectroscopía […]
Anticuerpos dirigidos contra metaloproteinasa 9 de matriz, del 17 de Abril de 2019, de Gilead Biologics, Inc: Un anticuerpo aislado o fragmento del mismo que se une específicamente a MMP9, que comprende una región variable de cadena pesada (VH) y una […]