Modulación de receptores de catecolaminas.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/IL2007/000741.
Solicitante: YEDA RESEARCH AND DEVELOPMENT CO. LTD..
Nacionalidad solicitante: Israel.
Dirección: THE WEIZMANN INSTITUTE OF SCIENCE P.O. BOX 95 76100 REHOVOT ISRAEL.
Inventor/es: RUBINSTEIN, MENACHEM, LAPIDOT, TSVEE, SPIEGEL,ASAF, KALINKOVICH,ALEXANDER, SHIVTIEL,SHOHAM.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K33/00 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › Preparaciones medicinales que contienen ingredientes activos inorgánicos.
- A61K35/00 A61K […] › Preparaciones medicinales que contienen sustancias de constitución indeterminada o sus productos de reacción.
- C12N5/0789 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 5/00 Células no diferenciadas humanas, animales o vegetales, p. ej. líneas celulares; Tejidos; Su cultivo o conservación; Medios de cultivo para este fin (reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00). › Células madre; Células progenitoras multipotentes.
PDF original: ES-2418433_T3.pdf
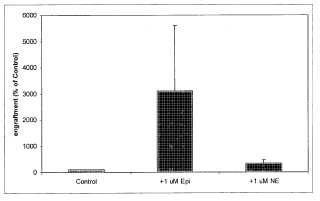
Fragmento de la descripción:
Modulación de receptores de catecolaminas Campo de la invención La invención se refiere a 7-hidroxi-2-dipropilaminotetralina (7-OH-DPAT) de uso para el tratamiento de una patología hematopoyética mediante terapia de trasplante de células pluripotenciales hematopoyéticas Antecedentes de la invención El trasplante de médula ósea (BMT) o el trasplante de células pluripotenciales hematopoyéticas (HSCT) es un procedimiento médico existente en el campo de la hematología y la oncología que lleva consigo el trasplante de células pluripotenciales hematopoyéticas (HSC) . El BMT y el HSCT se emplean con la mayor frecuencia para el tratamiento de pacientes aquejados de enfermedades de la sangre o de la médula ósea, o de ciertos tipos de cáncer. El objetivo del trasplante, BMT o HSCT, es dotar al paciente con una población de células pluripotenciales sanas que puedan diferenciarse en células sanguíneas maduras que reemplacen los linajes celulares deficientes o patológicos Las células pluripotenciales hematopoyéticas constituyen una población poco común de células del interior del microambiente de la médula ósea. Las células pluripotenciales hematopoyéticas mantienen activamente la producción continua de todos los linajes de células sanguíneas maduras, que comprenden los componentes principales del sistema inmunitario tales como los linfocitos T y B, durante toda la vida, al tiempo que mantienen una pequeña asociación de células pluripotenciales y células progenitoras sin diferenciar (Mayani, 2003) .
En el caso de un trasplante de médula ósea (BMT) , las HSC son separadas de un hueso largo del donante, típicamente la pelvis, por medio de una aguja larga que alcanza el centro del hueso. Esta técnica se conoce como una recolección de médula ósea y se lleva a cabo bajo anestesia general debido a que, literalmente, se requieren cientos de inserciones de la aguja para obtener suficiente material.
Las células pluripotenciales de sangre periférica (PBSC) son actualmente el origen más común de células pluripotenciales para el trasplante de células pluripotenciales hematopoyéticas. Las PBSC se recogen desde la sangre mediante un procedimiento conocido como aféresis. El rendimiento de células pluripotenciales periféricas se refuerza con inyecciones subcutáneas diarias de factor estimulante de colonias de granulocitos (G-CSF) .
Otro origen de células pluripotenciales es la sangre procedente de cordón umbilical. La sangre de cordón posee una concentración de HSC mayor que la que se encuentra normalmente en la sangre adulta. Sin embargo, la pequeña cantidad de sangre que puede obtenerse de un cordón umbilical (típicamente, unos 50 ml) hace que este origen sea menos adecuado para el trasplante en adultos. Técnicas más nuevas que utilizan expansión ex-vivo de unidades de sangre de cordón o el uso de 2 unidades de sangre de cordón procedente de donantes diferentes, están siendo exploradas para facilitar los trasplantes de sangre de cordón en adultos.
Durante el desarrollo, o en el trasplante experimental y clínico, las células pluripotenciales emigran por medio de la circulación de la sangre y se implantan en la médula ósea (BM) , repoblándola con células sanguíneas inmaduras y madurando en células sanguíneas mieloides y linfoides, que a su vez son liberadas a la circulación sanguínea El proceso de implantación y repoblación de células pluripotenciales hematopoyéticas, que es crucial para la función de las células pluripotenciales y el desarrollo del sistema inmunitario, no está bien comprendido.
Con objeto de estudiar los procesos de implantación y repoblación de células pluripotenciales hematopoyéticas, varios grupos han establecido in vivo modelos que incluyen el injerto (la incorporación de tejido o células injertadas en el cuerpo del hospedador) de células pluripotenciales humanas en ratones deficientes de sistema inmunitario tales como ratones irradiados, beige, desprovistos de sistema inmunitario, Xid (inmunodeficiencia ligada a X) , SCID y SCID diabéticos, no obesos (NOD/SCID) , y en trasplantes de útero en fetos de oveja, que han dado por resultado el injerto con éxito de multilinajes de ambos tipos de células, células mieloides y células linfoides (McCune et al., 1988; Nolta et al., 1994; Lapidot et al., 1992; Larochelle et al., 1996; Civin et al., 1996) .
Los presentes inventores han desarrollado un ensayo funcional in vivo de repoblación de ratones SCID con células humanas primitivas (SRCs) basado en su capacidad para repoblar de modo duradero la médula ósea de ratones SCID o NOD/SCID trasplantados por vía intravenosa con niveles elevados de células mieloides y linfoides (Lapidot et al., 1992; Larochelle et al., 1996) . Experimentos cinéticos han demostrado que solamente una pequeña fracción de las células trasplantadas se había injertado y que estas células habían repoblado la médula ósea murina mediante proliferación extensa y diferenciación. Además. las células humanas primitivas habían retenido también la capacidad de injertar receptores murinos secundarios (Cashman et al., 1997) . El trasplante de poblaciones enriquecidas para expresar el antígeno de superficie de células CD34 y CD38, reveló que el fenotipo de SRC es CD34+CD38- (Larochelle et al., 1996) Pueden existir otras células de repoblación, dado que otros estudios realizados sugieren que células CD34- humanas, inmaduras, y células CD34+CD38+ más diferenciadas, tienen potencial de injerto algo limitado (Zanjani et al., 1998; Conneally et al., 1997)
Se ha encontrado que la implantación de células pluripotenciales humanas y su proliferación y diferenciación subsiguiente en ratones inmunodeficientes trasplantados, dependía de interacciones entre el factor uno derivado estromal de quimioquina (SDF-1) , que es expresado por la médula ósea del hospedador, y su receptor CXCR4, que es expresado en las células de alojamiento del donante. La interferencia con interacciones de SDF-1/CXCR4 por tratamiento previo de células CD34+ humanas, inmaduras, con anticuerpo anti CXCR4 neutralizante, bloqueaba su implantación y repoblación in vivo, mientras que las células sin tratar podían implantarse al cabo de horas en la médula ósea de ratones receptores [Peled et al., 1999 (a) ].
Se ha encontrado que el aumento de la expresión de CXCR4 en la superficie celular de células pluripotenciales, por estimulación de citoquinas, intensificaba la respuesta a SDF-1 de esas células, manifestada por la mejora de la implantación e injerto. Las células CD34+ humanas, inmaduras, que no expresan CXCR4 de la superficie celular contienen CXCR4 interior, que puede oscilar in vivo después del trasplante. La prevención de esta regulación en alza de CXCR4 de la superficie celular bloqueaba los bajos niveles de injerto de las células CD34+CXCR4-humanas. Así pues, el fenotipo de las células pluripotenciales humanas de repoblación se definió como células CD34+CD38/bajoCXCR4+ (Kollet et al., 2002) ..
El SDF-1 (denominado también CXCL12) es producido por muchos tipos de células que comprenden células estromales y endoteliales de médula ósea, y como se ha indicado, es un quimioatractivo potente de células hematopoyéticas inmaduras y maduras, y regula el trafico de leucocitos en la homeostasia en estado estacionario. El SDF-1 sirve de factor de supervivencia de células pluripotenciales y progenitoras, y está implicado en el desarrollo de células B inmaduras y en el desarrollo de megacariocitos (McGrath et al., 1999; Nagasawa et al., 1996) . El SDF-1 está altamente preservado a través de toda la evolución. Por ejemplo, el SDF-1 humano y del ratón son de reacción cruzada y se diferencian solamente en un aminoácido.
La liberación y movilización de células pluripotenciales desde la médula ósea hacia la circulación se inducen para el trasplante clínico. Se emplean estimulaciones múltiples con citoquinas tales como la G-CSF, para reclutar células pluripotenciales humanas desde la circulación. Se encontró que la interacción de SDF-1/CXCR4 dentro de la médula ósea después de la administración de G-CSF, estaba implicada en el proceso de movilización (Petit et al., 2002) .
Se ha encontrado que las enzimas proteolíticas tales como la neutrófilo-elastasa degradaban el SDF-1 en la médula ósea durante la administración de G-CSF. En paralelo, se descubrió que los niveles de expresión de CXCR4 en células hematopoyéticas dentro de la médula ósea, aumentan antes de su movilización. La neutralización con anticuerpo de CXCR4 o SDF-1 reducía la movilización de células pluripotenciales humanas y del ratón, lo que demuestra señalización de SDF-1/CXCR4 en la salida de células (Petit et al., 2002) .
Por tanto, la implantación y la... [Seguir leyendo]
Reivindicaciones:
1. Uso de 7-hidroxi-2-dipropilaminotetralina (7-OH-DPAT) en la fabricación de un medicamento para tratar una patología hematopoyética mediante terapia de trasplante de células pluripotenciales hematopoyéticas (HSCT) .
2. El uso según la reivindicación 1, en donde se usa 7-OH-DPAT en combinación con una citoquina mieloide o un 5 vector de expresión que codifica un receptor de catecolaminas.
3. El uso según la reivindicación 1 ó 2, en donde el trasplante de células pluripotenciales hematopoyéticas (HSCT) es para la repoblación de linajes de células sanguíneas maduras,
4. El uso según cualquiera de las reivindicaciones 1 a 3, en donde el medicamento es para administración ex vivo a las células pluripotenciales antes del trasplante, aumentando con ello la migración, capacidad de injerto y/o proliferación de las células pluripotenciales.
5. El uso según la reivindicación 4, en donde las células pluripotenciales proceden de un donante tratado con G-CSF.
6. El uso según cualquiera de las reivindicaciones 2 a 5, en donde la citoquina mieloide es GM-CSF y/o G-CSF.
7. El uso según cualquiera de las reivindicaciones 1 a 3, en donde el medicamento es para administración in vivo a un donante sano o a un paciente sometido a terapia de cáncer, aumentando con ello la movilización de células pluripotenciales desde la médula ósea y otros tejidos, hacia la sangre, y facilitando la recogida de células pluripotenciales desde la sangre para el trasplante.
8. 7-Hidroxi-2-dipropilaminotetralina (7-OH-DPAT) para uso en el tratamiento de una patología hematopoyética, mediante terapia de trasplante de células pluripotenciales hematopoyéticas (HSCT) .
9. 7-OH-DPAT para el uso según la reivindicación 8, en donde se combina 7-OH-DPAT con una citoquina mieloide o un vector de expresión que codifica el receptor de catecolaminas.
10. 7-OH-DPAT para el uso según la reivindicación 8 ó 9, en donde el trasplante de células pluripotenciales hematopoyéticas (HSCT) es para la repoblación de linajes de células sanguíneas maduras.
11. 7-OH-DPAT para el uso según cualquiera de las reivindicaciones 8 a 10, en donde la 7-OH-DPAT es para administración ex vivo a las células pluripotenciales antes del trasplante, aumentando con ello la migración, capacidad de injerto y/o proliferación de las células pluripotenciales.
12. 7-OH-DPAT para el uso según cualquiera de las reivindicaciones 8 a 11, en donde la citoquina mieloide es GM-CSF y/o G-CSF.
13. 7-OH-DPAT para el uso según cualquiera de las reivindicaciones 8 a 10, en donde la 7-OH-DPAT es para administración in vivo a un donante sano o a un paciente sometido a terapia de cáncer, aumentando con ello la movilización de células pluripotenciales desde la médula ósea y otros tejidos, hacia la sangre, y facilitando la recogida de células pluripotenciales desde la sangre para el trasplante .
Patentes similares o relacionadas:
Conjugados de ligadores (ADCs) con inhibidores de KSP, del 24 de Junio de 2020, de Bayer Pharma Aktiengesellschaft: Conjugado de un ligador o un derivado del mismo con una o varias moléculas de principio activo, en donde la molécula de principio activo es un inhibidor de la proteína del huso […]
Actividad antitumoral de inhibidores de multicinasas en cáncer colorrectal, del 10 de Junio de 2020, de ENTRECHEM, S.L: Composición para uso en la prevención y/o el tratamiento de cáncer colorrectal en un paciente, que comprende: a) un compuesto de fórmula (I) **(Ver fórmula)** […]
Bacterias mutantes para la producción de módulos generalizados para antígenos de membrana, del 13 de Mayo de 2020, de GLAXOSMITHKLINE BIOLOGICALS SA: Un procedimiento para preparar vesículas a partir de una bacteria gramnegativa en el que al menos una proteína que contiene un dominio catalítico LytM se inactiva […]
Polipéptidos biespecíficos de unión a antígeno, del 29 de Abril de 2020, de X-Body, Inc: Un polipéptido biespecífico de unión a antígeno aislado desprovisto de cadenas ligeras de anticuerpo que comprende una cadena pesada de anticuerpo […]
Cepas termoestables, productos y métodos de las mismas, del 29 de Abril de 2020, de Triphase Pharmaceuticals Pvt. Ltd: Un producto alimenticio que comprende un microorganismo termoestable de Lactobacillus, en donde el microorganismo termoestable se selecciona […]
Terapias dirigidas a CD47 para el tratamiento de enfermedades infecciosas, del 25 de Marzo de 2020, de THE BOARD OF TRUSTEES OF THE LELAND STANFORD JUNIOR UNIVERSITY: Una composición para su uso en un método para tratar a un sujeto mamífero por infección por virus hepadna, el método comprendiendo: administrar al sujeto de un […]
Receptores de antígeno quimérico dirigidos a mesotelina y usos de los mismos, del 26 de Febrero de 2020, de The United States Of America, As Represented By The Secretary, Department Of Health And Human Services (100.0%): Receptor de antígeno quimérico (CAR), que comprende un dominio de unión a antígeno extracelular, un dominio transmembrana y un dominio intracelular, en el que el dominio de unión […]
Composición y productos que comprenden células senescentes para su uso en la regeneración de tejidos, del 8 de Enero de 2020, de QRSKIN GmbH: Una composición que comprende un componente celular, en la que el componente celular incluye un tipo de célula senescente o una combinación de tipos de células […]