Intervenciones de urgencia de carbón vegetal activo con sobredosificación con etexilato de dabigatrán.
opcionalmente en la forma de sus sales farmacéuticamente aceptables.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2010/062229.
Solicitante: BOEHRINGER INGELHEIM INTERNATIONAL GMBH.
Nacionalidad solicitante: Alemania.
Dirección: BINGER STRASSE 173 55216 INGELHEIM AM RHEIN ALEMANIA.
Inventor/es: VAN RYN,JOANNE, CLEMENS,ANDREAS.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K33/44 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 33/00 Preparaciones medicinales que contienen ingredientes activos inorgánicos. › Carbono elemental, p. ej. carbón de madera, negro de carbón.
- A61P39/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Protectores generales o productos antitóxicos.
- A61P39/02 A61P […] › A61P 39/00 Protectores generales o productos antitóxicos. › Antídotos.
PDF original: ES-2436076_T3.pdf
Fragmento de la descripción:
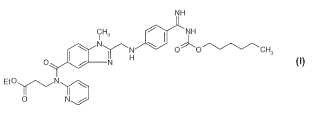
Intervenciones de urgencia de carbón vegetal activo con sobredosificación con etexilato de dabigatrán La invención se refiere a un carbón vegetal para uso en el tratamiento de una sobredosificación con la sustancia activa etexilato de dabigatrán de fórmula I
NH
NH
CH3
N
CH3
N OO
H
O
N
NEtO
ON I opcionalmente en forma de sus sales farmacéuticamente aceptables.
Antecedentes de la invención El compuesto de fórmula I se conoce de la técnica anterior y se describió por primera vez en el documento WO98/37075. Dicho compuesto es un potente inhibidor de la trombina que se puede usar, por ejemplo, en la prevención posoperatoria de trombosis venosa profunda y en la prevención de apoplejías, particularmente para evitar apoplejías en pacientes con fibrilación auricular. El documento WO 03/074056 describe la sal de adición del ácido metanosulfónico del etexilato de dabigatrán (es decir: metanosulfonato de etexilato de dabigatrán) por ser particularmente útil.
El compuesto se administra normalmente por vía oral. En particular, se pueden usar las llamadas formulaciones en pellas, como se describe, por ejemplo, en el documento WO 03/074056. Estas formulaciones son composiciones en las que una capa de sustancia activa que contiene aglutinante y opcionalmente agente separador se aplica a un material nuclear sustancialmente esférico que consiste en o contiene un ácido orgánico farmacéuticamente aceptable. La capa nuclear y la capa de sustancia activa están separadas la una de la otra por una llamada capa aislante. La estructura esquemática de una formulación de una sustancia activa de este tipo se muestra en la Figura 1 del documento WO 03/074056.
El etexilato de dabigatrán (I) es un profármaco, que se convierte rápidamente in vivo en el resto activo dabigatrán (compuesto de fórmula II) , un potente inhibidor directo de trombina. NH
es decir, el etexilato de dabigatrán sólo se convierte en el compuesto que es realmente eficaz, a saber dabigatrán, en el cuerpo.
Este fármaco se está probando actualmente con respecto a la prevención de la apoplejía en pacientes con fibrilación auricular (SPAF) y se administra durante períodos de tiempo más prolongados que el sustituto warfarina. Debido a 35 los riesgos de complicaciones hemorrágicas bajo un tratamiento crónico con anticoagulantes, existe una necesidad de una neutralización de urgencia del fármaco.
El objetivo de la presente invención es proporcionar un método adecuado para la neutralización de urgencia de etexilato de dabigatrán, en particular en caso de sobredosificación. 40 Descripción detallada de la invención
La presente invención se dirige a una posible solución del problema mencionado anteriormente.
La invención se refiere a un carbón vegetal para uso en el tratamiento de una sobredosificación con la sustancia activa etexilato de dabigatrán de fórmula I
NH
NHCH3
N
CH3H
N OO
O
N
NEtO ON
I
opcionalmente en forma de sus sales farmacéuticamente aceptables.
La invención se refiere a la neutralización de etexilato de dabigatrán en el estómago de un paciente, en el que una cantidad eficaz de carbón vegetal activo se administra oralmente a un paciente que lo necesite. La cantidad eficaz de carbón vegetal activo está habitualmente en un intervalo de 20 - 130 g, preferiblemente en el intervalo de 50 100g. La cantidad de carbón vegetal usada depende del grado de sobredosificación.
El etexilato de dabigatrán I es un doble profármaco de dabigatrán, el compuesto de Fórmula (II) NH
NH2
HO
II, es decir, el etexilato de dabigatrán I sólo se convierte en el compuesto que es realmente eficaz, a saber el dabigatrán II, en el cuerpo.
En otra realización, la invención se refiere a la neutralización de dabigatrán II en el plasma sanguíneo, comprendiendo el método la purificación del plasma sanguíneo del paciente sobre carbón vegetal activo. La absorción de dabigatrán II sobredosificado del plasma sanguíneo podría realizarse a través de hemoperfusión sobre un filtro de carbón vegetal.
El grado sorprendentemente alto de absorción de etexilato de dabigatrán y dabigatrán a carbón vegetal se verificó en el experimento descrito en la presente memoria posteriormente. En estos experimentos, la unión de etexilato de dabigatrán a carbón vegetal activo en agua simula la ingestión reciente (2-5, preferiblemente 2-3 h) de grandes cantidades de etexilato de dabigatrán en el fluido estomacal. La unión de dabigatrán a carbón vegetal activo en plasma simula situaciones en las que el dabigatrán se absorbía después de la ingestión y estaba presente en altas concentraciones en el plasma.
En la siguiente sección se describen un método para la fabricación de formas de dosificación de dabigatrán y la forma de dosificación así obtenida.
El procedimiento para la fabricación de las composiciones farmacéuticas usadas en las pruebas clínicas mencionadas se caracteriza por una serie de etapas parciales. En primer lugar, se produce el núcleo 1 a partir de un ácido orgánico farmacéuticamente aceptable. Dentro del ámbito de la presente invención, se usa ácido tartárico para preparar el núcleo 1. El material 1 nuclear así obtenido se convierte a continuación en los llamados núcleos 3 aislados de ácido tartárico mediante pulverización de una suspensión 2 de aislamiento. Sobre estos núcleos 3 revestidos se pulveriza una suspensión 4 de dabigatrán preparada posteriormente, por medio de un proceso de revestimiento en una o más etapas de proceso. Finalmente, las pellas 5 de sustancia activa así obtenidas se envuelven en cápsulas adecuadas.
Determinación de los tamaños de partícula de ácido tartárico mediante cribado a chorro de aire
Dispositivo y ajustes de medida: Dispositivo de medida: Tamiz a chorro de aire, por ejemplo, un Alpine A 200 LS Cribas: Las necesarias Peso utilizado: 10 g/criba Duración: 1 min/criba, luego 1 min cada hasta la pérdida máxima de peso de 0, 1 g
Preparación de la muestra / suministro del producto:
Se transfiere la sustancia a un mortero y se destruye cualquier grumo presente mediante machacado intensivo. Se coloca la criba, con tapa y cierre de caucho, en una balanza, se ajusta a cero y se pesan sobre la criba 10, 0 g de la sustancia pulverizada.
Se colocan en el dispositivo la criba junto con su contenido, la tapa y el cierre de caucho. Se pone el temporizador a 1 minuto y se trata el material mediante cribado a chorro de aire durante este tiempo. A continuación, se pesa el residuo y se anota el resultado. Este proceso se repite hasta que la disminución en el peso del residuo después del cribado a chorro de aire sea < 0, 1 g.
Ejemplo 1 - Preparación de las Pellas Iniciales Se calientan 480 kg de agua a una temperatura de 50ºC y se añaden con agitación 120 kg de acacia (goma arábiga) en un envase de mezcla convencional equipado con un plato y un agitador. Se continúa la agitación a temperatura constante hasta obtener una disolución transparente. Una vez que se tiene una disolución transparente (normalmente después de 1 ó 2 horas) se añaden con agitación 600 kg de ácido tartárico. El ácido tartárico se añade a temperatura constante al mismo tiempo que se continúa la agitación. Después de finalizar la adición, se agita la mezcla durante aproximadamente otras 5 a 6 horas.
Se añaden 1000 kg de ácido tartárico a una cuba horizontal no perforada en rotación lenta (3 revoluciones por minuto) equipada con una unidad de pulverización y aplicación de polvo (por ejemplo, Driamat 2000/2.5) . Antes de comenzar la pulverización, se toma una muestra de ácido para su análisis por cribado. El ácido en cuestión está formado por partículas de ácido tartárico con un tamaño de partícula en el intervalo de 0, 4 - 0, 6 mm. La disolución ácida de caucho obtenida mediante el método anterior se pulveriza sobre las partículas de ácido tartárico así proporcionadas. Durante la pulverización, se ajusta la cantidad de aire suministrado a 1000 m³/h y a una temperatura de 35°-75°C. La presión diferencial es 2 mbar y la velocidad de rotación de la cuba es 9 revoluciones por minuto. Las boquillas deben estar dispuestas a una distancia de 350 – 450 mm del relleno.
La disolución ácida de caucho se pulveriza en alternancia con las etapas siguientes. Una vez que se han pulverizado aproximadamente 4, 8 kg de la disolución ácida de caucho sobre las partículas de ácido tartárico de tamaño de partícula 0, 4 - 0, 6 mm y que la disolución... [Seguir leyendo]
Reivindicaciones:
1. Carbón vegetal para uso en el tratamiento de una sobredosis de la sustancia activa etexilato de dabigatrán de fórmula I NH
NH
CH3
N
CH3
N OO
H
O
N
N
ON 5
EtO
I
opcionalmente en la forma de sus sales farmacéuticamente aceptables.
2. Carbón vegetal para uso de acuerdo con la reivindicación 1, en donde el carbón vegetal se administra oralmente.
3. Carbón vegetal para uso de acuerdo con la reivindicación 2, en el que la cantidad de carbón vegetal administrado oralmente está en un intervalo d.
20. 130 g.
4. Carbón vegetal para la neutralización de etexilato de dabigatrán de fórmula I sobredosificado NH
NH
CH3
N
CH3
N OO
H
O
N
N ON
EtO
I
opcionalmente en forma de sus sales farmacéuticamente aceptables.
5. Carbón vegetal para uso de acuerdo con la reivindicación 4, en donde el carbón vegetal se administra oralmente.
6. Carbón vegetal para uso de acuerdo con la reivindicación 5, en donde la cantidad de carbón vegetal administrado 20 oralmente está en un intervalo d.
20. 130 g.
7. Carbón vegetal para el de absorber dabigatrán II NH
NH2CH3
N N HO
N
II, 25 a partir de plasma sanguíneo de un paciente, que comprende la etapa de purificar el plasma sanguíneo sobre carbón vegetal activo.
8. Carbón vegetal para uso de acuerdo con la reivindicación 7, en el que la absorción de dabigatrán II del plasma sanguíneo se realiza a través de hemoperfusión sobre un filtro de carbón vegetal.
Patentes similares o relacionadas:
 Formulaciones antioxidantes, del 29 de Julio de 2020, de KEMIN INDUSTRIES, INC.: Una composición antioxidante para mejorar la estabilidad de pienso para animales y constituyentes de pienso para animales que comprende un tocoferol y catequinas del té solubles […]
Formulaciones antioxidantes, del 29 de Julio de 2020, de KEMIN INDUSTRIES, INC.: Una composición antioxidante para mejorar la estabilidad de pienso para animales y constituyentes de pienso para animales que comprende un tocoferol y catequinas del té solubles […]
Combinación de un conjugado de naloxol-peg y un agonista opioide, del 15 de Julio de 2020, de ASTRAZENECA AB: Una composición farmacéutica en una forma de dosificación unitaria en tableta sólida en donde dicha forma de dosificación unitaria comprende una […]
Composiciones dietéticas y métodos de protección contra la quimioterapia o radioterapia, del 17 de Junio de 2020, de University Of Southern California, USC Stevens: Una composición dietética para su uso en un método de protección de un animal o humano contra la quimioterapia o radioterapia, incluida la administración […]
Derivados de z)-2-(1h-indol-3-il)-3-(isoquinolin-5-il)acrilonitrilo y compuestos relacionados con actividad inhibitoria de lisosoma y antimitótica para el tratamiento de enfermedades hiperproliferativas, del 10 de Junio de 2020, de NATIONAL UNIVERSITY OF SINGAPORE: Compuesto según la fórmula I, **(Ver fórmula)** donde, Z representa N o CR4; L representa -C(R6a)=C(R6b)-; X1 a X5 son independientemente […]
Células efectoras inmunitarias genomanipuladas con un receptor de antígeno químico específico de CS1, del 15 de Enero de 2020, de Ohio State Innovation Foundation: Un polipéptido del receptor de antígeno quimérico (CAR), que comprende un dominio de unión a antígeno, un dominio transmembrana, un dominio de señalización intracelular […]
Derivados de prolina sulfonamida como antagonistas del receptor de orexina, del 20 de Noviembre de 2019, de Idorsia Pharmaceuticals Ltd: El compuesto (3,5-dimetil-fenil)-amida del ácido (S)-1-(4-metoxi-bencenosulfonil)-pirrolidin-2-carboxílico; o una sal farmacéuticamente aceptable del mismo; […]
Cuerpos cetónicos para proteger los tejidos del daño por radiación ionizante, del 21 de Agosto de 2019, de The United States Of America, As Represented By The Secretary, Department Of Health And Human Services (100.0%): Una composición que comprende un agente seleccionado de un éster de (R)-3-hidroxibutirato y un oligómero de (R)-3-hidroxibutirato de Fórmula […]
Utilización de un extracto particular de propóleo para luchar contra los efectos secundarios de quimioterapias, del 24 de Julio de 2019, de Pollenergie: Composición que comprende por lo menos un extracto de propóleo de Populus, presentando dicho extracto de propóleo por lo menos las características […]