Hidrogel bioactivo.
Hidrogel bioactivo en calidad de material híbrido a base de heparina y polietilenglicol funcionalizado en los grupos extremos y ramificado en forma de estrella,
estando la heparina unida directamente mediante grupos carboxilo activados con 1-etil-3-(3-dimetilaminopropil) carbodiimida/N-hidroxisulfosuccinimida (EDC/s-NHS) con los grupos amino en posición terminal del polietilenglicol de forma covalente mediante enlaces amida.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2008/066484.
Solicitante: ZETASCIENCE GMBH.
Inventor/es: FREUDENBERG,UWE, WERNER,CARSTEN, MEINHOLD,DORIT, GOUZY,MARLE-FRANCOISE, WELZEL,PETRA.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61L27/52 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61L PROCEDIMIENTOS O APARATOS PARA ESTERILIZAR MATERIALES U OBJECTOS EN GENERAL; DESINFECCION, ESTERILIZACION O DESODORIZACION DEL AIRE; ASPECTOS QUIMICOS DE VENDAS, APOSITOS, COMPRESAS ABSORBENTES O ARTICULOS QUIRURGICOS; MATERIALES PARA VENDAS, APOSITOS, COMPRESAS ABSORBENTES O ARTICULOS QUIRURGICOS (conservación de cuerpos o desinfección caracterizada por los agentes empleados A01N; conservación, p. ej. esterilización de alimentos o productos alimenticios A23; preparaciones de uso medico, dental o para el aseo A61K). › A61L 27/00 Materiales para prótesis o para revestimiento de prótesis (prótesis dentales A61C 13/00; forma o estructura de las prótesis A61F 2/00; empleo de preparaciones para la fabricación de dientes artificiales A61K 6/80; riñones artificiales A61M 1/14). › Hidrogeles o hidrocoloides.
- C08B37/00 QUIMICA; METALURGIA. › C08 COMPUESTOS MACROMOLECULARES ORGANICOS; SU PREPARACION O PRODUCCION QUIMICA; COMPOSICIONES BASADAS EN COMPUESTOS MACROMOLECULARES. › C08B POLISACARIDOS; SUS DERIVADOS (polisacáridos que contienen menos de seis radicales sacáridos unidos entre sí por enlaces glucosídicos C07H; procesos de fermentación o procesos que utilizan enzimas C12P 19/00; producción de celulosa D21). › Preparación de polisacáridos no previstos en los grupos C08B 1/00 - C08B 35/00; Sus derivados (celulosa D21).
PDF original: ES-2394897_T3.pdf
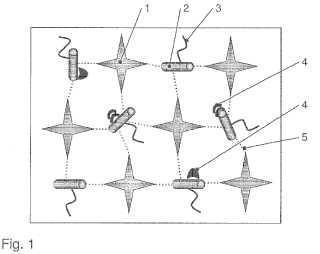
Fragmento de la descripción:
Hidrogel bioactivo La invención se refiere a un hidrogel bioactivo, el cual puede emplearse como biomaterial para el reemplazo de tejido biológico, como material de implante o, en el sentido más amplio, en productos de medicina.
Por un biomaterial en el sentido de la invención han de entenderse materiales que son puestos en contacto con un organismo biológico en aplicaciones diagnósticas o terapéuticas. Estos materiales deben satisfacer requisitos especiales en relación con la biocompatibilidad. Por biocompatibilidad se ha de entender la ausencia de reacciones del organismo clínicamente significativas sobre el empleo de materiales, productos de medicina o sistemas médicos.
Hidrogeles bioactivos conformes al género expuesto se emplean con particular ventaja como materiales de reemplazo de implantes o tejidos.
En el estado conocido de la técnica se conocen diversas estrategias para crear hidrogeles bioactivos. Se investigaron diferentes materiales de implantes o de reemplazo de tejidos para su empleo en terapias regenerativas, por ejemplo para sustentar la regeneración de vasos sanguíneos y vías nerviosas o como materiales de reemplazo de la piel. Para ello, se desarrollaron materiales de estructura o de soporte, los denominados andamios, a base de componentes principales biológicos o sintéticos los cuales, después del trasplante, deben desempeñar funciones temporalmente importantes de la matriz extracelular EZM (siglas en alemán) . Dentro de esta EZM existen células en tejidos naturales. La EZM es una red compleja supramolecular a base de diferentes proteínas estructurales, principalmente colágeno, proteoglicanos, glicoproteínas y elastina, cuya constitución estructural y composición funcional es esencial para la conservación de la arquitectura normal del tejido así como para funciones específicas para los tejidos.
Según el estado actual de la ciencia, para los procesos regenerativos arriba abordados se emplean los denominados andamios que para las células relevantes para los procesos de regeneración ejercen de forma primaria una función de soporte y sustentación y garantizan la protección frente a una solicitación mecánica.
A partir del documento US 6.306.922 A y el documento US 6.602.975 se conoce, por ejemplo, emplear materiales fuertemente hidratados, los denominados hidrogeles a base de componentes principales sintéticos o biológicos, que son degradables en el cuerpo a lo largo de prolongados espacios de tiempo sin un efecto dañino para las células.
Con el fin de poder sustentar también procesos multicelulares complejos, se desarrollaron para ello también mezclas a base de componentes de la EZM natural o también materiales para la unión reversible y liberación de moléculas señales terapéuticamente relevantes. Para las funciones mencionadas en último lugar se desarrollaron también combinaciones a base de componentes sintéticos y basados en polisacáridos de la EZM natural, las cuales aprovechan la afinidad particular de estas moléculas por importantes moléculas señal, por ejemplo factores de crecimiento.
A partir de Yamaguchi N et al: “Polysaccharide-poly (ethylene glicol) star copolymer as a scaffold for the production of bioactive hydrogels” BIOMACROMOLECULES JULIO/AGOSTO 2005 AMERCIAN CHEMICAL SOCIETY US, tomo 6, Nº 4, julio de 2005 (07-2005) , páginas 1921-1930, XP002539059’ y a partir de ZHANG L ET AL: “Manipulation of hydrogel assembly and growth factor deliver y via the use of peptide-polysaccharide interactions” JOURNAL OF CONTROLLED RELEASE, ELSEVIER, AMSTERDAM, NL, tomo 114, Nº 2, 28 de agosto de 2006 () , páginas 130-142, XP024957584 ISSN: 0168-3659’ así como a partir de SEAL ET AL: “Physical matrices stabilized by enzymatically sensitive covalent crosslinks” ACTA BIOMATERIALIA, ELSEVIER,
AMSTERDAM, NL, tomo 2, Nº 3, 1 de mayo de 2006 () , páginas 241-251, XP005394598 ISSN: 17427061 se conoce el enlace no covalente de polietilenglicol y heparina.
En NIE ET AL: “Production of heparin-functionalized hydrogels for the development of responsive and controlled growth factor deliver y systems” JOURNAL OF CONTROLLED RELEASE, ELSEVIER, AMSTERDAM, NL, tomo 122, Nº 3, 18 de septiembre de 2007 () , páginas 287-296, XP022336560 ISSN: 0168--3659, heparina y polietilenglicol están unidos a través de una reacción de Michael de PEG SH-funcionalizado y heparina.
Además, a partir del documento WO 2006/034467 A (JULIAZ INC [US]; HNOJEWYJ OLEXANDER [US]) 30 de marzo de 2006 () se desprende un PEG activado y una heparina que contiene un componente y un PEG amino-funcional.
El documento WO 2007/127198 A (INCEPT LLC [US]; PATHAK CHANDRASHEKHAR P [US]; SAWHNEY AMARPREET S [US]) 8 de noviembre del 2007 () se refiere a un gel, obtenido a partir de un PEG, heparina y un éster NHS de hidroxilaminosuccinato.
El documento WO 2008/108736 A (AGENCY SCIENCE TECH & RES [SG]; YING JACKIE Y [SG]; WAN ANDREW CA [SG]) 12 de septiembre de 2008 () da a conocer heparina y polietilenglicol, los cuales están unidos a través de una reacción de Michael de heparina SH-funcionalizada y PEG-vinilsulfona.
Lo desventajoso de los materiales conocidos en el estado de la técnica es que las complejas misiones terapéuticas de los hidrogeles conocidos no se resuelven de manera lo suficientemente eficaz en todas las exigencias.
Además, la mayoría de los materiales hasta ahora descritos, en virtud de una química de reticulación limitante o del uso exclusivo de sustancias naturales, están limitados a un estrecho intervalo en sus propiedades físicas, en particular en sus propiedades mecánicas en relación con rigidez y expansión.
La misión de la invención consiste en proporcionar un material fuertemente hidratado y a modo de gel con propiedades físicas y bioquímicas graduales de forma pre-establecida y un procedimiento para la preparación de un material de este tipo.
En tal caso, el material debe ser degradable y biocompatible a largo plazo en el cuerpo, sin productos de disociación tóxicos.
Además de ello, el material debería ofrecer una posibilidad de configurar todas las funciones importantes de la matriz extracelular natural de forma modular, es decir, ampliamente independientes una de otra.
Las misiones que se deducen de ello son, en particular:
● mejorar la función de la estructura, sustentación y protección para células en desarrollo, en función del sector de aplicación,
● posibilitar el control de la adhesión celular,
● posibilitar la unión reversible y la liberación de moléculas señal terapéuticamente relevantes y
● crear la posibilidad de la reconstrucción adaptada a las necesidades mediante células en desarrollo.
El problema de la invención se resuelve mediante un hidrogel bioactivo en calidad de material híbrido a base de heparina y polietilenglicol funcionalizado en los grupos extremos y ramificado en forma de estrella, estando la heparina unida directamente mediante grupos carboxilo de la heparina activados con 1-etil-3- (3-dimetilaminopropil) carbodiimida/N-hidroxisulfosuccinimida (EDC/s-NHS) con los grupos amino en posición terminal del polietilenglicol de forma covalente mediante enlaces amida.
Alternativamente, el problema se resuelve mediante un hidrogel bioactivo en calidad de material híbrido a base de heparina y polietilenglicol funcionalizado en los grupos extremos y ramificado en forma de estrella, estando la heparina unida de forma covalente con el polietilenglicol a través de cortas secuencias de péptidos disociables con enzimas en calidad de molécula de reticulación.
En este caso, son posibles dos vías:
la primera vía discurre a través de la funcionalización del PEG, teniendo lugar la funcionalización del polietilenglicol con secuencias de péptidos disociables con enzimas mediante reacción del grupo carboxilo activado con 1-etil-3- (3dimetilaminopropil) carbodiimida/N-hidroxisulfosuccinimida (EDC/s-NHS) en el extremo C del péptido con los grupos amino del polietilenglicol y, a continuación, tiene lugar la formación del gel propiamente dicha mediante reacción del grupo amino en el extremo N del péptido unido con el PEG con los grupos carboxilo de la heparina activados con 1etil-3- (3-dimetilaminopropil) carbodiimida/N-hidroxisulfosuccinimida (EDC/s-NHS) .
La segunda vía discurre a través de la funcionalización de la heparina, en donde la funcionalización de la heparina tiene lugar con secuencias de péptidos disociables con enzimas mediante reacción de los grupos carboxilo de la heparina activados con 1-etil-3- (3-dimetilaminopropil) carbodiimida/N-hidroxisulfosuccinimida (EDC/s-NHS) con el... [Seguir leyendo]
Reivindicaciones:
1. Hidrogel bioactivo en calidad de material híbrido a base de heparina y polietilenglicol funcionalizado en los grupos extremos y ramificado en forma de estrella, estando la heparina unida directamente mediante grupos carboxilo activados con 1-etil-3- (3-dimetilaminopropil) carbodiimida/N-hidroxisulfosuccinimida (EDC/s-NHS) con los grupos amino en posición terminal del polietilenglicol de forma covalente mediante enlaces amida.
2. Hidrogel bioactivo en calidad de material híbrido a base de heparina y polietilenglicol funcionalizado en los grupos extremos y ramificado en forma de estrella, estando la heparina unida de forma covalente con el polietilenglicol a través de cortas secuencias de péptidos disociables con enzimas en calidad de molécula de reticulación.
3. Hidrogel bioactivo según la reivindicación 2, caracterizado porque la funcionalización del polietilenglicol tiene lugar con secuencias de péptidos disociables con enzimas mediante reacción del grupo carboxilo activado con 1etil-3- (3-dimetilaminopropil) carbodiimida/N-hidroxisulfosuccinimida (EDC/s-NHS) en el extremo C del péptido con los grupos amino del polietilenglicol, y porque, a continuación, se forma el gel mediante reacción del grupo amino en el extremo N del péptido unido con el PEG con los grupos carboxilo de la heparina activados con 1-etil-3- (3dimetilaminopropil) carbodiimida/N-hidroxisulfosuccinimida (EDC/s-NHS) .
4. Hidrogel bioactivo según la reivindicación 2, caracterizado porque la funcionalización de la heparina tiene lugar con secuencias de péptidos disociables con enzimas mediante reacción de los grupos carboxilo de la heparina activados con 9-etil-3- (3-dimetilaminopropil) carbodiimida/N-hidroxisulfosuccinimida (EDC/s-NHS) con el grupo amino en el extremo N del péptido y porque, a continuación, tiene lugar la formación del gel mediante reacción de la heparina funcionalizada con los péptidos, al reaccionar el grupo carboxilo activado mediante 1-etil-3- (3dimetilaminopropil) carbodiimida/N-hidroxisulfosuccinimida (EDC/s-NHS) en el extremo C del péptido con los grupos amino del PEG.
5. Hidrogel bioactivo según una de las reivindicaciones 2 a 4, caracterizado porque como secuencia de péptidos corta se emplea arginina-glicina-ácido aspártico ligante de integrina.
6. Hidrogel bioactivo según una de las reivindicaciones 1 a 5, caracterizado porque moléculas señales están acopladas de forma electrostáticamente reversible a la heparina.
7. Hidrogel bioactivo según la reivindicación 6, caracterizado porque como moléculas señales están acoplados de forma electrostáticamente reversible a la heparina factores de crecimiento.
8. Hidrogel bioactivo según la reivindicación 7, caracterizado porque como factores de crecimiento están acoplados a la heparina de forma electrostáticamente reversible bFGF o VEGF.
9. Hidrogel bioactivo según una de las reivindicaciones 1 a 8, caracterizado porque la heparina se emplea con una longitud de cadena de PM 4.000 a 14.000.
10. Hidrogel bioactivo según una de las reivindicaciones 1 a 9, caracterizado porque se emplea star-PEG con una masa molar de PM 10.000 a 19.000.
11. Hidrogel bioactivo según una de las reivindicaciones 1 a 10, caracterizado porque como heparina se emplea una heparina modificada con secuencias peptídicas de la forma GPQG↓IAGQ o GPQG↓IWGQ disociables enzimáticamente.
12. Hidrogel bioactivo según una de las reivindicaciones 1 a 11, caracterizado porque como heparina se emplea una heparina modificada con la proteína de adhesión de la secuencia cicloRGDyK.
13. Láminas a base de hidrogeles según una de las reivindicaciones 1 a 12, que se pueden obtener mediante
-injerto de una cantidad definida de materiales de gel líquidos sobre superficies de soporte hidrofobizadas,
-formación del gel después de cubrir la superficie de soporte con una superficie de cubrición hidrofobizada,
-transferencia de las superficies de soporte a una disolución de lavado, y
-separación de las láminas de las superficies de soporte después de la expansión de los hidrogeles.
14. Soporte de cultivo celular con un hidrogel según una de las reivindicaciones 1 a 12, caracterizado porque el hidrogel está acoplado de forma covalente a través de capas delgadas de polímero reactivas a base de copolímeros de MSA alternantes, llevándose a cabo la formación de gel en presencia de soportes inorgánicos revestidos con polímero con contenido en grupos anhídrido, y uniendo los hidrogeles al soporte inorgánico a través de los grupos amino del star-PEG.
15. Procedimiento para la producción de hidrogel bioactivo según una de las reivindicaciones 1 a 12, en el que a) se disuelven por separado los componentes heparina, 1-etil-3- (3-dimetilaminopropil) carbodiimida EDC, N-hidroxisulfosuccinimida s-NHS y polietilenglicol en forma de estrella, star-PEG, tras lo cual b) se mezclan EDC y s-NHS en calidad de reactivos de activación para los grupos carboxilo de la heparina, en donde c) la heparina es activada mediante la adición de EDC y s-NHC, y porque seguidamente d) se añade star-PEG y se homogeneiza la mezcla, e) a continuación, tiene lugar la formación del gel, en donde f) a continuación de la formación del gel, se lava el gel formado.
16. Procedimiento según la reivindicación 15, caracterizado porque a) heparina, 1-etil-3- (3-dimetilaminopropil) carbodiimida EDC, N-hidroxisulfosuccinimida s-NHS y polietilenglicol en forma de estrella, star-PEG, se disuelven por separado en agua desionizada a 4ºC, tras lo cual b) EDC y s-NHS se mezclan, en calidad de reactivos de activación para los grupos carboxilo de la heparina, en la relación dos a uno, en donde c) la activación de la heparina tiene lugar después de la adición de EDC y s-NHS a lo largo de 15 min a 4ºC, y porque, a continuación, d) se añade star-PEG y la mezcla se homogeneiza a 8ºC a lo largo de 15 min, y e) la formación del gel tiene lugar a lo largo de un espacio de tiempo de 1 a 14 h a la temperatura ambiente, en donde f) a continuación, el gel formado se lava con disolución de sal de cocina tamponada con fosfato o, alternativamente, en disoluciones salinas de carácter ácido o básico y en disolución de sal de cocina tamponada con fosfato.
17. Procedimiento según la reivindicación 15 ó 16, caracterizado porque la relación de EDC y s-NHS, referida a los grupos amino del star-PEG, asciende a 1, 75 hasta 1, ascendiendo la relación de star-PEG a heparina a 1 hasta 1 a 6 hasta 1.
18. Procedimiento según una de las reivindicaciones 15 a 17, caracterizado porque el hidrogel se modifica, después de la etapa f) del procedimiento, con la proteína de adhesión cicloRGDyK, siendo activado el hidrogel lavado con una disolución a base de EDC/s-NHS en tampón fosfato 1/15 M con pH = 5 a lo largo de 30 min a 4ºC, tras lo cual la disolución se intercambia por una disolución que contiene 0, 2 mg/ml de cicloRGDyK, a base de tampón borato 100 mM con pH = 8 y se inmoviliza durante 2 h a la temperatura ambiente, tras lo cual el hidrogel modificado se aclara de nuevo con PBS.
19. Procedimiento según una de las reivindicaciones 15 a 18, caracterizado porque el hidrogel se carga con los factores de crecimiento b-FGF y VEGF, incubándose los hidrogeles con una disolución de b-FGF o VEGF con una concentración de 1-5 µg/ml en PBS a lo largo de 4 a 24 h, a la temperatura ambiente y, a continuación, lavando en PBS.
Patentes similares o relacionadas:
Separación de contaminantes de polisacárido de Streptococcus pneumoniae por manipulación del pH, del 17 de Junio de 2020, de WYETH LLC: Un procedimiento de reducción del contenido de proteínas y preservar el contenido de polisacárido capsular en un caldo de lisado celular complejo de Streptococcus pneumoniae, […]
Compuestos y sus efectos sobre el control del apetito y la sensibilidad a la insulina, del 10 de Junio de 2020, de IMPERIAL COLLEGE INNOVATIONS LIMITED: Un éster de propionato de inulina para su uso en la terapia para la reducción del apetito, ingesta de alimentos y/o ingesta de calorías y/o para mejorar […]
Evaluación de preparaciones de heparina, del 10 de Junio de 2020, de MOMENTA PHARMACEUTICALS, INC: Un procedimiento para identificar si se utilizó un procedimiento que incluye oxidación u oxidación seguido de tratamiento con un ácido para elaborar […]
Preparación de poli(ésteres de alfa-1,3-glucano) usando anhídridos orgánicos cíclicos, del 3 de Junio de 2020, de DuPont Industrial Biosciences USA, LLC: Una composición que comprende un compuesto de poli(éster de alfa-1,3-glucano) representado por la estructura **(Ver fórmula)** en donde (i) n es al menos […]
Composiciones detergentes, del 3 de Junio de 2020, de DuPont Industrial Biosciences USA, LLC: Una composición que comprende un derivado de polisacárido, en donde el derivado de polisacárido comprende un polisacárido sustituido con: a) uno o más grupos de poliamina; […]
 Método de desacetilación de biopolímeros, del 27 de Mayo de 2020, de GALDERMA S.A.: Un método para la desacetilación al menos parcial de un glucosaminoglucano que comprende grupos acetilo, que comprende:
a1) proporcionar un glucosaminoglucano que comprende […]
Método de desacetilación de biopolímeros, del 27 de Mayo de 2020, de GALDERMA S.A.: Un método para la desacetilación al menos parcial de un glucosaminoglucano que comprende grupos acetilo, que comprende:
a1) proporcionar un glucosaminoglucano que comprende […]
Reticulante de carbohidratos, del 6 de Mayo de 2020, de GALDERMA S.A.: Un producto de hidrogel que comprende moléculas de glucosaminoglucano como el polímero hinchable, en donde las moléculas de glucosaminoglucano se reticulan covalentemente […]
Derivados insaturados de polisacáridos, método de preparación y uso de los mismos, del 18 de Marzo de 2020, de Contipro a.s: Derivados insaturados de polisacáridos que comprenden, en su estructura, al menos un heterociclo que tiene un doble enlace en las posiciones 4 y […]