Formulación de liberación controlada.
SE PRESENTA UNA PREPARACION DE LIBERACION CONTROLADA PARA ADMINISTRACION ORAL QUE CONTIENE TRAMADOL,
O UNA SAL FARMACOLOGICAMENTE ACEPTABLE DEL MISMO, COMO AGENTE ACTIVO.
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E95114527.
Solicitante: EURO-CELTIQUE S.A..
Nacionalidad solicitante: Luxemburgo.
Dirección: 2, AVENUE CHARLES DE GAULLE 1653 LUXEMBOURG LUXEMBURGO.
Inventor/es: WIMMER, WALTER, HAHN, UDO, MILLER, RONALD BROWN, LESLIE, STEWART THOMAS, MALKOWSKA, SANDRA THERESE ANTOINETTE, SMITH, KEVIN JOHN, WINKLER, HORST, PRATER, DEREK ALLAN.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/135 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › que tienen ciclos aromáticos, p. ej. metadona.
- A61K9/16 A61K […] › A61K 9/00 Preparaciones medicinales caracterizadas por un aspecto particular. › Aglomerados; Granulados; Microbolitas.
- A61K9/20 A61K 9/00 […] › Píldoras, pastillas o comprimidos.
- C07C217/52 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07C COMPUESTOS ACICLICOS O CARBOCICLICOS (compuestos macromoleculares C08; producción de compuestos orgánicos por electrolisiso electroforesis C25B 3/00, C25B 7/00). › C07C 217/00 Compuestos que contienen grupos amino e hidroxi eterificados unidos a la misma estructura carbonada. › con grupos hidroxi eterificados o grupos amino unidos a átomos de carbono de ciclos distintos de los ciclos aromáticos de seis miembros de la misma estructura carbonada.
PDF original: ES-2159591_T3.pdf
Fragmento de la descripción:
Formulación de liberación controlada.
La presente invención se refiere a una preparación de liberación controlada para administración oral, a procesos para su preparación y a su uso médico. En particular, la invención se refiere a una preparación de liberación controlada que comprende tramadol o de una sal farmacéuticamente aceptable del mismo. El tramadol, el cual tiene el nombre químico ( ) -trans-2-[ (dimetilamino) metil]-1- (3-metoxifenil) ciclohexanol, es un analgésico opiáceo activo oralmente. Las preparaciones de liberación convencional en forma de cápsulas, gotas y
supositorios conteniendo tramadol, o más concretamente su sal de clorhidrato, han estado disponibles comercialmente durante muchos años para su uso en el tratamiento de dolor moderado a severo; tales preparaciones, sin embargo, no proporcionan una liberación controlada del tramadol. Además, a pesar del uso del tramadol desde hace mucho tiempo, no se han descrito en la bibliografía, ni siquiera anteriormente, preparaciones de liberación controlada, para administración oral, conteniendo tramadol como principio activo.
EP 147.780 se refiere a una liberación de fármacos, y menciona el tramadol.
Es un objeto de la presente invención proporcionar una preparación oral de tramadol de liberación controlada, apropiada para su administración cada veinticuatro horas para el tratamiento del dolor.
Por lo tanto, la presente invención proporciona una preparación de liberación controlada que comprende clorhidrato de tramadol (HCl) , para su administración oral.
Una preparación de liberación controlada según la presente invención es una que logra la liberación lenta de tramadol HCl durante un periodo de tiempo prolongado, de ese modo prolongando la duración de la acción del fármaco sobre esa lograda mediante liberación convencional. Tal preparación mantiene una concentración de fármaco en sangre, dentro del intervalo terapéutico, durante 24 horas.
De este modo, según la invención, se proporciona una preparación oral de liberación controlada de tramadol HCl, 30 eficaz para el tratamiento de dolor moderado a severo, durante 24 horas, en donde:
la preparación oral de liberación controlada consta de tramadol (HCl) , en una matriz de liberación controlada en forma de multipartículas, incluyendo la matriz tramadol HCl y aceite vegetal hidrogenado teniendo un punto de fusión de 35º a 140ºC, donde dichas multipartículas se mezclan con excipientes de compresión y se comprimen en un comprimido y en donde la preparación de liberación controlada proporciona una velocidad de liberación in vitro de la reivindicación 1
Los presentes inventores han descubierto que, la administración una vez al día, la velocidad de liberación in vitro corresponde a la siguiente proporción en % de tramadol liberado:
TABLA 1
TIEMPO (H) % LIBERADO
1 10-30
2 17-37
4 27-47
8 40-60
12 49-69
16 57-77
Una formulación según la invención, apropiada para administrar una vez al día, puede tener un tmax de 3 a 6 horas, 45 preferentemente 4 a 5 horas, y un valor W50 en el intervalo de 10 a 33 horas.
El parámetro W50 define la amplitud del perfil en plasma al 50% de la Cmax, esto es, la duración durante la cual las concentraciones en plasma son iguales o mayores del 50% de la concentración máxima. El parámetro se determina por interpolación lineal de los datos observados, y representa la diferencia en tiempo entre el primer (o único) cruzamiento de la pendiente ascendente y el último (o único) cruzamiento de la pendiente descendente en el perfil en plasma.
Las velocidades de liberación in vitro aquí son, excepto donde se especifique lo contrario, aquellas obtenidas por
medición utilizando el Método Paddle Ph. Eur. a 100 rpm en 900 ml de ácido clorhídrico 0’1N, a 37ºC, y utilizando detección por UV a 270 nm.
La preparación de liberación controlada según la invención contiene, preferentemente, una cantidad analgésicamente eficaz de tramadol HCl, convenientemente en el intervalo de 50 a 400 mg, especialmente 100, 200, 300 ó 400 mg de clorhidrato de tramadol por unidad de dosificación.
La preparación de liberación controlada según la invención se presenta como comprimidos.
El principio activo en la preparación según la invención será incorporado apropiadamente en una matriz de liberación controlada como se define en la reivindicación 1. Esta matriz que proporcione tramadol con liberación controlada durante un periodo de 24 horas y proporcione velocidades de disolución in vitro y velocidades de absorción in vivo de tramadol dentro de los intervalos especificados anteriormente.
Los materiales para su inclusión en una matriz de liberación controlada son aceites vegetales hidrogenados teniendo un punto de fusión entre 35 a 140ºC.
Una forma de dosis unitaria preferida según la invención comprende un comprimido hecho de partículas de liberación controlada en forma de multipartículas matriz que consiste en el principio activo y aceites vegetales hidrogenados teniendo un punto de fusión entre 35 a 140ºC. En concreto, las partículas de liberación controlada son preparadas, preferentemente, mediante un proceso que comprende el hacer una mezcla de principio activo seco y aceites vegetales hidrogenados teniendo un punto de fusión entre 35 a 140ºC. , seguido por trabajar mecánicamente la mezcla en un mezclador de alta velocidad, con una potencia energética suficiente para fundir o ablandar, aceites vegetales hidrogenados teniendo un punto de fusión entre 35 a 140ºC. por lo que se forman partículas con el principio activo. Las partículas resultantes, después de enfriar, son tamizadas convenientemente para dar partículas teniendo una distribución granulométrica de 0’1 a 3’0 mm, preferentemente 0’25 a 2’0 mm. Abajo se describe un ejemplo según la invención, el
cual es apropiado para la producción comercial de unidades de dosificación.
Utilizando tal técnica de procesamiento se ha descubierto que, para lograr más fácilmente las características deseadas de liberación (in vivo e in vitro, como se discutió antes) la composición a procesar debería incluir dos ingredientes esenciales, a saber:
(a) tramadol HCl; y
(b) aceites vegetales hidrogenados teniendo un punto de fusión entre 35 a 140ºC.
Hemos descubierto que la cantidad total de tramadol HCl, en la composición puede variar dentro de amplios límites, por ejemplo desde el 10 al 90% en peso del mismo.
Otro proceso preferido para la fabricación de una formulación según la invención comprende:
(a) trabajar mecánicamente, en un mezclador de alta velocidad, una mezcla de tramadol HCl, en forma de partículas, y una partículas, aceites vegetales hidrogenados teniendo un punto de fusión entre 35 a 140ºC a una velocidad y potencia energética que permita que el aceites vegetales hidrogenados teniendo un punto de fusión entre 35 a 140ºC. se fundan o ablanden, por lo que se formen aglomerados.
(b) romper los aglomerados más grandes para dar granos de liberación controlada; y
(c) continuar trabajando mecánicamente con, opcionalmente, una adición complementaria, de bajo porcentaje, de aceites vegetales hidrogenados teniendo un punto de fusión entre 35 a 140ºC.
(d) repetir, opcionalmente, las etapas (c) y, posiblemente, (b) una o más veces.
Este proceso es capaz de dar un alto rendimiento (por encima del 80%) de partículas en una distribución granulométrica deseada, con una deseada uniformidad de velocidad de liberación de tramadol o sal del mismo.
Se pueden tamizar las partículas resultantes para eliminar cualquier material sobre o infragranulado, luego formadas en comprimidos por compresión.
En este método según la invención, preferentemente se añade todo el tramadol HCl, en la etapa (a) junto con una mayor porción del aceites vegetales hidrogenados teniendo un punto de fusión entre 35 a 140ºC.
Preferentemente, la cantidad aceites vegetales hidrogenados teniendo un punto de fusión entre 35 a 140ºC añadida en la etapa (a) está entre el 10% y el 90% p/p de la cantidad total de ingredientes añadidos en la operación completa de fabricación, más preferentemente entre el 20% y el 70% p/p.
La etapa (a) del proceso se puede llevar a cabo en mezcladores convencionales de alta velocidad con interior de acero inoxidable estándar, por ejemplo, un mezclador Collette Vactron 75 o equivalente. La mezcla se procesa hasta que se alcance una temperatura en el lecho de unos 40ºC o superior, y la mezcla resultante adquiera una textura granular cohesiva, con tamaños... [Seguir leyendo]
Reivindicaciones:
1.Una preparación oral de liberación controlada de clorhidrato de tramadol eficaz para el tratamiento de dolor moderado a severo, durante 24 horas donde:
la preparación oral de liberación controlada comprende clorhidrato de tramadol, en una matriz de liberación controlada en forma de multipartículas, la matriz consiste en clorhidrato de tramadol y aceite vegetal hidrogenado teniendo un punto de fusión de 35º a 140ºC, donde dichas multipartículas se mezclan con excipientes de compresión y se comprimen en un comprimido y donde la velocidad de liberación in vitro de clorhidrato de tramadol , cuando se mide utilizando el Método Paddle Ph. Eur. a 100 rpm en 900 ml de ácido clorhídrico 0’1N, a 37ºC, y utilizando detección por UV a 270 nm, es
Tiempo (h) % liberado
1 10-30
2 17-37
4 27-47
8 40-60
12 49-69
16 57-77
Concentración en plasma (ng/ml)
Patentes similares o relacionadas:
Proceso para la síntesis de inhibidores de enzimas activadoras E1, del 9 de Octubre de 2019, de MILLENNIUM PHARMACEUTICALS, INC.: Un proceso para formar un compuesto de fórmula (VI):**Fórmula** o una de sus sales, en la que: las configuraciones estereoquímicas representadas […]
Intermedios para la síntesis de inhibidores de enzimas activadoras de actividad E1, del 9 de Octubre de 2019, de MILLENNIUM PHARMACEUTICALS, INC.: Un compuesto de fórmula (IIa):**Fórmula** o una de sus sales; en la que: las configuraciones estereoquímicas representadas en posiciones […]
Reactivo sulfamoilante, del 2 de Octubre de 2018, de MILLENNIUM PHARMACEUTICALS, INC.: Un compuesto de fórmula RuN--S(O)2X+, en la que: X es una amina terciaria seleccionada del grupo que consiste 5 en trietilendiamina, diazabiciclo [5.4.0] […]
Proceso para la síntesis de inhibidores de enzima de activación de E1, del 4 de Octubre de 2017, de MILLENNIUM PHARMACEUTICALS, INC.: Un proceso para formar un compuesto de fórmula (I):**Fórmula** o una sal del mismo; en donde: las configuraciones estereoquímicas […]
Inhibidores de desmetilasa específica de lisina-1 y su uso, del 12 de Octubre de 2016, de ORYZON GENOMICS, S.A.: Un compuesto de Fórmula 1 (A')x-(A)-(B)-(Z)-(L)-(D) 1 donde: (A) es heteroarilo o arilo; cada (A'), si está presente, se selecciona independientemente […]
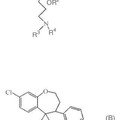 Derivados de benzocicloheptano y benzoxepina, del 10 de Diciembre de 2013, de JANSSEN PHARMACEUTICA N.V.: Compuesto de fórmula **Fórmula**
incluyendo cualquier forma estereoquímicamente isomérica del mismo, en la que:
A representa fenilo, tienilo, […]
Derivados de benzocicloheptano y benzoxepina, del 10 de Diciembre de 2013, de JANSSEN PHARMACEUTICA N.V.: Compuesto de fórmula **Fórmula**
incluyendo cualquier forma estereoquímicamente isomérica del mismo, en la que:
A representa fenilo, tienilo, […]
Derivado de aminoindano o sal del mismo, del 11 de Julio de 2013, de ASTELLAS PHARMA INC.: Un compuesto representado por la siguiente fórmula general (I) o una sal del mismo: donde los símbolos de la fórmula (I) tienen los siguientes significados, […]
ANTAGONISTAS DE NK1, del 23 de Septiembre de 2010, de SCHERING CORPORATION: Un compuesto que tiene la fórmula (I):