Procedimiento para la preparación de derivados halogenados de ácido benzoico.
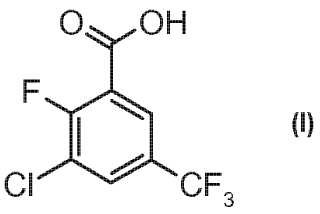
Procedimiento para la preparación de ácido 3-cloro-2-fluoro-5-trifluorometil-benzoico de fórmula:
**Fórmula**
o de una sal del mismo, que comprende la conversión de 3-cloro-4-fluorobenzotrifluoruro de fórmula:**Fórmula**
mediante:
a1) desprotonación del 3-cloro-4-fluorobenzotrifluoruro con una base metaloorgánica seguido de la adición deCO2 como electrófilo en un solvente orgánico a una temperatura de reacción de entre -100ºC y 25ºC, o
b1) formación de un compuesto de Grignard del 3-cloro-4-fluorobenzotrifluoruro con un haluro de alquilmagnesioen un solvente orgánico a una temperatura de reacción de entre 20ºC y 100ºC, seguido de la adición de CO2como electrófilo en un solvente orgánico a una temperatura de entre -100ºC y 25ºC,o mediante:
a2) transformación del 3-cloro-4-fluorobenzotrifluoruro de fórmula II en 3-cloro-2-fluoro-5-trifluorometilbenzaldehído de fórmula: **Fórmula**
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2009/056560.
Solicitante: F. HOFFMANN-LA ROCHE AG.
Nacionalidad solicitante: Suiza.
Dirección: GRENZACHERSTRASSE 124 4070 BASEL SUIZA.
Inventor/es: TRUSSARDI, RENE, HILDBRAND, STEFAN, BACHMANN,STEPHAN, PFLEGER,Christophe, JAPPY,JAMES, PATEL,DINESH MAGANBHAI, TIDSWELL,ROBERT JOHN ERNEST.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07C45/00 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07C COMPUESTOS ACICLICOS O CARBOCICLICOS (compuestos macromoleculares C08; producción de compuestos orgánicos por electrolisiso electroforesis C25B 3/00, C25B 7/00). › Preparación de compuestos que tienen grupos C=O unidos únicamente a átomos de carbono o hidrógeno; Preparación de los quelatos de estos compuestos.
- C07C45/51 C07C […] › C07C 45/00 Preparación de compuestos que tienen grupos C=O unidos únicamente a átomos de carbono o hidrógeno; Preparación de los quelatos de estos compuestos. › por pirólisis, reorganización o descomposición.
- C07C47/55 C07C […] › C07C 47/00 Compuestos que tienen grupos —CHO. › que contienen átomos de halógeno.
- C07C51/15 C07C […] › C07C 51/00 Preparación de ácidos carboxílicos o sus sales, haluros o anhídridos. › por reacción de compuestos orgánicos con anhídrido carbónico, p. ej. síntesis de Kolbe-Schmitt.
- C07C51/285 C07C 51/00 […] › con compuestos peroxidados.
- C07C51/29 C07C 51/00 […] › con compuestos que contienen átomos de halógeno, pudiendo éstos formarse in situ.
- C07C63/70 C07C […] › C07C 63/00 Compuestos que tienen grupos carboxilo unidos a los átomos de carbono de ciclos aromáticos de seis miembros. › Acidos monocarboxílicos.
PDF original: ES-2412755_T3.pdf
Fragmento de la descripción:
Procedimiento para la preparación de derivados halogenados de ácido benzoico La presente invención comprende un procedimiento para la preparación de ácido 3-cloro-2-fluoro-5-trifluorometilbenzoico de fórmula:
o de una sal del mismo. El ácido 3-cloro-2-fluoro-5-trifluorometil-benzoico o las sales del mismo son intermediarios versátiles para la preparación de agentes farmacéuticos o agroquímicos activos (documento DE nº A1 3935934) .
El documento DE nº A1 3935934 da a conocer una preparación de ácido 3-cloro-2-fluoro-5-trifluorometilbenzoico, que comprende la conversión de 1, 3-dicloro-2-fluoro- (trifluorometil) benceno con terc-butil-litio/pentano y el posterior tratamiento con dióxido de carbono. Esta síntesis conocida de la técnica adolece de que utiliza compuestos químicos corrosivos a temperaturas bajas, de -78ºC y, de esta manera, crea un problema de escalado.
Por lo tanto, el objetivo de la invención es encontrar un procedimiento capaz de superar las desventajas conocidas del procedimiento conocido de la técnica y que pueda llevarse a cabo a escala técnica.
Se ha encontrado que el objetivo podía alcanzarse utilizando el procedimiento de la presente invención tal como se 20 describe de manera general posteriormente.
El procedimiento para la preparación de ácido 3-cloro-2-fluoro-5-trifluorometil-benzoico de fórmula:
o de una sal del mismo comprende la conversión de 3-cloro-4-fluorobenzotrifluoruro de fórmula:
mediante:
a1) desprotonación del 3-cloro-4-fluorobenzotrifluoruro con una base metaloorgánica seguido de la adición de CO2 como electrófilo en un solvente orgánico a una temperatura de reacción de entre -100ºC y 25ºC, o b1) formación de un compuesto de Grignard del 3-cloro-4-fluorobenzotrifluoruro con un haluro de alquilmagnesio en un solvente orgánico a una temperatura de reacción de entre 20ºC y 100ºC, seguido de la adición de CO2 como electrófilo en un solvente orgánico a una temperatura de entre -100ºC y 25ºC:
o mediante:
a2) transformación del 3-cloro-4-fluorobenzotrifluoruro de fórmula II en 3-cloro-2-fluoro-5trifluorometilbenzaldehído de fórmula:
mediante desprotonación del 3-cloro-4-fluorobenzotrifluoruro con una base metaloorgánica seguido de la adición de un electrófilo seleccionado de entre N, N-dialquilformamida, una N, N-diarilformamida o una N-alcoxi-N5 alquilformamida en un solvente orgánico a una temperatura de reacción de entre -100ºC y 25ºC, y
b2) oxidación del benzaldehído de 3-cloro-2-fluoro-5-trifluoro-5-trifluorometilo con un oxidante seleccionado de entre hipocloritos, hipobromitos, cloritos, cloratos, persulfatos o permanganatos de elemento alcalino o alcalino
térreo, en presencia de una base hidróxido de álcali y un bromuro de álcali en un solvente acuoso a una temperatura de reacción de entre 10ºC y 100ºC, formando ácido 3-cloro-2-fluoro-5-trifluorometilbenzoico de fórmula I ó una sal del mismo:
o mediante:
a3) conversión de 3-cloro-4-fluorobenzotrifluoruro de fórmula II en 3-cloro-2-fluoro-5-trifluorometil-fenil) -hidroximetanosulfonato de álcali de fórmula:
en la que M es un átomo de metal alcalino, mediante: a4) desprotonación de 3-cloro-4-fluorobenzotrifluoruro con una base metaloorgánica, seguido de:
b4) la adición de un electrófilo seleccionado de entre N, N-dialquilformamida, N, N-diarilformamida o N-alcoxiN-alquilformamida en un solvente orgánico, a una temperatura de reacción de entre -100ºC y 25ºC, mediante: c4) adición de un ácido prótico como agente de apagado, y finalmente mediante:
d4) formación de (3-cloro-2-fluoro-5-trifluorometil-fenil) -hidroximetanosulfonato de álcali de fórmula IV con un pirosulfito de álcali: b3) transformando el (3-cloro-2-fluoro-5-trifluorometil-fenil) -hidroximetanosulfonato de álcali de fórmula IV en el 3cloro-2-fluoro-5-trifluorometil-benzaldehído de fórmula:
con una base acuosa de hidróxido de álcali, y
c3) oxidación del 3-cloro-2-fluoro-5-trifluorometil-benzaldehído de fórmula III con un oxidante seleccionado de entre hipocloritos, hipobromitos, cloritos, cloratos, persulfatos o permanganatos de elemento alcalino o alcalinotérreo, en presencia de una base hidróxido de álcali y un bromuro de álcali en un solvente acuoso a una temperatura de reacción de entre 10ºC y 100ºC, formando ácido 3-cloro-2-fluoro-5-trifluorometilbenzoico de fórmula I ó una sal del mismo:
El compuesto de partida 3-cloro-4-fluorobenzotrifluoruro se encuentra disponible comercialmente o puede prepararse según la patente US nº 4.469.893 (1984) o el documento WO nº 19970243 (1997) .
Las definiciones siguientes se proporcionan para ilustrar y definir el significado y alcance de los diversos términos utilizados para describir la presente invención.
El término "alquilo" se refiere a un radical hidrocarburo alifático saturado monovalente de cadena ramificada o lineal de uno a seis átomos de carbono, preferentemente de uno a cuatro átomos de carbono. Dicho término se ejemplifica adicionalmente mediante radicales tales como metilo, etilo, n-propilo, isopropilo, n-butilo, s-butilo, t-butilo y pentilo o hexilo y los isómeros de los mismos.
El término "arilo" se refiere al grupo fenilo o naftilo, preferentemente el grupo fenilo, que opcionalmente puede sustituirse con uno, dos, tres o múltiples sustituyentes, tales como halógeno, hidroxi, CN, halógeno-alquilo-C1-6, NO2, NH2, N (H, alquilo) , N (alquilo) 2, carboxi, aminocarbonilo, alquilo, alcoxi, alquilcarbonilo, alquil-C1-6-sulfonilo, SO2-arilo, SO3H, SO3-alquilo, SO2-NR'R'', arilo y/o ariloxi. El grupo arilo preferente es el fenilo.
Etapa a1)
Las bases metaloorgánicas adecuadas para la desprotonación en la etapa a1) pueden seleccionarse de entre bases de litio tales como n-butil-litio, s-butil-litio, t-butil-litio o aminas de metal alcalino. Resulta más preferente n-butil-litio o diisopropilamida de litio; todavía más preferentemente, n-butil-litio. La expresión "amina de metal alcalino" se refiere a una amina secundaria sustituida con un metal alcalino tal como se define en la presente memoria. La "amina de metal alcalino" se prepara in situ o ex situ previamente a la utilización, siguiendo rutas sintéticas bien conocidas por el experto en la materia o se encuentra disponible comercialmente. El metal alcalino de utilización más preferente es el litio. Entre las aminas de metal alcalino ejemplares se incluyen aductos con litio de diciclohexil-amina, diisopropilamina, tetrametil-piperidina o hexametil-disilazano. La amina de metal alcalino-litio más preferente es la diisopropilamina de litio. La expresión "metal alcalino" incluye litio, sodio y potasio. El metal alcalino preferible es el litio o el sodio.
La expresión "amina secundaria" se refiere a una amina de fórmula (a) :
en la que Ra y Rb pueden ser iguales o diferentes y se seleccionan independientemente de entre alquilo-C1-C6, cicloalquilo-C3-C6 o -Si-alquilo-C1-C6, o Ra y Rb conjuntamente con el átomo de nitrógeno al que se encuentran unidos forman un heterocicloalcano-C4-C8 que contiene opcionalmente un heteroátomo adicional seleccionado de entre O o N. Entre los ejemplos representativos se incluyen, aunque sin limitarse a ellos, piperidina, 4metilpiperidina, piperazina, pirrolidina, morfolina, dimetilamina, dietilamina, diisopropilamina, diciclohexilamina, etilmetilamina, etilpropilamina, metilpropilamina y hexametildisilazida. Preferentemente, la amina secundaria se selecciona de entre dietilamina, diisopropilamina, diciclohexilamina, etilmetilamina, etilpropilamina y metilpropilamina.
La base metaloorgánica puede utilizarse en una cantidad de entre 0, 9 y 2, 0 equivalentes, preferentemente entre 1, 0 y 1, 5 equivalentes y todavía más preferentemente en una cantidad de entre 1, 0 y 1, 1 equivalentes relativos al compuesto de partida 3-cloro-4-fluorobenzotrifluoruro.
La desprotonación como regla general se lleva a cabo en un solvente orgánico adecuado, preferentemente en un éter, tal como en tetrahidrofurano, 2-metiltetrahidrofurano, metoxiciclopentano, éter dietílico, éter t-butilmetílico o dioxano o en una combinación de éteres con hidrocarburos, tales como tolueno, pentano, hexano, ciclohexano o metilciclohexano, aunque preferentemente en tetrahidrofurano, 2-metiltetrahidrofurano o tetrahidrofurano/hexano.
La temperatura de reacción para la desprotonación se selecciona de entre -100ºC y 25ºC, preferentemente de entre -78ºC y -50ºC, todavía más preferentemente de entre -70ºC y -78ºC.
La reacción posterior con CO2 puede producirse mediante adición lenta de la mezcla de reacción a una solución de CO2 en un solvente orgánico,... [Seguir leyendo]
Reivindicaciones:
1. Procedimiento para la preparación de ácido 3-cloro-2-fluoro-5-trifluorometil-benzoico de fórmula:
o de una sal del mismo, que comprende la conversión de 3-cloro-4-fluorobenzotrifluoruro de fórmula:
mediante:
a1) desprotonación del 3-cloro-4-fluorobenzotrifluoruro con una base metaloorgánica seguido de la adición de CO2 como electrófilo en un solvente orgánico a una temperatura de reacción de entre -100ºC y 25ºC, o b1) formación de un compuesto de Grignard del 3-cloro-4-fluorobenzotrifluoruro con un haluro de alquilmagnesio en un solvente orgánico a una temperatura de reacción de entre 20ºC y 100ºC, seguido de la adición de CO2 como electrófilo en un solvente orgánico a una temperatura de entre -100ºC y 25ºC,
o mediante:
a2) transformación del 3-cloro-4-fluorobenzotrifluoruro de fórmula II en 3-cloro-2-fluoro-5trifluorometilbenzaldehído de fórmula:
mediante desprotonación del 3-cloro-4-fluorobenzotrifluoruro con una base metaloorgánica seguido de la adición de un electrófilo seleccionado de entre N, N-dialquilformamida, una N, N-diarilformamida o una N-alcoxi-Nalquilformamida en un solvente orgánico a una temperatura de reacción de entre -100ºC y 25ºC, y
b2) oxidación de 3-cloro-2-fluoro-5-trifluoro-5-trifluorometil-benzaldehído con un oxidante seleccionado de entre hipocloritos, hipobromitos, cloritos, cloratos, persulfatos o permanganatos de elemento alcalino o alcalino-térreo, en presencia de una base hidróxido de álcali y un bromuro de álcali en un solvente acuoso a una temperatura de reacción de entre 10ºC y 100ºC, formando ácido 3-cloro-2-fluoro-5-trifluorometilbenzoico de fórmula I ó una sal del mismo,
o mediante:
a3) conversión de 3-cloro-4-fluorobenzotrifluoruro de fórmula II en 3-cloro-2-fluoro-5-trifluorometil-fenil) -hidroximetanosulfonato de álcali de fórmula:
en la que M es un átomo de metal alcalino, mediante:
a4) desprotonación del 3-cloro-4-fluorobenzotrifluoruro con una base metaloorgánica seguido de la adición de un electrófilo seleccionado de entre N, N-dialquilformamida, una N, N-diarilformamida o una N-alcoxi-Nalquilformamida en un solvente orgánico a una temperatura de reacción de entre -100ºC y 25ºC, mediante c4) adición de un ácido prótico como agente de apagado, y finalmente mediante: d4) formación de (3-cloro-2-fluoro-5-trifluorometil-fenil) -hidroximetanosulfonato de álcali de fórmula IV con un pirosulfito de álcali,
b3) transformando el (3-cloro-2-fluoro-5-trifluorometil-fenil) -hidroximetanosulfonato de álcali de fórmula IV en el 3cloro-2-fluoro-5-trifluorometil-benzaldehído de fórmula:
con una base acuosa de hidróxido de álcali, y
c3) oxidación de 3-cloro-2-fluoro-5-trifluorometil-benzaldehído de fórmula III con un oxidante seleccionado de entre hipocloritos, hipobromitos, cloritos, cloratos, persulfatos o permanganatos de elemento alcalino o alcalinotérreo, en presencia de una base hidróxido de álcali y un bromuro de álcali en un solvente acuoso a una temperatura de reacción de entre 10ºC y 100ºC, formando ácido 3-cloro-2-fluoro-5-trifluorometilbenzoico de fórmula I ó una sal del mismo.
3. Procedimiento según la reivindicación 1, en el que el haluro de alquilmagnesio o de arilmagnesio es bromuro de etilmagnesio.
4. Procedimiento según la reivindicación 1, en el que en la etapa a2) se añade un ácido prótico como agente de apagado posteriormente a la desprotonación y a la adición del electrófilo.
6. Procedimiento según la reivindicación 1, en el que el ácido prótico se selecciona de entre ácido cítrico, ácido acético y ácido sulfúrico.
7. Procedimiento según la reivindicación 1, en el que el pirosulfito sódico se utiliza como pirosulfito de álcali.
8. Procedimiento según las reivindicaciones 1 a 7, en el que el ácido 3-cloro-2-fluoro-5-trifluorometil-benzoico puede
purificarse adicionalmente mediante cristalización con ciclohexano, heptano, metilciclohexano o mezclas de los 45 mismos.
Patentes similares o relacionadas:
Método para producir un compuesto de 2-(ariloximetil)benzaldehído, del 2 de Agosto de 2017, de SUMITOMO CHEMICAL COMPANY, LIMITED: Un procedimiento para producir un compuesto de 2-(ariloximetil)benzaldehído representado por la fórmula :**Fórmula** donde Q1, Q2, Q3 y Q4 representan cada uno independientemente […]
Procedimiento de producción de aldehídos aromáticos sustituidos con halógeno, del 25 de Septiembre de 2013, de MITSUBISHI GAS CHEMICAL COMPANY, INC.: Procedimiento de producción de un aldehído aromático sustituido con halógeno que comprende una etapa deconvertir un compuesto aromático sustituido […]
PROCEDIMIENTO DE RADIOFLUORACIÓN DE VECTORES BIOLOGICAMENTE ACTIVOS, del 22 de Febrero de 2011, de GE HEALTHCARE AS HAMMERSMITH IMANET, LTD: Un procedimiento para radiofluoración que comprende hacer reaccionar un compuesto de fórmula (I) con un compuesto de fórmula (II): **(Ver fórmula)**18F-(Engarce)-R2 […]
PURIFICACION DE CARBOXALDEHIDO., del 1 de Diciembre de 2004, de ELI LILLY AND COMPANY: Un procedimiento que comprende hacer reaccionar 4-cloro-4-bifenilcarboxaldehído con bisulfito de sodio para obtener el aducto de bisulfito.
PROCEDIMIENTO PARA LA PREPARACION DE HALOGENO-BENZALDEHIDOS., del , de AVENTIS RESEARCH & TECHNOLOGIES GMBH & CO. KG: LA INVENCION TRATA DE UN PROCEDIMIENTO PARA LA OBTENCION DE BENZALDEHIDOS DE HALOGENO DE FORMULA GENERAL (I), DONDE HAL ES FLUOR, CLORO, BROMO O IODO, Y Z […]
AGENTE HERBICIDA SOBRE LA BASE DE 2,6 - DICLORO - 3 - FLUOR BENZONITRILO Y NUEVOS PRODUCTOS INTERMEDIOS, del 16 de Noviembre de 1998, de BAYER AG: LA INVENCION SE REFIERE A LA UTILIZACION DE COMPUESTOS 2,6 DICLORO - 3 FLUOR - BENZONITRILO CONOCIDOS COMO SUSTANCIA ACTIVA EN MEDIOS HERBICIDAS SELECTIVOS, ASI COMO […]
PROCEDIMIENTO PARA LA ELABORACION DE 4,5 DEHIDOS, del 1 de Marzo de 1998, de BAYER AG: LOS 4,5 ELABORADOS POR MEDIO DE TRANSFORMACION DE LOS CORRESPONDIENTES BENZALDEHIDOS CON UN MEDIO DE FLUORACION.
 METODO PARA PREPARAR PARA-FENIL ALQUINIL BENZALDEHIDOS, del 16 de Abril de 2008, de LABORATOIRES SERONO SA: Procedimiento para la preparación de compuestos de fórmula (I): siendo R alquilo C1-C12, alquil-C1-C12-arilo, alquil-C1-C12-heteroarilo, alquenilo C2-C12, […]
METODO PARA PREPARAR PARA-FENIL ALQUINIL BENZALDEHIDOS, del 16 de Abril de 2008, de LABORATOIRES SERONO SA: Procedimiento para la preparación de compuestos de fórmula (I): siendo R alquilo C1-C12, alquil-C1-C12-arilo, alquil-C1-C12-heteroarilo, alquenilo C2-C12, […]