Derivados de piperidil-2,6-diona usados para inhibir la liberación del factor de necrosis tumoral de las células.
Un derivado de piperidina-2,6-diona, o sales orgánicas o inorgánicas de este,
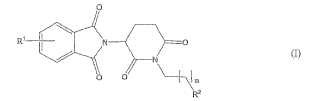
el derivado es de la fórmula general (I),
en donde
n es 1, 2, 3, 4, 5 o 6;
R1 representa de uno a cuatro de los mismos o diferentes sustituyentes seleccionados de F, Cl, Br, C1-4alquilo, OH, OC1-4 alquilo, NO2, NHC(O)C1-4 alquilo, NH2, NH(C1-4 alquilo), N(C1-4 alquilo)2;
R2 representa OR3 NR3R4, N(R3)COR4, O2CR5
R3 y R4 representan independientemente en cada aparición H o C1-4 alquilo;
R5 representa CHR6NR7R8, CHR6NR9C(O)CHR10NR7R8, W o CHR6NR9C(O)W;
R6, R9, R10 representan independientemente en cada aparición H, o C1-4alquilo;
R7 y R8 representan independientemente en cada aparición H, o C1-4alquilo, o R7 y R8 tomados juntos representan 1,3-propileno, 1,4-butileno, 1,5-pentileno, o 1,6-hexileno; opcionalmente sustituido por OH, COOH,C(O)NH2, NHC(O)R13, NH2, NHR14, NR15R16, NHC(O)NH2, NHC(NH)NH2, OR17, SR18, fenilo, o fenilo sustituido; R13, R14 , R15, R16 , R17 y R18 representan independientemente en cada aparición H, o C1-4alquilo; y
W representa un heterociclo saturado o insaturado de cuatro miembros, cinco miembros, seis miembros, siete miembros, ocho miembros.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/CN2005/001467.
Solicitante: TIAN JIN HEMAY BIO-TECH CO., LTD.
Nacionalidad solicitante: China.
Dirección: XIAO YUAN XIN CUN 31-101 TEDA TIANJIN 300457 CHINA.
Inventor/es: ZHANG,HESHENG.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/41 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › que tienen ciclos con cinco eslabones con varios heteroátomos, uno al menos nitrógeno, p. ej. tetraazoles.
- A61K31/454 A61K 31/00 […] › conteniendo un ciclo de cinco eslabones con el nitrógeno como heteroátomo del ciclo, p. ej. pimozida, domperidona.
- A61P35/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Agentes antineoplásicos.
- C07D487/04 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 487/00 Compuestos heterocíclicos que contienen átomos de nitrógeno como únicos heteroátomos del ciclo en el sistema condensado, no previstos por los grupos C07D 451/00 - C07D 477/00. › Sistemas condensados en orto.
PDF original: ES-2401281_T3.pdf
Fragmento de la descripción:
Derivados de piperidil–2, 6–diona usados para inhibir la liberación del factor de necrosis tumoral de las células
ANTECEDENTES DE LA INVENCIÓN
Campo de la invención Esta invención se refiere a los derivados de piperidina–2, 6–diona que son activos como inhibidores del factor de necrosis tumoral liberado por las células, la preparación de estos derivados, así como su aplicación como ingredientes farmacéuticamente–activos.
Descripción de la materia relacionada El factor de necrosis tumoral α (TNFα) es una citocina, producida principalmente por los macrófagos, que causa inflamación, fiebre, disfunción cardiovascular, hemorragia y una serie de reacciones agudas similares a la infección aguda y choque cuando se aplica en humanos y animales. El TNFα en exceso o incontrolado en animales o humanos indica frecuentemente una de las siguientes enfermedades:
1) Endotoxemia y/o síndrome de choque tóxico [Tracey y otros, Nature 330, 662–4 1987; Hinshaw y otros, Circ Shock 30, 279–92 (1990) ]; 2) Caquexia [Dezube y otros, Laucet, 335 (8690) , 662 (1990) ]; o 3) Síndrome de Distrés Respiratorio del Adulto (ARDS) [Millar y otros, Laucet 2 (8665) , 712–714 (1989) ].
El TNFα desempeña además una importante función en las enfermedades de resorción ósea que incluye la artritis [Betolinni y otros, Nature 319, 516–8 (1986) ]. El TNFα puede estimular la resorción ósea estimulando la formación y activación de osteoclastos y resiste la formación de huesos, lo que se demostró por experimentos in vitro e in vivo.
En la actualidad, una enfermedad que está muy comúnmente vinculada al TNFα liberado por el tejido huésped y de tumor es la hipercalcemia, que está estrechamente relacionada con los tumores malignos [Calci. Tissue Int. (Estados Unidos) 46 (Supl.) , S3–10 (1990) ]. La respuesta inmune está muy relacionado con una concentración incrementada de TNFα en el suero del paciente después del transplante de médula ósea [Holler y otros, Blood, 75 (4) , 1011–1016 (1990) ].
La malaria tipo tallo cerebral con síndrome neurogénico hiperagudo fatal, la cual es el tipo más peligroso de malaria, se asocia además con altos niveles de TNFα en la sangre. Cuando ocurre este tipo de malaria, los niveles de TNFα en suero están directamente relacionados con la enfermedad, que ocurre frecuentemente durante un ataque agudo de malaria en pacientes [Grau y otros, N. Engl. J. Med. 320 (24) , 1586–91 (1989) ].
El TNFα desempeña una importante función en la pneumonia crónica también. El almacenamiento de partículas que contienen silicio puede causar silicosis. La silicosis es una fibrosis pulmonar, que causa fallo respiratorio progresivo. En un modelo patológico animal, el anticuerpo TNFα puede bloquear completamente el progreso de fibrosis pulmonar en ratones causada por el polvo de sílice [Pignet y otros, Nature, 344:245–7 (1990) ]. Se probó además que los niveles de TNFα son anormalmente altos en el suero de animales con fibrosis pulmonar causada por el polvo de sílice o polvo de asbestos en experimentos animales [Bissonnette y otros, Inflammation 13 (3) , 329–339 (1989) ]. Las investigaciones patológicas revelan que los niveles de TNFα en los pulmones de pacientes con Sarcoidosis pulmonar son mucho mayores que en la población ordinaria [Baughman y otros, J. Lab. Clin. Med. 115 (1) , 36–42 (1990) ]. A esto sigue que el inhibidor TNFα debe tener un gran significado en el tratamiento de la enfermedad pulmonar crónica y lesión pulmonar.
La razón para que ocurra la inflamación en el cuerpo del paciente que tiene lesión por reperfusión puede ser niveles anormales de TNFα. El TNFα es visto como el jefe que causa la inducción de la lesión tisular causada por isquemia [Uadder y otros, PNAS 87, 2643–6 (1990) ].
Además, se demostró que el TNFα puede iniciar la replicación retroviral que incluye la del HIV–1 [Duh y otros, Proc. Nat. Acad. Sci., 86, 5974–8 (1989) ]. Las células T necesitan ser activadas antes que el HIV las infecte. Una vez que las células T activadas son infectadas por virus (HIV) , aquellas células T deben estar en estado activado de manera que los genes del virus HIV son capaces de expresarse y/o replicarse exitosamente. Las citocinas, especialmente el TNFα, desempañan una importante función en el proceso de expresión de la proteína HIV o replicación viral controlada por las células T. Así, la inhibición de la formación de TNFα puede inhibir a su vez la replicación de HIV en las células T [Poll y otros, Proc. Nat. Acad. Sci., 87, 782–5 (1990) ; Monto y otros, Blood 79, 2670 (1990) ; Poll y otros, AIDS Res. Human Retrovirus , 191–197 (1992) ].
cAMP puede controlar muchas funciones de las células, tal como respuesta a la inflamación, que incluyen asma, e inflamación [Lome and Cheng, Drugs of the futune, 17 (9) , 799–807, 1992]. Cuando ocurre la inflamación, la concentración de cAMP aumentada en las células blancas inhibe la activación de las células blancas y después libera los factores reguladores de la inflamación que incluyen TNFα de manera de exacerbarla inflamación en los pacientes. Consecuentemente, la inhibición de la liberación de TNFα puede aliviar las enfermedad inflamatorias que incluyen el asma.
Muchos doctores, incluyendo a Yu Yanyan, encontraron que el TNFα desempeña una importante función en el proceso de necrosis del hígado en pacientes con hepatitis viral. [Yu Yanyan etc., Chinese Journal of Internal Medicine 1996, 35:28–31]. Esto muestra que los inhibidores de TNFα pueden desempeñar una gran función en el tratamiento de la enfermedad hepática crónica y la lesión hepática.
Muchos investigadores, incluyendo a Li Yingxu, encontraron que los niveles de factores de necrosis tumoral aumentan significativamente en la síntesis y secreción de monocito humano en pacientes con enfermedad hepática crónica y se inducen otras secreciones del factor celular (por ejemplo, I1–1β, I1–6 e I1–8) . Ambos están involucrados en el proceso de lesión hepatocelular [Journal of Qiqihar Medical Colleg, 22 (10) :1119–1120, 2001]. Sus resultados están de acuerdo con las conclusiones de Yoshioka etc. [Hepatology, 1989, 10:769–777] y Wang Xin etc. [Chinese Journal of Infectious Diseases, 1997, 15 (2) :85–88]. Se encontró además que la talidomida, el inhibidor molecular pequeño de TNFα, es capaz de inhibir TNFα secretado por el monocito humano en pacientes con hepatitis, lo que descansa en una base de patología molecular para el inhibidor de TNFα aplicada a la terapia contra la hepatitis, cirrosis y cáncer de hígado.
El TNFα induce algunas respuestas a la inflamación, tales como agregación y adhesión de las células inflamatorias, permeabilidad y dilatación aumentada de los micro–vasos, fiebre, aumento de los neutrófilos en circulación, y cambios hemodinámicos, y además causa lesión a las células renales mediante la estimulación de la síntesis y liberación de citocina inflamatoria [Abboud H.E. Kidney Int. 1993; 43:252–267], expresión de molécula de adhesión celular [Egido J. y otros, Kidney Int. 1993; 43 (supl 39) :59–64], síntesis y liberación de prostaglandina G2 (PGE2) y factor de activación de plaqueta (PAF) [Gammusi G. y otros, Kidney Int., 43 (supl 39) :32–36]. Se demostró que TNFα desempeña una importante función en el desarrollo de la nefritis.
El TNFα regula la diferenciación de linfocitos B y refuerza la citotoxicidad de las células asesinas naturales (NK) , de manera de participar en la regulación de la función inmunológica por la activación de hiperplasia de macrófagos y la estimulación inmunológica de los linfocitos T.
Por lo tanto, es una estrategia efectiva disminuir los niveles de TNFα y/o aumentar los niveles de cAMP para curar muchas enfermedades inflamatorias, infecciosas, inmunológicas o tumores malignos, que incluyen pero sin limitarse a choque séptico, choque endotóxico, choque hemodinámico, síndrome séptico, lesión por reperfusión post isquémica, malaria, infección micobacteriana, meningitis, soriasis, insuficiencia cardiaca congestiva, enfermedad fibrótica, caquexia, rechazo inmune al transplante, cáncer, enfermedad autoinmunitaria, infección oportunista en SIDA, artritis reumatoide (RA) , hepatitis, nefritis, espondilitis reumatoide, y así sucesivamente. En consecuencia, la investigación y desarrollo de inhibidores de TNFα de molécula pequeña con baja toxicidad y alta eficiencia tiene... [Seguir leyendo]
Reivindicaciones:
1. Un derivado de piperidina–2, 6–diona, o sales orgánicas o inorgánicas de este, el derivado es de la fórmula general (I) ,
en donde n es 1, 2, 3, 4, 5 o 6; R1 representa de uno a cuatro de los mismos o diferentes sustituyentes seleccionados de F, Cl, Br, C1–4alquilo, OH, OC1–4 alquilo, NO2, NHC (O) C1–4 alquilo, NH2, NH (C1–4 alquilo) , N (C1–4 alquilo) 2; R2 representa OR3 NR3R4, N (R3) COR4, O2CR5 R3 y R4 representan independientemente en cada aparición H o C1–4 alquilo; R5 representa CHR6NR7R8, CHR6NR9C (O) CHR10NR7R8, W o CHR6NR9C (O) W; R6, R9, R10 representan independientemente en cada aparición H, o C1–4alquilo; R7 y R8 representan independientemente en cada aparición H, o C1–4alquilo, o R7 y R8 tomados juntos representan 1, 3– propileno, 1, 4–butileno, 1, 5–pentileno, o 1, 6–hexileno; opcionalmente sustituido por OH, COOH, C (O) NH2, NHC (O) R13, NH2, NHR14, NR15R16, NHC (O) NH2, NHC (NH) NH2, OR17, SR18, fenilo, o fenilo sustituido; R13, R14 , R15, R16 , R17 y R18 representan independientemente en cada aparición H, o C1–4alquilo; y W representa un heterociclo saturado o insaturado de cuatro miembros, cinco miembros, seis miembros, siete miembros, ocho miembros.
2. Un derivado de piperidina–2, 6–diona, o sales orgánicas o inorgánicas de este seleccionado de:
1) 2– (1– (2–hidroxietil) –2, 6–dioxopiperidin–3–il) isoindolina–1, 3–diona; 2) 2– (1– (4–hidroxibutil) –2, 6–dioxopiperidin–3–il) isoindolina–1, 3–diona; 3) 2– (1– (2–hidroxietil) –2, 6–dioxopiperidin–3–il) isoindolin–1, 3–diona 2– (dimetilamino) acetato; 4) 2– (1– (2–hidroxietil) –2, 6–dioxopiperidin–3–il) isoindolin–1, 3–diona 2– (dietilamino) acetato; 5) 2– (1– (2–hidroxietil) –2, 6–dioxopiperidin–3–il) isoindolin–1, 3–diona 2– (1–piperidil) acetato; 6) 2– (1– (2–hidroxietil) –2, 6–dioxopiperidin–3–il) isoindolin–1, 3–diona 2–aminoacetato; 7) 2– (1– (2–hidroxietil) –2, 6–dioxopiperidin–3–il) isoindolin–1, 3–diona (S) –2–aminopropanoato; 8) 2– (1– (2–hidroxietil) –2, 6–dioxopiperidin–3–il) isoindolin–1, 3–diona (S) –2–amino–3 –metilbutanoato; 9) 2– (1– (2–hidroxietil) –2, 6–dioxopiperidin–3–il) isoindolin–1, 3–diona (S) –2–pirrolidinacarboxilato; 10) 2– (1– (2–hidroxietil) –2, 6–dioxopiperidin–3–il) isoindolin–1, 3–diona (S) –2– (2–dietilaminoacetamido) propanoato; 11) 2– (1– (2–hidroxietil) –2, 6–dioxopiperidin–3–il) isoindolin–1, 3–diona (S) –2– (2–dietilaminoacetamido) –3–metilbutanoato; 12) 2– (1– (2–hidroxietil) –2, 6–dioxopiperidin–3–il) isoindolin–1, 3–diona (S) –2–amino–3–fenilpropanoato; 13) 2– (1– (4–hidroxibutil) –2, 6–dioxopiperidin–3–il) isoindolin–1, 3–diona 2– (dietilamino) acetato; 14) 2– (1– (2–hidroxietil) –2, 6–dioxopiperidin–3–il) isoindolin–1, 3–diona nicotinato; 15) 2– (1– (2–hidroxietil) –2, 6–dioxopiperidin–3–il) isoindolin–1, 3–diona isonicotinato; 16) 2– (1– (2–hidroxietil) –2, 6–dioxopiperidin–3–il) isoindolin–1, 3–diona N–etil– (S) –2–pirrolidinacarboxilato; 17) 2– (1– (2–hidroxietil) –2, 6–dioxopiperidin–3–il) isoindolin–1, 3–diona (S) –2– (terc–butoxicarbonilamino) –3– metilbutanoato; 18) 2– (1– (2–hidroxietil) –2, 6–dioxopiperidin–3–il) isoindolin–1, 3–diona (S) –2– (2–bromoacetamido) –3 –metilbutanoato; 19) 2– (1– (2–hidroxietil) –2, 6–dioxopiperidin–3–il) isoindolin–1, 3–diona (S) –2– (2–dietilaminoacetamido) –3– metilbutanoato; 20) 2– (1– (2–hidroxietil) –2, 6–dioxopiperidin–3–il) isoindolin–1, 3–diona (S) –2– (2–dietilaminoacetamido) –3–metilbutanoato hidrocloruro; 21) 2– (1– (2–hidroxietil) –2, 6–dioxopiperidin–3–il) isoindolin–1, 3–diona bromoacetato; 22) 2– (1– (2–hidroxietil) –2, 6–dioxopiperidin–3–il) isoindolin–1, 3–diona 2– (dietilamino) acetato hidrocloruro; 23) 2– (1– (2–hidroxietil) –2, 6–dioxopiperidin–3–il) isoindolin–1, 3–diona 2– (dimetilamino) acetato hidrocloruro; 24) 2– (1– (2–hidroxietil) –2, 6–dioxopiperidin–3–il) isoindolin–1, 3–diona 2– (1–piperidil) acetato hidrocloruro; 25) 2– (1– (2–hidroxietil) –2, 6–dioxopiperidin–3–il) isoindolin–1, 3–diona (S) –2– (dietilamino) –3–metilbutanoato;
26) 2– (1– (2–hidroxietil) –2, 6–dioxopiperidin–3–il) isoindolin–1, 3–diona N–tert–butoxicarbonil– (S) –2–pirrolidinacarboxilato; 27) 2– (1– (2–hidroxietil) –2, 6–dioxopiperidin–3–il) isoindolin–1, 3–diona (S) –2– (nicotinamido) –3–metilbutanoato; 28) 2– (1– (2–hidroxietil) –2, 6–dioxopiperidin–3–il) isoindolin–1, 3–diona N–etil– (S) –2–pirrolidinacarboxilato; 29) 2– (1– (4–hidroxibutil) –2, 6–dioxopiperidin–3–il) isoindolin–1, 3–diona nicotinato; 30) 2– (1– (4– (4–metilbenceno) sulfoniloxibutil) –2, 6–dioxopiperidin–3–il) isoindolin–1, 3–diona; o 31) 2– (1– (4– (dietilamino) butil) –2, 6–dioxopiperidin–3–il) isoindolina–1, 3–diona.
3. El derivado de piperidina–2, 6–diona de la reivindicación 1, en donde n es 1, 2, o 3.
4. El derivado de piperidina–2, 6–diona de la reivindicación 1, en donde R1 representa de uno a cuatro de los mismos o diferentes sustituyentes seleccionados de F, NO2, NH2, NHCH3, NHCH2CH3, N (CH3) 2, N (CH2CH3) 2, – NHCOCH3.
5. El derivado de piperidina–2, 6–diona de la reivindicación 1, en donde R2 representa OH, OCH3, OCH2CH3, OCH2CH2CH3, OCH (CH3) 2, NH2, NHCH3, NHCH2CH3, N (CH3) 2, or N (CH2CH3) 2.
6. El derivado de piperidina–2, 6–diona de la reivindicación 1, en donde R2 representa O2CCHR6NR7R8 or O2CCHR6NR9C (O) CHR10NR7R8; R6, R9, y R10 independientemente y en cada aparición representan H, o C1–4 alquilo; y R7 y R8 representan independientemente en cada aparición H, o C1–4alquilo, o R7 y R8 tomados juntos representan 1, 3– propileno, 1, 4–butileno, o 1, 5–pentileno, o 1, 6–hexileno; opcionalmente sustituido por OH, COOH, C (O) NH2, NHC (O) R13, NH2, NHR14, NR15R16, NHC (O) NH2, NHC (NH) NH2, OR17, SR18, fenilo, o fenilo sustituido.
7. El derivado de piperidina–2, 6–diona de la reivindicación 1, en donde R2 representa O2CW o O2CCHR6NR9C (O) W; R6 y R9 independientemente y en cada aparición representan H, o C1–4alquilo; y W representa 2–piridilo, 3–piridilo, 4–piridilo, pirrolidinil, o pirrolidinil sustituido.
8. Un método para la preparación de un derivado de piperidina–2, 6–diona de la fórmula general (I)
que comprende reaccionar un compuesto de la fórmula (VI)
con un compuesto de la fórmula Z–CH2 (CH2) n –R2 en presencia de una base en donde n es 1, 2, 3, 4, 5 o 6; R1 representa de uno a cuatro de los mismos o diferentes sustituyentes seleccionados de F, Cl, Br, C1–4alquilo, OH, OC1–4alquilo, NO2, NHC (O) C1–4alquilo, o N (C1–4 alquilo) 2; R2 representa OR3, NR3R4, N (R3) COR4, o O2CR5; R3 y R4 representan independientemente en cada aparición H o C1–4alquilo; R5 representa CHR6NR7R8, CHR6NR9C (O) CHR10NR7R8, W o CHR6NR9C (O) W; R6, R9, R10 representan independientemente en cada aparición H, o C1–4alquilo;
R7 y R8 representan independientemente en cada aparición H, o C1–4alquilo; o R7 y R8 tomados juntos representan1, 3– propileno, 1, 4–butileno, 1, 5–pentileno, o 1, 6–hexileno; W representa un heterociclo saturado o insaturado de cuatro miembros, de cinco miembros, de seis miembros, de siete miembros o de ocho miembros; y Z representa Br, o Cl.
9. El método de acuerdo con la reivindicación 8, en donde W representa 2–piridilo, 3–piridilo, 4–piridilo, 2– pirimidinilo, 3–pirimidinilo, 4–pirimidinilo, o heterociclos de la fórmula (II) , (III) , (IV) o (V) ;
X representa O, S, o NR12; Y representa 1, 2–etileno, 1, 3–propileno, 1, 4–butileno, 1, 5– pentileno, –CH2OCH2–– CH2SCH2–, o –CH2NR12CH2–; y R11 y R12 cada uno independientemente y en cada aparición representan H, o C1– 4alquilo.
10. Uso del derivado de piperidina–2, 6–diona oo las sales orgánicas o inorgánicas de este de acuerdo con la reivindicación 1 o 2 para la fabricación de un medicamento para usar en el tratamiento o curar una enfermedad inflamatoria o infecciosa, enfermedad del sistema inmune, tumores malignos, choque séptico, choque endotóxico, choque hemodinámico, síndrome séptico, lesión de reperfusión post–isquémica, malaria, infección micobacteriana, meningitis, soriasis, insuficiencia cardiaca congestiva, enfermedad fibrótica, caquexia, rechazo inmune al transplante,
cáncer, enfermedad autoinmunitaria, infección oportunista en SIDA, artritis reumatoide (RA) , hepatitis, nefritis, o espondilitis reumatoide.
11. El uso de la reivindicación 10, en donde el derivado de piperidina–2, 6–diona o sus sales orgánicas o inorgánicas de acuerdo con la reivindicación 1 o 2 se administran como los ingredientes farmacéuticos activos por un modo de administración seleccionado de gastrointestinal, oral, intravenoso, abdominal, dérmico, intramuscular, nasal, ocular, pulmonar, anal, vaginal, o transdérmico.
12. El uso de la reivindicación 10, en donde el derivado de piperidina–2, 6–diona o sus sales orgánicas o inorgánicas de acuerdo con la reivindicación 1 o 2 se administran como los ingredientes farmacéuticos activos en 30 combinación con otros compuestos farmacéuticos activos.
Patentes similares o relacionadas:
Compuestos de alquinilbenceno heterocíclicos, y composiciones médicas y usos de los mismos, del 29 de Julio de 2020, de Guangzhou Healthquest Pharma Co., Ltd: Un compuesto de alquinilbenceno heterocíclico que tiene la fórmula (I) y una sal farmacéuticamente aceptable, o estereoisómero del mismo, **(Ver […]
 Composiciones y métodos para el tratamiento de trastornos de células plasmáticas y trastornos prolinfocíticos de células b, del 29 de Julio de 2020, de Knopp Biosciences LLC: Una composición que comprende una cantidad terapéuticamente eficaz de dexpramipexol para su uso en el tratamiento de un trastorno de células B caracterizado por niveles elevados […]
Composiciones y métodos para el tratamiento de trastornos de células plasmáticas y trastornos prolinfocíticos de células b, del 29 de Julio de 2020, de Knopp Biosciences LLC: Una composición que comprende una cantidad terapéuticamente eficaz de dexpramipexol para su uso en el tratamiento de un trastorno de células B caracterizado por niveles elevados […]
Derivados de piperidina 1,4 sustituidos, del 29 de Julio de 2020, de 89Bio Ltd: Un compuesto de acuerdo con la Fórmula I: **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en donde: A se selecciona de […]
Profármacos de gemcitabina, del 29 de Julio de 2020, de NuCana plc: Una formulación farmacéutica que comprende gemcitabina-[fenil-benzoxi-L-alaninil)]-(S)-fosfato 3: **(Ver fórmula)** o una sal o solvato […]
Formas cristalinas de 6-((6,7-dimetoxiquinazolin-4-il)oxi)-N,2-dimetilbenzofuran-3-carboxamida, del 29 de Julio de 2020, de Hutchison Medipharma Limited: Forma I de 6-((6,7-dimetoxiquinazolin-4-il)oxi)-N,2-dimetilbenzofuran-3-carboxamida, en donde el difractograma de rayos X de polvo de la Forma […]
Compuestos y procedimientos de uso, del 29 de Julio de 2020, de Medivation Technologies LLC: Un compuesto de fórmula (Aa-1): **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en la que: A representa H, halógeno, amino, […]
Complejos de agentes terapéuticos de base vírica y poli(beta-amino-ésteres) modificados, del 29 de Julio de 2020, de Sagetis Biotech, SL: Un complejo de un agente terapéutico de base vírica con un polímero de fórmula I: **(Ver fórmula)** donde cada L1 y L2 están seleccionados […]
Análogos de éteres fosfolipídicos como vehículos de fármacos que seleccionan como objetivo el cáncer, del 22 de Julio de 2020, de Cellectar Biosciences, Inc: Un compuesto terapéutico que comprende la fórmula A-B-D, en donde: A es al menos un compuesto de fórmula (I), **(Ver fórmula)** […]