Anticuerpos anti-RANTES y métodos de uso de los mismos.
Anticuerpo anti-RANTES humana monoclonal completamente humano aislado o fragmento del mismo,
en el que dicho anticuerpo comprende:
a) una región CDR1 de VH que comprende la secuencia de aminoácidos de SEQ ID NO: 8; una región CDR2 de VH que comprende la secuencia de aminoácidos de SEQ ID NO: 9; una región CDR3 de VH que comprende la secuencia de aminoácidos de SEQ ID NO: 20; una región CDR1 de VL que comprende la secuencia de aminoácidos de SEQ ID NO: 14; una región CDR2 de VL que comprende la secuencia de aminoácidos de SEQ ID NO: 15; y una región CDR3 de VL que comprende una secuencia de aminoácidos de SEQ ID NO: 16, o
b) una región CDR1 de VH que comprende la secuencia de aminoácidos de SEQ ID NO: 8; una región CDR2 de VH que comprende la secuencia de aminoácidos de SEQ ID NO: 9, una región CDR3 de VH que comprende la secuencia de aminoácidos de SEQ ID NO: 10; una región CDR1 de VL que comprende la secuencia de aminoácidos de SEQ ID NO: 14; una región CDR2 de VL que comprende la secuencia de aminoácidos de SEQ ID NO: 15; y una región CDR3 de VL que comprende una secuencia de aminoácidos de SEQ ID NO: 16 o
c) una región CDR1 de VH que comprende la secuencia de aminoácidos de SEQ ID NO: 28; una región CDR2 de VH que comprende la secuencia de aminoácidos de SEQ ID NO: 29; una región CDR3 de VH que comprende la secuencia de aminoácidos de SEQ ID NO: 30, una región CDR1 de VL que comprende la secuencia de aminoácidos de SEQ ID NO: 34; una región CDR2 de VL que comprende la secuencia de aminoácidos de SEQ ID NO: 35; y una región CDR3 de VL que comprende una secuencia de aminoácidos de SEQ ID NO: 36;
en el que dicho anticuerpo se une a RANTES.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2008/009382.
Solicitante: NOVIMMUNE SA.
Nacionalidad solicitante: Suiza.
Dirección: 14 ch. Des Aulx, Plan-Les-Ouates 1228 Geneva SUIZA.
Inventor/es: KOSCO-VILBOIS, MARIE, FISCHER,NICOLAS, MACH,FRANCOIS.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K39/395 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 39/00 Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53). › Anticuerpos (aglutininas A61K 38/36 ); Inmunoglobulinas; Inmunosuero, p. ej. suero antilinfocitario.
- C07H21/00 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07H AZUCARES; SUS DERIVADOS; NUCLEOSIDOS; NUCLEOTIDOS; ACIDOS NUCLEICOS (derivados de ácidos aldónicos o sacáricos C07C, C07D; ácidos aldónicos, ácidos sacáricos C07C 59/105, C07C 59/285; cianohidrinas C07C 255/16; glicales C07D; compuestos de constitución indeterminada C07G; polisacáridos, sus derivados C08B; ADN o ARN concerniente a la ingeniería genética, vectores, p. ej. plásmidos o su aislamiento, preparación o purificación C12N 15/00; industria del azúcar C13). › Compuestos que contienen al menos dos unidades mononucleótido que tienen cada una grupos fosfato o polifosfato distintos unidos a los radicales sacárido de los grupos nucleósido, p. ej. ácidos nucleicos.
- C07K16/18 C07 […] › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 16/00 Inmunoglobulinas, p. ej. anticuerpos mono o policlonales. › contra materiales animales o humanos.
- C07K2/00 C07K […] › Péptidos con un número indeterminado de aminoácidos; Sus derivados.
PDF original: ES-2453592_T3.pdf
Fragmento de la descripción:
Anticuerpos anti-RANTES y métodos de uso de los mismos
Campo de la invención Esta invención se refiere en general a anticuerpos monoclonales completamente humanos que se unen a RANTES (regulada tras activación, expresada y secretada por células T normales) así como a métodos para el uso de los mismos.
Antecedentes de la invención RANTES (regulada tras activación, expresada y secretada por células T normales, CCL5) es una quimiocina que es un quimioatrayente para eosinófilos, monocitos y linfocitos.
Bums et al. (Journal of Experimental Medicine vol. 188 (1998) , págs. 1917-1927) se refiere a un anticuerpo monoclonal (Acm 4A12) que se une a RANTES humana, bloquea su actividad antiviral e inhibe la movilización de calcio intracelular provocada por RANTES.
Se han implicado niveles elevados de expresión de RANTES en una variedad de enfermedades y trastornos. Por consiguiente, existe una necesidad de terapias que seleccionen como diana la actividad de RANTES.
Sumario de la invención La presente invención proporciona anticuerpos monoclonales, tales como anticuerpos monoclonales completamente humanos, que se unen específicamente a regulada tras activación, expresada y secretada por células T normales (RANTES, también denominada en el presente documento CCL5) y que comprenden las secuencias de CDR de regiones variables SEQ ID NO 8, 9, 20, 14, 15 y 16; o SEQ ID NO 8, 9, 10, 14, 15 y 16; o SEQ ID NO 28, 29, 30, 34, 35 y 36. Los anticuerpos monoclonales según la invención incluyen los anticuerpos a los que se hace referencia en el presente documento como 1D9, 1E4 y C8. Los anticuerpos se denominan respectivamente en el presente documento anticuerpos frente a huRANTES. Los anticuerpos frente a huRANTES incluyen anticuerpos monoclonales completamente humanos, así como anticuerpos monoclonales humanizados y anticuerpos quiméricos.
Preferiblemente, los anticuerpos frente a huRANTES tienen un formato de isotipo IgG1. Más preferiblemente, los anticuerpos frente a huRANTES tienen un formato de isotipo IgG1.
Anticuerpos con formato de IgG1 a modo de ejemplo proporcionados por la presente invención son los anticuerpos 1D9, 1E4 y C8 con formato de IgG1 que comprenden la secuencia de cadena pesada y la secuencia de cadena ligera mostradas a continuación, y las secuencias de CDR se muestran en recuadros:
> Secuencia de aminoácidos de cadena pesada de 1D9 (SEQ ID NO: 263)
> Secuencia de aminoácidos de cadena ligera de 1D9 (SEQ ID NO: 264)
> Secuencia de aminoácidos de cadena pesada de 1E4 (SEQ ID NO: 238)
> Secuencia de aminoácidos de cadena ligera de 1E4 (SEQ ID NO: 254)
> Secuencia de aminoácidos de cadena pesada de C8 (SEQ ID NO: 186)
> Secuencia de aminoácidos de cadena ligera de C8 (SEQ ID NO: 187)
La línea germinal más cercana para los anticuerpos frente a huRANTES descritos en el presente documento se muestra a continuación en la tabla 1:
Tabla 1. Líneas germinales más cercanas para los anticuerpos frente a huRANTES. Los anticuerpos marcados en 20 cursiva se derivaron mediante un proceso de maduración por afinidad a partir del anticuerpo 2D1 (parte inferior de la tabla) .
ID de clon Número dp de VH Número dp de VL
C8 Vh3_DP-46_ (3-30.3) Vlambda3_3h
1D9 Vh1_DP-5_ (1-24) Vlambda3_3h
1E4 Vh1_DP-5_ (1-24) Vlambda3_3h
La invención también proporciona anticuerpos que se unen a RANTES humana cuando RANTES humana está
unida a glucosaminoglucano (GAG) , es decir, se unen a RANTES humana en el contexto de GAG. En una realización preferida, estos anticuerpos incluyen (a) una región CDR1 de VH que comprende la secuencia de aminoácidos de SEQ ID NO: 8; (b) una región CDR2 de VH que comprende la secuencia de aminoácidos de SEQ ID NO: 9; (c) una región CDR3 de VH que comprende la secuencia de aminoácidos de SEQ ID NO: 10 ó 20, (d) una región CDR1 de VL que comprende la secuencia de aminoácidos de SEQ ID NO: 14; (e) una región CDR2 de VL que comprende la secuencia de aminoácidos de SEQ ID NO: 15; y (f) una región CDR3 de VL que comprende la secuencia de aminoácidos de SEQ ID NO: 16; o anticuerpos que incluyen (a) una región CDR1 de VH que comprende la secuencia de SEQ ID NO: 28; (b) una región CDR2 de VH que comprende la secuencia de SEQ ID NO: 29; (c) una región CDR3 de VH que comprende la secuencia de SEQ ID NO: 30; (d) una región CDR1 de VL que comprende la secuencia de SEQ ID NO: 34; una región CDR2 de VL que comprende la secuencia de SEQ ID NO: 35; y (f) una región CDR3 de VL que comprende la secuencia de SEQ ID NO: 36.
En algunas realizaciones, el anticuerpo es un anticuerpo monoclonal o un fragmento de unión a antígeno del mismo. En algunas realizaciones, el anticuerpo es un anticuerpo monoclonal completamente humano o un fragmento de unión a antígeno del mismo. En algunas realizaciones, el anticuerpo es un isotipo IgG, tal como, por ejemplo, un isotipo IgG1.
En otro aspecto, la invención proporciona métodos de tratamiento, prevención o alivio de un síntoma de un trastorno relacionado con la inmunidad administrando un anticuerpo frente a huRANTES según la invención a un sujeto. Por ejemplo, los anticuerpos frente a huRANTES se usan para tratar, prevenir o aliviar un síntoma asociado con una enfermedad autoinmunitaria o un trastorno inflamatorio. Opcionalmente, al sujeto se le administra adicionalmente un segundo agente tal como, pero sin limitarse a, un reactivo anti-citocinas, reactivo anti-quimiocinas, un reactivo anticitocinas o un agente anti-receptor de quimiocinas que reconoce el ligando o receptor para proteínas tales como interleucina 1 (IL-1) , IL-2, IL-4, IL-6, IL-12, IL-13, IL-15, IL-17, IL-18, IL-20, IL-21, IL-22, IL-23, IL-27, IL-31, MIP1 alfa, MIP1 beta, IP-10, MCP1, ITAC, MIG, SDF y fractalquina.
El sujeto está padeciendo o está predispuesto a desarrollar un trastorno relacionado con la inmunidad, tal como, por ejemplo, una enfermedad autoinmunitaria o un trastorno inflamatorio. Preferiblemente, el sujeto es un mamífero, y más preferiblemente, el sujeto es un ser humano.
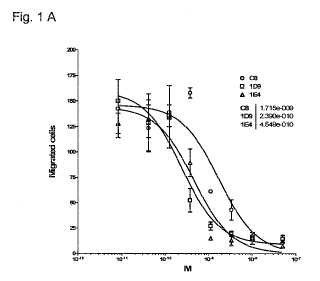
Breve descripción de los dibujos La figura 1 es una serie de gráficos que representan la actividad de anticuerpos anti-huRANTES en ensayos de quimiotaxis usando células L1.2 transfectadas con hCCR5 y 1 nM o 0, 2 nM de RANTES humana recombinante (figura 1A y B respectivamente) así como RANTES humana nativa (figuras 1C) .
La figura 2 es un gráfico que representa la capacidad de anticuerpos anti-huRANTES para unirse a huRANTES en el contexto de glucosaminoglucanos y en un ensayo ELISA.
La figura 3 es una serie de gráficos que representan la actividad del anticuerpo anti-huRANTES 1E4 en ensayos de flujo de calcio usando: células L1.2 que expresan hCCR1 y RANTES humana recombinante 25 nM (figura 3A) ; células L1.2 que expresan hCCR3 y RANTES humana recombinante 25 nM (figura 3B) ; células L1.2 que expresan hCCR5 y RANTES humana recombinante 4 nM (figura 3C) .
La figura 4 es una serie de gráficos que representan la actividad del anticuerpo anti-huRANTES 1E4 en ensayos de quimiotaxis usando: células L1.2 que expresan hCCR1 y 2 nM de RANTES humana recombinante (figura 4A) ; células L1.2 que expresan hCCR3 y 10 nM de RANTES humana recombinante (figura 4B) ; células L1.2 que expresan hCCR5 y 1 nM de RANTES humana recombinante (figura 4C) ; células L1.2 que expresan hCCR5 y aproximadamente 1 nM de RANTES humana nativa (figura 4D) .
La figura 5 es un gráfico que representa el perfil de reactividad cruzada de anticuerpo 1E4 contra un panel de quimiocinas de ser humano, mono cynomolgus, ratón y rata en un ELISA.
La figura 6 es una alineación de secuencias de proteína RANTES madura de ser humano (SEQ ID NO: 170) , mono cynomolgus (SEQ ID NO: 171) , ratón (SEQ ID NO: 172) y rata (SEQ ID NO: 206) . Las flechas indican las posiciones que están conservadas en RANTES de ser humano y mono cynomolgus pero no en las secuencias de ratón o rata y que se seleccionaron como diana mediante mutagénesis dirigida al sitio.
La figura 7 es un gráfico que representa la unión de anticuerpo 1E4 (barras blancas) o de un anticuerpo policlonal generado contra RANTES de ratón (barras con trama diagonal) a RANTES humana, RANTES de ratón y variantes de RANTES de ratón en las que los aminoácidos de ratón indicados se han reemplazado por los aminoácidos encontrados en la secuencia humana en la misma posición.
La figura 8 es una ilustración que representa el protocolo de un modelo de isquemia-reperfusión murino proporcionado en el presente documento.
La figura 9 es una serie de gráficos que representan que el tratamiento con anticuerpo anti-RANTES disminuyó el tamaño del infarto en un modelo murino... [Seguir leyendo]
Reivindicaciones:
1. Anticuerpo anti-RANTES humana monoclonal completamente humano aislado o fragmento del mismo, en el que dicho anticuerpo comprende:
a) una región CDR1 de VH que comprende la secuencia de aminoácidos de SEQ ID NO: 8; una región CDR2 de VH que comprende la secuencia de aminoácidos de SEQ ID NO: 9; una región CDR3 de VH que comprende la secuencia de aminoácidos de SEQ ID NO: 20; una región CDR1 de VL que comprende la secuencia de aminoácidos de SEQ ID NO: 14; una región CDR2 de VL que comprende la secuencia de aminoácidos de SEQ ID NO: 15; y una región CDR3 de VL que comprende una secuencia de aminoácidos de SEQ ID NO: 16, o b) una región CDR1 de VH que comprende la secuencia de aminoácidos de SEQ ID NO: 8; una región CDR2 de VH que comprende la secuencia de aminoácidos de SEQ ID NO: 9, una región CDR3 de VH que comprende la secuencia de aminoácidos de SEQ ID NO: 10; una región CDR1 de VL que comprende la secuencia de aminoácidos de SEQ ID NO: 14; una región CDR2 de VL que comprende la secuencia de aminoácidos de SEQ ID NO: 15; y una región CDR3 de VL que comprende una secuencia de aminoácidos de SEQ ID NO: 16 o c) una región CDR1 de VH que comprende la secuencia de aminoácidos de SEQ ID NO: 28; una región CDR2 de VH que comprende la secuencia de aminoácidos de SEQ ID NO: 29; una región CDR3 de VH que comprende la secuencia de aminoácidos de SEQ ID NO: 30, una región CDR1 de VL que comprende la secuencia de aminoácidos de SEQ ID NO: 34; una región CDR2 de VL que comprende la secuencia de aminoácidos de SEQ ID NO: 35; y una región CDR3 de VL que comprende una secuencia de aminoácidos de SEQ ID NO: 36;
en el que dicho anticuerpo se une a RANTES.
2. Anticuerpo según la reivindicación 1, en el que a) dicho anticuerpo es un isotipo IgG o b) dicho anticuerpo es un isotipo IgG1.
3. Anticuerpo según la reivindicación 1, en el que dicho anticuerpo comprende una región CDR1 de VH que comprende la secuencia de aminoácidos de SEQ ID NO: 8; una región CDR2 de VH que comprende la secuencia de aminoácidos de SEQ ID NO: 9; una región CDR3 de VH que comprende la secuencia de aminoácidos de SEQ ID NO: 20; una región CDR1 de VL que comprende la secuencia de aminoácidos de SEQ ID NO: 14; una región CDR2 de VL que comprende la secuencia de aminoácidos de SEQ ID NO: 15; y una región CDR3 de VL que comprende una secuencia de aminoácidos de SEQ ID NO: 16, y en el que dicho anticuerpo comprende una secuencia variable de cadena pesada que comprende la secuencia de aminoácidos de SEQ ID NO: 18 y una secuencia variable de cadena ligera que comprende la secuencia de aminoácidos de SEQ ID NO: 4.
4. Anticuerpo según la reivindicación 1, en el que dicho anticuerpo comprende una región CDR1 de VH que comprende la secuencia de aminoácidos de SEQ ID NO: 8; una región CDR2 de VH que comprende la secuencia de aminoácidos de SEQ ID NO: 9; una región CDR3 de VH que comprende la secuencia de aminoácidos de SEQ ID NO: 10; una región CDR1 de VL que comprende la secuencia de aminoácidos de SEQ ID NO: 14; una región CDR2 de VL que comprende la secuencia de aminoácidos de SEQ ID NO: 15; y una región CDR3 de VL que comprende una secuencia de aminoácidos de SEQ ID NO: 16, y en el que dicho anticuerpo comprende una secuencia variable de cadena pesada que comprende la secuencia de aminoácidos de SEQ ID NO: 2 y una secuencia variable de cadena ligera que comprende la secuencia de aminoácidos de SEQ ID NO: 4.
5. Anticuerpo según la reivindicación 1, en el que dicho anticuerpo comprende una región CDR1 de VH que comprende la secuencia de aminoácidos de SEQ ID NO: 28; una región CDR2 de VH que comprende la secuencia de aminoácidos de SEQ ID NO: 29; una región CDR3 de VH que comprende la secuencia de aminoácidos de SEQ ID NO: 30; una región CDR1 de VL que comprende la secuencia de aminoácidos de SEQ ID NO: 34; una región CDR2 de VL que comprende la secuencia de aminoácidos de SEQ ID NO: 35; y una región CDR3 de VL que comprende una secuencia de aminoácidos de SEQ ID NO: 36, y en el que dicho anticuerpo comprende una secuencia variable de cadena pesada que comprende la secuencia de aminoácidos de SEQ ID NO: 22 y una secuencia variable de cadena ligera que comprende la secuencia de aminoácidos de SEQ ID NO: 24.
6. Anticuerpo según la reivindicación 3, en el que dicho anticuerpo comprende una secuencia de cadena pesada que comprende la secuencia de aminoácidos de SEQ ID NO: 238 y una secuencia de cadena ligera
que comprende la secuencia de aminoácidos de SEQ ID NO: 254.
7. Anticuerpo según la reivindicación 4, en el que dicho anticuerpo comprende una secuencia de cadena pesada que comprende la secuencia de aminoácidos de SEQ ID NO: 263 y una secuencia de cadena ligera que comprende la secuencia de aminoácidos de SEQ ID NO: 264.
8. Anticuerpo según la reivindicación 5, en el que dicho anticuerpo comprende una secuencia de cadena pesada que comprende la secuencia de aminoácidos de SEQ ID NO: 186 y una secuencia de cadena ligera que comprende la secuencia de aminoácidos de SEQ ID NO: 187.
9. Anticuerpo según una cualquiera de las reivindicaciones anteriores, en el que dicho anticuerpo se une a RANTES humana cuando RANTES humana está unida a un glucosaminoglucano (GAG) .
10. Anticuerpo según una cualquiera de las reivindicaciones anteriores, en el que el fragmento se selecciona de Fv, Fab, Fab’, F (ab’) 2, scFv, anticuerpos de cadena sencilla, anticuerpos biespecíficos y anticuerpos heteroconjugados.
11. Composición farmacéutica que comprende el anticuerpo según una cualquiera de las reivindicaciones anteriores y un portador.
12. Anticuerpo según una cualquiera de las reivindicaciones 1 a 8 para su uso en un método de tratamiento para aliviar un síntoma de una enfermedad autoinmunitaria o un trastorno inflamatorio, comprendiendo dicho método administrar el anticuerpo a un sujeto que lo necesita en una cantidad suficiente para aliviar el síntoma de la enfermedad autoinmunitaria o el trastorno inflamatorio en el sujeto.
13. Anticuerpo según la reivindicación 9, en el que dicho sujeto es un ser humano.
Patentes similares o relacionadas:
Proteínas de unión a interleuquina-13, del 15 de Julio de 2020, de AbbVie Bahamas Ltd: Un anticuerpo anti-IL-13 recombinante, o fragmento de unión a antígeno del mismo, en donde dicho anticuerpo anti-IL-13 recombinante, o fragmento de unión a antígeno del mismo, […]
Polinucleótidos aislados y métodos y plantas que usan los mismos para regular la acidez de las plantas, del 10 de Junio de 2020, de The State of Israel, Ministry of Agriculture and Rural Development, Agricultural Research Organization, (A.R.O.), Volcani Cent: Una célula de planta o una planta que comprende una construcción de ácido nucleico que comprende una secuencia de ácido nucleico que codifica un polipéptido […]
Métodos y composiciones para modular PD1, del 13 de Mayo de 2020, de Sangamo Therapeutics, Inc: Célula aislada que comprende una inserción o una deleción en un gen de PD1 endógeno dentro de, o entre, las secuencias mostradas en SEQ ID NO: 56 y SEQ ID NO: 60 del gen de PD1 […]
Compuesto de tioéter para la protección del grupo 2''-hidroxi en nucleósidos que van a ser utilizados en la síntesis de oligonucleótidos, del 6 de Mayo de 2020, de Bonac Corporation: Un éter representado por la siguiente fórmula química : **(Ver fórmula)** en dicha fórmula química , R4 es un grupo alquilo de cadena lineal o ramificada […]
Métodos de preparación de polinucleótidos usando composiciones de sales de catiónicas multivalentes, del 6 de Mayo de 2020, de GERON CORPORATION: Un método para preparar un polinucleótido, comprendiendo el método: a) poner en contacto una primera composición polinucleotídica con una sal catiónica […]
Nucleótidos modificados para secuenciación de polinucleótidos, del 8 de Abril de 2020, de ILLUMINA CAMBRIDGE LIMITED: Una molécula de nucleótido que tiene una unidad estructural de azúcar ribosa o desoxirribosa y una base enlazada a un marcador detectable a través de […]
Análogos de oligonucleótidos que incorporan 5-aza-citosina en los mismos, del 8 de Enero de 2020, de Astex Pharmaceuticals, Inc: Un análogo de oligonucleótido aislado o sintético, o una sal o éster del mismo, de fórmula general 5'-DpG-3' o 5'-GpD-3', en los que D es decitabina; p es un […]
Nucleótidos modificados, del 1 de Enero de 2020, de ILLUMINA CAMBRIDGE LIMITED: Un kit que comprende cuatro moléculas de nucleótido trifosfato modificadas, cada una de las cuales comprende una base de purina o pirimidina y una unidad estructural […]