Procedimiento para la preparación de 2-fenoxiacetales y los 2-fenoxicarbaldehídos correspondientes a los mismos.
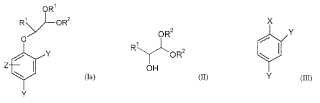
Procedimiento para la preparación de 2-fenoxi-acetales de fórmula general (Ia)
en la que
R1 es un resto alquilo C1-C2 ramificado o no ramificado,
un resto arilo C5-C6 o heteroarilo pobre en electrones,no sustituido o sustituido con halógeno, un grupo NO2, -CN, -CF3, acilo o un grupo alquilo ramificado o noramificado y
R2 es un resto alquilo C1-C5 ramificado o no ramificado o ambos restos R2 10 están unidos directamente entre sí ouno con otro a través de una unidad C1-C4,
Y siempre una Y representa hidrógeno y la otra Y, un resto -NO2, -CN o -CF3 o flúor o cloro o ambos restos Yrepresentan, independientemente entre sí, respectivamente un resto NO2, CN o CF3 o flúor o cloro,Z representa hidrógeno o un resto -NO2 o un resto alquilo C1-C6 ramificado o no ramificado o resto acilo,
mediante reacción de un compuesto de 2-hidroxiacetal de fórmula general (II)
en la que
R1 y R2 tienen el significado indicado para fórmula (Ia),
con un compuesto aromático sustituido de fórmula general (III)
en la que
Y tiene el significado indicado para fórmula (I) y
X representa flúor, cloro, bromo o un grupo NO2.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2008/057303.
Solicitante: SALTIGO GMBH.
Nacionalidad solicitante: Alemania.
Dirección: 51369 LEVERKUSEN ALEMANIA.
Inventor/es: DOCKNER, MICHAEL, MÜLLER,THOMAS-NORBERT.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07C201/12 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07C COMPUESTOS ACICLICOS O CARBOCICLICOS (compuestos macromoleculares C08; producción de compuestos orgánicos por electrolisiso electroforesis C25B 3/00, C25B 7/00). › C07C 201/00 Preparación de ésteres de ácido nítrico o nitroso o de compuestos que contienen grupos nitro o nitroso unidos a una estructura carbonada. › por reacciones que no crean grupos nitro.
- C07C205/37 C07C […] › C07C 205/00 Compuestos que contienen grupos nitro unidos a una estructura carbonada. › estando unido el átomo de oxígeno de al menos uno de los grupos hidroxi eterificados a un átomo de carbono acíclico.
PDF original: ES-2432520_T3.pdf
Fragmento de la descripción:
Procedimiento para la preparación de 2-fenoxiacetales y los 2-fenoxicarbaldehídos correspondientes a los mismos La invención se refiere a un nuevo procedimiento para la preparación de 2-fenoxiacetales y los 2fenoxicarbaldehídos correspondientes a los mismos. Estos compuestos son importantes productos intermedios para la preparación de principios activos farmacéuticos.
La única vía descrita hasta ahora que lleva hasta los 2-fenoxiacetales incluye, como etapa clave, una reacción de Rosenmund para la preparación del aldehído (figura 1) . El cloruro de ácido necesario para esto se puede conseguir mediante reacción de un éster de ácido α-halocarboxílico con el correspondiente fenolato, seguido de una saponificación del 2-fenoxiéster formado y tratamiento posterior con cloruro de tionilo. El correspondiente acetal se prepara mediante tratamiento del aldehído con metanol en presencia de cantidades catalíticas de ácido. Por esta vía se prepararon en primer lugar compuestos aromáticos con sustituyentes ricos en electrones (R = OMe, alquilo)
[Kwiecien, Polish J. Chem. 2004, 78, 249 - 254; Synth. Commun. 2005, 35, 2223 - 2250]. Una desventaja de este método es la vía de síntesis de 5 pasos de larga duración.
Figura 1 Preparación de hidroxiacetales según Kwiecien.
La síntesis de compuestos de 2-fenoxicarbonilo con sustituyentes pobres en electrones de los correspondientes fenolatos y compuestos de carbonilo α-halogenados se consigue en condiciones considerablemente más rigurosas. De este modo, para la reacción son necesarias elevadas temperaturas de 190 - 200 ºC [Bischorf, Chem. Ber. 1900, 33, 1603 - 1611] o largos tiempos de reacción [Harfenist, J. Org. Chem. 1971, 36, 1171 - 1175]. Una variante para la esterificación incluye la desprotonación del fenol con hidruro sódico (figura 2) . A este respecto, son desventajosas la capacidad de autoinflamación del hidruro sódico y las medidas en cuanto a la técnica de seguridad necesarias que esto conlleva. Para obtener el carbaldehído deseado, en primer lugar se tiene que reducir el ácido carboxílico obtenido mediante saponificación del éster hasta dar alcohol, después de lo cual el mismo se oxida hasta dar el producto diana [Yi, Bull. Korean Chem. Soc. 2004, 25, 1003 - 1008]. Otra desventaja de este método es la larga ruta de síntesis y el rendimiento reducido que esto conlleva (32 % a lo largo de 5 pasos) .
Figura 2 Preparación de 2-carboxialdehídos con sustituyentes pobres en electrones de los correspondientes fenoles según Yi.
La preparación de éteres de arilalquilo con sustituyentes pobres en electrones se consigue también mediante reacción de alcoholes alifáticos con los correspondientes halogenuros de arilo (figura 3) .
Figura 3 Preparación de éteres de arilalquilo en el sentido de una sustitución aromática nucleófila (SNAr) .
Normalmente se hace reaccionar el alcohol directamente como sal de metal alcalino con el fluoruro o cloruro de arilo o se prepara in situ mediante adición de hidruros de metal alcalino o bases fuertes tales como hexametildisilazanos de metal alcalino o terc-butanolatos de metal alcalino. El uso de hidruros de metal alcalino a gran escala no es deseable debido a su reactividad extremadamente intensa con agua y su mala manejabilidad y representa un gran riesgo para la seguridad.
Otra posibilidad es el uso de un sistema bifásico en el que el alcohol y el halogenuro de arilo están disueltos en un disolvente no miscible con agua tal como tolueno y la base necesaria para la desprotonación del nucleófilo está presente en una solución acuosa. Como mediadores se emplean catalizadores de transferencia de fase, normalmente halogenuros de amonio cuaternario.
El uso de compuestos aromáticos de cloro, sin embargo, conduce a rendimientos muy variables debido a reacciones secundarias indeseadas del material de partida aromático. De este modo, con la selección de condiciones de reacción inapropiadas se forman, por ejemplo, en gran medida a partir de cloronitrobencenos los nitrofenoles como componente secundario.
Debido a su mayor reactividad, los fluoruros de arilo se pueden hacer reaccionar con alcoholatos primarios,
secundarios y terciarios como nucleófilos [ejemplo de la reacción con alcoholes terciarios: documento EP1564201A1]. La reacción de cloruros de arilo con alcoholes terciarios solo se consigue, según la bibliografía, en una medida muy reducida o no se consigue en absoluto [Paradisi/Scorrano, J. Org. Chem. 1983, 48, 3022 - 3026; Seguchi, Yukagaku 1982, 31, 609 - 611.]. Para la reacción de cloruros de arilo con alcoholatos secundarios no funcionalizados existen solo pocos ejemplos. Una reacción está representada, a modo de ejemplo, en la figura 4
[Bansho, documento JP 2002-255905]. El rendimiento ascendió al 86 %.
Figura 4 Ejemplo de la preparación de éteres de arilalquilo con un alcohol secundario como nucleófilo.
Se encuentra solo un ejemplo en la bibliografía [Kawamatsu, Chem. Pharm. Bull. 1984, 32, 2267 - 2278] de la preparación de un éter de arilalquilo con una funcionalidad carbonilo protegida como acetal en la cadena lateral mediante sustitución nucleófila (figura 5) . A este respecto, el alcohol primario preparado más adelante se hizo reaccionar con el 4-fluoronitrobenceno considerablemente más reactivo con respecto al derivado de cloro. El
producto deseado se obtuvo con un rendimiento del 87 %. En este caso, es de nuevo problemático el uso de hidruro sódico como base y las medidas complejas que esto conlleva para el manejo seguro de esta sustancia.
Figura 5 Preparación de éteres de arilalquilo por SNAr en presencia de funcionalidades acetal.
El objetivo de la presente invención era poner a disposición un nuevo procedimiento más rentable para la preparación de 2-fenoxiacetales y los 2-fenoxicarbaldehídos correspondientes a los mismos con un rendimiento mejorado.
En la presente invención se consigue reducir la vía de síntesis hasta los 2-fenoxiacetales de cinco o seis etapas a una etapa (figura 6) . Los 2-hidroxiacetales necesarios para esto están disponibles de forma sencilla en cantidades técnicas. El rendimiento total partiendo del aldehído se pudo aumentar, con respecto al método de Yi (figura 5) , del 31 % al 55 %. Además se evitaron operaciones de síntesis problemáticas a escala técnica, tales como una reacción de Rosenmund o una oxidación de Swern. La reacción de 4-cloronitrobenceno con alcoholes secundarios hasta ahora está descrita solo para alcoholes no funcionalizados.
Figura 6 síntesis de acuerdo con la invención de 2-fenoxiacetales mediante sustitución aromática nucleófila.
Se conocen otros procedimientos para la preparación de compuestos de 2-fenoxiacetaldehído-acetal mediante sustituyentes aromáticos nucleófilos de un halogenuro aromático activado con 2-hidroxi-acetaldehído-acetales en presencia de hidruro sódico en DMF anhidra por los documentos WO 03/033476A, WO2006/066174A y EP
1103551A.
Se halló un procedimiento en el que se pueden hacer reaccionar compuestos aromáticos de flúor y cloro pobres en electrones con 2-hidroxiacetales, 2-fenoxiacetales sorprendentemente en condiciones poco rigurosas. A este respecto, el derivado de alcohol se desprotona en presencia de una base fuerte y, a continuación, se hace reaccionar con el compuesto aromático de cloro deseado.
Por tanto, el objeto de la invención es un procedimiento para la preparación de 2-fenoxiacetales de fórmula general (Ia)
en la que R1
es un resto alquilo C1-C2 ramificado o no ramificado, un resto arilo C5-C6 o heteroarilo pobre en electrones, no sustituido o sustituido con halógeno, un grupo -NO2, -CN, -CF3, acilo o un grupo alquilo ramificado o no 15 ramificado y
R2
es un resto alquilo C1-C5 ramificado o no ramificado o ambos restos R2 están unidos directamente entre sí o uno con otro a través de una unidad C1-C4,
Y siempre una Y representa hidrógeno y la otra Y, un resto -NO2, -CN o -CF3 o flúor o cloro o ambos restos Y representan, independientemente entre sí, un resto NO2, CN o CF2 o flúor o cloro y
Z representa hidrógeno o un resto -NO2 o un resto alquilo C1-C6 ramificado o no ramificado o resto acilo, mediante reacción de un compuesto de 2-hidroxiacetal de fórmula general (II) 25
en la que 30 R1 y R2 tienen el significado indicado para fórmula (Ia) , con un compuesto aromático sustituido de fórmula general (III)
en la que Y tiene el significado indicado para fórmula (I) y
X representa flúor, cloro, bromo o un grupo NO2,
en presencia de un alcoholato de metal alcalino o un hidróxido sólido de metal alcalino en combinación... [Seguir leyendo]
Reivindicaciones:
1. Procedimiento para la preparación de 2-fenoxi-acetales de fórmula general (Ia)
en la que R1 es un resto alquilo C1-C2 ramificado o no ramificado, un resto arilo C5-C6 o heteroarilo pobre en electrones, no sustituido o sustituido con halógeno, un grupo NO2, -CN, -CF3, acilo o un grupo alquilo ramificado o no ramificado y
R2 es un resto alquilo C1-C5 ramificado o no ramificado o ambos restos R2 están unidos directamente entre sí o uno con otro a través de una unidad C1-C4, Y siempre una Y representa hidrógeno y la otra Y, un resto -NO2, -CN o -CF3 o flúor o cloro o ambos restos Y representan, independientemente entre sí, respectivamente un resto NO2, CN o CF3 o flúor o cloro, Z representa hidrógeno o un resto -NO2 o un resto alquilo C1-C6 ramificado o no ramificado o resto acilo,
mediante reacción de un compuesto de 2-hidroxiacetal de fórmula general (II)
en la que R1 y R2 tienen el significado indicado para fórmula (Ia) , con un compuesto aromático sustituido de fórmula general (III)
en la que Y tiene el significado indicado para fórmula (I) y X representa flúor, cloro, bromo o un grupo NO2,
en presencia de un alcoholato de metal alcalino o de un hidróxido sólido de metal alcalino en combinación con carbonato sólido de metal alcalino. 35
2. Procedimiento para la preparación de 2-fenoxicarbaldehídos de fórmula general (Ib) ,
en la que R1, Z e Y tienen el significado indicado para fórmula (Ia) , caracterizado por que un 2-fenoxiacetal de fórmula (Ia) obtenido de acuerdo con la reivindicación 1 se suministra a una hidrólisis ácida.
3. Procedimiento de acuerdo con una de las reivindicaciones 1 o 2, caracterizado por que R1 es un resto alquilo C4. 10
4. Procedimiento de acuerdo con la reivindicación 1, caracterizado por que se lleva a cabo la reacción en dimetilformamida anhidra como disolvente.
5. Procedimiento de acuerdo con la reivindicación 1, caracterizado por que el compuesto de 2-hidroxiacetal de
fórmula (II) se trata previamente, antes de la reacción con el compuesto aromático sustituido de fórmula general (III) , con un alcoholato.
6. 2-fenoxiacetales de fórmula general (Ia)
en la que R1 es un resto alquilo C1-C2 ramificado o no ramificado, un resto arilo C5-C6 o heteroarilo pobre en electrones, no sustituido o sustituido con halógeno, un grupo NO2, CN, -CF3, acilo o un grupo alquilo ramificado o no ramificado y R2 es un resto alquilo C1-C5 ramificado o no ramificado, Y siempre una Y representa hidrógeno y la otra Y un resto -NO2, -CN o -CF3 o flúor o cloro y Z representa hidrógeno o representa un resto -NO2 o un resto alquilo C1-C6 ramificado o no ramificado o resto acilo.
7. 2-fenoxiacetales de acuerdo con la reivindicación 6, caracterizados por que Z es hidrógeno, una Y es un grupo NO2, la otra Y es hidrógeno, R1 es un grupo alquilo C1-C4 y R2 es un grupo metilo.
8. 2-fenoxicarbaldehídos de fórmula general (Ib)
en la que R1, Z e Y tienen el significado indicado para fórmula (Ia) .
Patentes similares o relacionadas:
Proceso para preparar 1-(3,5-diclorofenil)-2,2,2-trifluoroetanona y sus derivados, del 18 de Septiembre de 2019, de SYNGENTA PARTICIPATIONS AG: Un proceso para preparar un compuesto de fórmula I**Fórmula** donde R1 es hidrógeno, fluoro o cloro; dicho proceso comprende a) hacer […]
Procedimiento para la hidroxilación de compuestos arilo halogenados, del 15 de Marzo de 2019, de CENTRE NATIONAL DE LA RECHERCHE SCIENTIFIQUE (C.N.R.S.): Procedimiento de hidroxilación de compuestos arilo halogenados que comprende una reacción de hidroxilación llevada a cabo a una temperatura inferior a 150 °C, en presencia […]
Trifluorometilaciones directas usando trifluorometano, del 22 de Febrero de 2019, de UNIVERSITY OF SOUTHERN CALIFORNIA: Método para preparar directamente un producto trifluorometilado, que comprende hacer reaccionar un sustrato que puede fluorometilarse con trifluorometano en presencia […]
Compuesto intermedios y proceso para la preparación de fingolimod, del 25 de Enero de 2019, de Mapi Pharma Limited: Un proceso para la preparación de Fingolimod de fórmula ,**Fórmula** o una sal farmacéuticamente aceptable del mismo, que comprende las etapas de: a) reaccionar […]
Procedimiento de preparación de un compuesto mediante una novedosa reacción similar a Sandmeyer usando un compuesto de radical nitróxido como catalizador de reacción, del 23 de Agosto de 2017, de DAIICHI SANKYO COMPANY, LIMITED: Un procedimiento de preparación de un compuesto representado por la fórmula (11b) siguiente:**Fórmula** en el que el procedimiento comprende: añadir y disolver un […]
Procedimiento para la preparación catalítica de aldehídos insaturados, del 10 de Mayo de 2017, de EVONIK DEGUSSA GMBH: Un procedimiento para la preparación de aldehídos insaturados en α,ß a partir de alquenos, caracterizado por la conversión química de un alqueno (una olefina) en presencia […]
Procedimiento de preparación para derivado de gamma-aminoácido bicíclico ópticamente activo, del 31 de Agosto de 2016, de Daiichi Sankyo Co., Ltd: Una mezcla de compuestos representados por la fórmula general (I) y (I'): **Fórmula** en las que R1 y R2 son el mismo o diferente y cada […]
Procedimiento de tetraarilborato para la preparación de bifenilos sustituidos, del 14 de Enero de 2015, de Bayer Intellectual Property GmbH: Procedimiento para la preparación de bifenilos sustituidos de fórmula (I)**Fórmula** en la que X1 se selecciona de átomos de halógeno y grupos alquilo […]