Peptidomiméticos con actividad antagonista de glucagón y agonista de GLP-1.
Un peptidomimético aislado que tiene una secuencia de fórmula (I),
incluyendo sus tautómeros, solvatos
A-Z1-Z2-Z3-Z4-Z5-Z6-Z7-Z8-Z9-Z10-Z11-B
donde,
A representa los grupos -NH-R1, R3-CO-, R3-O-CO- o R3-SO2-, donde R1 representa hidrógeno, o una cadena alquílica (C1-C10) lineal o ramificada opcionalmente sustituida; R3 se selecciona entre los grupos alquilo (C1-C10) lineal o ramificado, cicloalquilo (C3-C6), arilo, heteroarilo o arilalquilo; B representa -COOR2, -CONHR2 o CH2OR2, donde R2 representa H, grupos opcionalmente sustituidos seleccionados entre un grupo alquilo (C1-C10) lineal o ramificado, grupos arilo o aralquilo; Z1 a Z11 representan aminoácidos naturales o innaturales, conectados entre sí mediante enlace amida, donde Z1 representa L-Histidina (H), DHistidina (dH) o Ácido urocánico (UA); **Fórmula**
ácido urocánico (UA)
Z2 representa un aminoácido de origen natural o innatural seleccionado del grupo que comprende L-Serina (S), D-Serina (dS), L-Alanina (A), D-Alanina (dA), α-metilprolina (α-Me-Pro), ácido α-amino-isobutírico (Aib), ácido 1-aminociclopropanocarboxílico (ACP), ácido 1-amino-ciclopentanocarboxílico (APP); **Fórmula**
Z3 representa L-Glutamina (GIn; Q), D-Glutamina (dQ) o compuestos de fórmula II (CNB o HfI); **Fórmula**
Ácido 2-amino-4-ciano-butírico (CNB) Hexafluoroleucina (HfI) Z4 representa Glicina (G) o los aminoácidos innaturales ácido 1-aminociclopropanocarboxílico (ACP) o
ácido 1-amino-ciclopentanocarboxílico (APP);
Z5 representa un aminoácido de origen natural o no natural que comprende una cadena lateral hidroxilada; un Z5 preferido es L-Treonina (T), D-Treonina (dT), L-Alo-treonina (alo-Thr; alo-T), D-alotreonina (d-alo-Thr; d-alo-T);
Z6 representa un aminoácido de origen natural o innatural con un carbono alfa disustituido que tiene dos cadenas laterales, donde cada una de ellas puede ser independientemente un grupo alquilo o arilo sustituido opcionalmente o un grupo aralquilo donde los sustituyentes se pueden seleccionar entre uno o más grupos alquilo o uno o más grupos halo;
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/IN2008/000831.
Solicitante: CADILA HEALTHCARE LIMITED.
Nacionalidad solicitante: India.
Dirección: ZYDUS TOWER SATELLITE CROSS ROADS AHMEDABAD 380 015, GUJARAT INDIA.
Inventor/es: JAIN,MUKUL,R, PATEL,PANKAJ,RAMANBHAI, BAHEKAR,Rajesh H.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K38/26 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Glucagón.
- C07K14/605 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › Glucagones.
PDF original: ES-2382579_T3.pdf
Fragmento de la descripción:
Peptidomiméticos con actividad antagonista de glucagón y agonista de GLP-1
Campo de la Invención La presente invención se refiere a compuestos de fórmula general (I) , sus sales farmacéuticamente aceptables y las composiciones farmacéuticas que los contienen.
A-Z1-Z2-Z3-Z4-Z5-Z6-Z7-Z8-Z9-Z10-Z11-B (I)
La presente invención también se refiere a un procedimiento para la preparación de compuestos de fórmula general (I) , sus sales farmacéuticamente aceptables y las composiciones farmacéuticas que los contienen.
Antecedentes de la Invención
La diabetes está caracterizada por el deterioro de la secreción de insulina desde las células º pancreáticas, la resistencia a la insulina o ambas (Cavaghan, M.K., et al., J. Clin. Invest. 2000, 106, 329) . La mayoría de los pacientes diabéticos de tipo 2 se pueden tratar con agentes que reducen la producción de glucosa hepática (antagonistas de glucagón) , reducen la absorción de glucosa desde el TGI, estimulan la función de las células º (secretagogos de insulina) o con agentes que aumentan la sensibilidad de los tejidos de los pacientes a la insulina (sensibilizan a la insulina) . Los fármacos utilizados en la actualidad para tratar la diabetes de tipo 2 incluyen inhibidores de a-glucosidasa, sensibilizadores a la insulina, secretagogos de insulina y bloqueadores del canal KATP (Chehade, J. M., et al., Drugs, 2000, 60, 95) . Sin embargo, casi la mitad de los sujetos diabéticos de tipo 2 pierden su respuesta a estos agentes a lo largo de un período de tiempo y por tanto requieren terapia con insulina. El tratamiento con insulina tiene varios inconvenientes, es inyectable, produce hipoglicemia y ocasiona ganancia de peso (Burge, M.R., Diabetes Obes. Metab., 1999, 1, 199) .
Los problemas con el tratamiento actual necesitan nuevas terapias para tratar la diabetes de tipo 2. A este respecto, se encontró que el agonista del péptido 1 de tipo glucagón (GLP-1) , que promueve la secreción de insulina dependiente de glucosa en el páncreas y el antagonista del receptor de glucagón, que inhibe la producción de glucosa hepática mediante la inhibición de la glicogenolisis y gluconeogénesis, eran potencialmente terapéuticos. De este modo se encontró que el agonista de GLP-1 y el antagonista de glucagón juntos reducen los niveles de glucosa circulante y representan agentes terapéuticos útiles para el tratamiento y la prevención de la diabetes de tipo 2 (Perr y , T.A., et al., Trends Pharmacol. ScL, 2003, 24, 377) .
El glucagón y el GLP-1 son miembros de la familia de hormonas peptídicas relacionadas estructuralmente (familia de la secretina) . El glucagón y el GLP-1 constituyen un grupo de péptidos altamente homólogos debido a que estas dos hormonas se originan a partir de un precursor común, el preproglucagón, que después de un procesamiento específico del tejido conduce a la producción de GLP-1 predominantemente en el intestino y glucagón en el páncreas (Jiang, G., et al., Am. J. Physiol. Endocrinol. Metab., 2003, 284, E671-678) . Los receptores para estos dos péptidos son homólogos (identidad de 58%) y pertenecen a la familia de receptores acoplados a proteína G de clase B (GPCR) . Las GPCR de clase B también se denominan familia de receptores de secretina, que consisten en receptores de unión del péptido-15 en seres humanos. Los receptores GPCR comprenden un dominio extracelular N-terminal de 100-160 residuos, conectado a un dominio yuxtamembrana (dominio J) de siete hélices a que abarcan la membrana con bucles interpuestos y una cola C-terminal (Brubaker, P. L., et al., Receptors Channels, 2002, 8, 179) . Los GPCR de clase B son activados por ligandos peptídicos endógenos de tamaño intermedio, típicamente de 30-40 aminoácidos (Hoare, S.R.J., Drug. Discover y Today, 2005, 10, 423; Gether, U., Endocrine Reviews, 2000, 21, 90) .
El glucagón es una hormona peptídica de 29 aminoácidos procesada a partir del proglucagón en las células a pancreáticas por PC2. El glucagón actúa a través de GPCR transmembrana de siete dominios, que consisten en 485 aminoácidos. El glucagón se libera al torrente sanguíneo cuando la glucosa circulante es poca. El papel fisiológico principal del glucagón es estimular la producción de glucosa hepática, conduciendo de ese modo a un aumento de la glicemia (Tan, K., et al., Diabetologia, 1985, 28, 435) . El glucagón proporciona el mecanismo contrarregulador principal para la insulina al mantener la homeostasis de la glucosa in vivo. El glucagón y su receptor representan dianas potenciales para el tratamiento de la diabetes. El antagonismo de la acción del glucagón mediante el bloqueo de la acción del glucagón secretado en el receptor de glucagón (antagonista de glucagón) o mediante la inhibición (supresión) de la producción de glucagón representa en sí mismo una nueva posibilidad para la intervención de la diabetes y los trastornos metabólicos (Unson, C. G., et al., Peptides, 1989, 10, 1171; Parker, J. C, Diabetes, 2000, 49, 2079; Johnson, D. G., Science, 1982, 215, 1115; Ahn, J. M., JMC, 2001, 44 (9) , 1372-1379) .
La amida de GLP-1 (7-36) es un producto del gen del preproglucagón, que es secretado por las células L intestinales, en respuesta a la ingestión de alimento. La acción fisiológica de GLP-1 ha adquirido un interés considerable. El GLP-1 ejerce una acción múltiple por medio de la estimulación de la secreción de insulina a partir de las células º pancreáticas, de una manera dependiente de la glucosa (acción insulinotrópica) . El GLP-1 disminuye la concentración de glucagón en plasma circulante, inhibiendo su secreción (producción) desde las células a (Drucker D. J., Endocrinology, 2001, 142, 521-527) . El GLP-1 también exhibe propiedades como la
estimulación del crecimiento de las células º, la supresión del apetito, el retraso del vaciado gástrico y la estimulación de la sensibilidad a la insulina (Nauck, M. A., Horm. Metab. Res., 2004, 36, 852) . En la actualidad, se encuentran en diferentes fases de desarrollo clínico diversos análogos de GLP-1 y EX-4, tales como Liraglutida / NN2211 (Novo Nordisk; Fase-Ill; documento WO 1998 008871) , BIM 51077 (Ipsen; Fase-II; documento WO 2000 034331) , CJC-1131 (ConjuChem; Fase-II; documento WO 2000 069911) y ZP-10 (Zealand y Aventis; Fase-II; documento WO 2001 004156) (Nauck M. A., Regulator y Peptides, 2004, 115, 13) . Recientemente, BYETTA® (Exendina-4, AC 2933; documento US 5424286) , se ha lanzado al mercado de los Estados Unidos (Amylin y Lilly) . Sin embargo, todos los agonistas de GLP-1 existentes son liberados por medio de la ruta de administración parenteral, de manera que la aceptación por el paciente es un problema principal con la terapia basada en GLP-1 existente.
El sistema efector de los receptores de glucagón y GLP-1 es la enzima Adenilil Ciclasa (AC) . La interacción del agonista de glucagón o GLP-1 con los receptores de glucagón o GLP-1 (GLP-1 R) ocasiona respectivamente la activación de AC, que convierte el ATP en AMPc. El aumento del nivel de AMPc intracelular eleva la razón de ADP/ATP, iniciando de ese modo la despolarización celular (debido al cierre del canal de KATP) . El aumento del nivel de AMPc intracelular también activa la Proteína Quinasa (PK-A y PK-C) , que eleva la concentración de Ca2+ cistólico, por medio de la apertura del canal de Ca2+ de tipo L. Un aumento del Ca2+ intracelular conduce a la exocitosis de insulina, en las células º pancreáticas y de péptido glucagón en las células a (Fehmann, H.C., Endocr. Rev., 1995, 16, 390) .
El alineamiento de secuencias de GLP-1 y glucagón mostrado más abajo representa las relaciones estructurales primarias:
Glucagón: NH2-1HSQGTFTSD9YSKYLDSRRAQDFVQWLMNT29-CONH2 (Seq. ID No: 1)
GLP-1 (7-36) : NH2-1HAEGTFTSD9VSSYLEGQAAKEFIAWLVKGR30-CONH2 (Seq. ID No: 2)
Primeros 1-9 residuos N-terminales del péptido GLP-1, con la amida C-terminal:
NH3 (+) -1HAE (-) GTFTSD9 (-) -CONH2 (Seq. ID No: 3) : Carga neta Negativa
Primeros 1-9 residuos N-terminales del péptido glucagón, con la amida C-terminal:
NH3 (+) -1HSQGTFTSD9 (-) -CONH2 (Seq. ID No: 4) : Carga neta Neutra La abreviaturas de una sola letra para los aminoácidos se pueden encontrar en Zubay, G., Biochemistr y 2a ed., 1988, MacMillan Publishing, Nueva York, pág. 33.
Los péptidos GLP-1 nativos o sintéticos son metabolizados rápidamente por las enzimas proteolíticas, tales como la dipeptidil peptidasa-IV (DPP-IV) a un metabolito inactivo, limitando de ese modo el uso de GLP-1 como fármaco... [Seguir leyendo]
Reivindicaciones:
1. Un peptidomimético aislado que tiene una secuencia de fórmula (I) , incluyendo sus tautómeros, solvatos A-Z1-Z2-Z3-Z4-Z5-Z6-Z7-Z8-Z9-Z10-Z11-B
(I)
donde, A representa los grupos -NH-R1, R3-CO-, R3-O-CO- o R3-SO2-, donde R1 representa hidrógeno, o una cadena alquílica (C1-C10) lineal o ramificada opcionalmente sustituida; R3 se selecciona entre los grupos alquilo (C1-C10) lineal o ramificado, cicloalquilo (C3-C6) , arilo, heteroarilo o arilalquilo; B representa -COOR2, -CONHR2 o CH2OR2, donde R2 representa H, grupos opcionalmente sustituidos seleccionados entre un grupo alquilo (C1-C10) lineal o ramificado, grupos arilo o aralquilo; Z1 a Z11 representan aminoácidos naturales o innaturales, conectados entre sí mediante enlace amida, donde Z1 representa L-Histidina (H) , D-Histidina (dH) o Ácido urocánico (UA) ;
Z2 representa un aminoácido de origen natural o innatural seleccionado del grupo que comprende L-Serina (S) , D-Serina (dS) , L-Alanina (A) , D-Alanina (dA) , a-metilprolina (a-Me-Pro) , ácido a-amino-isobutírico (Aib) , ácido 1-aminociclopropanocarboxílico (ACP) , ácido 1-amino-ciclopentanocarboxílico (APP) ;
Z3 representa L-Glutamina (GIn; Q) , D-Glutamina (dQ) o compuestos de fórmula II (CNB o HfI) ;
Ácido 2-amino-4-ciano-butírico (CNB) Hexafluoroleucina (HfI)
Fórmula II
Z4 representa Glicina (G) o los aminoácidos innaturales ácido 1-aminociclopropanocarboxílico (ACP) o 25 ácido 1-amino-ciclopentanocarboxílico (APP) ;
Z5 representa un aminoácido de origen natural o no natural que comprende una cadena lateral hidroxilada; un Z5 preferido es L-Treonina (T) , D-Treonina (dT) , L-Alo-treonina (alo-Thr; alo-T) , D-alotreonina (d-alo-Thr; d-alo-T) ;
Z6 representa un aminoácido de origen natural o innatural con un carbono alfa disustituido que tiene dos cadenas laterales, donde cada una de ellas puede ser independientemente un grupo alquilo o arilo sustituido opcionalmente o un grupo aralquilo donde los sustituyentes se pueden seleccionar entre uno o más grupos alquilo o uno o más grupos halo;
Z7 y Z8 representan independientemente un aminoácido de origen natural o no natural que comprende una cadena lateral hidroxilada;
Z9 representa independientemente un aminoácido de origen natural o no natural que tiene una cadena lateral aminoacídica que comprende un grupo ácido; Z10 representa un aminoácido innatural L o D de fórmula III (a-c) ;
Z11 representa un aminoácido innatural L o D de fórmula IV (a-1) ;
2. Un peptidomimético de fórmula 1 como se reivindica en la reivindicación 1, donde Z6 representa los grupos alfametil-fenilalanina (-a-Me-Phe-) , alfa-metil-2-fluorofenilalanina (-a-Me-2F-Phe-) o alfa-metil-2, 6-difluorofenilalanina (-aMe-2, 6-F-Phe-) .
3. Un peptidomimético de fórmula 1 como se reivindica en la reivindicación 1, donde cada uno de Z7 y Z8 se selecciona entre treonina, serina, ácido 1-aminociclopropanocarboxílico.
4. Un peptidomimético de fórmula 1 como se reivindica en la reivindicación 1, donde Z9 se selecciona entre Ácido Laspártico (D) , Ácido D-aspártico (dD) o compuestos de fórmula II.
5. Un peptidomimético de fórmula 1 como se reivindica en la reivindicación 1, donde el grupo arilo se selecciona entre los grupos fenilo, naftilo, indanilo, fluorenilo o bifenilo; el grupo heteroarilo se selecciona entre los grupos piridilo, tienilo, furilo, imidazolilo, benzofuranilo;
6. Un peptidomimético de fórmula (I) de la reivindicación 1, donde el enlace amídico entre Z9 y Z10 o Z10 y Z11 o Z9-Z11 es adicionalmente N-metilado, representado por " (NMe) ".
7. Un peptidomimético de fórmula (I) de la reivindicación 1, donde el enlace amídico entre Z9 y Z10 o Z10 y Z11 o Z9-Z11 es adicionalmente un enlace tioamida.
8. Un peptidomimético de fórmula 1 de la reivindicación 7, donde el enlace tioamida adicional entre Z9 y Z10 o Z10 y Z11 o Z9-Z11 está reducido a un enlace "-CH2-".
9. Un peptidomimético de fórmula I de acuerdo con la reivindicación 1,
donde, A representa los grupos -NH-R1, R3-CO-, R3-O-CO- o R3-SO2-, donde R1 representa hidrógeno, o una cadena alquílica (C1-C10) lineal o ramificada opcionalmente sustituida; R3 se selecciona entre los grupos alquilo (C1-C10) lineal o ramificado, cicloalquilo (C3-C6) , arilo, heteroarilo o arilalquilo; B representa -COOR2, -CONHR2 o CH2OR2, donde R2 representa H, grupos opcionalmente sustituidos seleccionados entre los grupos alquilo (C1-C10) lineal o ramificado, arilo o aralquilo; Z1 representa L-Histidina (H) , D-Histidina (dH) oÁcido urocánico (UA) ; Z2 se selecciona entre L-Serina, D-Serina, L-Alanina, D-Alanina o ácido a-aminoisobutírico, ácido 1-aminociclopropanocarboxílico;
Z3 representa L-Glutamina (GIn; Q) , D-Glutamina (dQ) o compuestos de fórmula II (CNB o HfI) ;
Ácido 2-amino-4-ciano-butírico (CNB) Hexafluoroleucina (HfI)
Fórmula II
Z4 representa Glicina (G) o los aminoácidos innaturales ácido 1-aminociclopropanocarboxílico (ACP) o ácido 1-amino-ciclopentanocarboxílico (APP) ; Z5 representa L-Treonina (T) , D-Treonina (dT) , L-Alo-treonina (alo-Thr; alo-T) , D-alotreonina (d-alo-Thr; d-alo-T) ; Z6 representa fenilalanina (Phe; F) , alfa-metil-fenilalanina (-a-Me-Phe) , alfa-metil-2-fluorenilfenilalanina (-a-Me-2F-Phe-) , alfa-metil-2, 6-difluorofenilalanina (-a-Me-2, 6F-Phe-) ;
Z7 y Z8 se seleccionan independientemente entre Treonina, Serina, ácido 1-amino-ciclopropanocarboxílico (ACP) ; Z9 se selecciona entre ácido L-aspártico (D) , ácido D-aspártico (dD) o compuestos de fórmula II; Z10 representa un aminoácido innatural L o D de fórmula III (a-c) ;
Z11 representa un aminoácido innatural L o D de fórmula IV (a-1) ;
10. Un peptidomimético de fórmula I, de acuerdo con la reivindicación 1, seleccionado entre
11. Una composición farmacéutica que comprende los peptidomiméticos de fórmula (I) según se reivindica en cualquiera de las reivindicaciones anteriores, y uno o varios portadores farmacéuticamente aceptables adecuados.
12. Los peptidomiméticos de fórmula (I) o sus composiciones farmacéuticas según se reivindica en cualquiera de las 5 reivindicaciones anteriores, que actúan como antagonista del receptor de glucagón.
13. Los peptidomiméticos de fórmula (I) o sus composiciones farmacéuticas según se reivindica en cualquiera de las reivindicaciones anteriores, que actúan adicionalmente como agonista del receptor de GLP-1.
14. Los peptidomiméticos o sus composiciones farmacéuticas según se reivindica en cualquiera de las reivindicaciones anteriores, útiles para el tratamiento o la prevención de enfermedades causadas por la
hiperlipidemia, hipercolesterolemia, hiperglicemia, hiperinsulinemia, niveles elevados en sangre de ácidos grasos libres o glicerol, hipertrigliceridemia, curación de heridas, alteración de la tolerancia a la glucosa, resistencia a la leptina, resistencia a la insulina u otras complicaciones diabéticas.
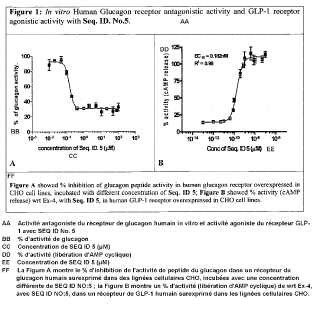
Figura 1. Actividad antagónica del receptor de Glucagón Humano in vitro y actividad agonística del receptor de GLP-1 con el Seq. ID. No. 5. La Figura A muestra el % de inhibición de la actividad del péptido glucagón en receptor de glucagón humano expresado en exceso en líneas de células CHO, incubadas con diferente concentración de Seq. ID. No. 5; La Figura B muestra el % de actividad (liberación de AMPc) wrt Ej-4, con Seq. ID. 5, en receptor de GLP-1 humano expresado en exceso en líneas de células CHO.Figura 2. Ejemplos de aminoácidos protegidos ortogonalmente utilizados en la síntesis de péptidos en fase sólida basada en Fmoc (SPPS) de peptidomiméticos.
Figura 4: Reducción de glucosa in vivo en ratones C57, con Seq. ID No. 38, después de la administración intraperitoneal (i.p.= (curva dosis respuesta (CDR) )
Figura 5: Reducción de glucosa in vivo en ratones C57, con Seq. ID No. 38, (después de la administración oral (po) (curva dosis respuesta (CDR) )
Figura 6: Reducción de glucosa in vitro en ratones db/db, con Seq. ID No. 38, después de la administración oral (po)
Figura 7: Niveles de insulina en suero después de una única administración oral de vehículos / compuestos de ensayo (Seq. ID No. 10, 20 y 25) , en ratones C57BL/6J (in vivo) .
Patentes similares o relacionadas:
Agonistas del receptor de glucagón, del 24 de Junio de 2020, de ELI LILLY AND COMPANY: Un compuesto agonista del receptor de glucagón que comprende la fórmula: YX1QGTFX2SDYSKYLDX3KKAX4EFVX5WLLEX6X7 en la que X1 es Aib; X2 es T o L; X3 es Aib; […]
Profármacos de GLP-1, del 17 de Junio de 2020, de NOVO NORDISK A/S: Un compuesto de GLP-1 de la fórmula general I: R1 -(NHXaa1)-Xaa2-(OHis)-(péptido GLP-1) (Fórmula I) en donde el péptido GLP-1 es […]
Método para preparar semaglutida, del 13 de Mayo de 2020, de Hybio Pharmaceutical Co., Ltd: Método de preparación de semaglutida, que comprende las etapas de: etapa 1: acoplar Gly a una resina mediante síntesis en fase sólida para obtener Gly-resina; y […]
Coagonistas estables del receptor de GLP-1/glucagón basados en GLP-1, del 6 de Mayo de 2020, de NOVO NORDISK A/S: Un derivado de GLP-1 caracterizado por tener la fórmula: amida de Nε34-[2-[2-[2-[[2-[2-[2-[[(4S)-4-carboxi-4- [[(4S)-4-carboxi-4-(17- carboxiheptadecanoilamino)butanoil]amino]butanoil]amino]etoxi]etoxi]acetil]amino]etoxi]etoxi]acetil]- […]
Una composición para el tratamiento de la diabetes que comprende un análogo de oxintomodulina, del 11 de Marzo de 2020, de HANMI PHARM. CO., LTD.: Una composición para su uso en la prevención o el tratamiento de la diabetes, la composición comprende un conjugado de análogo de oxintomodulina como un ingrediente […]
Modificador de exenatida y uso del mismo, del 12 de Febrero de 2020, de BrightGene Bio-Medical Technology Co., Ltd: Un modificador de exenatida o sales farmacéuticamente aceptables del mismo que tienen actividad del agonista del receptor de GLP-1, como se muestra en la fórmula (I): (Ex-4)-L-Y […]
Derivados de GLP-1 doble-acilados, del 4 de Diciembre de 2019, de NOVO NORDISK A/S: Un derivado de un análogo de GLP-1, cuyo análogo comprende un primer residuo de K en una posición correspondiente a la posición 26 de GLP-1 […]
Análogos de glucagón, del 13 de Noviembre de 2019, de ZEALAND PHARMA A/S: Un compuesto que tiene la fórmula: R1-X-Z-R2 en donde R1 es H (es decir, hidrógeno), alquilo C1-4, acetilo, formilo, benzoílo o trifluoroacetilo; […]