USO DE INHIBIDORES DE LA TRANSACTIVACIÓN DE EGFR EN CÁNCER HUMANO.
Uso de un compuesto que es capaz de inhibir la activación de un receptor del factor de crecimiento de la familia EGFR para la fabricación de un agente para la prevención o el tratamiento de procesos seleccionados de proliferación de células,
migración de células, invasividad y anti-apoptosis en un cáncer, que está asociado con una transducción incrementada de señales mediada por proteína G y que se selecciona de cáncer de colon, riñones, vejiga, próstata, mama, pulmones u ovarios, en donde el compuesto es un anticuerpo que es capaz de unirse a pro-HB-EGF y, con ello, bloquea su procesamiento
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2003/002361.
Solicitante: MAX-PLANCK-GESELLSCHAFT ZUR FORDERUNG DER WISSENSCHAFTEN E.V..
Nacionalidad solicitante: Alemania.
Dirección: HOFGARTENSTRASSE 8 80539 MUNCHEN ALEMANIA.
Inventor/es: ULLRICH, AXEL, SCHÄFER,Beatrix, FISCHER,Oliver, GSCHWIND,Andreas, LESERER,Michael.
Fecha de Publicación: .
Fecha Solicitud PCT: 7 de Marzo de 2003.
Clasificación Internacional de Patentes:
- A61K38/16B
- A61K38/18A
- A61K38/48N
- A61K38/55 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Inhibidores de proteasas.
Clasificación PCT:
- A61K31/16 A61K […] › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › Amidas, p. ej. ácidos hidroxámicos.
- A61K31/381 A61K 31/00 […] › teniendo ciclos de cinco eslabones.
- A61K38/16 A61K 38/00 […] › Péptidos que tienen más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados.
- A61K38/18 A61K 38/00 […] › Factores de crecimiento; Reguladores de crecimiento.
- A61K38/48 A61K 38/00 […] › que actúan sobre enlaces peptídicos (3.4).
- C07K16/28 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 16/00 Inmunoglobulinas, p. ej. anticuerpos mono o policlonales. › contra receptores, antígenos celulares de superficie o determinantes celulares de superficie.
Clasificación antigua:
- A61K31/16 A61K 31/00 […] › Amidas, p. ej. ácidos hidroxámicos.
- A61K31/381 A61K 31/00 […] › teniendo ciclos de cinco eslabones.
- A61K38/16 A61K 38/00 […] › Péptidos que tienen más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados.
- A61K38/18 A61K 38/00 […] › Factores de crecimiento; Reguladores de crecimiento.
- A61K38/48 A61K 38/00 […] › que actúan sobre enlaces peptídicos (3.4).
- C07K16/28 C07K 16/00 […] › contra receptores, antígenos celulares de superficie o determinantes celulares de superficie.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia, Ex República Yugoslava de Macedonia, Albania.
PDF original: ES-2359136_T3.pdf




Fragmento de la descripción:
La presente invención se refiere al uso de un compuesto que es capaz de inhibir la activación de receptores del factor de crecimiento de la familia EGFR para la prevención o el tratamiento de procesos asociados con una transducción incrementada de señales mediada por proteína G.
La señalización a través de tirosina quinasas (RTK- siglas en inglés) receptoras está implicada en la regulación de procesos celulares fundamentalmente importantes, y se ha demostrado que su sobre-regulación está relacionada con enfermedades hiperproliferativas tales como el cáncer. Receptores acoplados a proteína G (GPCR – siglas en inglés) constituyen el grupo mayor de receptores de la superficie celular que controlan múltiples cascadas de señalización y su resultado biológico. Recientemente, se ha descrito una interferencia entre los miembros de las dos familias de receptores que conecta a multitud de diferentes estímulos a través de ligandos de GPCR con la capacidad de señalización de RTKs tales como el receptor del factor de crecimiento epidérmico (EGFR- siglas en inglés), véase, p. ej. el documento WO 01/12182. El mecanismo de señalización que implica desprenderse de precursores del factor de crecimiento por parte de una metaloproteasa ha conducido a los autores de la invención a proponer el modelo de la vía de señal de paso por la membrana triple (TMPS – siglas en inglés).
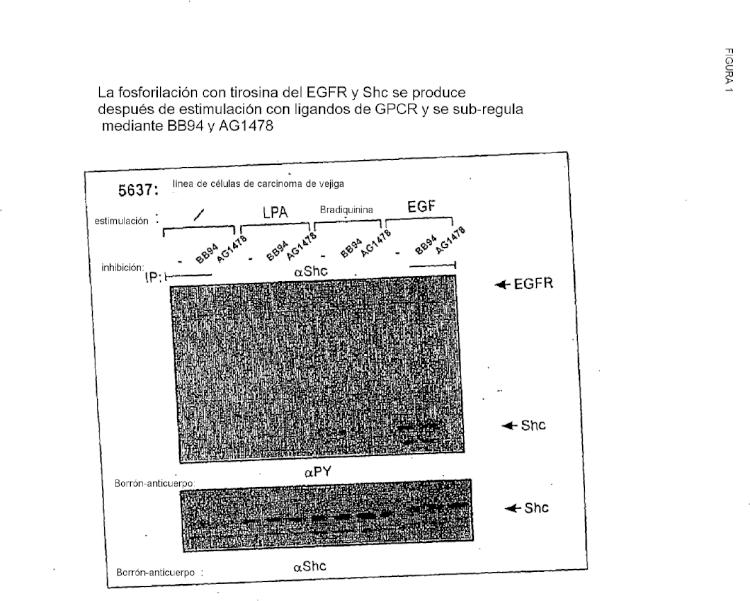
El objetivo de los autores de la invención era investigar los procesos fisiológicos que son regulados por la vía de TMPS y su importancia en fenómenos patofisiológicos tales como el progreso neoplástico. Por lo tanto, los autores de la invención rastrearon líneas de células cancerígenas humanas en cuanto a la transactivación de EGFR mediante estimulación con ligandos de GPCR, así como la inhibición de metaloproteasas. Específicamente, dichos autores investigaron episodios estimulados por el factor de crecimiento en la transducción de señales y en procesos fisiológicos definidos. Sus resultados demuestran que los episodios de fosforilación de EGFR así como de señalización aguas abajo tales como el reclutamiento de proteínas adaptadoras y la fosforilación de la proteína quinasa activada por mitógenos se produce después de la estimulación con ligandos de GPCR y son sub-regulados por el inhibidor de metaloproteasa batimastat. Adicionalmente, la fosforilación basal del EGFR es sensible a batimastat. Además, los autores de esta invención revelaron que la transactivación de EGRF es parte del sistema regulador que modula el progreso del ciclo celular y la proliferación de las células. La vía TMPS es también capaz de fomentar la anti-apoptosis y la migración e invasividad celular.
Mientras que las células somáticas requieren señales mitogénicas externas, las células cancerígenas se caracterizan por un comportamiento en el crecimiento anormal debido a la producción autocrina de factores mitogénicos. Dado que muchos de éstos son ligandos de GPCR, la transactivación de EGFR constituye un mecanismo para la progresión del cáncer mediante la des-regulación de la proliferación de células y la supresión de la muerte de las células. Por lo tanto, la inhibición de esta vía es una estrategia prometedora para el tratamiento del cáncer.
Así, una materia objeto descrita es el uso de un compuesto que es capaz de inhibir la activación de un receptor del factor de crecimiento de la familia EGFR para la fabricación de un agente para la prevención o el tratamiento de procesos seleccionados de la proliferación celular, la migración de células, la invasividad y la anti-apoptosis en un trastorno, que está asociado con una transducción incrementada de señales mediada por proteína G y que se selecciona de cáncer de colon, riñones, vejiga, próstata, mama, pulmones u ovarios, en donde el compuesto es un anticuerpo que es capaz de unirse a pro HB-EGF.
Sorprendentemente, se encontró que la inhibición de la activación del receptor del factor de crecimiento provocada por una transducción incrementada de señales mediada por proteína G conduce a una inhibición del progreso del cáncer, particularmente a la migración de células y a la invasividad, así como a una inhibición de la anti-apoptosis. Así, inhibidores de la activación del receptor del factor de crecimiento inducida por GPCR son adecuados para la fabricación de medicamentos para la prevención o el tratamiento de indicaciones específicas de enfermedades hiper-proliferativas asociadas con la proliferación celular, la migración de células, la invasividad y/o la antiapoptosis y para restablecer el control de estos fenómenos en las células u organismos tratados, respectivamente.
El receptor del factor de crecimiento es EGFR u otro miembro de la familia EGFR tal como HER-2, HER-3 o HER
4.
El compuesto puede actuar sobre un precursor del ligando del receptor del factor de crecimiento, que es preferiblemente una molécula asociada a la membrana. El precursor del ligando del factor de crecimiento es proHB-EGF, el cual es escindido a HB-EGF por parte de una proteasa.
Un ejemplo de un compuesto que actúa sobre un precursor del ligando del receptor del factor de crecimiento es CRM 197, una forma catalíticamente inactiva de la toxina difteria que se une específicamente a pro-HB-EGF y que es capaz de bloquear el procesamiento de pro-HB-EGF. Un ejemplo adicional es un anticuerpo que es capaz de unirse a pro-HB-EGF y que, con ello, bloquea su procesamiento.
Debe señalarse que la presente invención se refiere a una inhibición fijada como objetivo de vías de señales celulares “aguas abajo” de la transactivación de EGFR en células cancerígenas, particularmente en células cancerígenas humanas.
El trastorno a tratar o prevenir está asociado con y es provocado preferiblemente por una transducción incrementada de señales mediada por proteína G. Esta transducción incrementada de señales mediada por proteína G puede estar asociada con o ser provocada por un incremento patológico en la actividad de una proteína G y/o un receptor acoplado a proteína G (GPCR). Debe señalarse que los trastornos que son prevenidos o tratados de acuerdo con la presente invención pueden delimitarse de otros trastornos hiperproliferativos que tienen una expresión potenciada del receptor del factor de crecimiento, debido a que tiene lugar una transactivación de la expresión del receptor del factor de crecimiento a través de las vías de señales de la proteína G. El trastorno es un tumor de colon, riñones, vejiga, próstata, mama, pulmones u ovarios.
Composiciones farmacéuticas adecuadas para su uso incluyen composiciones en donde los ingredientes activos están contenidos en una cantidad eficaz para conseguir su fin pretendido. Una dosis terapéuticamente eficaz se refiere a la cantidad del compuesto que resulta para aliviar los síntomas o prolongar la supervivencia de un paciente. La toxicidad y la eficacia terapéutica de compuestos de este tipo se puede determinar mediante procesos farmacéuticos convencionales en cultivos de células o animales experimentales, p. ej. para determinar la DL50 (la dosis letal para el 50% de la población) y la DE50 (la dosis terapéuticamente eficaz en el 50% de la población). Para cualquier compuesto utilizado en el método de la invención, la dosis terapéuticamente eficaz se puede estimar inicialmente a partir de ensayos en cultivos de células. Por ejemplo, se puede formular una dosis en modelos con animales para lograr un intervalo de concentraciones circulante que incluye la CI50 según se determina en el cultivo celular (es decir, la concentración del compuesto de ensayo que consigue una inhibición semi-máxima de la actividad del receptor del factor del crecimiento). Una información de este tipo se puede utilizar para determinar con mayor precisión dosis útiles en seres humanos. La relación de dosis entre los efectos tóxicos y terapéuticos es el índice terapéutico, y se puede expresar como la relación entre DL50 y DE50. Se prefieren compuestos que exhiban altos índices terapéuticos. La formulación, la vía de administración y la dosificación exactas se pueden elegir por parte del médico individual a la vista del estado del paciente (véase, p. ej., Fingl et al., 1975, en “The Parmacological Basis of Therapeutics”, Cap. 1, pág. 1). La cantidad y el intervalo de dosificación se pueden ajustar individualmente para proporcionar niveles en plasma del resto activo que sean suficientes para mantener los efectos moduladores del receptor, o la concentración eficaz mínima (MEC – siglas en inglés). La MEC variará... [Seguir leyendo]
Reivindicaciones:
1. Uso de un compuesto que es capaz de inhibir la activación de un receptor del factor de crecimiento de la familia EGFR para la fabricación de un agente para la prevención o el tratamiento de procesos seleccionados de
5 proliferación de células, migración de células, invasividad y anti-apoptosis en un cáncer, que está asociado con una transducción incrementada de señales mediada por proteína G y que se selecciona de cáncer de colon, riñones, vejiga, próstata, mama, pulmones u ovarios, en donde el compuesto es un anticuerpo que es capaz de unirse a pro-HB-EGF y, con ello, bloquea su procesamiento.
10 2. El uso de la reivindicación 1, en donde el receptor del factor de crecimiento es EGFR.
3. El uso de cualquiera de las reivindicaciones 1 a 2, en donde el agente es una composición farmacéutica que comprende al menos un soporte, diluyente y/o adyuvante farmacéuticamente aceptable.
15 4. El uso de una cualquiera de las reivindicaciones 1 a 3, en donde el cáncer es un cáncer humano.
Patentes similares o relacionadas:
INHIBIDORES DE LA CASPASA 1 PARA USO EN EL TRATAMIENTO DE LA ANEMIA, del 2 de Julio de 2020, de UNIVERSIDAD DE MURCIA: La presente invención se refiere a una composición que comprende al menos un inhibidor de caspasa-1 para su uso en un método de tratamiento de una enfermedad […]
Composición farmacéutica para el tratamiento o la paliación de pacientes con cáncer ancianos o en estado terminal, del 6 de Mayo de 2020, de Delta-Fly Pharma, Inc: Una composición farmacéutica para su uso en el tratamiento de cáncer, que comprende, como principio activo, ácido (2S)-2-(2S,3R)-3-amino-2-hidroxi-4-fenilbutanoilamino]-4-metilpentanoico […]
Nuevo tripéptido, del 19 de Febrero de 2020, de SUNSTAR INC.: Tripéptido que consiste en Leu-Arg-Ala. Composición que comprende el tripéptido según la reivindicación 1.
Preparaciones enzimáticas estables y métodos de uso de las mismas, del 6 de Noviembre de 2019, de RAMOT AT TEL AVIV UNIVERSITY LTD.: Una composición que comprende un concentrado no activo de una tiol-proteasa, siendo dicho concentrado un concentrado hipertónico y comprendiendo al menos 20 mg/ml de una […]
Agente para prevenir y/o tratar dolor neuropático periférico causado por un fármaco anticancerígeno, del 26 de Junio de 2019, de Kinki University: Un medicamento que comprende trombomodulina como principio activo para uso en el tratamiento profiláctico y/o terapéutico de dolor neuropático periférico inducido por quimioterapia.
Polipéptidos de fusión de serpina y métodos de uso de los mismos, del 19 de Junio de 2019, de Inhibrx, LP: Una proteína de fusión aislada que comprende al menos un polipéptido de alfa-1 antitripsina humana (AAT) que comprende una secuencia de aminoácidos […]
Uso de polipéptidos de aprotinina como portadores en conjugados farmacéuticos, del 5 de Junio de 2019, de ANGIOCHEM INC: Un conjugado, o una sal farmacéuticamente aceptable de este, que comprende: (a) un polipéptido que comprende un análogo biológicamente activo de […]
Terapia de combinación que usa inmunoglobulina e inhibidor de C1, del 31 de Mayo de 2019, de CSL BEHRING GMBH: Una composición para su uso en la prevención, el tratamiento o la reducción de los efectos de daño por inflamación o lesión por reperfusión tras isquemia cerebral, […]