MÉTODOS DE GENERACIÓN DE MATRICES DE EXPRESIÓN DE PROTEÍNAS Y EL USO DE LAS MISMAS EN DETECCIÓN RÁPIDA.
Un método para generar una selección de proteínas que consiste en:
(a)proporcionar un conjunto de moléculas de ADN codificadoras de proteínas que se etiquetan bien en la terminal N o C con una porción de molécula marcadora; (b)expresar las proteínas individuales etiquetadas en un formato especialmente separado; (c) purificar e inmovilizar cada proteína etiquetada en un formato espacialmente definido para producir una selección de proteínas sobre un soporte sólido, y de este modo las interacciones específicas entre la etiqueta y el soporte sólido se usan tanto en la purificación como en la inmovilización
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/GB2001/000395.
Solicitante: SENSE PROTEOMIC LIMITED.
Nacionalidad solicitante: Reino Unido.
Dirección: BEGBROKE SCIENCE PARK SANDY LANE YARNTON OXFORD OXFORDSHIRE OX5 REINO UNIDO.
Inventor/es: MULDER,MICHELLE,ANNE, SAMADDAR,MITALI, KOZLOWSKI,ROLAND,Z.,SENSE PROTEOMIC LTD, SUTHERLAND,JOHN,DAVID, BLACKBURN,JONATHON,MICHAEL,SENSE PROTEOMIC LIMITED.
Fecha de Publicación: .
Fecha Solicitud PCT: 31 de Enero de 2001.
Fecha Concesión Europea: 11 de Agosto de 2010.
Clasificación PCT:
- B01J19/00 TECNICAS INDUSTRIALES DIVERSAS; TRANSPORTES. › B01 PROCEDIMIENTOS O APARATOS FISICOS O QUIMICOS EN GENERAL. › B01J PROCEDIMIENTOS QUÍMICOS O FÍSICOS, p. ej. CATÁLISIS O QUÍMICA DE LOS COLOIDES; APARATOS ADECUADOS. › Procedimientos químicos, físicos o físico-químicos en general; Aparatos apropiados.
- C07K1/00 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › Procedimientos generales de preparación de péptidos.
- G01N33/543 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › con un soporte insoluble para la inmovilización de compuestos inmunoquímicos.
- G01N33/68 G01N 33/00 […] › en los que intervienen proteínas, péptidos o aminoácidos.
Clasificación antigua:
- C12N15/00 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K).
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia, Ex República Yugoslava de Macedonia, Albania.
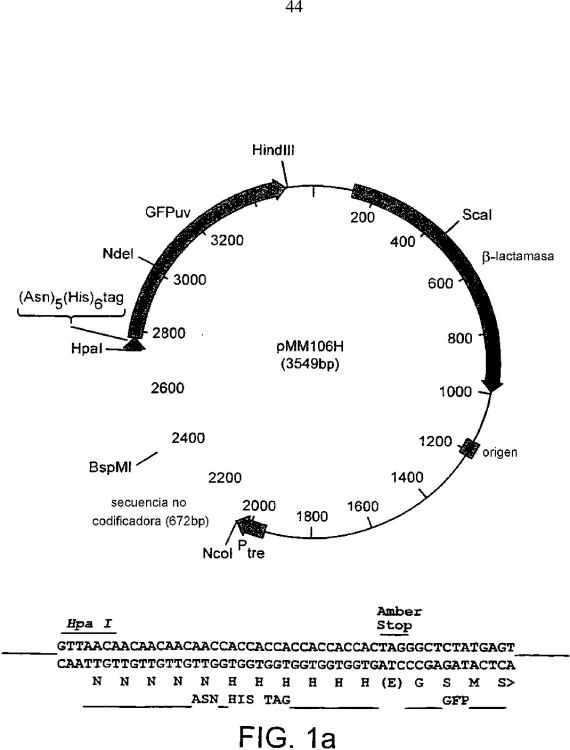
Fragmento de la descripción:
La presente invención hace referencia a nuevos métodos para generar selecciones de expresión de proteínas, así como el uso de dichas selecciones en rápidas revisiones médicas.
Los proyectos relativos al mapeo genómico están revolucionando el proceso de descubrimiento de objetivos terapéuticos y con ello el proceso de descubrimiento de fármacos. A medida que se identifican nuevos objetivos terapéuticos, el análisis de una elevada producción de bibliotecas químicas existentes y combinatorias sugerirá muchos compuestos principales potenciales que son activos contra estos objetivos. Claramente, no resulta económico perseguir todos los compuestos principales incluso a través de ensayos clínicos en la primera fase; sin embargo, actualmente no existen métodos rápidos para evaluar tales compuestos principales en términos de sus perfiles de posible actividad contra todas las proteínas en el organismo. Si estuviera disponible, este método permitiría potenciales perfiles de toxicología de todos los compuestos principales que van a analizarse en una primera fase y esta información mejoraría en gran medida el proceso de decidir qué compuestos buscar y qué compuestos dejar de lado.
Existe una necesidad complementaria en la industria farmacéutica por identificar todos los objetivos de fármacos existentes (ya disponibles en el mercado o aún en desarrollo) y, a partir de ello, definir su mecanismo de acción. La disponibilidad de esta información facilitará enormemente el proceso de conseguir aprobación reguladora para nuevos fármacos ya que está muy claro que los cuerpos reguladores ahora consideran que un conocimiento del mecanismo de acción es de primordial importancia. Además, este tipo de información permitía diseñar mejores fármacos de segunda generación. Esto se deduce porque la mayoría de los fármacos tienen al menos efectos secundarios menores, que probablemente son el resultado de combinar el fármaco o un metabolito del mismo con objetivos no deseados; todas estas proteínas objetivos necesitan ser identificadas con el fin de definir los criterios necesarios para diseñar fármacos mejorados. Sin embargo, en la actualidad, no existen métodos simples para generar esta información y un gran número de fármacos potenciales que cuestan millones de dólares se quedan por el camino simplemente por falta de conocimiento del objetivo de acción.
Las interacciones proteína-proteína se están reconociendo cada vez más por ser de vital importancia al determinar las respuestas celulares para tensiones tanto internas como externas. Por lo tanto, las interacciones específicas proteína-proteína representan objetivos potenciales para la intervención mediada por fármacos en infecciones y otros estados de enfermedad. Actualmente, el ensayo de doble híbrido en levadura es el único método fiable para evaluar las interacciones proteína-proteína pero los ensayos in vivo de este tipo no serán fácilmente compatibles incluso en un formato de baja productividad con la identificación de agonistas o antagonistas específicos de interacciones proteína-proteína. Las selecciones de expresión proteómica funcional, o “chips de proteoma”, permitirán la especificidad de las interacciones proteína-proteína y la especificidad de cualquier efecto mediado por el fármaco que se determinará en un formato in vitro. Por lo tanto, tendrán un enorme potencial porque simplemente revolucionarán esta área de investigación.
Un modo en el que las selecciones proteómicas funcionales podrían generarse es para individualmente clonar, expresar, purificar e inmovilizar todas las proteínas expresadas en el proteoma específico. Sin embargo, aquí una importante consideración inicial concierne el tamaño absoluto del genoma de interés junto con las consideraciones sobre la disponibilidad de datos secuenciales para el genoma completo. A modo de ilustración de estos puntos, un genoma bacteriano habitual tiene ~5Mbp y ahora se han secuenciado completamente un pequeño número (por ejemplo Helicobacter pylori, Escherichia coli y Mycobacterium tuberculosis); los genomas fúngicos tienen normalmente ~40Mbp, genomas de mamíferos en ~3Gbp y genomas de plantas en ~10GBP. Las estimaciones actuales establecen que la secuencia de genoma humano acabará alrededor de 2003, aunque se cuestiona que mucha de esta información llegue al dominio público. Claramente, no resulta nada práctico esperar que los genomas de elementos diferentes a los organismos que sirven de modelo representativo se encontrarán disponibles en un plazo de tiempo real, ya que desde la perspectiva de proteómica funcional, los organismos modelos solamente tienen un valor limitado. De modo que, mientras en principio durante los próximos cuatro años puede ser posible diseñar y sintetizar cebadores para clonar cada uno de los ~100,000 genes en el genoma humano a partir de bibliotecas de ADN, en la práctica resultará muy caro (el coste sólo de los cebadores ronda varios millones de dólares) y un proceso enormemente laboriosos, incluso si los datos secuenciales necesarios están disponibles.
Pero qué ocurre con aquellos organismos farmacéuticamente relevantes para los que no se dispondrá datos secuenciales completos? La proteómica funcional no puede simplemente ignorarlos de modo que cuáles son las alternativas? En principio, las bibliotecas de expresión de cADN pueden usarse junto con una inmovilización no específica para crear una selección de proteínas, pero esta tecnología es significativamente limitada debido al hecho de que la inmovilización no específica normalmente se asocia con la pérdida de función porque afecta al pliegue de la proteína. Además, todas las proteínas de células huéspedes también se inmovilizarán lo que, en el mejor de los casos, reducirá notablemente los radios señal-a-ruido, y en el peor de los casos, dará como resultado una confusión de resultados positivos. Por lo tanto, la habilidad para crear una selección de proteoma funcional en el que las proteínas individuales se inmovilicen específicamente y se purifiquen a través de un motivo o etiqueta sin afectar la función y sin requerir conocimientos de la secuencia completa del genoma representará un gran avance en el campo de proteómica funcional.
Nosotros hemos desarrollado en la actualidad una nueva técnica que soluciona los problemas anteriormente descritos proporcionando una metodología que permite que cada proteína en un proteoma se etiquete con un marcador común en una posición definida en la proteína sin requerir ningún conocimiento previo sobre la secuencia de ADN de los genes correspondientes. Esta “etiqueta” puede usarse a continuación para dar una similitud y especificidad a la inmovilización que se realiza hacia abajo y a los procedimientos de purificación, lo que a su vez permite la creación de selecciones espacialmente definidas en las que se muestran cientos de proteínas de un proteoma determinado.
Hay que tener en especial consideración el hecho relacionado con el posicionamiento precios de la “etiqueta”. Si la etiqueta se inserta dentro del marco en un gen pero en una posición no definida y arbitraria, existe el riesgo de que la proteína resultante etiquetada se trunque de manera no definida y en la mayoría de los casos se destruirá el correcto pliegue, y por ello la función. La metodología aquí descrita salva este problema insertando la etiqueta inmediatamente después del codón de inicio e inmediatamente antes del codón de parada de un gen determinado de modo que las proteínas individuales etiquetadas y de longitud complete se plieguen correctamente y puedan de este modo conservar la función cuando se inmovilizan específicamente en la selección.
Debido a que cada proteína en la selección será completamente funcional, a continuación las selecciones pueden analizarse directamente para identificar los objetivos de los fármacos u otras moléculas biológicamente relevantes. La definición espacial de las selecciones permitirá que el fenotipo de cada proteína pueda relacionarse directamente con su genotipo posibilitando así la identificación de “blancos” o “impactos”.
WO 00/04382 describe selecciones de proteínas, que incluyen proteínas que se inmovilizan en un soporte sólido por medio de una etiqueta que puede localizarse en la terminal N o C. Las proteínas se purifican y a continuación se imprimen en una película orgánica. WO 99/39210 describe la generación de una selección secundaria de anticuerpos a partir de una selección primaria de proteínas. Las proteínas se purifican y a continuación se inmovilizan en la selección por...
Reivindicaciones:
1ª. – Un método para generar una selección de proteínas que consiste en:
(a)proporcionar un conjunto de moléculas de ADN codificadoras de proteínas que se etiquetan bien en la terminal N o C con una porción de molécula marcadora;
(b)expresar las proteínas individuales etiquetadas en un formato especialmente separado;
(c)purificar e inmovilizar cada proteína etiquetada en un formato espacialmente definido para producir una selección de proteínas sobre un soporte sólido, y de este modo las interacciones específicas entre la etiqueta y el soporte sólido se usan tanto en la purificación como en la inmovilización.
2ª. El método de la reivindicación 1, donde la porción de molécula marcadora es una secuencia de péptido seleccionada del grupo consistente en:
(a)una etiqueta hexa-histidina; (b)una proteína completa o dominio de proteína;
(c)un epítope de anticuerpo; (d)un imitador de biotina; y (e)dominio de proteína que se enlaza con maltosa. 3ª. El método de las reivindicaciones previas, donde la porción
de molécula marcadora se modifica post-translacionalmente. 4ª. El método de la reivindicación 3, done la modificación posttranslacional incluye la adición de una biotina o molécula lípida.
5ª. – El método de las reivindicaciones anteriores, donde las proteínas etiquetadas se pliegan correctamente para mantener la función.
6ª. El método de las reivindicaciones previas, donde las proteínas etiquetadas tienen longitud completa.
7ª. – El método de cualquiera de las reivindicaciones previas, donde las moléculas cADN que codifican proteínas etiquetadas se producen mediante un método que consiste en la inserción de una secuencia adicional y conocida de ADN que codifica la porción de molécula marcadora bien inmediatamente tras un codón de parada o
bien inmediatamente antes de un codón de parada presente en dichas moléculas de ADN que consiste en los siguientes pasos: (a)generar un conjunto de eliminaciones anidadas a partir de dichas moléculas de ADN; (b)alinear y ligar con el conjunto de eliminaciones anidadas un primer y un segundo conjunto de oligonucleótidos; en los que
(i) la secuencia o secuencia complementaria de uno o más de los tres posibles codones de parada está representado en la mezcla del primer conjunto de oligonucleótidos, y
(ii) la secuencia o secuencia complementaria de uno o más de los tres principales codones de parada está representado en la mezcla del segundo conjunto de oligonucleótidos
(c)amplificar de manera específica los productos ligados mediante una reacción de extensión con cebador utilizando un cebador de oligonucleótido elegido por ser complementario con el primer y segundo conjunto de oligonucleótidos.
8ª. – El método de cualquiera de las reivindicaciones 1 a 6, que además comprende los pasos de poner en contacto uno más compuestos de la prueba con la selección de proteínas y medir el enlace de uno o más compuestos con las proteínas en la selección, cribando de este modo uno o más compuestos para actividad biológica.
9ª. – El método de cualquiera de las reivindicaciones 1 a 6, que además comprende el paso de poner en contacto una o más proteínas, p. ej. Un receptor de superficie celular, con la selección de proteínas y medir el enlace de una o más proteínas específicas con las proteínas de la selección, cribando de este modo una o más proteínas para interacción específicas proteína-proteína.
10ª. – El método de cualquiera de las reivindicaciones 1 a 6, que además comprende el paso de poner en contacto sondas ácidas con la selección de proteínas, y medir el enlace de las sondas con las proteínas, cribando de este modo una o más proteínas para interacciones específicas proteína-ácido nucleico.
11ª. El método de cualquiera de las reivindicaciones 1 a 6, que además comprende el paso de poner en contacto la selección de proteínas con una biblioteca de anticuerpos, de modo que una o más proteínas en la selección de proteínas está ligada con al menos un anticuerpo de la biblioteca de anticuerpos, retirando aquellos anticuerpos que no estén ligados, e inmovilizar aquellos anticuerpos ligados a las proteínas en la selección de proteínas, produciendo de este modo una selección de anticuerpos.
Patentes similares o relacionadas:
Método de determinación de la presencia y/o cantidad de moléculas diana, del 22 de Julio de 2020, de Canopy Biosciences, LLC: Método para el análisis de células individuales en una muestra de sangre mediante la determinación de la presencia y/o cantidad de una o más moléculas […]
Kit de reactivos utilizado para detectar gastrina-17 y método de preparación y aplicación para el kit de reactivos, del 15 de Julio de 2020, de Shenzhen New Industries Biomedical Engineering Co., Ltd: Un kit para detectar gastrina-17, caracterizado porque comprende un componente A y un componente B, en donde el componente A es un primer […]
Un sustrato para inmovilizar sustancias funcionales y un método para preparar las mismas, del 15 de Julio de 2020, de Temasek Polytechnic: Un sustrato sólido que tiene compuestos dispuestos sobre el mismo, en donde se inmoviliza una molécula funcional sobre los compuestos, teniendo cada compuesto una cadena que […]
Análisis biológico autónomo de alta densidad, del 1 de Julio de 2020, de BioFire Diagnostics, LLC: Recipiente para realizar reacciones de amplificación en un sistema cerrado que comprende una porción flexible que tiene una serie de blísteres […]
Chip de análisis y aparato de análisis de muestras, del 1 de Julio de 2020, de Takano Co., Ltd: Un chip de análisis que comprende: un sustrato conformado sustancialmente en forma de disco; un puerto de inyección formado […]
Dispositivo para la detección de analitos, del 1 de Julio de 2020, de TECHLAB, INC.: Un dispositivo para detectar por lo menos una sustancia de interés en una muestra líquida, comprendiendo el dispositivo: (a) una unidad que […]
Estructuras para controlar la interacción de luz con dispositivos microfluídicos, del 3 de Junio de 2020, de Opko Diagnostics, LLC: Un sistema de ensayo múltiplex que comprende: un artículo que soporta ensayos en fase sólida, comprendiendo dicho artículo un sustrato plano rígido y comprendiendo […]
Uso de un estándar para la detección de agregados de proteínas de una enfermedad por plegamiento incorrecto de proteínas, del 27 de Mayo de 2020, de FORSCHUNGSZENTRUM JULICH GMBH: Uso de un estándar, que comprende una nanopartícula inorgánica con un tamaño de 2 a 200 nm, en cuya superficie ya sea mediante i) ácido carboxílico-espaciador-maleimida […]