INHIBICIÓN DE LA EXPRESIÓN GÉNICA MEDIADA POR INTERFERENCIA DE ARN USANDO UN ÁCIDO NUCLEICO DE INTERFERENCIA CORTO (ANIC).
Una molécula de ácido nucleico de interferencia corto (ANic) modificada químicamente que regula negativamente la expresión de un gen diana por interferencia de ARN (iARN),
en la que: (a) el ANic comprende una cadena con sentido y una cadena antisentido distinta, en el que dicha cadena antisentido comprende una secuencia que es complementaria al ARN del gen diana, y en el que la cadena con sentido comprende una secuencia de nucleótidos que es complementaria a la cadena antisentido; (b) cada cadena de la molécula de ácido nucleico tiene independientemente una longitud de 18 a 24 nucleótidos y el dúplex de ANic comprende de 17 a 23 pares de bases; (c) 10 o más nucleótidos de pirimidina de la cadena del ANic con sentido y/o antisentido se modifican químicamente con nucleótidos 2'-desoxi, 2'-O-metilo o 2'-desoxi-2'-fluoro, estando presentes uno o más enlaces internucleotídicos de fosforotioato y/o, una molécula de protección terminal en el extremo 3', el extremo 5' o en ambos extremos 3' y 5', en la misma cadena o en una cadena diferente
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2003/005028.
Solicitante: SIRNA THERAPEUTICS, INC.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 2950 WILDERNESS PLACE BOULDER, CO 80301 ESTADOS UNIDOS DE AMERICA.
Inventor/es: USMAN, NASSIM, BEIGELMAN, LEONID, CHOWRIRA,BHARAT, PAVCO,PAMELA, MCSWIGGEN,JAMES, JAMISON,SHARON, FOSNAUGH,KATHY, THOMPSON,JAMES.
Fecha de Publicación: .
Fecha Solicitud PCT: 20 de Febrero de 2003.
Fecha Concesión Europea: 1 de Septiembre de 2010.
Clasificación PCT:
- A61K48/00 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › Preparaciones medicinales que contienen material genético que se introduce en las células del cuerpo vivo para tratar enfermedades genéticas; Terapia génica.
- C07H21/02 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07H AZUCARES; SUS DERIVADOS; NUCLEOSIDOS; NUCLEOTIDOS; ACIDOS NUCLEICOS (derivados de ácidos aldónicos o sacáricos C07C, C07D; ácidos aldónicos, ácidos sacáricos C07C 59/105, C07C 59/285; cianohidrinas C07C 255/16; glicales C07D; compuestos de constitución indeterminada C07G; polisacáridos, sus derivados C08B; ADN o ARN concerniente a la ingeniería genética, vectores, p. ej. plásmidos o su aislamiento, preparación o purificación C12N 15/00; industria del azúcar C13). › C07H 21/00 Compuestos que contienen al menos dos unidades mononucleótido que tienen cada una grupos fosfato o polifosfato distintos unidos a los radicales sacárido de los grupos nucleósido, p. ej. ácidos nucleicos. › con ribosilo como radical sacárido.
- C07H21/04 C07H 21/00 […] › con desoxirribosilo como radical sacárido.
- C12N15/85 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › para células animales.
- C12N15/86 C12N 15/00 […] › Vectores virales.
- C12P19/34 C12 […] › C12P PROCESOS DE FERMENTACION O PROCESOS QUE UTILIZAN ENZIMAS PARA LA SINTESIS DE UN COMPUESTO QUIMICO DADO O DE UNA COMPOSICION DADA, O PARA LA SEPARACION DE ISOMEROS OPTICOS A PARTIR DE UNA MEZCLA RACEMICA. › C12P 19/00 Preparación de compuestos que contienen radicales sacárido (ácido cetoaldónico C12P 7/58). › Polinucleótidos, p. ej. ácidos nucleicos, oligorribonucleótidos.
- C12Q1/68 C12 […] › C12Q PROCESOS DE MEDIDA, INVESTIGACION O ANALISIS EN LOS QUE INTERVIENEN ENZIMAS, ÁCIDOS NUCLEICOS O MICROORGANISMOS (ensayos inmunológicos G01N 33/53 ); COMPOSICIONES O PAPELES REACTIVOS PARA ESTE FIN; PROCESOS PARA PREPARAR ESTAS COMPOSICIONES; PROCESOS DE CONTROL SENSIBLES A LAS CONDICIONES DEL MEDIO EN LOS PROCESOS MICROBIOLOGICOS O ENZIMOLOGICOS. › C12Q 1/00 Procesos de medida, investigación o análisis en los que intervienen enzimas, ácidos nucleicos o microorganismos (aparatos de medida, investigación o análisis con medios de medida o detección de las condiciones del medio, p. ej. contadores de colonias, C12M 1/34 ); Composiciones para este fin; Procesos para preparar estas composiciones. › en los que intervienen ácidos nucleicos.
Clasificación antigua:
- A61K48/00 A61K […] › Preparaciones medicinales que contienen material genético que se introduce en las células del cuerpo vivo para tratar enfermedades genéticas; Terapia génica.
- C07H21/04 C07H 21/00 […] › con desoxirribosilo como radical sacárido.
- C12N15/85 C12N 15/00 […] › para células animales.
- C12N15/86 C12N 15/00 […] › Vectores virales.
- C12P19/34 C12P 19/00 […] › Polinucleótidos, p. ej. ácidos nucleicos, oligorribonucleótidos.
- C12Q1/68 C12Q 1/00 […] › en los que intervienen ácidos nucleicos.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia, Ex República Yugoslava de Macedonia, Albania.
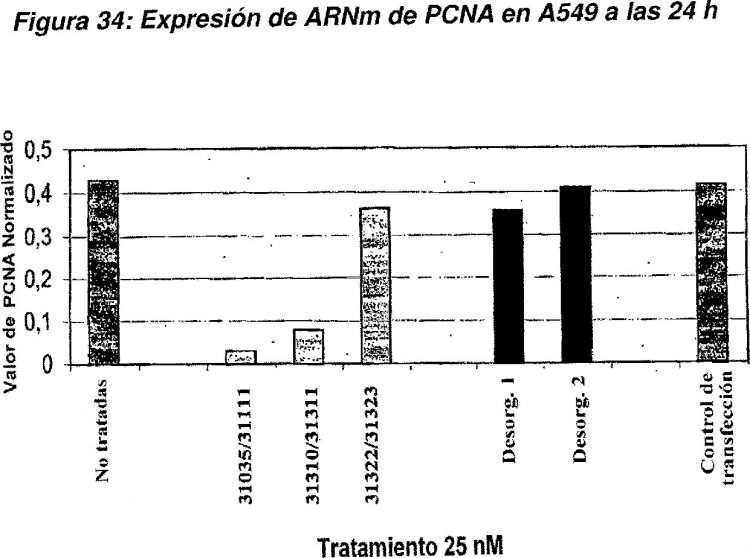
Fragmento de la descripción:
Inhibición de la expresión génica mediada por interferencia de ARN usando un ácido nucleico de interferencia corto (ANic).
La presente invención reivindica el beneficio de los documentos USSN 60/358.580 de Beigelman presentado el 20 de febrero de 2002, USSN 60/363.124 de Beigelman presentado el 11 de marzo de 2002, USSN 60/386.782 de Beigelman presentado el 6 de junio de 2002, USSN 60/406.784 de Beigelman presentado el 29 de agosto de 2002, USSN 60/408.378 de Beigelman presentado el 5 de septiembre de 2002, USSN 60/409.293 de Beigelman presentado el 9 de septiembre de 2002 y USSN 60/440.129 de Beigelman presentado el 15 de enero de 2003. La totalidad, incluyendo los dibujos, de dichas solicitudes se incorporan en el presente documento por referencia.
Campo de la invención
La presente invención se refiere a procedimientos y reactivos útiles para modular la expresión génica en una diversidad de aplicaciones, incluyendo el uso en aplicaciones terapéuticas, de diagnóstico, de validación de dianas y descubrimiento genómico. Específicamente, la invención se refiere a moléculas pequeñas de ácido nucleico, tales como moléculas de ácido nucleico de interferencia corto (ANic), ARN de interferencia corto (ARNic), ARN bicatenario (ARNbc), micro-ARN (miARN) y ARN de horquilla corto (ARNhc) capaces de mediar la interferencia de ARN (iARN).
Antecedentes de la invención
Lo siguiente es una discusión de la técnica pertinente que concierne a la iARN. La discusión se proporciona sólo para la comprensión de la siguiente invención. El sumario no es una admisión de que cualquiera de los trabajos descritos más adelante sea de la técnica anterior a la invención reivindicada. En el presente documento el solicitante demuestra que los ácidos nucleicos de interferencia cortos modificados químicamente poseen la misma capacidad para mediar la iARN que las moléculas de ARNic, y se espera que posean una estabilidad y actividad in vivo mejoradas; por lo tanto, esta discusión no tiene por objeto limitarse sólo a ARNic y puede aplicarse a ANic de manera general.
La interferencia de ARN se refiere al procedimiento de silenciamiento génico postranscripcional específico de secuencia en animales mediado por los ARN de interferencia cortos (ARNic) (Fire y col., 1998, Nature, 391, 806). El procedimiento correspondiente en plantas se denomina comúnmente silenciamiento génico postranscripcional o silenciamiento de ARN, y también se denomina supresión en hongos. Se piensa que el procedimiento de silenciamiento génico postranscripcional es un mecanismo de defensa celular conservado de forma evolutiva usado para evitar la expresión de genes extraños, y flora y filos diversos lo comparten comúnmente (Fire y col., 1999, Trends Genet., 15, 358). Dicha protección frente a la expresión de genes extraños puede haber evolucionado como respuesta a la producción de ARN bicatenarios (ARNbc) derivados de una infección viral o de la integración aleatoria de elementos transponibles en un genoma huésped mediante una respuesta celular que destruye específicamente ARN monocatenario homólogo o ARN genómico viral. La presencia de ARNbc en células desencadena la respuesta de iARN a través de un mecanismo que aún tiene que caracterizarse completamente. Este mecanismo parece ser diferente de la respuesta de interferón que se produce como resultado de la activación mediada por ARNbc de la proteína quinasa PKR y 2',5'-oligoadenilato sintetasa, dando como resultado una escisión inespecífica del ARNm por la ribonucleasa L.
La presencia de ARNbc largos en células estimula la actividad de una enzima ribonucleasa III denominada dicer. La dicer está implicada en el procesamiento de los ARNbc en trozos cortos de ARNbc conocidos como ARN de interferencia cortos (ARNic) (Berstein y col., 2001, Nature, 409, 363). Los ARN de interferencia cortos derivados de la actividad de dicer típicamente tienen de aproximadamente 21 a aproximadamente 23 nucleótidos de longitud y comprenden dúplex de aproximadamente 19 pares de bases (Elbashir y col., 2001, Genes Dev., 15, 188). También se ha implicado a dicer en la escisión de ARN temporales pequeños (ARNtp) de 21 y 22 nucleótidos a partir de ARN precursor de estructura conservada que están implicados en el control traduccional (Hutvagner y col., 2001, Science, 293, 834). La respuesta de iARN también presenta un complejo de endonucleasa, denominado comúnmente complejo de silenciamiento inducido por ARN (RISC), que media la escisión de ARN monocatenario que tiene una secuencia complementaria a la cadena antisentido del dúplex de ARNic. La escisión del ARN diana tiene lugar en el centro de la región complementaria a la cadena antisentido del dúplex de ARNic (Elbashir y col., 2001, Genes Dev., 15, 188).
La iARN se ha estudiado en una diversidad de sistemas. Fire y col., 1998, Nature, 391, 806, fueron los primeros en observar la iARN en C. elegans. Wianny y Goetz, 1999, Nature Cell Biol., 2, 70, describen la iARN mediada por ARNbc en embriones de ratón. Hammond y col., 2000, Nature, 404, 293, describen la iARN en células de Drosophila transfectadas con ARNbc. Elbashir y col., 2001, Nature, 411, 494, describen la iARN inducida introduciendo dúplex de ARN sintéticos de 21 nucleótidos en células de mamífero cultivadas incluyendo células embrionarias de riñón humano y células HeLa. Trabajos recientes en lisados embrionarios de Drosophila (Elbashir y col., 2001, EMBO J., 20, 6877) han revelado determinados requisitos de longitud, estructura, composición química y secuencia de ARNic que son esenciales para mediar una actividad de iARN eficaz. Estos estudios han demostrado que los dúplex de ARNic de 21 nucleótidos son más activos cuando contienen salientes dinucleotídicos 3'-terminales. Además, la sustitución completa de una o ambas cadenas de ARNic con nucleótidos 2'-desoxi (2'-H) o 2'-O-metilo suprime la actividad de iARN, mientras que se demostró que se toleraba la sustitución de los nucleótidos salientes de ARNic 3'-terminales con el nucleótido 2'-desoxi (2'-H). También se demostró que secuencias con un solo emparejamiento erróneo en el centro del dúplex de ARNic suprimía la actividad de iARN. Además, estos estudios también indican que la posición del sitio de escisión en el ARN diana está definida por el extremo 5' de la secuencia guía de ARNic en lugar del extremo 3' de la secuencia guía (Elbashir y col., 2001, EMBO J., 20, 6877). Otros estudios han indicado que es necesario un fosfato 5' en la cadena complementaria diana de un dúplex de ARNic para la actividad del ARNic y que, para mantener el resto fosfato 5' en el ARNic, se utiliza ATP (Nykanen y col., 2001, Cell, 107, 309).
Los estudios han demostrado que la sustitución de los segmentos salientes de nucleótidos 3'-terminales de un dúplex de ARNic de 21 unidades, que tiene salientes 3' de dos nucleótidos, con desoxirribonucleótidos no tiene un efecto adverso sobre la actividad de iARN. Se ha indicado que la sustitución de hasta cuatro nucleótidos en cada extremo del ARNic con desoxirribonucleótidos se tolera bien, mientras que la sustitución completa con desoxirribonucleótidos da como resultado la ausencia de actividad de iARN (Elbashir y col., 2001, EMBO J., 20, 6877). Además, Elbashir y col., anteriormente, también indican que la sustitución de ARNic con nucleótidos 2'-O-metilo suprime completamente la actividad de iARN. Li y col., Publicación Internacional PCT Nº WO 00/44914, y Beach y col., Publicación Internacional PCT Nº WO 01/68836 sugieren de forma preliminar que el ARNic puede incluir modificaciones en la cadena principal de azúcar-fosfato o en el nucleósido para incluir al menos uno de un heteroátomo de nitrógeno o de azufre, sin embargo, ninguna solicitud postula en qué medida se tolerarían tales modificaciones en moléculas de ARNic, ni proporciona ninguna orientación adicional o ejemplos de dicho ARNic modificado. Kreutzer y col., solicitud de patente canadiense Nº 2.359.180, también describen determinadas modificaciones químicas para su uso en construcciones de ARNbc con el fin de contrarrestar la activación de la proteína quinasa PKR dependiente de ARN bicatenario, específicamente nucleótidos 2'-amino o 2'-O-metilo y nucleótidos que contienen un puente de 2'-O- o 4'-C-metileno. Sin embargo, de manera similar, Kreutzer y col. no proporcionan ejemplos u orientaciones con respecto a en qué medida se tolerarían estas modificaciones en moléculas de ARNic.
Parrish y col., 2000, Molecular Cell, 6, 1977-1087, ensayaron determinadas modificaciones químicas dirigidas al gen unc-22 en...
Reivindicaciones:
1. Una molécula de ácido nucleico de interferencia corto (ANic) modificada químicamente que regula negativamente la expresión de un gen diana por interferencia de ARN (iARN), en la que:
(a) el ANic comprende una cadena con sentido y una cadena antisentido distinta, en el que dicha cadena antisentido comprende una secuencia que es complementaria al ARN del gen diana, y en el que la cadena con sentido comprende una secuencia de nucleótidos que es complementaria a la cadena antisentido;
(b) cada cadena de la molécula de ácido nucleico tiene independientemente una longitud de 18 a 24 nucleótidos y el dúplex de ANic comprende de 17 a 23 pares de bases;
(c) 10 o más nucleótidos de pirimidina de la cadena del ANic con sentido y/o antisentido se modifican químicamente con nucleótidos 2'-desoxi, 2'-O-metilo o 2'-desoxi-2'-fluoro, estando presentes uno o más enlaces internucleotídicos de fosforotioato y/o, una molécula de protección terminal en el extremo 3', el extremo 5' o en ambos extremos 3' y 5', en la misma cadena o en una cadena diferente.
2. La molécula de ANic de la reivindicación 1, en la que dicha molécula de ANic comprende ribonucleótidos en aproximadamente el 5, 10, 30, 40 ó 50% de las posiciones de nucleótidos.
3. La molécula de ANic de la reivindicación 1, en la que dicha molécula de ANic se ensambla a partir de dos fragmentos oligonucleotídicos distintos, en la que un fragmento comprende la región con sentido y un segundo fragmento comprende la región antisentido, en la que el fragmento que comprende dicha región con sentido incluye un resto de protección terminal en el extremo 5', el extremo 3' o en ambos extremos 5' y 3'.
4. La molécula de ANic de la reivindicación 3, en la que los nucleótidos de purina en la región con sentido son nucleótidos de 2'-desoxi purina y en la que los nucleótidos de pirimidina en la región con sentido son nucleótidos de 2'-desoxi-2'-fluoro pirimidina.
5. La molécula de ANic de cualquiera de las reivindicaciones anteriores, en la que dicho resto de protección terminal es un resto abásico desoxi invertido.
6. La molécula de ANic de la reivindicación 3, en la que los nucleótidos de pirimidina de dicha región antisentido son nucleótidos de 2'-desoxi-2'-fluoro pirimidina y en la que los nucleótidos de purina en la región antisentido son nucleótidos de 2'-O-metil purina.
7. La molécula de ANic de la reivindicación 3, en la que los nucleótidos de purina presentes en dicha región antisentido son nucleótidos de 2'-desoxi purina y en la que los nucleótidos de pirimidina presentes en dicha región antisentido son nucleótidos de 2'-desoxi-2'-fluoro pirimidina.
8. La molécula de ANic de una cualquiera de las reivindicaciones 3, 6 y 7, en la que dicha región antisentido comprende un enlace internucleotídico de fosforotioato en el extremo 3' de dicha región antisentido.
9. La molécula de ANic de la reivindicación 3, en la que cada uno de los dos fragmentos de dicha molécula de ANic comprende 21 nucleótidos.
10. La molécula de ANic de la reivindicación 3, en la que 19 nucleótidos de cada fragmento de la molécula de ANic están formando pares de bases con los nucleótidos complementarios del otro fragmento de la molécula de ANic, y en la que al menos dos nucleótidos 3'-terminales de cada fragmento de la molécula de ANic no están formando pares de bases con los nucleótidos del otro fragmento de la molécula de ANic.
11. La molécula de ANic de la reivindicación 3, en la que 19 nucleótidos de la región antisentido están formando pares de bases con la secuencia de nucleótidos del ARN que codifica el gen diana o una parte del mismo.
12. La molécula de ANic de la reivindicación 3, en la que 21 nucleótidos de la región antisentido están formando pares de bases con la secuencia de nucleótidos del ARN que codifica el gen diana o una parte del mismo.
13. La molécula de ANic de la reivindicación 3, en la que los nucleótidos de purina en la región con sentido son ribonucleótidos de purina y en la que los nucleótidos de pirimidina en la región con sentido son nucleótidos de 2'-desoxi-2'-fluoro pirimidina, y en la que el fragmento con sentido incluye un resto de protección terminal en los extremos 5' y 3'.
14. La molécula de ANic de la reivindicación 3, en la que los nucleótidos de purina en la región con sentido son ribonucleótidos de purina, y en la que los nucleótidos de pirimidina en la región con sentido son nucleótidos de 2'-O-metil pirimidina, y en la que el fragmento con sentido incluye un resto de protección terminal en los extremos 5' y 3'.
15. Una composición que comprende la molécula de ácido nucleico de cualquier reivindicación anterior y un vehículo o diluyente farmacéuticamente aceptable.
Patentes similares o relacionadas:
Composiciones útiles en el tratamiento de la deficiencia de ornitina transcarbamilasa (OTC), del 8 de Julio de 2020, de THE TRUSTEES OF THE UNIVERSITY OF PENNSYLVANIA: Un vector vírico recombinante que comprende una secuencia de ácido nucleico que codifica la proteína ornitina transcarbamilasa humana (hOTC) y secuencias […]
Terapia génica para la diabetes, del 8 de Julio de 2020, de UCL Business Ltd: Una molécula de ácido nucleico que comprende una secuencia de nucleótidos que codifica una proteína preproinsulina funcional en donde la secuencia de nucleótidos tiene al menos […]
Vacuna de ADN que contiene un epítopo específico de VEGF y/o un epítopo específico de angiopoyetina-2, del 1 de Julio de 2020, de OSAKA UNIVERSITY: Un vector de expresión que codifica un polipéptido del antígeno del núcleo del virus de la hepatitis B quimérico con una inserción para uso en el tratamiento o la profilaxis […]
Composiciones para modular la expresión de SOD-1, del 24 de Junio de 2020, de Biogen MA Inc: Un compuesto antisentido según la siguiente fórmula: mCes Aeo Ges Geo Aes Tds Ads mCds Ads Tds Tds Tds mCds Tds Ads mCeo Aes Geo mCes Te (secuencia […]
Ácido nucleico antisentido, del 24 de Junio de 2020, de NIPPON SHINYAKU CO., LTD.: Un oligómero antisentido de 14 a 32 bases de longitud, que comprende dos unidades de oligómeros conectadas seleccionadas del grupo que consiste […]
Plekhg5 como diana farmacéutica para trastornos neurológicos, del 15 de Junio de 2020, de CONSEJO SUPERIOR DE INVESTIGACIONES CIENTIFICAS (CSIC): Plekhg5 como diana farmacéutica para trastornos neurológicos. La invención hace referencia al uso del gen Plekhg5 como diana farmacológica para el cribado, […]
Método para activar células T auxiliares, del 10 de Junio de 2020, de OTSUKA PHARMACEUTICAL CO., LTD.: Una composición para su uso en el tratamiento o prevención del cáncer mediante la activación de células T auxiliares en un sujeto, en donde dicha composición […]
Ratón nuligénico para Pint que muestra un fenotipo asociado a envejecimiento prematuro, del 10 de Junio de 2020, de REGENERON PHARMACEUTICALS, INC.: Un ratón cuyo genoma comprende una inactivación de un locus del ARN no codificante largo (ARNlnc) Pint endógeno, en donde la inactivación (i) da como resultado que el […]