FORMA NO ESCINDIBLE DE LA PROTEINA GB DE HCMV.
Una forma no escindible de la proteína gB de HCMV, que comprende una o más sustituciones de aminoácidos en un sitio de escisión de la proteína,
en la que la proteína es una proteína truncada que carece del dominio de anclaje a la membrana
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E05075216.
Solicitante: GLAXOSMITHKLINE BIOLOGICALS S.A..
Nacionalidad solicitante: Bélgica.
Dirección: RUE DE L'INSTITUT, 89 1330 RIXENSART BELGICA.
Inventor/es: GHEYSEN,DIRK RICHARD.
Fecha de Publicación: .
Fecha Solicitud PCT: 11 de Mayo de 1995.
Fecha Concesión Europea: 6 de Octubre de 2010.
Clasificación Internacional de Patentes:
- A61K39/245 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 39/00 Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53). › Herpetoviridae, p. ej. virus del herpes simple.
- C07K14/035 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › Virus herpes simple I o II.
- C07K14/045 C07K 14/00 […] › Citomegalovirus.
Clasificación PCT:
- A61K39/245 A61K 39/00 […] › Herpetoviridae, p. ej. virus del herpes simple.
- C07K14/035 C07K 14/00 […] › Virus herpes simple I o II.
- C07K14/045 C07K 14/00 […] › Citomegalovirus.
- C12N15/62 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Secuencias de ADN que codifican proteínas de fusión.
- C12N15/85 C12N 15/00 […] › para células animales.
- C12N5/10 C12N […] › C12N 5/00 Células no diferenciadas humanas, animales o vegetales, p. ej. líneas celulares; Tejidos; Su cultivo o conservación; Medios de cultivo para este fin (reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00). › Células modificadas por introducción de material genético extraño, p. ej. células transformadas por virus.
Clasificación antigua:
- A61K39/245 A61K 39/00 […] › Herpetoviridae, p. ej. virus del herpes simple.
- C07K14/035 C07K 14/00 […] › Virus herpes simple I o II.
- C07K14/045 C07K 14/00 […] › Citomegalovirus.
- C12N15/62 C12N 15/00 […] › Secuencias de ADN que codifican proteínas de fusión.
- C12N15/85 C12N 15/00 […] › para células animales.
- C12N5/10 C12N 5/00 […] › Células modificadas por introducción de material genético extraño, p. ej. células transformadas por virus.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia.
Fragmento de la descripción:
La presente invención se refiere a proteínas de citomegalovirus recombinante, más particularmente a formas no escindibles de una proteína de citomegalovirus humano (HCMV), y a su expresión en células eucariotas. La invención se refiere además a procedimientos para construir y expresar dichas proteínas, a intermedios para su uso en los mismos y a proteínas recombinantes que pueden obtenerse a partir de los intermedios. Las proteínas recombinantes de la invención tienen utilidad potencial en el desarrollo de vacunas para la prevención de la infección por HCMV.
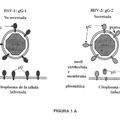
El HCMV es un virus de ADN humano que pertenece a familia de los herpesvirus. En común con otros virus herpéticos (tales como el Virus Herpes Simplex (HSV) y el Virus Varicella Zoster (VZV)) el HCMV está constituido por un núcleo de ADN y una cápsida externa y está cubierto por una membrana lipídica que incorpora glicoproteínas específicas de virus.
El citomegalovirus humano es endémico en la mayoría de las partes del mundo. Sin embargo, la infección primaria normalmente tiene como resultado una enfermedad subclínica después de la cual el virus permanece latente conservando la capacidad de reactivarse en cualquier momento. Sin embargo, en dos poblaciones, el HCMV es responsable de situaciones médicas graves. El HCMV es una causa importante de defectos congénitos en recién nacidos. También están asociados con la infección en estos bebés la pérdida auditiva y un bajo rendimiento intelectual. La segunda población de riesgo son pacientes inmunocomprometidos tales como los que padecen infección por VIH y los pacientes que se han sometido a trasplantes. En esta situación, el virus se convierte en un patógeno oportunista y produce una enfermedad grave con una alta morbilidad y mortalidad. La enfermedad clínica produce una diversidad de síntomas que incluyen fiebre, hepatitis, neumonitis y mononucleosis infecciosa.
Esto, por lo tanto, explica los amplios esfuerzos de los expertos en la materia y la importancia de los estudios dedicados a la biología de estos virus. Sin embargo, actualmente no se dispone de ninguna vacuna eficaz contra el HCMV.
Por lo tanto, aún existe la necesidad de antígenos que protejan eficazmente contra la exposición al virus HCMV.
De acuerdo con un primer aspecto de la presente invención, se proporciona una forma no escindible de proteína gB de HCMV que comprende una o más sustituciones de aminoácidos en un sitio de escisión de la proteína y que es una proteína truncada que carece del dominio de anclaje a la membrana.
La proteína gB de HCMV cepa AD 169 contiene 906 restos de aminoácidos; los aminoácidos 1 a 24 corresponden al péptido señal y los restos 712 a 776 el dominio de anclaje a la membrana. La molécula presenta 19 sitios potenciales para la glicosilación. Usada sola para inmunización, la proteína gB genera una respuesta inmune que es insuficiente para conferir protección contra la exposición al virus.
Spaete y col. (J. Virol, 64(6): 2922-31, 1990) notificaron que mutaciones en gB de HCMV de la cepa Towne bloquean la escisión de gB. La proteína gB de HCMV de la invención comprende una forma no escindible de gB de HCMV. Convenientemente, esto se consigue cambiando uno o más aminoácidos en un sitio de escisión de la proteína. Preferentemente, esto se hace cambiando la Arg 458 y la Arg 459 por Glu y Thr respectivamente. La forma no escindible y truncada de gB que carece del dominio de anclaje a la membrana es nueva y es el objeto de la invención. Presenta la ventaja de tener una proteína gB con mayor secreción cuando se expresa de forma adecuada.
Las proteínas de la presente invención son inmunogénicas. La expresión derivado inmunogénico, como se usa en la presente invención, incluye cualquier molécula que es una proteína que es inmunológicamente reactiva con anticuerpos inducidos contra la proteína de la presente invención o partes de la misma o con anticuerpos que reconocen la proteína gB de HCMV o el virus HCMV, o que induce a anticuerpos que reconocen la proteína, la proteína gB de HCMV o el virus HCMV. En particular, pueden usarse derivados inmunogénicos que son ligeramente más largos o más cortos que la proteína de la presente invención. Estos derivados pueden prepararse, por ejemplo, por sustitución, adición o reordenación de aminoácidos o por modificaciones químicas de los mismos incluyendo las que permiten el acoplamiento de la proteína de fusión a otras proteínas de soporte, tales como el toxoide tetánico o el antígeno de superficie de la hepatitis B. Todas estas sustituciones y modificaciones generalmente son bien conocidas para los expertos en la materia de la química de péptidos.
Los fragmentos inmunogénicos de la proteína de la presente invención que pueden ser útiles en la preparación de vacunas pueden prepararse por expresión de los fragmentos génicos apropiados o por síntesis de péptidos, por ejemplo, usando la síntesis de Merrifield (The Peptides, Vol 2., Academic Press, Nueva York, p3).
En un aspecto adicional de la invención, se proporciona un ADN recombinante que codifica la proteína de la invención. El ADN recombinante de la invención puede formar parte de un vector, por ejemplo, un plásmido, especialmente un plásmido de expresión a partir del cual puede expresarse la proteína de la invención. Estos vectores también forman parte de la invención, así como las células hospedadoras en las que se han introducido los vectores.
Para construir el ADN que codifica una proteína de acuerdo con la invención, puede manipularse un ADNc que contiene las secuencias codificantes completas de la proteína gB de HCMV usando técnicas convencionales [véase, por ejemplo, Maniatis T. y col Molecular Cloning, Cold Spring Harbor Laboratory, Cold Spring Harbor N.Y. (1982)] como se describe
adicionalmente más adelante en la presente invención.
En el transcurso de la realización de las técnicas descritas anteriormente, pueden obtenerse fragmentos codificantes de ADN recombinante de la proteína gB de HCMV, que también forman parte de la presente invención.
En particular, los segmentos de ADN que codifican una forma no escindible de gB de
HCMV y la proteína truncada gB de HCMV (gB que carece del dominio de anclaje a la membrana) son intermedios importantes y son un objeto de la presente invención. Los vectores que comprenden dicho ADN, los huéspedes transformados de estamanera y las propias proteínas truncadas, expresadas como se describe más adelante en el presente documento, forman parte de la invención.
Para la expresión de las proteínas de la invención, pueden construirse plásmidos que sean adecuados para la transferencia en vaccinia virus o la transfección en células de Ovario de Hámster Chino (CHO) o células Vero. Más adelante se describen vectores de expresión adecuados.
Para la expresión en vaccinia, puede usarse un plásmido de transferencia de vaccinia tal como pULB 5213 que es un derivado de pSC11 (Chakrabati y col. Molecular and Cellular Biology 5, 3403 -3409, 1985). En un aspecto, la proteína puede expresarse bajo el control del promotor P7.5 de vaccinia.
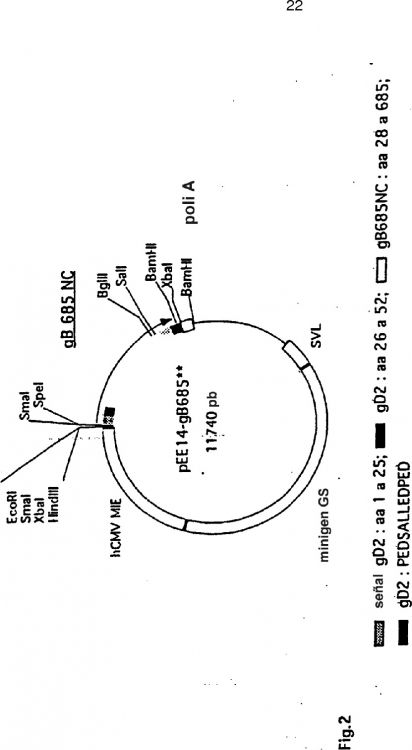
Para la expresión en células CHO-K1, convenientemente puede usarse un vector de glutamina sintetasa (GS) tal como pEE14 de forma que la proteína se exprese bajo el control del promotor temprano inmediato principal del citomegalovirus humano (hCMV-MIE). Como alternativa, convenientemente puede usarse un vector que permita la expresión del módulo codificante como un transcrito policistrónico con el gen de selección neo. En un aspecto preferido, el módulo codificante está bajo el control del promotor de la Repetición Terminal Larga (LTR) del Sarcoma de Rous.
Preferentemente, el plásmido para la expresión en células CHO-K1 lleva un casete de expresión de GS adecuado para la amplificación génica usando metionina sulfoximina (MSX). Como alternativa, el plásmido para la expresión en células CHO-K1 lleva un casete de expresión de DHFR adecuado para la amplificación génica usando metotrexato (MTX).
La expresión de las proteínas de la presente invención se realiza en presencia de butirato sódico y/o dimetil sulfóxido (DMSO) que, según se ha descubierto, aumentan la expresión génica.
En otro aspecto más de la invención se proporciona una composición de vacuna que comprende una proteína de acuerdo con la invención en combinación con un vehículo farmacéuticamente aceptable,...
Reivindicaciones:
1. Una forma no escindible de la proteína gB de HCMV, que comprende una o más sustituciones de aminoácidos en un sitio de escisión de la proteína, en la que la proteína es una proteína truncada que carece del dominio de anclaje a la membrana.
2. Una proteína de acuerdo con la reivindicación 1, en la que la Arg 458 y la Arg 459 se cambian por Glu y Thr respectivamente.
3. Una proteína de acuerdo con la reivindicación 2, que está truncada en el aminoácido 685 (gB685 NC).
4. Una proteína de acuerdo con cualquier reivindicación anterior, en la que la proteína gB procede de la cepa AD169 de HCMV.
5. ADN recombinante que codifica una forma no escindible de la proteína gB de HCMV de acuerdo con una cualquiera de las reivindicaciones 1 a 4.
6. Un vector de expresión que comprende ADN recombinante de acuerdo con la reivindicación 5.
7. Un huésped transformado con un vector de acuerdo con la reivindicación 6.
8. Un procedimiento para la producción de una forma no escindible de la proteína gB de HCMV de acuerdo con una cualquiera de las reivindicaciones 1 a 4, comprendiendo dicho procedimiento la expresión de una secuencia de ADN que codifica dicha proteína en una célula huésped y la recuperación de la proteína.
9. Una composición de vacuna que comprende una proteína de acuerdo con una cualquiera de las reivindicaciones 1 a 4 o un derivado inmunogénico de la misma, mezclada con un vehículo farmacéuticamente aceptable.
10. Una composición de vacuna de acuerdo con la reivindicación 9, que comprende además monofosforil lípido A 3D y/o QS-21.
11. Una composición de vacuna de acuerdo con la reivindicación 9 ó 10, en la que el vehículo es una emulsión de aceite en agua.
12. Una forma no escindible de la proteína gB de HCMV de acuerdo con una cualquiera de 5 las reivindicaciones 1 a 4 o un derivado inmunogénico de la misma para su uso en medicina.
13. Una composición de vacuna de acuerdo con una cualquiera de las reivindicaciones 9 a 11 para su uso en medicina.
14. Uso de una forma no escindible de la proteína gB de HCMV de acuerdo con una cualquiera de las reivindicaciones 1 a 4 o un derivado inmunogénico de la misma, en la fabricación de un medicamento para su uso en el tratamiento de infecciones virales.
Patentes similares o relacionadas:
Dirección del virus del herpes simple a receptores específicos, del 5 de Junio de 2019, de UNIVERSITY OF CHICAGO: Una partícula del virus del herpes simple (VHS) recombinante que tiene en su superficie: (a) una proteína de la superficie vírica de VHS alterada que comprende […]
Vacunas de herpesvirus basadas en vectores del virus de la enfermedad de Newcastle, del 5 de Octubre de 2016, de MERIAL, INC.: Una composición o vacuna que comprende (i) uno o más vectores de virus de la enfermedad de Newcastle (NDV)-herpesvirus recombinantes, y (ii) un vehículo aceptable […]
Composición y método para tratar el cáncer usando herpes virus, del 25 de Marzo de 2015, de TAKARA BIO INC.: Un herpes virus, en el que al menos dos genes no esenciales para la replicación del mismo están inactivados, en el que el herpes virus es virus del herpes simple, […]
Construcciones de ácidos nucleicos, del 5 de Marzo de 2014, de POWDERJECT VACCINES, INC.: Una construcción de ácido nucleico que comprende: (i) una secuencia promotora quimérica que comprende: (a) una secuencia promotora temprana inmediata de […]
Virus del herpes simple (VHS) con tropismo modificado, utilizaciones y procedimiento de preparación del mismo, del 15 de Octubre de 2013, de Alma Mater Studiorum -Universita' di Bologna: Virus del herpes simple (VHS) modificado que comprende una envoltura glucoproteica en la que un anticuerpomonocatenario heterólogo sustituye una parte eliminada del dominio […]
 COMPOSICIONES DE LIPOSOMAS INMUNOGENICAS, del 29 de Septiembre de 2010, de MOLECULAR EXPRESS INC: Una composición de liposomas inmunogénica que comprende:
lípidos formadores de vesículas; y
una construcción de proteína antigénica que es un producto de fusión hidrosoluble […]
COMPOSICIONES DE LIPOSOMAS INMUNOGENICAS, del 29 de Septiembre de 2010, de MOLECULAR EXPRESS INC: Una composición de liposomas inmunogénica que comprende:
lípidos formadores de vesículas; y
una construcción de proteína antigénica que es un producto de fusión hidrosoluble […]
 USO DE UN COMPUESTO PROTEICO DERIVADO DE LA GLICOPROTEINA (GG) DE HSV PARA LA ELABORACION DE UNA COMPOSICION FARMACEUTICA UTIL PARA LA INDUCCION DE MIGRACION CELULAR MEDIADA POR QUIMIOQUINAS, del 19 de Febrero de 2010, de CONSEJO SUPERIOR INVESTIG. CIENTIFICAS: Uso de un compuesto proteico derivado de la glicoproteína (gG) de HSV para la elaboración de una composición farmacéutica útil para la inducción de migración […]
USO DE UN COMPUESTO PROTEICO DERIVADO DE LA GLICOPROTEINA (GG) DE HSV PARA LA ELABORACION DE UNA COMPOSICION FARMACEUTICA UTIL PARA LA INDUCCION DE MIGRACION CELULAR MEDIADA POR QUIMIOQUINAS, del 19 de Febrero de 2010, de CONSEJO SUPERIOR INVESTIG. CIENTIFICAS: Uso de un compuesto proteico derivado de la glicoproteína (gG) de HSV para la elaboración de una composición farmacéutica útil para la inducción de migración […]
 NUEVA PROTEINA DE FUSION, GEN QUE LA CODIFICA, VECTOR RECOMBINANTE, VIRUS RECOMBINANTE, Y SU USO, del 16 de Diciembre de 2008, de NIPPON ZEON CO., LTD.: LA INVENCION SE REFIERE A LA PREPARACION DE UN ADN QUE CODIFICA PARA UNA PROTEINA DE FUSION QUE COMPRENDE UN POLIPEPTIDO CON LA ANTIGENICIDAD DE MYCOPLASMA GALLISEPTICUM, Y A […]
NUEVA PROTEINA DE FUSION, GEN QUE LA CODIFICA, VECTOR RECOMBINANTE, VIRUS RECOMBINANTE, Y SU USO, del 16 de Diciembre de 2008, de NIPPON ZEON CO., LTD.: LA INVENCION SE REFIERE A LA PREPARACION DE UN ADN QUE CODIFICA PARA UNA PROTEINA DE FUSION QUE COMPRENDE UN POLIPEPTIDO CON LA ANTIGENICIDAD DE MYCOPLASMA GALLISEPTICUM, Y A […]