Composición y método para tratar el cáncer usando herpes virus.
Un herpes virus, en el que al menos dos genes no esenciales para la replicación del mismo están inactivados,
en el que el herpes virus es virus del herpes simple, en el que el primer gen no esencial es UL56 y el segundo gen no esencial para la replicación es UL43, y en el que dicho herpes virus incluye una deleción desde la posición 116515 a 120346 del genoma del herpes virus y una deleción en la parte del genoma que codifica UL56 de modo que se deleciona la secuencia que codifica 136 aminoácidos en el lado N terminal de un total de 197 aminoácidos de UL56, junto con su región cadena arriba.
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E10000308.
Solicitante: TAKARA BIO INC..
Inventor/es: NISHIYAMA, YUKIHIRO.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K39/245 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 39/00 Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53). › Herpetoviridae, p. ej. virus del herpes simple.
- C07K14/035 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › Virus herpes simple I o II.
PDF original: ES-2539941_T3.pdf
Fragmento de la descripción:
Composición y método para tratar el cáncer usando herpes virus CAMPO TÉCNICO
La presente invención se refiere a un nuevo virus del herpes simple (a partir de ahora en este documento puede abreviarse como HSV). Más específicamente, la presente invención se refiere a un uso y una composición para el tratamiento o prevención del cáncer usando un nuevo herpes virus.
TÉCNICA ANTECEDENTE
El primer registro de herpes virus en la historia data de la era de la antigua Grecia antes de Cristo. El herpes virus infrecuentemente se desarrolla después de infección primaria, pero se oculta en los ganglios o similares durante un largo periodo de tiempo. Cuando la capacidad inmune de un ser humano está reducida, el virus se activa y prolifera para desarrollar síntomas. En este caso, el herpes virus se dirige a un amplio intervalo de tejidos, tales como la piel, órganos genitales, globo ocular, nervios, y similares. Aunque haya anticuerpos presentes en la sangre que neutralizan el virus, a menudo aparecen síntomas. Por tanto se cree que una reducción en la función inmune celular está implicada en la aparición de los síntomas.
Ejemplos de herpes virus que se transmiten al ser humano incluyen virus del herpes simple (HSV-1), virus del herpes simple (HSV-2), virus varicela zoster (VZV), virus EB (EBV), citomegalovirus (HCMV), virus del herpes humano 6 (HHV-6), virus del herpes humano 7 (HHV-7), virus del herpes humano 8 (HHV-8), y similares.
HSV-1 causa gingivostomatitis o herpes facial como síntoma de infección primaria y herpes labial, queratoconjuntivitis por herpes, encefalitis por herpes como síntoma de infección recurrente. Un sitio de infección latente principal de HSV-1 es los ganglios trigéminos. HSV-2 causa herpes genital como síntoma de infección primaria y herpes genital o herpes neonatal como síntoma de infección recurrente. Un sitio de infección latente principal de HSV-2 es los ganglios sacros. VZV causa varicela (varicella) como síntoma de infección primaria y varicela y herpes zoster como síntoma de infección recurrente. Un sitio de infección latente principal de VZV es el ganglio de la raíz dorsal. EBV no causa síntomas o causa mononucleosis infecciosa como síntoma de infección primaria y linfoma de Burkitt, o cáncer rinofaríngeo como síntoma de infección recurrente. Un sitio de infección latente principal de EBV son las células B. HCMV no causa síntomas como síntoma de infección primaria y causa neumonía, enfermedad de inclusión citomegálica o similares como síntoma de infección recurrente. Se cree que los sitios de infección latente de HCMV son macrófagos y células progenitoras sanguíneas. HHV-6 causa exantema súbito como síntoma de infección primaria y exantema súbito (neumonía) como síntoma de infección recurrente. Se cree que los sitios de infección latente de HHV-6 son macrófagos y células progenitoras sanguíneas. HHV-7 causa exantema súbito como síntoma de infección primaria. Un sitio de infección latente principal de HHV-7 son las células T. HHV-8 no causa síntomas como síntoma de infección primaria y causa sarcoma de Kaposi, PEL, y enfermedad de Castleman como síntoma de infección recurrente. Un sitio de infección latente principal de HHV-8 son las células B. Por tanto, una diversidad de enfermedades infecciosas está causada por herpes virus.
Una vacuna viva atenuada contra el virus de la varicela es la única vacuna exitosa contra virus de herpes humano (Takahashi M., et al., Lancet, 2: 1288, 1974). Sin embargo, este virus vivo atenuado se obtuvo accidentalmente y se basa en la característica de que la varicela es más eficaz para inmunidad humoral ya que causa infección sistémica debido a viremia, a diferencia de otros herpes virus. Por lo tanto, aún no está disponible una vacuna que pueda utilizarse de forma universal para herpes virus.
HSV es un herpes virus representativo que es infeccioso para los seres humanos. La infección por HSV resulta de la inoculación del virus en la mucosa, o la invasión del virus a través de una rotura de la piel. La mayoría de las infecciones primarias suceden en los periodos neonatos, pero la mayoría de los niños con una infección primaria mejoran rápidamente. HSV se transmite a un bebé desde una niñera infectada o más generalmente una madre infectada (específicamente, un bebé encuentra herpes genital según el bebé pasa a través del canal de parto). En este caso, la infección por HSV causa síntomas graves. Por ejemplo, infección diseminada del neonato por herpes causa hepatitis o similares, de modo que el bebé puede morir.
Una vez que se adquiere HSV en el organismo, el HSV se mantiene en el organismo durante toda la vida. Durante el periodo de latencia, el HSV se localiza en neuronas de ganglios sensoriales (en el caso de lesiones faciales, habitualmente están implicados los ganglios trigéminos), y un paciente infectado es asintomático. Sin embargo, el HSV se activa por estímulos, tales como menstruación, exposición excesiva a luz solar o a viento frío, hormonas de la glándula pituitaria o glándula suprarrenal, reacciones alérgicas, o fiebre. El HSV activado se replica e invade el mecanismo de una célula hospedadora, produciendo partículas virales maduras infecciosas y causando muerte celular. Los síntomas causados por dicho ataque recurrente a menudo aparecen en la boca, cara, y órganos genitales. Por ejemplo, la queratitis debida a HSV recurrente se considera una causa principal de ceguera. Además, la infección por HSV en órganos genitales es frecuente, y la incidencia de enfermedades transmitidas por vía sexual (por ejemplo, herpes genital) causa por HSV es significativamente elevada. Más específicamente, ejemplos de
enfermedades inducidas por HSV recurrente que están causadas por el ataque recurrente incluyen enfermedades mucocutáneas, tales como herpes labial (un trastorno de los labios habltualmente llamado "ampolla febril" o "úlcera bucal"), glnglvostomatitis (la boca y las encías se cubren de vesículas y las vesículas se rompen formando úlceras), faringitis, tonsilitis, queratoconjuntivitis (queratitis o inflamación de la córnea, que progresa a úlcera dendriforme y finalmente a cicatrización de la córnea, provocando ceguera), y herpes genital. En casos raros, la infección por HSV causa encefalitis, eczema herpético, herpes traumático, y hepatitis.
El virus del herpes simple 2 (en este documento a partir de ahora también mencionado como HSV-2) Induce infección de la mucosa cutánea en órganos genitales. Después de la infección, el virus se mantiene en los ganglios sensoriales, y después se activa causando infección recurrente por HSV (Price, R. W., Walz, M. A., Wohlenberg, C., y Notkins, A. L. (1975) "Latent infection of sensory ganglia with herpes simplex virus: efficacy of immunization", Science 188, 938-940). Muchos investigadores han estudiado extensivamente las reacciones inmunes con infección por HSV-2 usando modelos animales.
Se ha informado de que una célula presentadora de antígenos principal (APC) es la célula dendrítlca (DC), incluyendo célula de Langerhans (LC), y varios macrófagos (M<|>) y células B en la vagina (Parr, M. B., y Parr, E. L. (1991), "Langerhans cells and T lymphocyte subsets in the murine vagina and cervix", Biol. Reprod. 44:491-498; Nandi, D., y Allison, J. P. (1993), "Characterization of neutrophiles and T lymphocytes associated with the murine vaginal epithelium", Reg. Immunol., 5, 332-338).
Se ha informado de que las células T desempeñan un papel importante como linfocitos T citotóxicos (CTL), y producen citoquinas antivirales contra infección por HSV-2 (Milligan, G. N., y Bernstein, D. I. (1995), "Analysis of herpes simplex virus-specific T cells in the murine female genital tract following genital infection with herpes simplex virus type 2", Virology 212, 481-489. ; Parr, M.B., y Parr, E L. (1998), "Mucosal immunity to herpes simplex virus type 2 infection in the mouse vagina is impaired by in vivo depletion of T lymphocytes", J. Virol. 72, 2677-2685; Milligan, G. N., Bernstein, D. I., y Bourne, N. (1998), "T lymphocytes are required for protection of the vaginal mucosae and sensory ganglia of immune mice against reinfection with herpes simplex virus type 2", J. Immunol. 160, 6093-6100).
Se ha informado de que mutantes que carecen de la capacidad de replicación pueden provocar un amplio espectro de reacciones inmunes (Morrison, L. A., Da Costa, X. J., y Knipe, D. M. (1998), "Influence of mucosal and parenteral immunization with a replication-defective mutant of HSV-2 on immune responses and protection from genital infection", Virology 243, 178-187; McLean, C. S., Ni Challanain, D., Duncan, I., Boursnell, M. E. G., Jennings, R., y Inglis, S. C. (1996), "Induction of a protective... [Seguir leyendo]
Reivindicaciones:
1. Un herpes virus, en el que al menos dos genes no esenciales para la replicación del mismo están inactivados, en el que el herpes virus es virus del herpes simple, en el que el primer gen no esencial es UL56 y el segundo gen no esencial para la replicación es UL43, y en el que dicho herpes virus incluye una deleción desde la posición 116515 a 120346 del genoma del herpes virus y una deleción en la parte del genoma que codifica UL56 de modo que se deleciona la secuencia que codifica 136 aminoácidos en el lado N terminal de un total de 197 aminoácidos de UL56, junto con su región cadena arriba.
2. Un herpes virus de acuerdo con la reivindicación 1, en el que el virus tiene capacidad de seleccionar células cancerosas.
3. Un herpes virus de acuerdo con la reivindicación 1, en el que la inactivación incluye al menos una sustitución, adición, deleción o modificación de nucleótido en la secuencia del gen no esencial para la replicación.
4. Un herpes virus de acuerdo con la reivindicación 1, en el que se inserta una señal para detener la traducción en la secuencia del gen no esencial para la replicación.
5. Un herpes virus de acuerdo con la reivindicación 1, en el que el virus es un virus del herpes simple modificado.
6. Un herpes virus de acuerdo con la reivindicación 1, en el que el virus es un HSV-1 o HSV-2 modificado.
7. Una composición farmacéutica para tratar o prevenir el cáncer, que comprende:
un herpes virus de acuerdo con cualquier reivindicación precedente; y un vehículo farmacéuticamente aceptable.
8. Una composición farmacéutica de acuerdo con la reivindicación 7, en la que el cáncer se selecciona entre el grupo que consiste en cáncer de ovario, cáncer de hígado, cáncer pancreático, cáncer de vejiga, cáncer de uretra, cáncer de intestino grueso, cáncer de piel, melanoma maligno, osteosarcoma, carcinoma de células escamosas de cabeza y cuello, cáncer de mama, cáncer de pulmón, cáncer de colon y cáncer de estómago.
9. Un herpes virus de acuerdo con cualquiera de las reivindicaciones 1-6 para tratar o prevenir el cáncer.
Patentes similares o relacionadas:
Dirección del virus del herpes simple a receptores específicos, del 5 de Junio de 2019, de UNIVERSITY OF CHICAGO: Una partícula del virus del herpes simple (VHS) recombinante que tiene en su superficie: (a) una proteína de la superficie vírica de VHS alterada que comprende […]
Vacunas de herpesvirus basadas en vectores del virus de la enfermedad de Newcastle, del 5 de Octubre de 2016, de MERIAL, INC.: Una composición o vacuna que comprende (i) uno o más vectores de virus de la enfermedad de Newcastle (NDV)-herpesvirus recombinantes, y (ii) un vehículo aceptable […]
Construcciones de ácidos nucleicos, del 5 de Marzo de 2014, de POWDERJECT VACCINES, INC.: Una construcción de ácido nucleico que comprende: (i) una secuencia promotora quimérica que comprende: (a) una secuencia promotora temprana inmediata de […]
Virus del herpes simple (VHS) con tropismo modificado, utilizaciones y procedimiento de preparación del mismo, del 15 de Octubre de 2013, de Alma Mater Studiorum -Universita' di Bologna: Virus del herpes simple (VHS) modificado que comprende una envoltura glucoproteica en la que un anticuerpomonocatenario heterólogo sustituye una parte eliminada del dominio […]
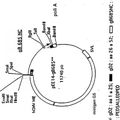 FORMA NO ESCINDIBLE DE LA PROTEINA GB DE HCMV, del 25 de Febrero de 2011, de GLAXOSMITHKLINE BIOLOGICALS S.A.: Una forma no escindible de la proteína gB de HCMV, que comprende una o más sustituciones de aminoácidos en un sitio de escisión de la proteína, en la que la […]
FORMA NO ESCINDIBLE DE LA PROTEINA GB DE HCMV, del 25 de Febrero de 2011, de GLAXOSMITHKLINE BIOLOGICALS S.A.: Una forma no escindible de la proteína gB de HCMV, que comprende una o más sustituciones de aminoácidos en un sitio de escisión de la proteína, en la que la […]
 COMPOSICIONES DE LIPOSOMAS INMUNOGENICAS, del 29 de Septiembre de 2010, de MOLECULAR EXPRESS INC: Una composición de liposomas inmunogénica que comprende:
lípidos formadores de vesículas; y
una construcción de proteína antigénica que es un producto de fusión hidrosoluble […]
COMPOSICIONES DE LIPOSOMAS INMUNOGENICAS, del 29 de Septiembre de 2010, de MOLECULAR EXPRESS INC: Una composición de liposomas inmunogénica que comprende:
lípidos formadores de vesículas; y
una construcción de proteína antigénica que es un producto de fusión hidrosoluble […]
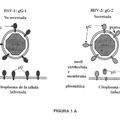 USO DE UN COMPUESTO PROTEICO DERIVADO DE LA GLICOPROTEINA (GG) DE HSV PARA LA ELABORACION DE UNA COMPOSICION FARMACEUTICA UTIL PARA LA INDUCCION DE MIGRACION CELULAR MEDIADA POR QUIMIOQUINAS, del 19 de Febrero de 2010, de CONSEJO SUPERIOR INVESTIG. CIENTIFICAS: Uso de un compuesto proteico derivado de la glicoproteína (gG) de HSV para la elaboración de una composición farmacéutica útil para la inducción de migración […]
USO DE UN COMPUESTO PROTEICO DERIVADO DE LA GLICOPROTEINA (GG) DE HSV PARA LA ELABORACION DE UNA COMPOSICION FARMACEUTICA UTIL PARA LA INDUCCION DE MIGRACION CELULAR MEDIADA POR QUIMIOQUINAS, del 19 de Febrero de 2010, de CONSEJO SUPERIOR INVESTIG. CIENTIFICAS: Uso de un compuesto proteico derivado de la glicoproteína (gG) de HSV para la elaboración de una composición farmacéutica útil para la inducción de migración […]
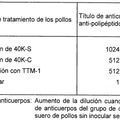 NUEVA PROTEINA DE FUSION, GEN QUE LA CODIFICA, VECTOR RECOMBINANTE, VIRUS RECOMBINANTE, Y SU USO, del 16 de Diciembre de 2008, de NIPPON ZEON CO., LTD.: LA INVENCION SE REFIERE A LA PREPARACION DE UN ADN QUE CODIFICA PARA UNA PROTEINA DE FUSION QUE COMPRENDE UN POLIPEPTIDO CON LA ANTIGENICIDAD DE MYCOPLASMA GALLISEPTICUM, Y A […]
NUEVA PROTEINA DE FUSION, GEN QUE LA CODIFICA, VECTOR RECOMBINANTE, VIRUS RECOMBINANTE, Y SU USO, del 16 de Diciembre de 2008, de NIPPON ZEON CO., LTD.: LA INVENCION SE REFIERE A LA PREPARACION DE UN ADN QUE CODIFICA PARA UNA PROTEINA DE FUSION QUE COMPRENDE UN POLIPEPTIDO CON LA ANTIGENICIDAD DE MYCOPLASMA GALLISEPTICUM, Y A […]