AGENTE DE CAPTACIÓN MARCADO ISOTOPICAMENTE Y PROCEDIMIENTO PARA IDENTIFICAR METABOLITOS REACTIVOS.
Un compuesto marcado isotópicamente de fórmula (I*) **Fórmula** en la que uno o más de los átomos de carbono,
nitrógeno, oxígeno, azufre o hidrógeno no intercambiable en los grupos con asterisco está marcado isotópicamente
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2007/079298.
Solicitante: JANSSEN PHARMACEUTICA NV.
Nacionalidad solicitante: Bélgica.
Dirección: TURNHOUTSEWEG 30 2340 BEERSE BELGICA.
Inventor/es: HUEBERT,Norman D, ZHENGYIN,Yan.
Fecha de Publicación: .
Fecha Solicitud PCT: 24 de Septiembre de 2007.
Clasificación Internacional de Patentes:
- C07K5/02F
- C12Q1/26 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12Q PROCESOS DE MEDIDA, INVESTIGACION O ANALISIS EN LOS QUE INTERVIENEN ENZIMAS, ÁCIDOS NUCLEICOS O MICROORGANISMOS (ensayos inmunológicos G01N 33/53 ); COMPOSICIONES O PAPELES REACTIVOS PARA ESTE FIN; PROCESOS PARA PREPARAR ESTAS COMPOSICIONES; PROCESOS DE CONTROL SENSIBLES A LAS CONDICIONES DEL MEDIO EN LOS PROCESOS MICROBIOLOGICOS O ENZIMOLOGICOS. › C12Q 1/00 Procesos de medida, investigación o análisis en los que intervienen enzimas, ácidos nucleicos o microorganismos (aparatos de medida, investigación o análisis con medios de medida o detección de las condiciones del medio, p. ej. contadores de colonias, C12M 1/34 ); Composiciones para este fin; Procesos para preparar estas composiciones. › en los que interviene una oxidorreductasa.
Clasificación PCT:
- C07K5/00 C […] › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › Péptidos con hasta cuatro aminoácidos en una secuencia totalmente determinada; Sus derivados.
- C07K5/037 C07K […] › C07K 5/00 Péptidos con hasta cuatro aminoácidos en una secuencia totalmente determinada; Sus derivados. › el enlace anormal lo forma la cadena lateral de un alfa-aminoácido, p. ej. gamma-Glu, epsilon-Lys, glutatión.
- C07K5/09 C07K 5/00 […] › la cadena lateral del primer aminoácido contiene más grupos amino que grupos carboxilo, o sus derivados, p. ej. Lys, Arg.
- C07K5/093 C07K 5/00 […] › la cadena lateral del primer aminoácido contiene más grupos carboxilo que grupos amino, o sus derivados, p. ej. Asp, Glu, Asn.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia.
PDF original: ES-2359109_T3.pdf



Fragmento de la descripción:
Campo de la invención
La presente invención se refiere a un agente de captación marcado isotópicamente, a procedimientos para detectar metabolitos reactivos y a procedimientos para identificar candidatos a fármaco. Más específicamente, el agente de captación marcado isotópicamente y los procedimientos para detectar metabolitos reactivos pueden usarse para detectar metabolitos reactivos tanto "duros" como "blandos", eliminando de esta manera falsos positivos.
Antecedentes de la invención
Una causa de morbilidad y mortalidad de pacientes, es la toxicidad idiosincrásica de los fármacos, que sigue siendo una grave preocupación de seguridad tanto en el desarrollo clínico del fármaco como en el posterior lanzamiento en el mercado. Estas reacciones idiosincrásicas a fármacos pueden conducir a un uso restringido e incluso a la retirada del mercado, que en consecuencia da como resultado mayores costes de desarrollo para la industria farmacéutica. Por ejemplo, troglitazona, benoxaprofeno y zomepirac se retiraron del mercado poco después de su puesta en venta debido a perfiles de toxicidad inaceptables.
Las reacciones idiosincrásicas a fármacos son un acontecimiento poco frecuente que normalmente se muestra como un alto grado de susceptibilidad del individuo. Además, estas reacciones no son normalmente dependientes de la dosis. Actualmente, no hay modelos animales que puedan usarse para evaluar dichas reacciones que ocurren exclusivamente en seres humanos. Por lo tanto, las toxicidades idiosincrásicas del fármaco no pueden evaluarse eficazmente en estudios preclínicos, y a menudo pasan desapercibidas en los ensayos clínicos.
En este momento, los mecanismos de las reacciones idiosincrásicas al fármaco no se entienden bien. Hay una cantidad sustancial de evidencia que sugiere que hay metabolitos químicamente reactivos implicados en toxicidades idiosincrásicas, especialmente para toxicidad en el hígado. Todos los fármacos asociados con toxicidad idiosincrásica forman metabolitos reactivos por diversas rutas metabólicas mediadas predominantemente por enzimas de tipo citocromo P450 (CIP), así como por otras enzimas oxidativas tales como peroxidasas, ciclooxigenasas y mieloperoxidasas. Se plantea la hipótesis de que los fármacos asociados con dichas toxicidades experimentan en primer lugar una activación metabólica para generar metabolitos reactivos tóxicos que se unen covalentemente a proteínas celulares. Estas proteínas modificadas covalentemente son inmunógenas y, de esta manera, desencadenan una respuesta inmune, dando como resultado reacciones idiosincrásicas al fármaco. Una hipótesis alternativa establece que las modificaciones covalentes de proteínas celulares por metabolitos reactivos afectan a las cascadas de transducción de señales y a las funciones vitales de las células, conduciendo a graves consecuencias observadas en la clínica. De esta manera, sigue habiendo una necesidad de procedimientos para identificar metabolitos reactivos.
Los metabolitos químicamente reactivos pueden clasificarse en dos categorías basándose en sus propiedades químicas
- metabolitos reactivos "blandos" y "duros". Los metabolitos reactivos "blandos" comprenden una mayoría de metabolitos electrófilos que incluyen quinonas, quinona iminas, iminoquinona metiuros, epóxidos, óxidos de areno e iones nitrenio, y reaccionan fácilmente con electrófilos "blandos", tales como el grupo sulfhidrilo en cisteína. En contraste, los metabolitos reactivos "duros", vistos más habitualmente como aldehídos, reaccionan preferentemente con electrófilos "duros", tales como aminas de lisina, arginina y ácidos nucleicos. Debido a su instabilidad, la detección y caracterización directa de metabolitos reactivos ha resultado ser extremadamente difícil. Un procedimiento utilizado habitualmente es atrapar los metabolitos reactivos con una molécula de captura, que da como resultado la formación de un aducto estable que puede caracterizarse posteriormente por procedimientos de detección conocidos, por ejemplo por espectrometría de masas en tándem.
Recientemente, Avery, Michael, J., en la Publicación de Patente Europea EP 1.150.120 desvelaron un procedimiento de selección con alta capacidad de producción para identificar compuestos de ensayo que producen metabolitos reactivos. El procedimiento comprende incubar un compuesto de ensayo con un sistema de enzima microsómica de metabolización de fármaco en presencia de glutatión, y detectar aductos de glutatión formados a partir de los mismos usando espectrometría de masas en tándem.
Sin embargo, este procedimiento, identificará metabolitos reactivos así como componentes no reactivos, (incluyendo tanto metabolitos no reactivos como componentes de la mezcla de reacción), formados como resultado de una respuesta común en la detección por espectroscopía de masas, dando como resultado, de esta manera, falsos positivos.
Yan et al., en la Publicación de Patente de Estados Unidos 2005 0287623 A1 desvelan un procedimiento para detectar metabolitos reactivos usando captación de isótopo estable y espectroscopía de masas. Sin embargo, el procedimiento como se describe en Yan et al., solo detecta metabolitos "blandos", no detecta, simultáneamente, metabolitos reactivos tanto "duros" como "blandos".
Yan et al. describen también en Rapid Commun. Mass Spectrom. 2005, 19, 3322-3330 el uso del isótopo estable marcado -Glu-Cys-Gly para la captación de metabolitos y detección de aductos usando técnicas de espectrometría de masas.
Adang et al. desvelan en Biochem. J. 1990, 269, 47-54 -Glu-Cys-Lys no marcado como análogos de glutatión para estudiar el sitio de unión a glutatión en glutatión-S-transferasa.
Sumario de la invención
La presente invención se refiere a un agente de captación marcado isotópicamente para identificar metabolitos reactivos, un compuesto de fórmula (I*)
**(Ver fórmula)**
conocido también como ácido 6-amino-2-[2-(4-amino-4-carboxi-butirilamino)-3-mercapto-propionilamino]-hexanoico, en el que uno o más de los átomos de carbono, nitrógeno, oxígeno, azufre y / o hidrógeno no intercambiable en los grupos con asterisco está marcado isotópicamente.
La presente invención se refiere adicionalmente a un procedimiento de identificación de metabolitos reactivos que comprende (a) incubar un compuesto de fórmula (I)
**(Ver fórmula)**
y / o un compuesto marcado isotópicamente de fórmula (I*)
**(Ver fórmula)**
en la que uno o más de los átomos de carbono, nitrógeno, oxígeno, azufre y / o hidrógeno no intercambiable en los grupos con asterisco está marcado isotópicamente; con un compuesto de ensayo y una enzima de metabolización de fármaco; para dar una mezcla de producto que comprende uno o más aductos; y
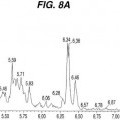
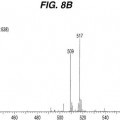
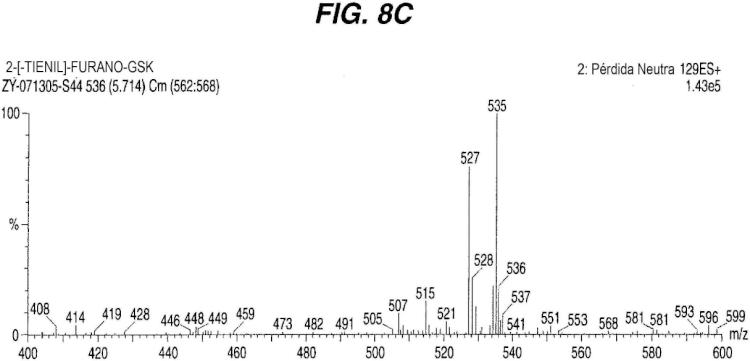
(b) detectar dicho uno o más aductos, de acuerdo con procedimientos conocidos y / o de acuerdo con los procedimientos descritos en el presente documento, por ejemplo mediante espectroscopía de masas con pérdida neutra.
La presente invención se refiere adicionalmente a un procedimiento para detectar metabolitos reactivos de un compuesto de ensayo que comprende
(a) incubar un compuesto de ensayo con una mezcla que comprende un compuesto de fórmula (I)
**(Ver fórmula)**
un compuesto marcado isotópicamente de fórmula (I*)
**(Ver fórmula)**
en la que uno o más de los átomos de carbono, nitrógeno, oxígeno, azufre o hidrógeno no intercambiable en los grupos con asterisco está marcado isotópicamente; y una enzima de metabolización de fármaco;
para producir una mezcla de producto que comprende uno o más aductos;
(b) detectar uno o más dobletes isotópicos en un espectro de masas con pérdida neutra del uno o más aductos producidos en la Etapa (a), en el que el doblete difiere en masa por la diferencia en masa entre el compuesto de fórmula
(I) y el compuesto marcado isotópicamente de fórmula (I*).
La presente invención se refiere adicionalmente a un procedimiento de identificación de metabolitos reactivos (incluyendo metabolitos reactivos tanto "blandos" como "duros"), usando una mezcla de un compuesto de fórmula (I) y un compuesto marcado isotópicamente de fórmula (I*), en la que uno o más de los átomos de carbono, nitrógeno, oxígeno, azufre o hidrógeno no intercambiable en los... [Seguir leyendo]
Reivindicaciones:
1. Un compuesto marcado isotópicamente de fórmula (I*)
**(Ver fórmula)**
en la que uno o más de los átomos de carbono, nitrógeno, oxígeno, azufre o hidrógeno no intercambiable en los grupos con asterisco está marcado isotópicamente.
**(Ver fórmula)**
3. Un procedimiento para detectar metabolitos reactivos de un compuesto de ensayo que comprende
(a) incubar un compuesto de ensayo con una mezcla que comprende un compuesto de fórmula (I)
**(Ver fórmula)**
un compuesto marcado isotópicamente de fórmula (I*)
**(Ver fórmula)**
en la que uno o más de los átomos de carbono, nitrógeno, oxígeno, azufre o hidrógeno no intercambiable en los grupos con asterisco está marcado isotópicamente; y una enzima de metabolización de fármaco;
para dar una mezcla de producto que comprende uno o más aductos;
(b) detectar uno o más dobletes isotópicos en un espectro de masas con pérdida neutra del uno o más aductos producidos en la Etapa (a), en el que el doblete difiere en masa por la diferencia en masa entre el compuesto de fórmula
(I) y el compuesto marcado isotópicamente de fórmula (I*).
4. El compuesto de la reivindicación 1 o el procedimiento de la reivindicación 3, en el que el compuesto marcado isotópicamente de fórmula (I*) está marcado con al menos un isótopo seleccionado entre el grupo que consiste en 13C,15N, 18O y 2H.
5. El compuesto o el procedimiento de la reivindicación 4, en el que el compuesto marcado isotópicamente de fórmula (I*) está marcado con de uno a diez isótopos seleccionados entre el grupo que consiste en 13C y 15N.
6. El procedimiento de la reivindicación 3, en el que la proporción molar del compuesto de fórmula (I) al compuesto marcado isotópicamente de fórmula (I*) es 1:1 y en el que el doblete isotópico difiere en una masa de 8 unidades de masa.
7. El procedimiento de la reivindicación 3, en el que el compuesto marcado isotópicamente de fórmula (I) es el compuesto de fórmula (l-IS)
8. El procedimiento de la reivindicación 7, en el que la proporción molar del compuesto de fórmula (I) al compuesto marcado isotópicamente de fórmula (l-IS) es 1:1.
9. El procedimiento de la reivindicación 8, en el que la enzima de metabolización de fármaco se selecciona entre el grupo que consiste en microsomas hepáticos humanos, enzimas de tipo citocromo P450 en combinación con el cofactor NADPH y enzimas de tipo citocromo P450 en combinación con el sistema de regeneración de NADPH.
**(Ver fórmula)**
**(Ver fórmula)**
y un compuesto marcado isotópicamente de fórmula (I*)
**(Ver fórmula)**
en la que uno o más de los átomos de carbono, nitrógeno, oxígeno, azufre o hidrógeno no intercambiable en los grupos con asterisco está marcado isotópicamente.
11. Un procedimiento para detectar metabolitos reactivos de un compuesto de ensayo que comprende
(a) incubar un compuesto de ensayo con una mezcla que comprende un compuesto de fórmula (I),
**(Ver fórmula)**
un compuesto marcado isotópicamente de fórmula (l-IS)
**(Ver fórmula)**
y una enzima de metabolización de fármaco; para dar una mezcla de producto que comprende uno o más aductos;
(b) medir un espectro de masas con pérdida neutra del uno o más aductos producidos en la etapa (a); y
(c) detectar uno o más dobletes isotópicos en el espectro de masas con pérdida neutra de la etapa (b), en el que los dobletes isotópicos difieren en masa de 8 Da.
12. Un procedimiento para detectar metabolitos reactivos de un compuesto de ensayo que comprende Etapa A: incubar una mezcla que comprende
(a) un compuesto de ensayo;
(b) un compuesto de fórmula (I)
(c) un compuesto marcado isotópicamente de fórmula (l-IS)
en la que la proporción molar del compuesto de fórmula (I) al compuesto marcado isotópicamente de fórmula (l-IS) es 1:1; y
(c) una enzima de metabolización de fármaco seleccionada ente el grupo que consiste en microsomas hepáticos
**(Ver fórmula)**
**(Ver fórmula)**
15 humanos, enzimas de tipo citocromo P450 en combinación con el co-factor NADPH y enzimas de tipo citocromo P450 en combinación con el sistema de regeneración de NADPH;
para dar una mezcla de producto que comprende uno o más productos de incubación seleccionados ente el grupo que consiste en
(a) un metabolito no reactivo; 20 (b) un aducto formado entre el compuesto de fórmula (I) y un metabolito reactivo; y
(c) un aducto formado entre el compuesto marcado isotópicamente de fórmula (l-IS) y un metabolito reactivo; Etapa B: medir un espectro de masas con pérdida neutra de la mezcla de producto producida en la Etapa (A); y Etapa C: detectar uno o más dobletes isotópicos en un espectro de masas con pérdida neutra de la Etapa (B), en el que
los dobletes isotópicos difieren en masa de 8 Da. 25 13. Un procedimiento para detectar metabolitos reactivos de un compuesto de ensayo que comprende
(a) incubar un compuesto de ensayo con una mezcla que comprende un compuesto no marcado isotópicamente de fórmula (I)
**(Ver fórmula)**
un compuesto marcado isotópicamente de fórmula (I*) en la que uno o más de los átomos de carbono, nitrógeno, oxígeno, azufre y / o hidrógeno no intercambiable en los grupos con asterisco está marcado isotópicamente;
**(Ver fórmula)**
y una enzima de metabolización de fármaco para dar una mezcla de producto que comprende uno o más aductos;
(b) separar el uno o más aductos de la etapa (a);
(c) medir un espectro de masas con pérdida neutra de dichos aductos separados;
(d) detectar uno o más dobletes isotópicos en el espectro de masas con pérdida neutra de dichos aductos separados, en el que el doblete difiere en masa por la diferencia en masa entre el compuesto no marcado isotópicamente de fórmula (I) y el compuesto marcado isotópicamente de fórmula (I).
14. Un procedimiento para detectar metabolitos reactivos de un compuesto de ensayo que comprende
(a) incubar un compuesto de ensayo con una mezcla que comprende un compuesto no marcado isotópicamente de fórmula (I)
**(Ver fórmula)**
un compuesto marcado isotópicamente de fórmula (l-IS)
**(Ver fórmula)**
en la que la proporción molar del compuesto de fórmula (I) al compuesto marcado isotópicamente de fórmula (l-IS) es 1:1; y una enzima de metabolización de fármaco para dar una mezcla de producto que comprende uno o más aductos;
(b) separar el uno o más aductos de la etapa (a);
(c) medir un espectro de masas con pérdida neutra de dichos aductos separados;
(d) detectar uno o más dobletes isotópicos en el espectro de masas con pérdida neutra de dichos aductos separados, en el que el doblete difiere en masa de 8 Da.
15. Un procedimiento para identificar un candidato a fármaco que comprende
(a) incubar un compuesto de ensayo con una mezcla que comprende un compuesto no marcado isotópicamente de fórmula (I)
**(Ver fórmula)**
un compuesto marcado isotópicamente de fórmula (I*)
**(Ver fórmula)**
en la que uno o más de los átomos de carbono, nitrógeno, oxígeno, azufre o hidrógeno no intercambiable en los grupos con asterisco está marcado isotópicamente; y una enzima de metabolización de fármaco; para dar una mezcla de producto;
(b) medir un espectro de masas con pérdida neutra de la mezcla de producto producida en la Etapa (a); y 15 (c) detectar la ausencia de dobletes isotópicos en el espectro de masas con pérdida neutra de la Etapa (b).
16. El procedimiento de la reivindicación 1, el compuesto de la reivindicación 3 o el procedimiento de la reivindicación 15, en el que el compuesto marcado isotópicamente de fórmula (I) está marcado con seis átomos 13C y dos átomos 15N.
17. La mezcla de la reivindicación 10 o el procedimiento de la reivindicación 16, en el que el compuesto marcado
isotópicamente de fórmula (I*) está marcado con seis átomos 13C y dos átomos 15N y en el que la proporción molar del 20 compuesto de fórmula (I) al compuesto marcado isotópicamente de fórmula (I*) es 1:1.
18. El procedimiento de la reivindicación 17, en el que la enzima de metabolización de fármaco son enzimas de tipo citocromo P450 en combinación con el co-factor NADPH o enzimas de tipo citocromo P450 en combinación con el sistema de regeneración de NADPH.
19. Un procedimiento para identificar un candidato a fármaco que comprende
25 (a) incubar un compuesto de ensayo con una mezcla que comprende un compuesto no marcado isotópicamente de fórmula (I)
**(Ver fórmula)**
un compuesto marcado isotópicamente de fórmula (l-IS)
38
**(Ver fórmula)**
y una enzima de metabolización de fármaco; para dar una mezcla de producto;
(b) medir un espectro de masas con pérdida neutra de la mezcla de producto producida en la Etapa (a); y
(c) detectar la ausencia de dobletes isotópicos en el espectro de masas con pérdida neutra de la Etapa (b).
20. El procedimiento de la reivindicación 3, la mezcla de la reivindicación 10 o el procedimiento de la reivindicación 19, en el que la proporción molar del compuesto de fórmula (I) al compuesto marcado isotópicamente de fórmula (I*) es 1:1.
21. El procedimiento de la reivindicación 3, en el que la enzima de metabolización de fármaco son enzimas de tipo citocromo P450 en combinación con el co-factor NADPH o enzimas de tipo citocromo P450 en combinación con el sistema de regeneración de NADPH.
22. El procedimiento de la reivindicación 19, en el que la proporción molar del compuesto de fórmula (I) al compuesto marcado isotópicamente de fórmula (I*) es 1:1 y en el que la enzima de metabolización de fármaco son enzimas de tipo citocromo P450 en combinación con el co-factor NADPH o enzimas de tipo citocromo P450 en combinación con el sistema de regeneración de NADPH.
23. El procedimiento de la reivindicación 3, el procedimiento de la reivindicación 9 o el procedimiento de la reivindicación 21, en el que el espectro de masas con pérdida neutra se mide usando IEN-EM/EM o EM/EM.
Patentes similares o relacionadas:
Determinación de sarcosina utilizando sarcosina oxidasa y peroxidasa de rábano picante unidas a nanopartículas de Fe2O3/AU mediante quitosano, del 19 de Junio de 2019, de Prevention Medicals s.r.o: Método de unión delas enzimas sarcosina oxidasa yperoxidasa de rábano picante a las nanopartículas de Fe2O3/Au utilizando quitosano, caracterizado […]
Microsomas inhibidos de forma irreversible para CYP450 y su uso en el fenotipado enzimático de rutas metabólicas, del 29 de Mayo de 2019, de LES LABORATOIRES SERVIER: Método para la preparación de microsomas aislados y conservados, que comprenden un citocromo P450 (CYP450) inhibido irreversiblemente, para su […]
DISPOSITIVO ELECTRÓDICO Y PROCEDIMIENTO DE MEDIDA PARA LA DETECCIÓN DE ÁCIDO LÁCTICO, del 25 de Abril de 2019, de UNIVERSIDAD DE BURGOS: Dispositivo electródico para la detección de ácido láctico sencillo y portable que comprende un soporte plástico cuadrangular con una primera […]
Arsenito oxidasa modificada y un biosensor para detectar arsenito, del 9 de Abril de 2019, de The Bio Nano Centre Limited: Un microorganismo modificado para expresar una enzima arsenito oxidasa heteróloga modificada para prevenir la translocación al periplasma en donde la enzima comprende la […]
Ensayos rápidos, con bajo volumen de muestra, para colesterol y triglicéridos, del 20 de Marzo de 2019, de Theranos IP Company, LLC: Un método para medir al menos dos componentes lipoproteicos en una muestra de sangre procedente de un sujeto, en donde dichos al menos dos componentes lipoproteicos se seleccionan […]
Fructosil aminoácido oxidasa, del 13 de Febrero de 2019, de F. HOFFMANN-LA ROCHE AG: Una fructosil aminoácido oxidasa mutante modificada en una posición correspondiente a la posición 56 de la secuencia de aminoácidos expuesta en SEQ ID NO: 1 sustituyendo […]
Método para señalar al usuario para que añada una muestra adicional a una tira de prueba, método para medir la temperatura de una muestra y métodos para determinar la concentración de un analito basados en amperometría controlada, del 9 de Enero de 2019, de Ascensia Diabetes Care Holdings AG: Un método para señalar a un usuario para que añada una muestra adicional a una tira de sensor, que comprende: determinar si la tira de sensor es llenada […]
Composición y uso de sustancias para la estabilización in vitro de glucosa, lactato y homocisteína en sangre, del 18 de Octubre de 2017, de Weser-Bissé, Petra: Un método para el tratamiento de una muestra de sangre in vitro, en el que la sangre se mezcla in vitro con una composición que comprende i) al menos un […]