PROCESO ESCALABLE PARA LA OBTENCION DE FICOCIANINA.
Proceso escalable para la obtención de ficocianina. Proceso de tres etapas para la obtención y purificación de ficocianina procedente de microalgas del género Anabaena,
caracterizado por ser escalable y tener un alto rendimiento. La primera etapa consiste en una ruptura celular mediante choque osmótico que libera el material citoplasmático, usando tampón de fosfatos. La segunda etapa utiliza una columna cromatográfica de adsorción en lecho expandido constituida por un intercambiador iónico como fase adsorbente. La tercera etapa es un proceso adicional cromatográfico en columna de intercambio iónico que utiliza como fase estacionaria un cambiador aniónico, funcionando en formato empaquetado. En condiciones óptimas, tras la segunda etapa se obtiene un rendimiento en torno al 87% de recuperación de ficocianina, mientras que tras la tercera etapa se obtiene un rendimiento global del proceso del 64% de ficocianina pura
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P200702782.
Solicitante: UNIVERSIDAD DE JAEN
UNIVERSIDAD DE ALMERIA.
Nacionalidad solicitante: España.
Provincia: JAÉN.
Inventor/es: BERMEJO ROMAN,RUPERTO, ACIEN FERNANDEZ,FCO. GABRIEL.
Fecha de Solicitud: 16 de Octubre de 2007.
Fecha de Publicación: .
Fecha de Concesión: 24 de Junio de 2010.
Clasificación Internacional de Patentes:
- C07K1/18 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 1/00 Procedimientos generales de preparación de péptidos. › Cromatografía de intercambio iónico.
- C07K1/22 C07K 1/00 […] › Cromatografía de afinidad o técnicas análogas basadas en procesos de absorción selectiva.
- C07K1/30 C07K 1/00 […] › por precipitación.
- C07K1/36 C07K 1/00 […] › por una combinación de varios procesos de diferentes tipos.
- C07K14/405 C07K […] › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › de algas.
- C07K14/795 C07K 14/00 […] › Péptidos que contienen anillos de porfirina o corrina.
Clasificación PCT:
- C07K1/18 C07K 1/00 […] › Cromatografía de intercambio iónico.
- C07K1/22 C07K 1/00 […] › Cromatografía de afinidad o técnicas análogas basadas en procesos de absorción selectiva.
- C07K1/30 C07K 1/00 […] › por precipitación.
- C07K1/36 C07K 1/00 […] › por una combinación de varios procesos de diferentes tipos.
- C07K14/405 C07K 14/00 […] › de algas.
- C07K14/795 C07K 14/00 […] › Péptidos que contienen anillos de porfirina o corrina.
Fragmento de la descripción:
Proceso escalable para la obtención de ficocianina.
Sector de la técnica
La C-ficocianina es una macromolécula biológica perteneciente a la familia de las ficobiliproteinas con aplicaciones en diversos sectores industriales como consecuencia de sus extraordinarias propiedades espectroscópicas, tanto absorciométricas como fluorimétricas.
En concreto, su elevado coeficiente de extinción molar a ? = 620 nm, le confiere un intenso color azul muy apropiado para su empleo como colorante natural, mientras que su elevado rendimiento cuántico de fluorescencia permite su detección con mayor o similar sensibilidad que otros fluoróforos convencionales.
Estado de la técnica
Las ficobiliproteinas son una familia de proteínas que poseen grupos prostéticos tetrapirrólicos, denominados bilinas, que en su estado funcional se encuentran enlazados covalentemente a los residuos cisteína de las cadenas de las apoproteínas. Estas proteínas se encuentran en algas verde-azuladas denominadas cianobacterias, en una clase de algas unicelulares biflageladas eucariotas denominadas algas criptomonadales y en algas rojas o rodofitas. En todos estos organismos las ficobiliproteínas actúan como pigmentos fotosintéticos antena y suelen estar organizadas formando parte de unas macroestructuras celulares denominadas ficobilisomas. Atendiendo a sus propiedades espectroscópicas de absorción se clasifican en tres grupos principales: ficoeritrinas (PEs, ?max-540-570 nm), ficocianinas (PCs, ?max-610-620 nm) y aloficocianinas (APCs, ?max-650-655 nm).
Debido a sus ventajosas propiedades espectrales, así como a su estabilidad y condiciones de solubilidad, las ficobiliproteínas se utilizan actualmente en multitud de aplicaciones, entre las que destacan su uso como marcadores fluorescentes de células y macromoléculas en investigación biomédica y clínica y en diversas técnicas fluorimétricas. Otra aplicación de las ficobiliproteínas es su uso como colorantes naturales en alimentación y cosmética reemplazando a colorantes de tipo sintético que, en general, suelen ser tóxicos e incluso cancerígenos en organismos sensibles. Por último, se conoce también su importante valor terapéutico debido a su actividad inmunomoduladora y anticancerígena.
Dentro de la familia de las ficobiliproteínas, la C-ficocianina constituye una macromolécula interesante para el conjunto de aplicaciones anteriormente citadas como consecuencia de sus características espectroscópicas. Además, posee propiedades fluorescentes específicas tales como su elevado rendimiento cuántico y desplazamiento de Stokes, que evitan interferencias en la detección procedente de matrices biológicas u otros medios en los que puede utilizarse. Todas estas ventajas hacen que la C-ficocianina se esté utilizando en la actualidad como marcador fluorescente conjugado a anticuerpos, lectinas, polisacáridos, DNA y otras macromóleculas y macroestructuras supramoleculares. También se usa en el diseño y caracterización de elementos fotosensibles en biosensores y en tratamientos terapéuticos desarrollados a nivel de animales de experimentación. Otras utilidades, debidas a su intenso y único color azul, son el empleo como colorante natural en preparaciones cosméticas, farmacéuticas y de la industria alimentaria.
Es habitual que los esquemas de purificación de proteínas contengan un considerable número de etapas que, a su vez, se suelen dividir en subetapas que, usualmente, no son escalables. En el estado de la técnica actual, la C-ficocianina se obtiene, en la mayoría de los casos, mediante metodologías que utilizan tratamientos previos que involucran ruptura celular usando ultrasonidos, congelación-descongelación, tratamiento con lisozima, etc., posterior precipitación con sulfato amónico y procesos de diálisis, seguidos de cromatografia de intercambio iónico, cromatografia de filtración por gel o bien cromatografia de adsorción sobre hidroxiapatito. Todos estos procedimientos presentan algunos inconvenientes que hasta ahora han limitado la obtención de cantidades elevadas de esta proteína, de entre los cuales cabe destacar:
- Poseen rendimientos globales bajos porque la abundancia de etapas en los procesos de purificación conlleva una paralela y significante pérdida del producto de interés al no optimizar cada una de las etapas utilizadas al objeto de minimizar esas pérdidas.
- Son económicamente muy costosos porque involucran una gran cantidad de etapas y subetapas que repercuten negativamente en el coste global medio de producción.
- Son difícilmente escalables porque los procesos implicados en la obtención del producto sólo han sido estudiados a escala analítica de laboratorio y en la mayoría de los casos las etapas que se precisan no permiten su paso al nivel de planta piloto o industrial.
- Pueden alterar la estructura nativa de la proteína porque algunas de las etapas utilizadas en las metodologías comentadas utilizan sistemas físicos o químicos que influyen en la estructura de la proteína a purificar, sin que se haya estudiado la posible reversibilidad o irreversibilidad de los efectos producidos en la macromolécula por los mencionados tratamientos.
Por todo lo anterior, la presente invención aporta, respecto a otros procedimientos conocidos, un mayor rendimiento del proceso, extrayéndose del orden del 64% del contenido de la C-ficocianina contenida en la biomasa de ciertas microalgas, y una reducción de costes de obtención. Además, a diferencia de los procesos conocidos, las etapas en que se divide la purificación son fácilmente escalables.
Explicación de la invención
La presente invención tiene por objeto el desarrollo de un proceso basado en las propiedades de la cromatografía de adsorción en lecho expandido, para la purificación a elevado rendimiento de la proteína C-ficocianina procedente de microalgas del género Anabaena.
Proceso de tres etapas para la obtención y purificación de ficocianina procedente de microalgas del género Anabaena, caracterizado por ser escalable y tener un alto rendimiento. La primera etapa consiste en una ruptura celular mediante choque osmótico que libera el material citoplasmático, usando tampón de fosfatos. La segunda etapa utiliza una columna cromatográfica de adsorción en lecho expandido constituida por un intercambiador iónico como fase adsorbente. La tercera etapa es un proceso adicional cromatográfico en columna de intercambio iónico que utiliza como fase estacionaria un cambiador aniónico, funcionando en formato empaquetado. En condiciones óptimas, tras la segunda etapa se obtiene un rendimiento en torno al 87% de recuperación de ficocianina, mientras que tras la tercera etapa se obtiene un rendimiento global del proceso del 64% de ficocianina pura.
Se describen a continuación las tres etapas para la obtención y purificación de C-ficocianina a partir de microalgas del género Anabaena.
Primera etapa: Pretratamiento inicial en el que se mezcla la biomasa de microalga con tampón y tras la correspondiente homogeneización, se produce la ruptura celular debido al choque osmótico. De esta forma, se permite la liberación del contenido intracelular del cual forman parte los ficobilisomas, que son las macroestructuras que contienen las ficobiliproteínas.
A continuación, el homogeneizado se somete a un proceso de centrifugación que sedimenta las macroestructuras supramoleculares (como restos de paredes celulares) y proporciona un sobrenadante (extracto crudo) en el que se encuentran solubilizadas la mayor parte de los componentes del microalga. En este extracto crudo, junto a otras macromoléculas y solutos moleculares, se encuentra la C-ficocianina. El rendimiento de esta primera etapa alcanza el 100% de recuperación de la ficocianina contenida en el microalga.
Segunda etapa: Consiste en la utilización de una columna cromatográfica de adsorción en lecho expandido constituida por un intercambiador iónico como fase adsorbente. Esta etapa permite simplificar mucho el proceso frente a metodologías previas convencionales. Se han estudiado y optimizado las características y condiciones que deben tener tanto la columna de lecho expandido, como la fase móvil utilizada y la muestra a cromatografiar. Los resultados muestran que utilizando una fase móvil compuesta por tampón fosfato, tras la aplicación de la muestra a la columna, se adsorbe preferencialmente...
Reivindicaciones:
1. Proceso de obtención y purificación de C-ficocianina en dos etapas, mediante la ruptura celular por choque osmótico y la posterior utilización de cromatografía de adsorción en lecho expandido, que utiliza como materia prima microalgas del género Anabaena y obtiene un porcentaje de recuperación de C-ficocianina mayor del 75% del contenido en la materia prima.
2. Proceso de obtención y purificación de C-ficocianina según reivindicación 1, caracterizado por la obtención de disoluciones concentradas de C-ficocianina con ligeras impurezas de otras proteínas, de pureza suficiente para diversos usos, entre ellos el uso en la industria alimentaria y cosmética.
3. Proceso de obtención y purificación de C-ficocianina según reivindicaciones 1 ó 2, caracterizado por el empleo de tampón, preferentemente tampón fosfato a pH entre 5 y 7.5, más preferentemente tampón fosfato 50 mM pH 7, en la primera etapa de ruptura celular mediante choque osmótico.
4. Proceso de obtención y purificación de C-ficocianina según cualquiera de las reivindicaciones anteriores, caracterizado por utilizar, tras la etapa de ruptura celular mediante choque osmótico, fases sucesivas de mezcla, homogeneización mecánica y centrifugación.
5. Proceso de obtención y purificación de C-ficocianina según cualquiera de las reivindicaciones anteriores, caracterizado por el empleo en la primera etapa de una razón de 1 litro de tampón por cada 0.1-1.0 kilogramos de biomasa liofilizada, preferentemente 1 litro de tampón por cada 0.25 kilogramos de biomasa liofilizada.
6. Proceso de obtención y purificación de C-ficocianina según cualquiera de las reivindicaciones anteriores, caracterizado porque la centrifugación se realiza durante 5-30 minutos a 5000-30000 rpm, preferentemente durante 10 minutos a 15000 rpm.
7. Proceso de obtención y purificación de C-ficocianina según cualquiera de las reivindicaciones anteriores, caracterizado porque en la segunda etapa se utiliza una columna cromatográfica de adsorción en lecho expandido, preferentemente de 1.5-6.0 cm. de diámetro interno y 50 cm. de altura, constituida por un intercambiador iónico como fase adsorbente. La columna se desarrolla utilizando una fase móvil constituida por tampón, preferentemente tampón fosfato 50 mM pH 7 en las fases de aplicación de la muestra y lavado de la columna y tampón fosfato 500 mM pH 7 en la fase de desorción.
8. Proceso de obtención y purificación de C-ficocianina según cualquiera de las reivindicaciones anteriores, caracterizado por la utilización en la segunda etapa de una velocidad de flujo de fase móvil de 200 cm h-1, en las fases de aplicación de la muestra y lavado de la columna y de 86 cm. h-1 en la fase de elución de la muestra.
9. Proceso de obtención y purificación de C-ficocianina según cualquiera de las reivindicaciones anteriores, en el que después de la ruptura celular y la cromatografía de adsorción en lecho expandido se emplea una tercera etapa de cromatografía de intercambio iónico en lecho empaquetado clásico, de forma que el proceso compuesto por las tres etapas alcanza un porcentaje de recuperación de C-ficocianina mayor del 60% del contenido en la materia prima.
10. Proceso de obtención y purificación de C-ficocianina según reivindicación 9, caracterizado porque en la tercera etapa se utiliza una columna cromatográfica de intercambio iónico en lecho empaquetado clásico, preferentemente de DEAE-celulosa DE-52.
11. Proceso de obtención y purificación de C-ficocianina según reivindicaciones 9 ó 10, caracterizado por utilizar en la tercera etapa una columna cromatográfica con un diámetro interno de entre 2.5 - 9.0 cm., y 20 cm. de altura.
12. Proceso de obtención y purificación de C-ficocianina según reivindicación 9, 10 u 11, caracterizado porque la columna es desarrollada utilizando una fase móvil constituida por tampón fosfato, preferentemente tampón fosfato 50 mM pH 7, en las fases de equilibrado y aplicación de la muestra.
13. Proceso de obtención y purificación de C-ficocianina según reivindicación 9, 10, 11 ó 12, caracterizado porque la columna es desarrollada utilizando una fase móvil constituida por tampón fosfato, preferentemente tampón fosfato 290 mM pH 7, en la fase de elución.
14. Proceso de obtención y purificación de C-ficocianina según reivindicaciones 9, 10, 11, 12 o 13, caracterizado por el empleo en la tercera etapa de una velocidad de flujo de fase móvil de 21 cm h-1 en las fases de aplicación, elución y lavado de la columna.
15. Proceso de obtención y purificación de C-ficocianina según cualquiera de las reivindicaciones anteriores, en el que la especie utilizada como materia prima es Anabaena marina.
Patentes similares o relacionadas:
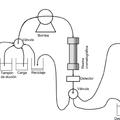 Purificación de proteínas, del 29 de Julio de 2020, de UCB Biopharma SRL: Un proceso para la purificación de una proteína de interés a partir de una mezcla que comprende las etapas de
a) en un ciclo de cromatografía operativo, […]
Purificación de proteínas, del 29 de Julio de 2020, de UCB Biopharma SRL: Un proceso para la purificación de una proteína de interés a partir de una mezcla que comprende las etapas de
a) en un ciclo de cromatografía operativo, […]
Membranas para cromatografía formadas por reacciones de polimerización clic de tiol-eno o tiol-ino, del 10 de Junio de 2020, de Merck Millipore Ltd: Un material compuesto, que comprende: un miembro de soporte, que comprende una pluralidad de poros que se extienden a través del miembro de […]
Un procedimiento de cromatografía de reparto débil, del 6 de Mayo de 2020, de WYETH LLC: Un procedimiento de recuperación de un producto purificado de un fluido de carga que incluye una o más impurezas, que comprende las etapas de: hacer pasar el fluido […]
Procedimiento de purificación de polipéptidos, del 22 de Abril de 2020, de CSL LIMITED: Procedimiento de purificación de un polipéptido de interés por cromatografía de intercambio catiónico en el que un compuesto químico se añade en una concentración de al menos […]
Etiqueta de epítopo y método de detección, captura y/o purificación de polipéptidos etiquetados, del 15 de Abril de 2020, de ChromoTek GmbH: Péptido epítopo aislado que tiene de 12 a 25 aminoácidos, en donde la secuencia de aminoácidos comprende una secuencia según se define en SEQ ID NO: 32 (X1X2RX4X5AX7SX9WX11X12), […]
Matriz de cromografía de afinidad, del 25 de Marzo de 2020, de LABORATOIRE FRANCAIS DU FRACTIONNEMENT ET DES BIOTECHNOLOGIES SOCIETE ANONYME: Matriz de cromatografía de afinidad, en forma de gel, que comprende unas partículas de polímero sobre las cuales se injerta al menos un oligosacárido […]
Sistema de tampón para purificación de proteína, del 26 de Febrero de 2020, de GLAXOSMITHKLINE LLC: Un sistema de cromatografía que comprende: (i) un sistema de tampón de múltiples componentes libre de cloruro de sodio para la purificación de una […]
Proteína mutante, del 19 de Febrero de 2020, de Cytiva BioProcess R&D AB: Una proteína de unión a inmunoglobulina que se une a regiones de una molécula de inmunoglobulina distintas de las regiones determinantes de […]