MOLECULAS DE ANTICUERPO ESPECIFICAS DE LA PROTEINA DE ACTIVACION DE FIBROBLASTOS E INMUNOCONJUGADOS QUE LAS CONTIENEN.
- Molécula de anticuerpo anti FAP-α, fragmento o derivado del mismo,
seleccionado entre: a. un anticuerpo monoclonal murino definido por: i. una cadena pesada variable que comprende la región de aa 20 a 136 de la secuencia SEQ ID NO: 1; ii. una cadena ligera variable que comprende una región de aa 23 a 129 de la secuencia SEQ ID NO:2 y iii. la subclase IgG2a kappa; b. un anticuerpo quimérico derivado del anticuerpo monoclonal murino definido en a) por injerto CDR o por reconstrucción superficial; c. un anticuerpo humanizado derivado del anticuerpo monoclonal murino definido en a) por injerto CDR o por reconstrucción superficial
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2006/070185.
Solicitante: BOEHRINGER INGELHEIM INTERNATIONAL GMBH.
Nacionalidad solicitante: Alemania.
Dirección: BINGER STR. 173 55216 INGELHEIM AM RHEIN ALEMANIA.
Inventor/es: HEIDER, KARL-HEINZ, OSTERMANN, ELINBORG, KALAT,MILENA, ADOLF,GUENTHER.
Fecha de Publicación: .
Fecha Solicitud PCT: 22 de Diciembre de 2006.
Fecha Concesión Europea: 18 de Agosto de 2010.
Clasificación Internacional de Patentes:
- A61K47/48T2C
- C07K16/40 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 16/00 Inmunoglobulinas, p. ej. anticuerpos mono o policlonales. › contra enzimas.
Clasificación PCT:
- A61K47/48
- A61P19/02 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 19/00 Medicamentos para el tratamiento de problemas del esqueleto. › para problemas de las articulaciones, p.ej. artritis, artrosis.
- A61P35/00 A61P […] › Agentes antineoplásicos.
- C07K16/40 C07K 16/00 […] › contra enzimas.
- C07K16/46 C07K 16/00 […] › Inmoglobulinas híbridas (híbridos de una inmunoglobulina con un péptido distinto de una inmunoglobulina C07K 19/00).
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia.
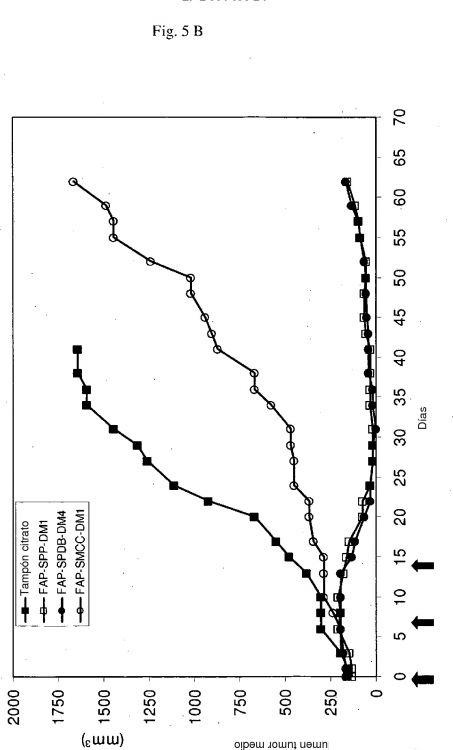
Fragmento de la descripción:
La invención se refiere a nuevas moléculas de anticuerpos anti-FAP-α y a inmunoconjugados citotóxicos que contienen dicho anticuerpo y un agente citotóxico, por ejemplo, un maitansinoide, a compuestos farmacéuticos que comprenden dichos inmunoconjugados y a su utilización en la terapia de tumores.
Se han producido numerosos intentos de mejorar la eficacia de los medicamentos antineoplásicos por conjugación de dichos medicamentos con anticuerpos contra antígenos asociados a tumores, a efectos de aumentar la concentración local del medicamento por administración direccionada hacia el tumor. Muchos de estos intentos han tenido un éxito limitado y se han discutido algunas de las razones en la literatura para explicar el fallo. Para medicamentos anticáncer que actúan de forma estequiométrica, tales como por ejemplo la doxorubicina o metotrexato, son necesarias concentraciones intracelulares relativamente altas para ejercer la citotoxicidad requerida. Estas concentraciones se cree que son difíciles de conseguir con muchos conjugados anticuerpo-medicamento a causa de (a) insuficiente efectividad de muchos medicamentos anticáncer habituales, (b) baja concentración en la superficie celular de las dianas antígeno, (c) internalización poco eficaz de los complejos antígeno-anticuerpo en la célula diana y (d) liberación poco eficaz del medicamento libre con respecto al conjugado dentro de la célula objetivo o diana (Chari y otros, 1992).
Dos de los inconvenientes antes mencionados, es decir,
(a) y (d) fueron objeto del trabajo de Chari y colaboradores
(Chari y otros, 1992; Liu y otros, 1996; patente US 5.208.020). Estos autores desarrollaron conjugados de anticuerpos en los que el anticuerpo está ligado a unmaitansinoide con intermedio de un enlace de bisulfuro. Las maitansinas pertenecen a la clase de antibióticos macrólidos Ansa que derivan de Nocardia sp.. La maitansina ansamitocina P-3, producida por fermentación bacteriana, es utilizada como molécula precursora para la fabricación de maitansinoide DM1. La maitansina y derivados actúan como agentes antimitóticos (inhibidores de la polimerización de la tubulina) similar a la vincristina, pero con una efectividad notablemente más elevada que la vincristina u otros agentes quimioterapéuticos conocidos (DM1 es tóxico con respecto a células in vitro a una concentración de ~10-10 M). En contraste con la elevada citotoxicidad del maitansinoide libre, el conjugado del anticuerpo tiene una toxicidad que es varios órdenes de magnitud inferior en células antígeno-negativas en comparación con células antígeno-positivas. El enlace por unión de bisulfuro tiene la ventaja de que estos enlaces son fraccionados fácilmente dentro de las células objetivo por glutationa intracelular, liberando el medicamento libre altamente tóxico. Este enfoque ha sido aplicado a anticuerpos contra antígenos asociados a tumor, por ejemplo, el conjugado C242-DM1 (Liu y otros, 1996; Lambert y otros, 1998) y HuN901DM1 (Chari y otros, 2000). No obstante, la aplicación de estos conjugados está restringida debido a la expresión limitada de los respectivos antígenos diana. Por ejemplo, el antígeno reconocido por N901 (CD56, N-CAM) es expresado predominantemente por tumores de origen neuroendocrino, la expresión del antígeno C242 (CanAg) está limitada principalmente a tumores derivados del tracto G1.
Para mejorar este enfoque aplicándolo a antígenos apropiados asociados a tumor con modelo de expresión de antígeno favorable, elevada y específica concentración de antígeno en la superficie de la célula dentro de los tejidos objetivo y un eficaz proceso de internalización que transporta el conjugado antígeno de complejo-anticuerpo a las células, se desarrollaron inmunoconjugados anti-CD44-anticuerpo-DM1 (WO 02/094325).
No obstante, existe todavía la necesidad de agentes inmunoterapéuticos innovativos que tengan un efecto inhibitorio en antígenos diana asociados a tumores que tienen baja expresión en tejidos normales y elevada expresión en gran variedad de tumores.
Los análisis inmunohistoquímicos han demostrado que la Proteína de Activación de Fibroblastos (a continuación designada también “FAP”) muestra una distribución restringida en tejidos normales. Entre tejidos lesionados de adultos no neoplásicos, la expresión del FAP ha sido observada en los fibroblastos activados de la curación de heridas, en artritis reumatoide y en células estrelladas hepáticas activadas durante la cirrosis, mientras que en tejidos adultos normales solamente son positivos a FAP las células isleta (A) pancreáticas. En contraste, se observan fibroblastos estromales positivos a FAP en el estroma de más de 90% de tumores malignos de pecho, ovarios, colorrectales, pulmón, piel, próstata y pancreáticos. Una determinada proporción de células tumorales de sarcoma de huesos y tejidos blandos es también FAP positiva (Rettig y otros, 1998). Debido a su amplia expresión en muchos cánceres y su modelo de expresión restringido en tejidos normales, la proteína alfa de
activación de fibroblastos (FAP-α; a continuación designada FAP) se ha considerado que es un objetivo antigénico
atractivo, no obstante, las inmunoterapias basadas en el direccionado del antígeno FAP no han tenido éxito.
El crecimiento invasivo de cánceres epiteliales está asociado a una serie de cambios celulares y moleculares en el estroma de soporte. Un rasgo molecular muy continuado estromal reactivo de muchos tipos de cáncer epitelial es la inducción de FAP, una molécula de la superficie celular de fibroblastos estromales reactivos (Garin-Chesa y otros, 1990). Dado que el antígeno FAP es expresado selectivamente en el estroma de una serie de carcinomas epiteliales, independientes de la localización y tipo histológico, el concepto de estroma diana por direccionado de FAP ha sido desarrollado para la formación de imágenes, diagnóstico y tratamiento de cánceres epiteliales y algunos otros estados. Con este objetivo, un anticuerpo monoclonal designado F19 (segregado por la línea celular de hibridoma con acceso ATCC nºHB 8269), que se une específicamente a FAP fue desarrollado y descrito en las patentes US 5.059.523 y WO 93/05804. Para mejorar adicionalmente este concepto, el anticuerpo F19 fue humanizado; el anticuerpo conseguido que se une específicamente a FAP se describe en el documento WO 99/57151 (ver más adelante).
Si bien la acumulación selectiva de un anti-FAP MAb murino en tejidos estromales tumoral fue demostrado con MAb F19 monoclonal murino marcado con trazas (131I-radiomarcado) en estudios de formación de imágenes de biodistribución (Welt y otros, 1994; Tanswell y otros, 2001), el concepto de inhibición de tumor por direccionado al estroma no ha sido satisfactorio en la terapia del cáncer. Si bien una fase I de MAb sibrotuzumab (BIBH1) anti-FAP 131I-radiomarcado demostró que la administración de repetidas infusiones de sibrotuzumab es segura y bien tolerada (Scott y otros, 2001; Hofheinz y otros, 2003), en un estudio de fase II con sibrotuzumab no marcado que fue llevada a cabo en pacientes con cáncer
colorrectal metastático avanzado se observó en la mayor parte de pacientes el progreso continuado del tumor. Por lo tanto, dado que no se cumplieron las exigencias mínimas, este estudio fue interrumpido.
Era un objetivo de la invención el dar a conocer agentes inmunoterapéuticos mejorados basados en anticuerpos anti-FAP que se dirigían a las células tumorales malignas expresando el antígeno FAP. Otro objetivo de la invención era el de dar a conocer inmunoterapéuticos mejorados basados en anticuerpos anti-FAP. Estos inmunoterapéuticos deben direccionarse a células estromales no malignas expresando FAP en tumores, de manera que las células malignas no expresan FAP, pero a pesar de ello son exterminadas eficazmente por el medicamento inmunoterapéutico.
Para solucionar el problema que subyace en la invención era un requisito previo proporcionar en primer lugar modelos animales apropiados para la prueba del concepto. La factibilidad de experimentos en animales, que son cruciales para demostrar el concepto de direccionado de células estromales y como consecuencia exterminar células tumorales de manera directa o indirecta, se basa en la disponibilidad de un anticuerpo anti-FAP que reacciona con FAP tanto humano como de ratón. Dicha reactividad cruzada es una exigencia para llevar a cabo estudios en modelos de cáncer basados en xenoinjertos de tumor humano, desarrollándose en ratones inmunodeficientes, porque en estos modelos, si bien la células...
Reivindicaciones:
1. Molécula de anticuerpo anti FAP-α, fragmento o derivado del mismo, seleccionado entre:
a. un anticuerpo monoclonal murino definido por:
i. una cadena pesada variable que comprende la región de aa 20 a 136 de la secuencia SEQ ID NO: 1;
ii. una cadena ligera variable que comprende una región de aa 23 a 129 de la secuencia SEQ ID NO:2 y
iii. la subclase IgG2a kappa;
b. un anticuerpo quimérico derivado del anticuerpo monoclonal murino definido en a) por injerto CDR o por reconstrucción superficial;
c. un anticuerpo humanizado derivado del anticuerpo monoclonal murino definido en a) por injerto CDR o por reconstrucción superficial.
2. Molécula de anticuerpo, según la reivindicación 1, en la que dicho anticuerpo quimérico b) está definido por:
i. una cadena pesada variable que comprende la región de aa 20 a 136 de la secuencia SEQ ID NO: 1;
ii. una cadena ligera variable que comprende una región de aa 23 a 129 de la secuencia SEQ ID NO:2 y
iii. cadenas pesada y ligera constantes que son de origen humano.
3. Molécula de anticuerpo, según la reivindicación 2, en la que dicho anticuerpo quimérico tiene la región de cadena pesada variable que comprende la región de aa 20 a 136 SEQ ID NO:1 fusionada a la región constante de la cadena pesada humana SEQ ID NO:3 y la región variable de cadena ligera que comprende la región de aa 23 a 129 de la secuencia SEQ ID NO:2 fusionada a la región constante de cadena ligera humana SEQ ID NO:4.
4. Molécula de anticuerpo, según cualquiera de las reivindicaciones 1 a 3, que reacciona tanto con el FAP-α murino como humano.
5. Inmunoconjugado de fórmula:
A(LB)n (Formula (I))
en la que:
A es un anticuerpo anti-FAP-α o un fragmento o derivado del mismo, según se define en la reivindicación 4,
L es una fracción enlazadora;
B un agente citotóxico; y
n es un número decimal con n = 1 a 10.
6. Inmunoconjugado, según la reivindicación 5, en el que dicha fracción enlazadora tiene capacidad de enlace químico de ser segmentado dentro de una célula.
7. Inmunoconjugado, según la reivindicación 5 ó 6, en el que dicho agente citotóxico B es un maitansinoide.
8. Inmunoconjugado, según la reivindicación 7, en el que el maitansinoide es DM1 ó DM4.
9. Inmunoconjugado, según la reivindicación 5, en el que el enlazador es seleccionado entre N-succinimidil 3-(2piridilditio)propionato (SPDP), N-succinimidil 4-(2piridilditio)pentanoato (SPP), N-succinimidil 4-(Nmalcimidometil)ciclohexan-1-carboxilato (SMCC).
10. Procedimiento para la producción de un inmunoconjugado, según cualquiera de las reivindicaciones 7 a 9, cuyo procedimiento comprende las etapas:
a. introducir uno o varios grupos tiol en una molécula de anticuerpo definida en la reivindicación 1;
b. hacer reaccionar la molécula de anticuerpo obtenida en la etapa (a) con un maitansinoide;
c. recuperar el conjugado maitansinoide del anticuerpo resultante.
11. Composición farmacéutica que comprende un inmunoconjugado, según cualquiera de las reivindicaciones 5 a
9, y un portador, diluyente o excipiente farmacéuticamente aceptable. 12. Composición farmacéutica, según la reivindicación 11, para su utilización en el tratamiento de cáncer.
5 13. Composición farmacéutica para utilización según la reivindicación 12, en el que dicho cáncer es seleccionado entre: cánceres colorrectales, cánceres de pulmón de células no pequeñas, cáncer de seno, cáncer de cabeza y cuello, cáncer de ovario, cánceres de pulmón, cánceres invasivos de vejiga, cánceres pancreáticos, cánceres metastáticos del cerebro, cánceres de tiroides, carcinoma de células escamosas de cabeza y cuello, carcinoma de células escamosas de esófago, carcinoma de células escamosas de pulmón, carcinoma de células escamosas de piel, melanoma, adenocarcinoma de seno, adenocarcinoma de pulmón, carcinoma de células escamosas de cérvix, carcinoma de células escamosas de páncreas, carcinoma de células escamosas de colon o carcinoma de células escamosas de estómago, cáncer de próstata, osteosarcoma o sarcoma de tejidos blandos y tumores benignos
20 que expresan FAP. 14. Composición farmacéutica, según la reivindicación 11, para su utilización en el tratamiento de artritis reumatoide.
Patentes similares o relacionadas:
Bloqueo de CD73, del 22 de Julio de 2020, de Innate Pharma: Un anticuerpo aislado que específicamente se une a un polipéptido CD73 humano en la superficie de una célula y que tiene capacidad de neutralizar […]
Formulaciones estables que contienen anticuerpos anti-PCSK9, del 15 de Julio de 2020, de AMGEN INC.: Una formulación estable que comprende un anticuerpo monoclonal que se une específicamente a PCSK9, en donde PCSK9 comprende los aminoácidos de la SEQ ID NO: […]
PTPRS y proteoglicanos en enfermedad autoinmune, del 15 de Julio de 2020, de LA JOLLA INSTITUTE FOR ALLERGY AND IMMUNOLOGY: Una proteína recombinante no enzimática que comprende una secuencia de aminoácidos de un dominio extracelular de PTPRS, donde la proteína comprende tanto el dominio 1 (Ig1) […]
Uso de un anticuerpo antipresenilina para la prevención y/o tratamiento del cáncer, del 20 de Mayo de 2020, de ALZHEIMUR 2012 S.L: Un anticuerpo o un fragmento del mismo que se une específicamente a la SEQ ID NO: 1 de la presenilina para su uso en la prevención y/o tratamiento del cáncer.
Inmunotoxinas de unión a CD20 para inducir la internalización celular y procedimientos que usan las mismas, del 6 de Mayo de 2020, de MOLECULAR TEMPLATES, INC: Una proteína de unión a CD20 que comprende: a) una región de unión a CD20 que comprende una región de unión de tipo inmunoglobulina: (i) capaz […]
Proteínas de unión a antígeno para proproteína convertasa subtilisina kexina tipo 9 (PCSK9), del 6 de Mayo de 2020, de AMGEN INC.: Una proteína de unión a antígeno, donde dicha proteína de unión a antígeno (i) comprende (a) un dominio variable de cadena ligera que comprende una secuencia […]
Anticuerpos frente a CD73 y sus usos, del 6 de Mayo de 2020, de BRISTOL-MYERS SQUIBB COMPANY: Un anticuerpo aislado que se une a Grupo de Diferenciación 73 (CD73) humano y que comprende las secuencias CDR1, CDR2 y CDR3 de la cadena pesada que comprenden las […]
Composiciones y métodos terapéuticos, del 6 de Mayo de 2020, de INSTITUT PASTEUR: Un compuesto para su uso en un método para tratar una inmunodeficiencia de células T CD4 en un sujeto que lo necesita, en el que el compuesto es […]