MODULADORES DEL PEPTIDO 1 SIMILAR AL GLUCAGON HUMANO Y SU USO EN EL TRATAMIENTO DE DIABETES Y AFECCIONES RELACIONADAS.
Un polipéptido aislado que comprende un polipéptido que tiene una secuencia de Fórmula I:
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2005/023076.
Solicitante: BRISTOL-MYERS SQUIBB COMPANY.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: ROUTE 206 AND PROVINCE LINE ROAD,PRINCETON, NJ 08543-4000.
Inventor/es: EWING, WILLIAM, R., SULSKY, RICHARD, B., RIEXINGER, DOUGLAS JAMES, MAPELLI,CLAUDIO, HAQUE,TASIR S, LEE,VING G, MARTINEZ,ROGELIO L, ZHU,YEHENG.
Fecha de Publicación: .
Fecha Concesión Europea: 17 de Marzo de 2010.
Clasificación Internacional de Patentes:
- C07K14/605 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › Glucagones.
- C07K7/06B
Clasificación PCT:
- C07K14/605 C07K 14/00 […] › Glucagones.
Clasificación antigua:
- C07K14/605 C07K 14/00 […] › Glucagones.
Fragmento de la descripción:
Moduladores del péptido 1 similar al glucagón humano y su uso en el tratamiento de diabetes y afecciones relacionadas.
La presente solicitud reivindica prioridad de la solicitud de patente provisional de Estados Unidos nº de serie 60/585.358 presentada el 2 de julio de 2004 y de la solicitud de patente provisional de Estados Unidos nº de serie 60/684.805 presentada el 26 de mayo de 2005, cada una de las cuales se incorpora por este documento por referencia en su totalidad.
Campo de la invención
La presente invención proporciona moduladores, agonistas o agonistas parciales novedosos del receptor de péptidos péptido 1 similar al glucagón humano (GLP-1) que presentan propiedades biológicas superiores del péptido nativo, GLP-1, y presentan un aumento de la estabilidad a la escisión proteolítica con respecto a secuencias nativas de GLP-1 y, por tanto, son útiles para la mejora de la afección diabética.
Antecedentes de la invención
El GLP-1 es una importante hormona del intestino con función reguladora en el metabolismo de la glucosa y la secreción gastrointestinal y el metabolismo. El GLP-1 humano es un péptido de 30 aminoácidos que se origina a partir de preproglucagón que se sintetiza, por ejemplo, en las células L del íleon distal, en el páncreas y en el cerebro. El procesamiento del preproglucagón para dar amida de GLP-1(7-36) y GLP-2 se produce principalmente en las células L y el tronco encefálico. El GLP-1 es normalmente secretado en respuesta a la ingesta de alimentos, en particular los carbohidratos y los lípidos estimulan la secreción de GLP-1. El GLP-1 se ha identificado como un estimulador muy potente y eficaz de la liberación de insulina dependiente de glucosa con un riesgo reducido de inducir hipoglucemia. El GLP-1 reduce las concentraciones de glucagón en plasma, ralentiza el vaciamiento gástrico, estimula la biosíntesis de insulina y potencia la sensibilidad a insulina (Nauck, 1997, Horm. Metab. Res. 47:1253-1258). EL GLP-1 también potencia la capacidad de las células beta pancreáticas para sentir y responder a glucosa en sujetos con tolerancia alterada a la glucosa (Byrne, Eur. J. Clin. Invest., 28:72-78, 1998). El efecto insulinotrópico de GLP-1 en seres humanos aumenta la tasa del metabolismo de glucosa parcialmente debido en parte a niveles de insulina elevados y debido en parte a una sensibilidad a la insulina potenciada (D'Alessio, Eur. J. Clin. Invest., 28:72-78, 1994). Se cree que la inhibición de la liberación de glucagón es un mecanismo adicional que contribuye a las mejoras en la homeostasis de glucosa observada tras el tratamiento de pacientes diabéticos de tipo II con GLP-1 (Nauck, M.A., y col., Diabetologia 36:741-744, 1993). Las propiedades farmacológicas anteriormente establecidas de GLP-1 hacen que sea un agente terapéutico sumamente deseable para el tratamiento de diabetes tipo II.
Adicionalmente, estudios recientes han mostrado que infusiones de cantidades ligeramente suprafisiológicas de GLP-1 potencian significativamente la saciedad y reducen la ingesta de alimentos en sujetos normales (Flint, A., Raben, A., Astrup, A. y Holst, J.J., J. Clin. Invest, 101:515-520, 1998; Gutswiller, J.P., Goke, B., Drewe, J., Hildebrand, P., Ketterer, S., Handschin, D., Winterhaider, R., Conen, D y Beglinger, C. Gut 44:81-86, 1999). También se ha notificado que el efecto sobre la ingesta de alimentos y la saciedad se preserva en sujetos obesos (Naslund, E., Barkeling, B., King, N., Gutniak, M., Blundell, J.E., Holst, J.J., Rossner, S. y Hellstrom, P.M., Int. J. Obes. Relat. Metab. Disord., 23:304-311, 1999).
En los estudios anteriormente citados también se sospechó que se producía un efecto pronunciado del GLP-1 sobre el vaciamiento gástrico. El vaciamiento gástrico produce excursiones de glucosa posprandial. También se ha mostrado que, además de la estimulación de la secreción de insulina, el GLP-1 estimula la expresión del factor de transcripción, homeosecuencia 1 duodenal de islotes (IDX-1), a la vez que estimula la neogénesis de células B y así puede ser un tratamiento eficaz y/o agente preventivo para diabetes (Stoffers, D.A., Kieffer, T.J., Hussain, M.A., Drucker, D.J., Bonner-Weir, S., Habener, J.F. y Egan, J.M. Diabetes, 40:741-748, 2000). También se ha mostrado que el GLP-1 inhibe la secreción de ácidos gástricos (Wettergren, A., Schjoldager, B., Mortensen, P.E., Myhre, J., Christiansen, J., Holst, J.J., Dig. Dis. Sci., 38:665-673, 1993) que puede proporcionar la protección contra úlceras gástricas.
Recientemente se ha notificado que el GLP-1 tiene varios efectos extra-pancreáticos adicionales que podrían producir, por ejemplo, cardioprotección, neuroprotección e inducción de aprendizaje y memoria (revisado en Ahren, B., Horm. Metab. Res. 36:842-845, 2004). Por tanto, también se ha propuesto que el GLP-1 podría usarse en el tratamiento de insuficiencia cardiaca (Nikolaidis, L.A., y col., Circulation 110:955-961, 2004), lesión por isquemia/reperfusión (Nikolaidis, L.A., y col., Circulation 109:962-965, 2004) y enfermedad de Alzheimer (Perry, T. y Greig, N.H., J. Alzheimers Dis. 4:487-496, 2002).
El GLP-1 es una hormona incretina, por ejemplo, una hormona intestinal que potencia la secreción de insulina inducida por la comida (Holst, J.J., Curr. Med. Chem., 6:1005-1017, 1999). Es un producto del gen de glucagón que codifica proglucagón. Este gen se expresa no sólo en las células A del páncreas, sino también en las células L endocrinas de la mucosa intestinal. El proglucagón es un péptido (proteína) que contiene 160 aminoácidos. El procesamiento adicional del proglucagón produce la generación de a) glucagón, b) un extremo N, supuestamente el fragmento inactivo y c) un gran fragmento del extremo C comúnmente denominado "el fragmento de proglucagón mayor". Este fragmento se considera que es biológicamente inactivo. Aún cuando este fragmento está presente en tanto el páncreas como en las células L del intestino, sólo en los intestinos se observa que los productos de descomposición de "el fragmento de proglucagón mayor" producen dos péptidos altamente homólogos denominados GLP-1 y GLP-2. Estos dos péptidos tienen importantes actividades biológicas. Como tal, la secuencia de aminoácidos de GLP-1, que está presente en las células L, es idéntica a la parte 78-107 de proglucagón.
Actualmente, la terapia que implica el uso de moléculas de tipo GLP-1 ha presentado un problema significativo debido a que la semivida en suero de tales péptidos es bastante corta. Por ejemplo, el GLP-1(7-37) tiene una semivida en suero inferior a 5 minutos. Por tanto, existe una necesidad crítica de moduladores, agonistas o antagonistas de receptores de GLP-1 biológicamente activos que posean perfiles farmacodinámicos extendidos. Es a esta y a otras necesidades a las que se refiere la presente invención.
Por tanto, la presente invención proporciona péptidos novedosos que actúan de moduladores, agonistas o agonistas parciales de receptores de GLP-1 que presentan propiedades biológicas similares o superiores del péptido nativo, GLP-1, y, por tanto, son útiles para la mejora de las condiciones diabéticas y relacionadas.
Resumen de la invención
En un aspecto, la presente invención se refiere a un polipéptido aislado que comprende un polipéptido que tiene una secuencia de Fórmula I:
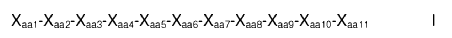
en la que
Xaa1 es un aminoácido que se produce naturalmente o no naturalmente que comprende un imidazol; en el que uno o más átomos de carbono del aminoácido están opcionalmente sustituidos con uno o más grupos alquilo; en el que el aminoácido tiene opcionalmente un grupo amino libre que está opcionalmente sustituido con alquilo, acilo, benzoílo, L-lactilo, alquiloxicarbonilo, ariloxicarbonilo, arilalquiloxicarbonilo, heterocicliloxicarbonilo, heteroarilalquiloxicarbonilo, alquilcarbamoílo, arilcarbamoílo, arilalquilcarbamoílo, heterociclilsulfonilo, alquilsulfonilo, arilsulfonilo, arilalquilsulfonilo, heteroarilalquilsulfonilo o heteroarilsulfonilo; y en el que cuando el grupo amino libre no está presente, Xaa1 es el des-aminoácido de histidina en el que uno o más átomos de carbono del aminoácido están opcionalmente sustituidos con uno o más grupos alquilo;
Xaa2 es un aminoácido que se produce naturalmente o no naturalmente seleccionado del grupo que está constituido por D-alanina, ácido a-amino-isobutírico (Aib), N-metil-D-alanina, N-etil-D-alanina, ácido 2-metil-azetidin-2-carboxílico, alfa-metil-(L)-prolina,...
Reivindicaciones:
1. Un polipéptido aislado que comprende un polipéptido que tiene una secuencia de Fórmula I:
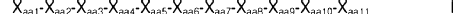
en la que
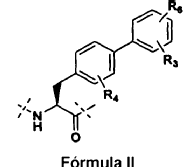
Xaa11 es un aminoácido que se produce naturalmente o no naturalmente de Fórmula IVa:
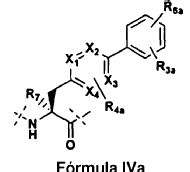
2. El polipéptido aislado de la reivindicación 1, en el que Xaa3 es histidina, en el que dicha histidina está opcionalmente sustituida con uno o más grupos alquilo.
3. El polipéptido aislado de la reivindicación 1, en el que Xaa3 es ácido L-aspártico o ácido L-glutámico, en el que cada uno de dicho ácido L-aspártico o ácido L-glutámico está opcionalmente sustituido con uno o más grupos alquilo.
4. El polipéptido aislado de una cualquiera de las reivindicaciones 1 a 3, en el que Xaa6 es alfa-metil-fenilalanina, alfa-metil-2-fluorofenilalanina o alfa-metil-2,6-difluorofenilalanina, en el que cada una de dicha alfa-metil-fenilalanina, alfa-metil-2-fluorofenilalanina o alfa-metil-2,6-difluorofenilalanina está opcionalmente sustituida con uno o más grupos alquilo.
5. El polipéptido aislado de una cualquiera de las reivindicaciones 1 a 4, en el que Xaa7 es L-treonina, en el que dicha treonina está opcionalmente sustituida con uno o más grupos alquilo.
6. El polipéptido aislado de una cualquiera de las reivindicaciones 1 a 5, en el que Xaa9 es ácido L-aspártico o ácido L-glutámico, en el que cada uno de dicho ácido L-aspártico o ácido L-glutámico está opcionalmente sustituido con uno o más grupos alquilo.
7. El polipéptido aislado de una cualquiera de las reivindicaciones 1 a 6, en el que Xaa1 es L-histidina, teniendo dicha histidina un grupo amino terminal que está opcionalmente sustituido con alquilo, dialquilo, acilo, benzoílo, L-lactilo, alquiloxicarbonilo, ariloxicarbonilo, aralquiloxicarbonilo, heterocicliloxicarbonilo, heteroarilalquiloxicarbonilo, alquilcarbamoílo, arilcarbamoílo, aralquilcarbamoílo, heterociclilsulfonilo, alquilsulfonilo, arilsulfonilo, arilalquilsulfonilo, heteroarilalquilsulfonilo o heteroarilsulfonilo.
8. El polipéptido aislado de una cualquiera de las reivindicaciones 1 a 7, en el que Xaa1 se selecciona del grupo que está constituido por L-N-metil-His, L-a-metil-His, des-amino-His, 3-(1H-imidazol-4-il)-2-metilpropanoílo y (S)-3-(1H-imidazol-4-il)-2-hidroxipropanoílo (L-ß-imidazol-lactilo).
9. El polipéptido aislado de una cualquiera de las reivindicaciones 1 a 8, en el que Xaa2 se selecciona del grupo que está constituido por ácido a-amino-isobutírico (Aib), D-alanina, N-metil-D-alanina, alfa-metil-(L)-prolina, ácido 2-metil-azetidin-2-carboxílico y ácido 2-metilpiperidin-2-carboxílico.
10. El polipéptido aislado de una cualquiera de las reivindicaciones 1 a 9, en el que Xaa4 es glicina.
11. El polipéptido aislado de una cualquiera de las reivindicaciones 1 a 10, en el que Xaa5 se selecciona del grupo que está constituido por L-Thr y L-Nva.
12. El polipéptido aislado de una cualquiera de las reivindicaciones 1 a 11, en el que Xaa6 se selecciona del grupo que está constituido por L-a-Me-Phe, L-a-Me-2-fluoro-Phe y L-a-Me-2,6-difluoro-Phe.
13. El polipéptido aislado de una cualquiera de las reivindicaciones 1 a 12, en el que Xaa7 es L-Th.
14. El polipéptido aislado de una cualquiera de las reivindicaciones 1 a 13, en el que Xaa8 se selecciona del grupo que está constituido por L-Ser y L-His.
15. El polipéptido aislado de una cualquiera de las reivindicaciones 1 a 14, en el que Xaa9 es L-Asp.
16. El polipéptido aislado de una cualquiera de las reivindicaciones 1 a 15, en el que Xaa10 se selecciona del grupo que está constituido por 4-fenil-fenilalanina, 4-[(4'-metoxi-2'-etil)fenil]fenilalanina, 4-[(4'-etoxi-2'-etil)fenil]fenilalanina, 4-[(4'-metoxi-2'-metil)fenil]fenilalanina, 4-[(4'-etoxi-2'-metil)fenil]fenilalanina, 4-(2'-etilfenil)fenilalanina, 4-(2'-metilfenil)fenilalanina, 4-[(3',5'-dimetil)fenil]fenilalanina y 4-[(3',4'-dimetoxi)fenil]fenilalanina.
17. El polipéptido aislado de una cualquiera de las reivindicaciones 1 a 16, en el que Xaa11 se selecciona del grupo que está constituido por 4-fenil-3-piridilalanina, 4-(2'-metilfenil)-3-piridilalanina, 4-(2'-fluorofenil)-3-piridilalanina, 4-(2'-clorofenil)-3-piridilalanina, 4-[(3',5'-dimetil)fenil]-3-piridilalanina, 4-(4'-trifluorometilfenil)-3-piridilalanina, 4-(3'-metoxifenil)-3-piridilalanina, 4-(3'-metilfenil)-3-piridilalanina, 4-(2'-metilfenil)-3,5-pirimidilalanina, (S)4-(2'-metilfenil)-a-Me-3-piridilalanina y 4-(2'-etilfenil)-3-piridilalanina;
en el que el carbono de carbonilo del extremo C de Xaa11 está unido a un nitrógeno para formar una carboxamida (NH2); y
en el que R7 se selecciona del grupo que está constituido por hidrógeno y metilo.
18. El polipéptido aislado de la reivindicación 1, en el que dicho polipéptido es un polipéptido de Fórmula VI:
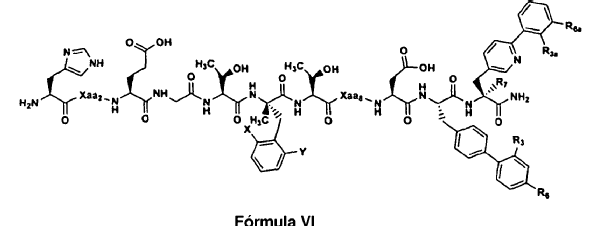
en la que:
19. El polipéptido aislado de la reivindicación 18, en el que:
20. El polipéptido aislado de la reivindicación 1, en el que dicho polipéptido es un polipéptido de Fórmula VII:
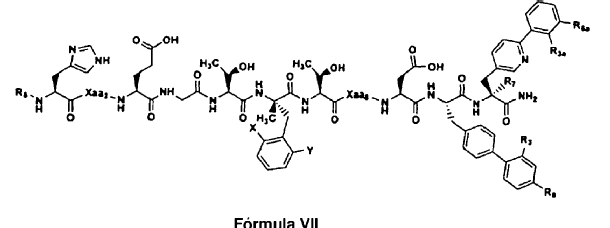
en la que:
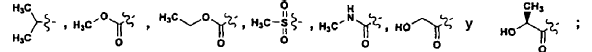
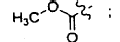
21. El polipéptido aislado de la reivindicación 20, en el que:
22. El polipéptido aislado de la reivindicación 1, en el que dicho polipéptido es un polipéptido de Fórmula VIII:
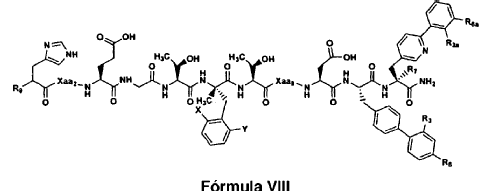
en la que:
23. El polipéptido aislado de la reivindicación 22, en el que:
24. Un compuesto de Fórmula VIa:
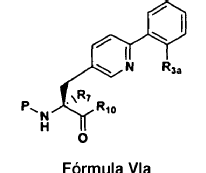
25. Un compuesto de Fórmula VIIa:
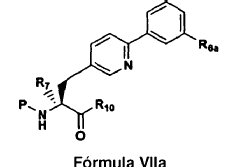
26. Un polipéptido aislado, en el que dicho polipéptido es un polipéptido de Fórmula VI:
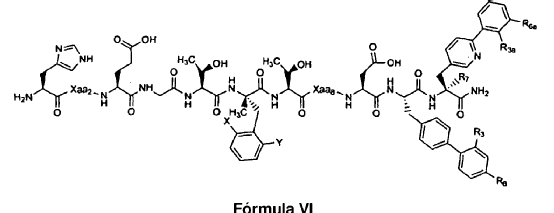
en la que:
27. El polipéptido aislado de la reivindicación 26, en el que:
28. Un polipéptido aislado, en el que dicho polipéptido es un polipéptido de Fórmula VII:
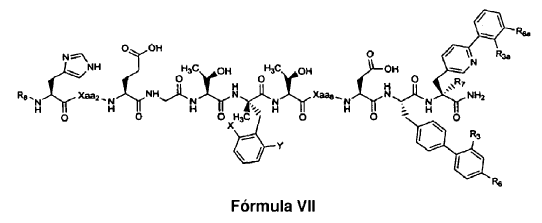
en la que:
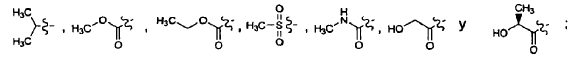
29. El polipéptido aislado de la reivindicación 28, en el que:
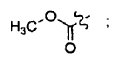
30. Un polipéptido aislado, en el que dicho polipéptido es un polipéptido de Fórmula VIII:
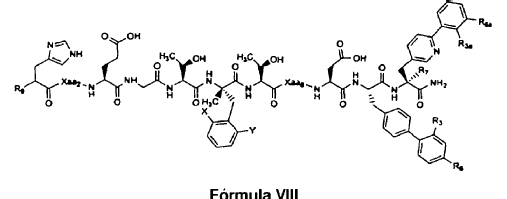
en la que:
31. El polipéptido aislado de la reivindicación 30, en el que:
32. Un polipéptido aislado de la reivindicación 1, en el que Xaa1, Xaa2, Xaa3, Xaa4, Xaa5, Xaa6, Xaa7, Xaa8, Xaa9, Xaa10 y Xaa11 se definen del siguiente modo:
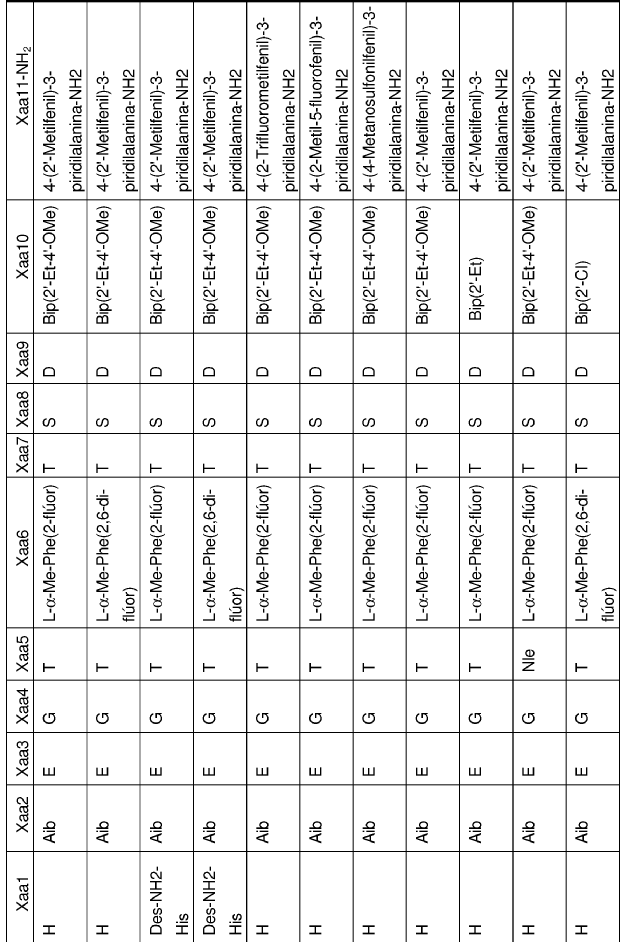
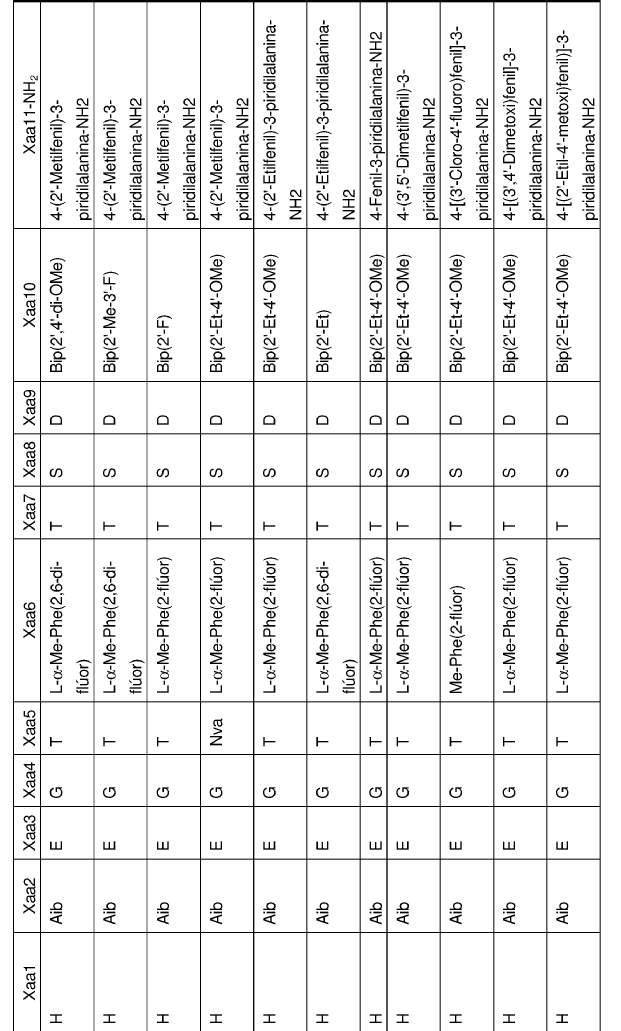
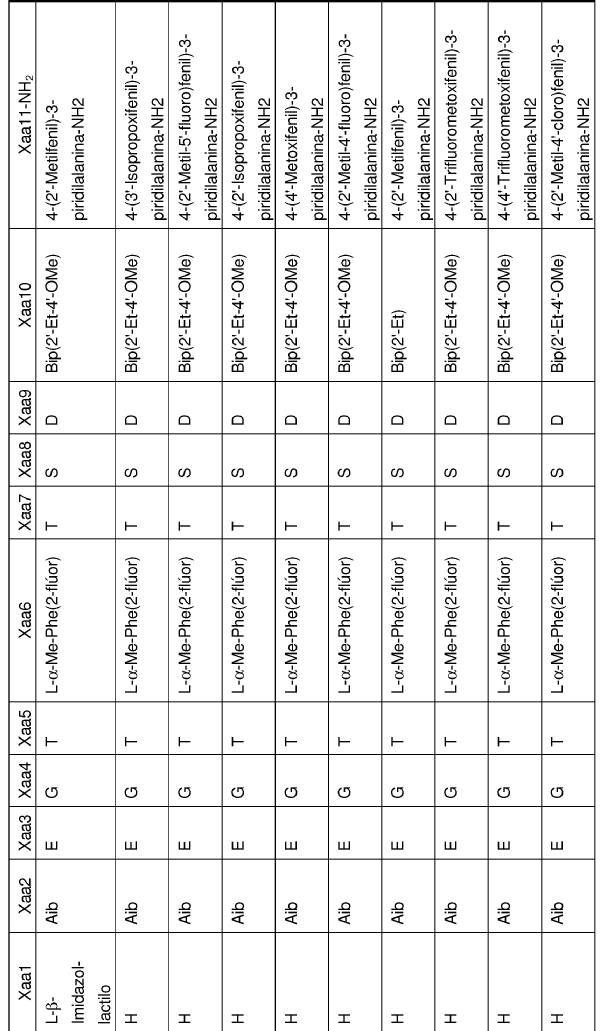
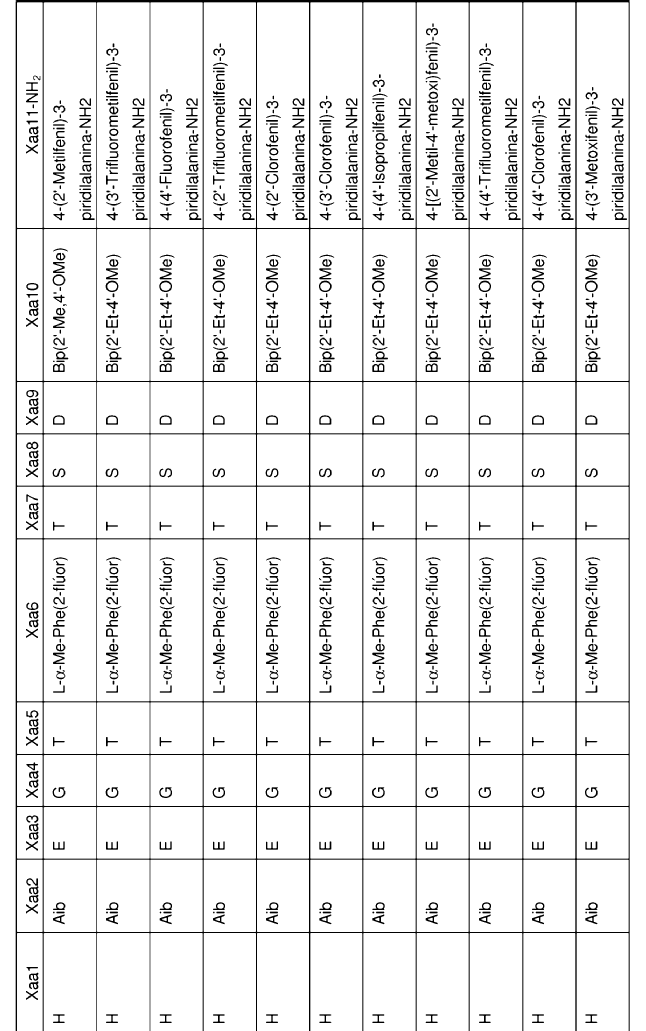
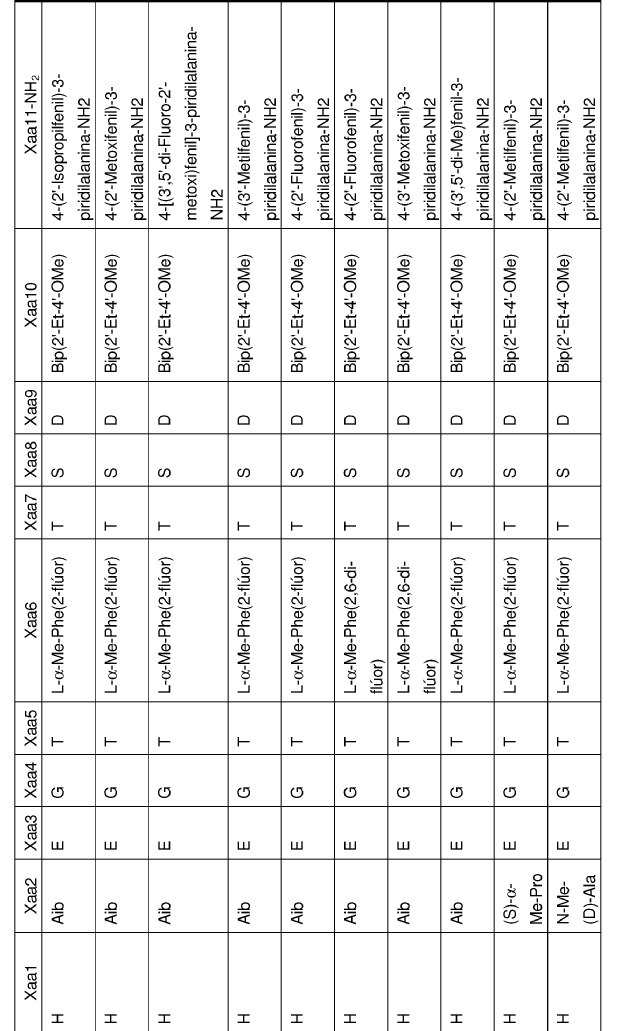
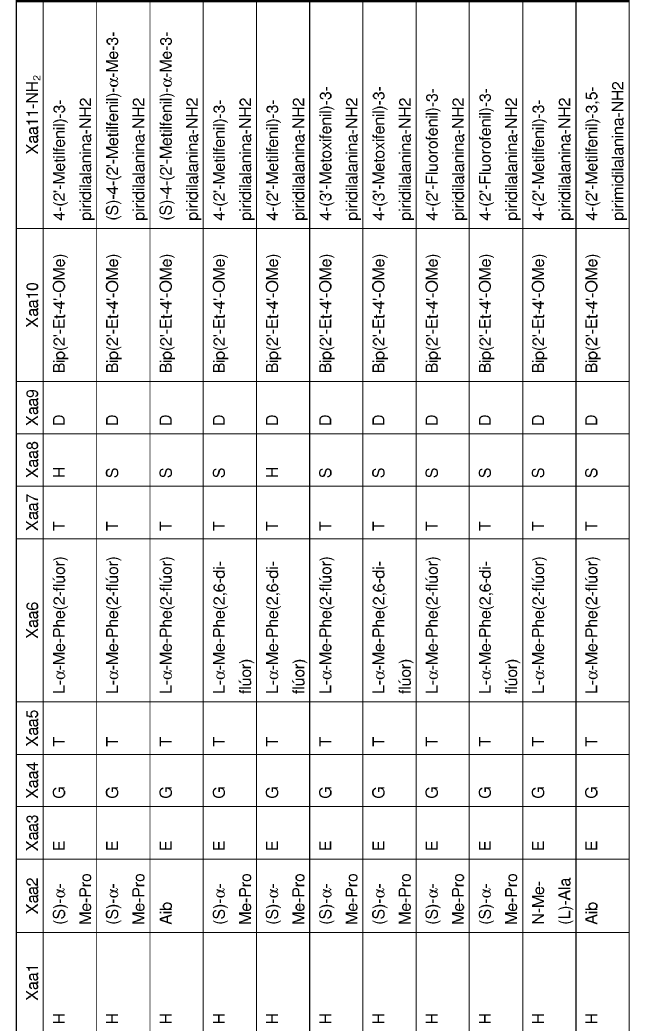
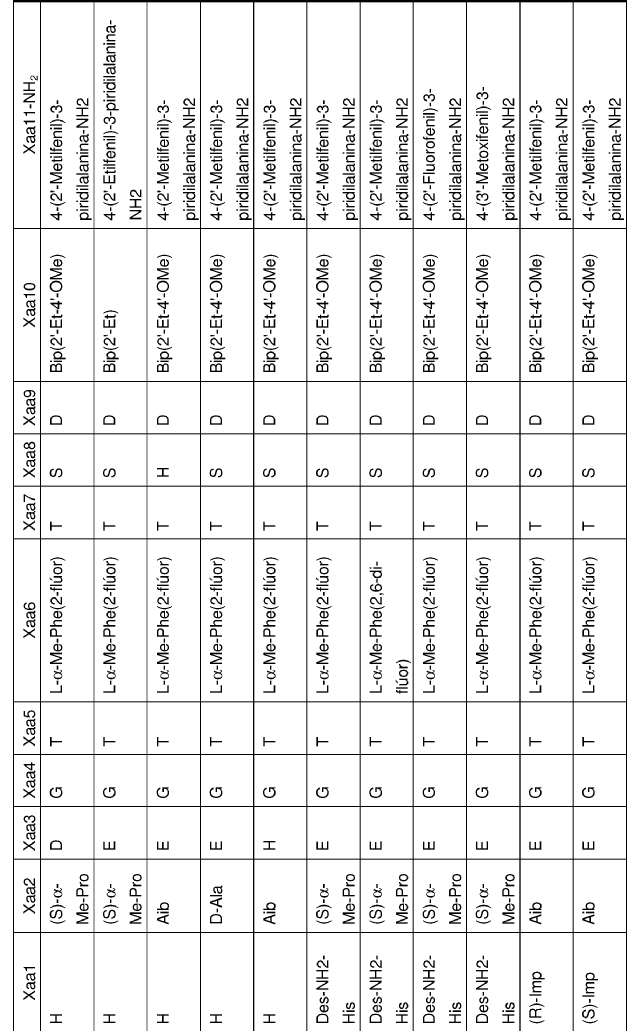
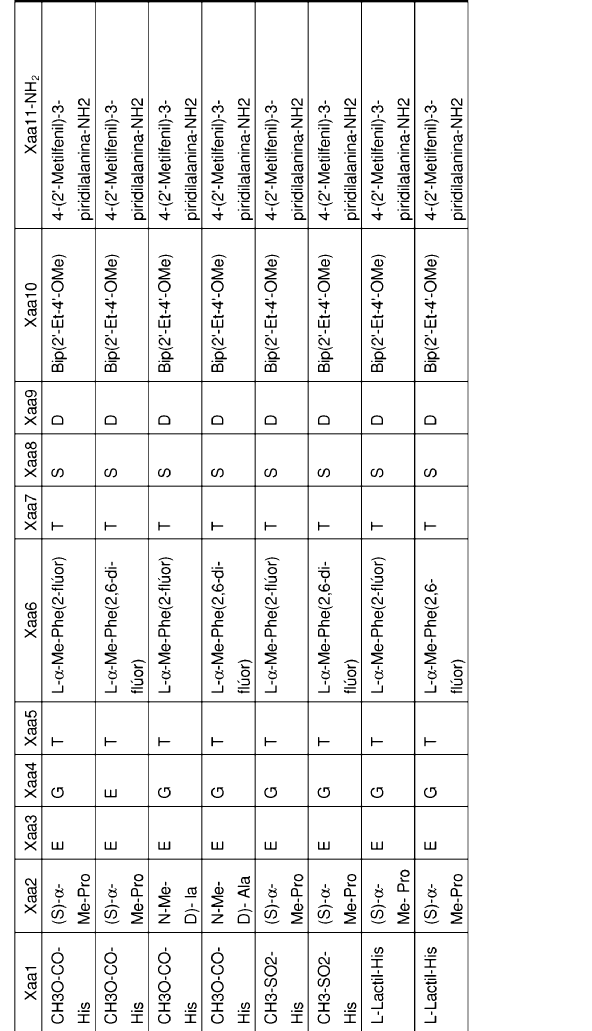
33. Un polipéptido aislado, en el que dicho polipéptido aislado es un polipéptido seleccionado del grupo de polipéptidos de Fórmula I:
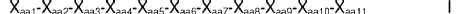
en la que Xaa1, Xaa2, Xaa3, Xaa4, Xaa5, Xaa6,Xaa7, Xaa8, Xaa9, Xaa10 y Xaa11 se definen del siguiente modo:
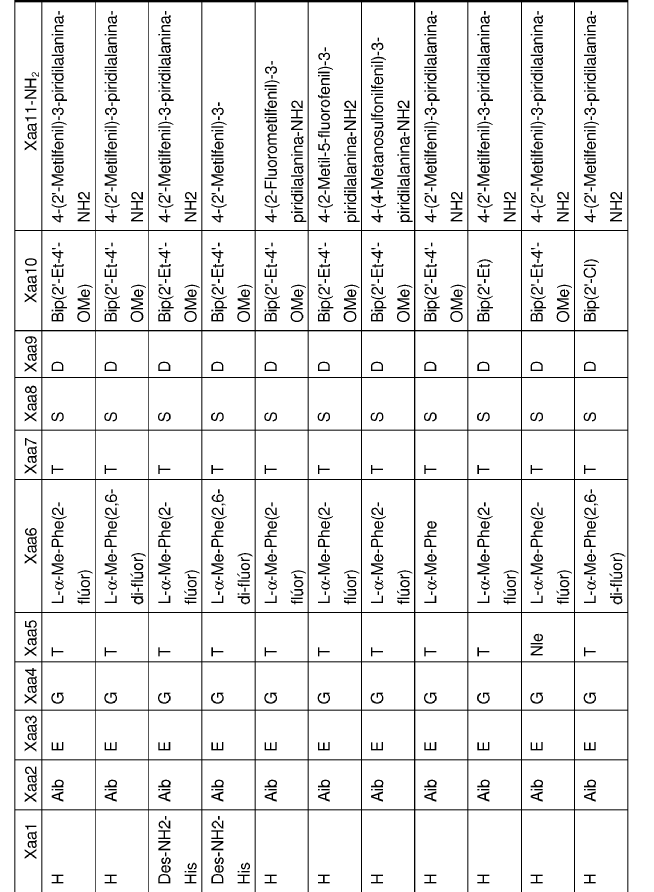
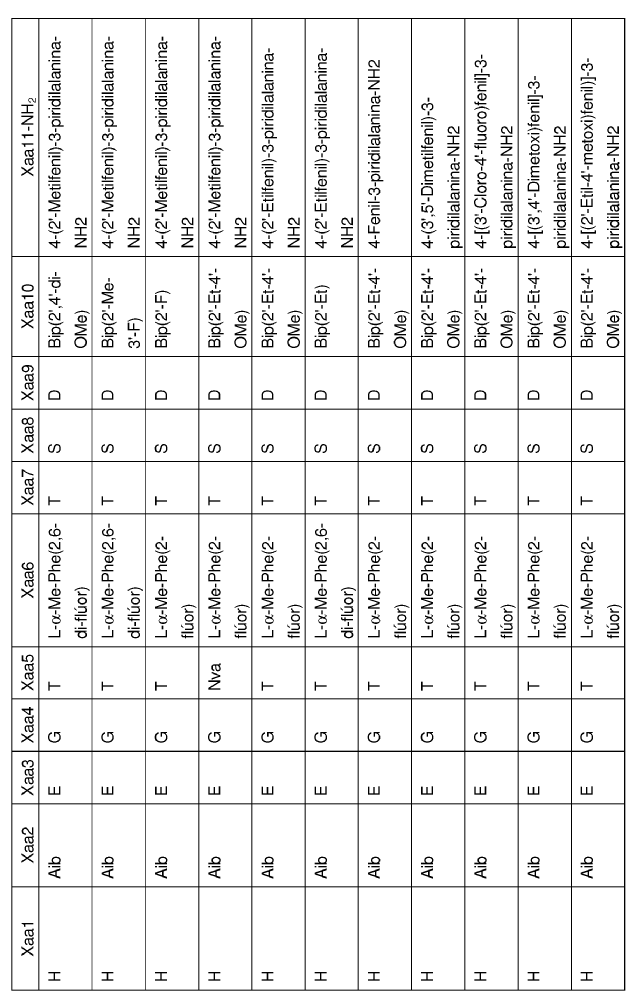
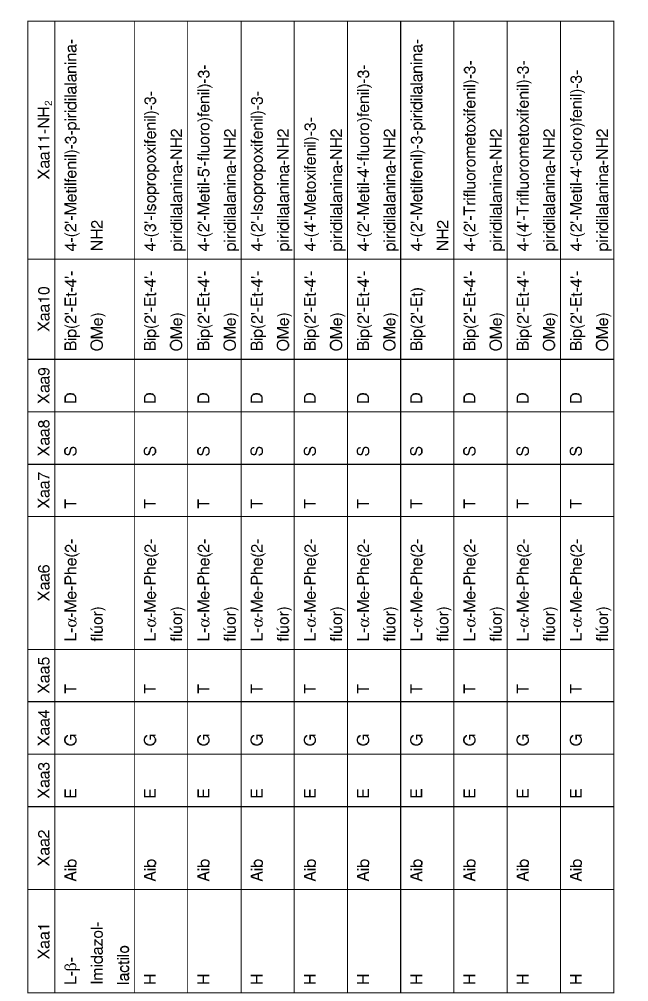
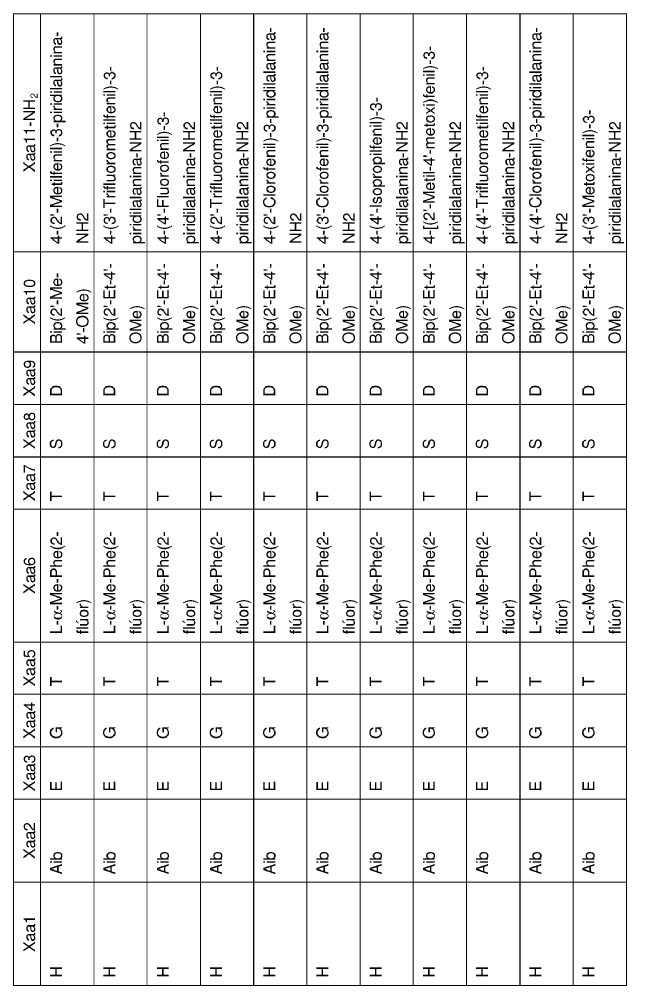
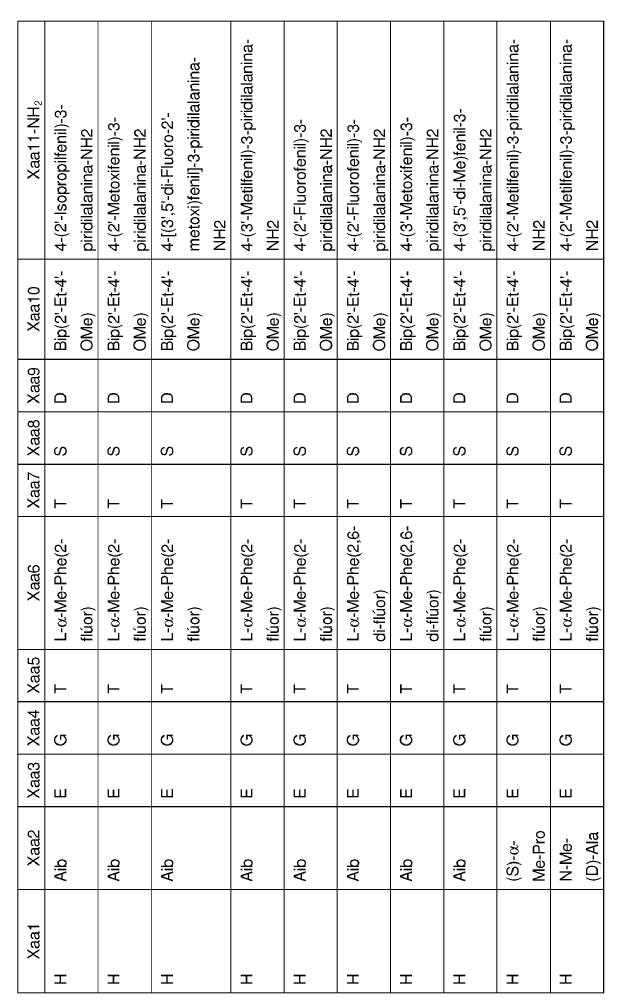
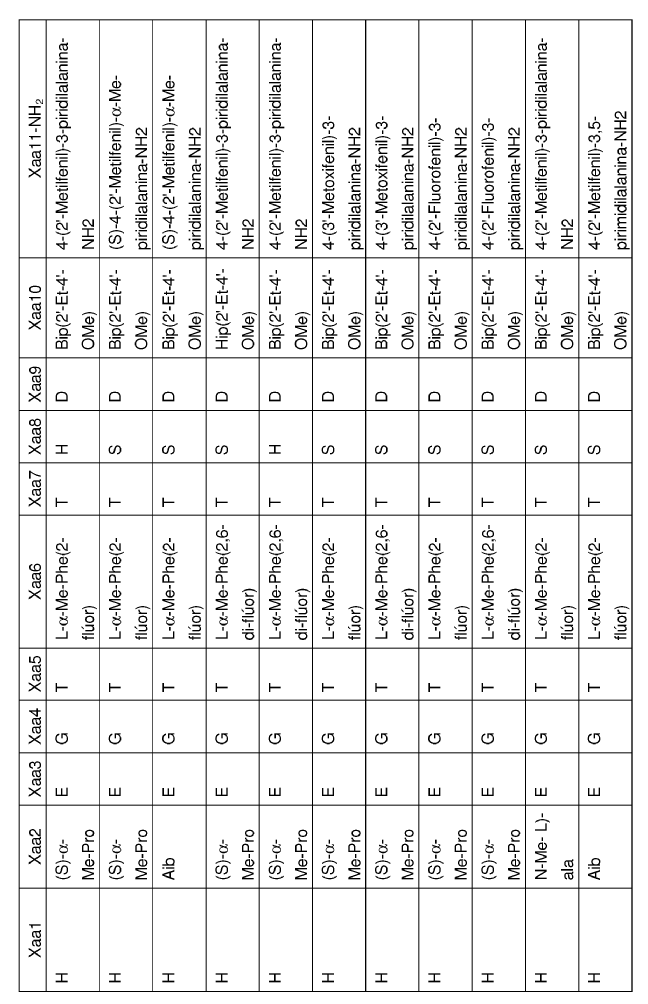

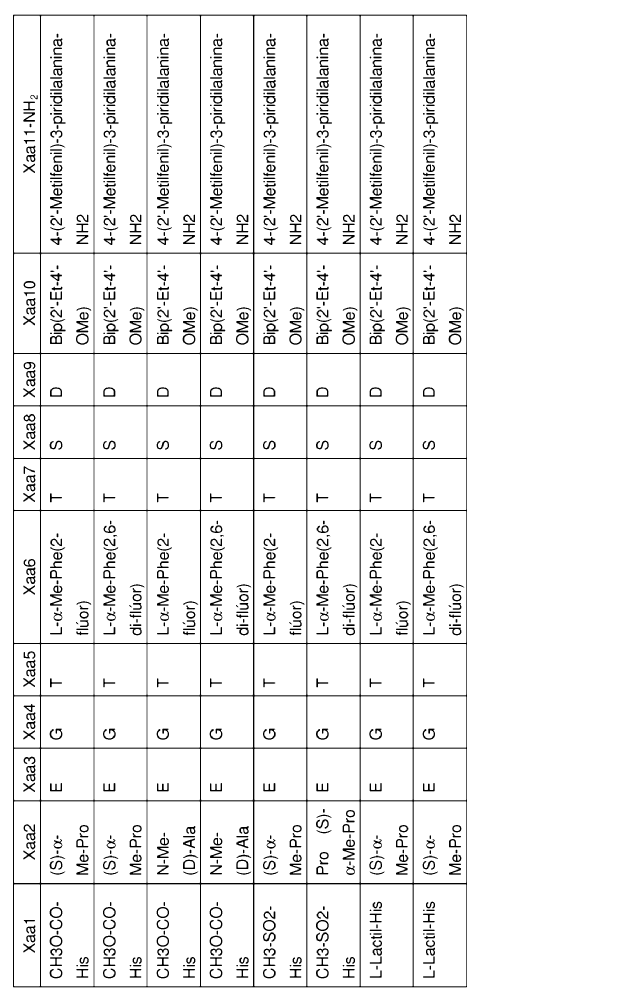
34. Un polipéptido que comprende la secuencia de aminoácidos de SEQ ID NO: 93 en el que dicho polipéptido se une a y activa un receptor de GLP-1.
35. Un polipéptido de la reivindicación 34 seleccionado del grupo que está constituido por SEQ ID Nº:1-16, 18-59, 61-63, 65-77, 79, 81-89 y 91-92.
36. Un polipéptido de la reivindicación 34 en el que dicho péptido comprende la secuencia de aminoácidos SEQ ID Nº: 1, 58, 59, 61, 70, 81, 82, 91 ó 92.
37. Un polipéptido que comprende una secuencia seleccionada del grupo que está constituido por SEQ ID Nº: 1-16, 18-59, 61-63, 65-77, 79, 81-89 y 91-92.
38. Un polipéptido seleccionado del grupo que está constituido por
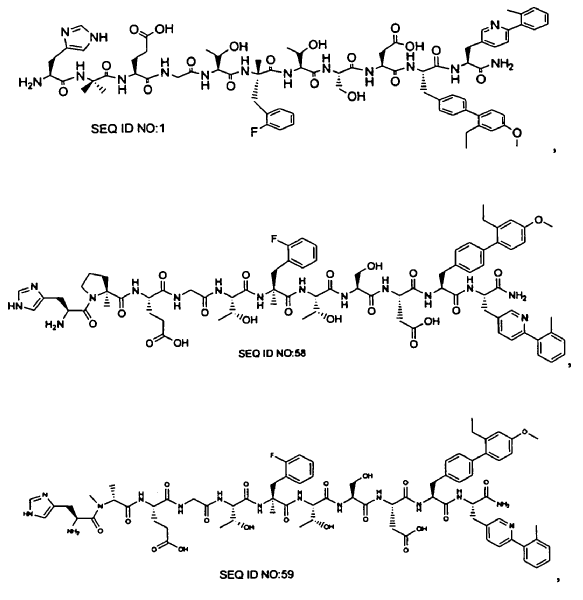
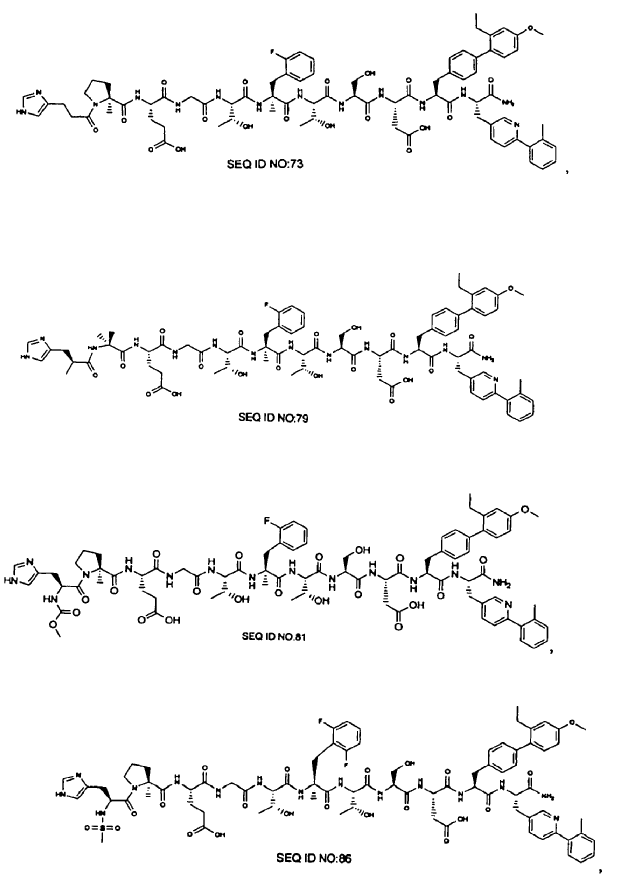
y
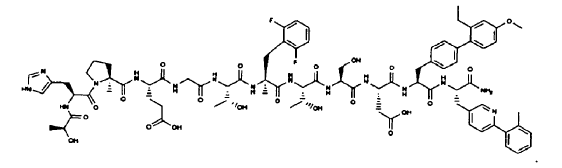
39. Un polipéptido que comprende la secuencia de aminoácidos de SEQ ID NO: 1.
40. Un polipéptido que está constituido por la siguiente estructura:
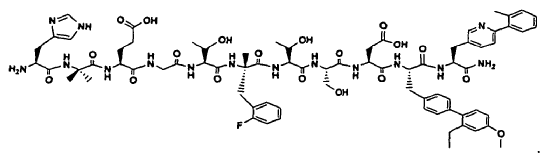
41. Una composición farmacéutica que comprende un polipéptido de una cualquiera de las reivindicaciones 1 a 40 y un vehículo farmacéuticamente aceptable.
42. Una combinación farmacéutica que comprende un polipéptido de una cualquiera de las reivindicaciones 1 a 40 y al menos un agente terapéutico seleccionado del grupo que está constituido por un agente antidiabético, un agente contra la obesidad, un agente antihipertensor, un agente antiaterosclerótico y un agente hipolipemiante.
43. La combinación de la reivindicación 42, en la que el agente antidiabético es al menos un agente seleccionado del grupo que está constituido por una biguanida, una sulfonilurea, un inhibidor de glucosidasa, un agonista ? del receptor activado por proliferador de peroxisoma (PPAR), un agonista dual de PPAR a/?, un inhibidor de proteína de unión a lípidos de adipocitos (aP2), un inhibidor de dipeptidilpeptidasa 4 (DP4), un sensibilizador de insulina, un péptido 1 similar al glucagón (GLP-1), insulina y una meglitinida.
44. La combinación de la reivindicación 42, en la que el agente antidiabético es al menos un agente seleccionado del grupo que está constituido por metformina, gliburida, glimepirida, glipirida, glipizida, clorpropamida, gliclazida, acarbosa, miglitol, pioglitazona, troglitazona, rosiglitazona, insulina, farglitizar, isaglitazona, reglitizar, balaglitazona, (Z)-1,4-bis{4-[(3,5-dioxo-1,2,4-oxadiazolidin-2-il) metil]fenoxi}but-2-eno, rivoglitazona, rafaegron, repaglinida, nateglinida, sal de calcio de ácido (S)-2-bencil-4-oxo-4-(cis-perhidroisoindol-2-il)butírico, tesaglitizar, L-fenilalanina,N-[(1Z)-1-metil-3-oxo-3-fenil-1-propenil]-4-[3-(5-metil-2-fenil-4-oxazolil)propilo], 5-[(2,4-dioxo-5-tiazolidinil)metil]-2-metoxi-N-[[4-(trifluorometil) fenil]metil]-benzamida, exenatida, péptido 1 similar al 8-37-glucagón (humano)-N-[3-(1H-imidazol-4-il)-1-oxopropil]-26-L-arginina-34-[N6-(1-oxooctil)-L-lisina] y vildagliptina.
45. La combinación de la reivindicación 42, en la que el agente contra la obesidad es al menos un agente seleccionado del grupo que está constituido por un agonista adrenérgico beta 3, un inhibidor de lipasa, un inhibidor de la recaptación de serotonina, un inhibidor de la recaptación de dopamina, un inhibidor de la recaptación de serotonina y dopamina, un compuesto de receptor beta tiroideo y un agente anorexígeno.
46. La combinación de la reivindicación 42, en la que el agente contra la obesidad es al menos un agente seleccionado del grupo que está constituido por orlistat, cetilistat, rafabregon, N-[4-[2-[[(2S)-3-[(6-amino-3-piridinil)oxi]-2-hidroxipropil]amino]etil]fenil]-4-(1-metiletil)-bencenosulfonamida, sibutramina, topiramato, axocina, dexanfetamina, fentermina, fenilpropanolamina y mazindol.
47. La combinación de la reivindicación 42, en la que el agente hipolipemiante es al menos un agente seleccionado del grupo que está constituido por un inhibidor de proteína microsómica de transferencia de triglicéridos (MTP), proteína de transferencia de ésteres de colesterol, un inhibidor de hidroxi-3-metil-glutaril-coenzima A (HMG CoA) reductasa, un inhibidor de la escualeno sintetasa, un derivado de ácido fíbrico, un regulador por incremento de la actividad de receptores de lipoproteínas de baja densidad (LDL), un inhibidor de lipoxigenasa o un inhibidor de la acil-coenzima A-colesterol-aciltransferasa (ACAT).
48. La combinación de la reivindicación 42, en la que el agente hipolipemiante es al menos un agente seleccionado del grupo que está constituido por pravastatina, lovastatina, simvastatina, atorvastatina, cerivastatina, fluvastatina, nisvastatina, visastatina, fenofibrato, gemfibrozilo, clofibrato, avasimiba, N-[2,6-bis(1-metiletil)fenil]-2-(tetradeciltio)-acetamida, 3-(13-hidroxi-10-oxotetradecil)-5,7-dimetoxi-1(3H)-isobenzofuranona, torcetrapib y (3-alfa,4-alfa,5-alfa)-4-(2-propenilcolestan-3-ol).
49. El uso de un polipéptido de una cualquiera de las reivindicaciones 1 a 40 para la preparación de una composición farmacéutica para tratar o retrasar la progresión o aparición de diabetes, retinopatía diabética, neuropatía diabética, nefropatía diabética, cicatrización, resistencia a insulina, hiperglucemia, hiperinsulinemia, síndrome X, complicaciones diabéticas, niveles elevados en sangre de ácidos grasos libres o glicerol, hiperlipidemia, obesidad, hipertrigliceridemia, aterosclerosis o hipertensión.
50. El uso de la reivindicación 49, que comprende además la administración simultánea o secuencial de uno o más agentes terapéuticos seleccionados del grupo que está constituido por un agente antidiabético, un agente contra la obesidad, un agente antihipertensor y un agente antiaterosclerótico y un agente hipolipemiante.
51. El uso de la reivindicación 50, en el que la composición farmacéutica es la combinación farmacéutica de una cualquiera de las reivindicaciones 42 a 48.
52. El uso de una cualquiera de las reivindicaciones 49 a 51, en el que la composición farmacéutica es una formulación para administración parenteral.
53. El uso de una cualquiera de las reivindicaciones 49 a 51, en el que la composición farmacéutica es una formulación para administración no parenteral.
54. El uso de la reivindicación 52, en el que dicha administración parenteral se selecciona del grupo que está constituido por inyección en bolo intravenosa (iv), infusión iv, administración subcutánea, administración intramuscular, administración intranasal, administración por vía oral, administración pulmonar y administración oftálmica.
55. El uso de la reivindicación 54, en el que dicha administración subcutánea implica el uso de una formulación de liberación inmediata o sostenida.
56. El uso de la reivindicación 54, en el que dicha administración intramuscular implica el uso de una formulación de liberación inmediata o sostenida.
57. El uso de la reivindicación 52, en el que dicha formulación comprende además un excipiente farmacéuticamente aceptable seleccionado del grupo que está constituido por un disolvente y codisolvente, un agente solubilizante, un agente emulsionante, un espesante, un agente quelante, un antioxidante, un agente reductor, un conservante antimicrobiano, un tampón y agente de ajuste de pH, un agente de carga, un protector y agente de ajuste de la tonicidad y un aditivo especial.
58. El uso de la reivindicación 52, en el que dicha formulación comprende además un sistema de administración encapsulado.
Patentes similares o relacionadas:
Agonistas del receptor de glucagón, del 24 de Junio de 2020, de ELI LILLY AND COMPANY: Un compuesto agonista del receptor de glucagón que comprende la fórmula: YX1QGTFX2SDYSKYLDX3KKAX4EFVX5WLLEX6X7 en la que X1 es Aib; X2 es T o L; X3 es Aib; […]
Profármacos de GLP-1, del 17 de Junio de 2020, de NOVO NORDISK A/S: Un compuesto de GLP-1 de la fórmula general I: R1 -(NHXaa1)-Xaa2-(OHis)-(péptido GLP-1) (Fórmula I) en donde el péptido GLP-1 es […]
Método para preparar semaglutida, del 13 de Mayo de 2020, de Hybio Pharmaceutical Co., Ltd: Método de preparación de semaglutida, que comprende las etapas de: etapa 1: acoplar Gly a una resina mediante síntesis en fase sólida para obtener Gly-resina; y […]
Coagonistas estables del receptor de GLP-1/glucagón basados en GLP-1, del 6 de Mayo de 2020, de NOVO NORDISK A/S: Un derivado de GLP-1 caracterizado por tener la fórmula: amida de Nε34-[2-[2-[2-[[2-[2-[2-[[(4S)-4-carboxi-4- [[(4S)-4-carboxi-4-(17- carboxiheptadecanoilamino)butanoil]amino]butanoil]amino]etoxi]etoxi]acetil]amino]etoxi]etoxi]acetil]- […]
Una composición para el tratamiento de la diabetes que comprende un análogo de oxintomodulina, del 11 de Marzo de 2020, de HANMI PHARM. CO., LTD.: Una composición para su uso en la prevención o el tratamiento de la diabetes, la composición comprende un conjugado de análogo de oxintomodulina como un ingrediente […]
Modificador de exenatida y uso del mismo, del 12 de Febrero de 2020, de BrightGene Bio-Medical Technology Co., Ltd: Un modificador de exenatida o sales farmacéuticamente aceptables del mismo que tienen actividad del agonista del receptor de GLP-1, como se muestra en la fórmula (I): (Ex-4)-L-Y […]
Derivados de GLP-1 doble-acilados, del 4 de Diciembre de 2019, de NOVO NORDISK A/S: Un derivado de un análogo de GLP-1, cuyo análogo comprende un primer residuo de K en una posición correspondiente a la posición 26 de GLP-1 […]
Análogos de glucagón, del 13 de Noviembre de 2019, de ZEALAND PHARMA A/S: Un compuesto que tiene la fórmula: R1-X-Z-R2 en donde R1 es H (es decir, hidrógeno), alquilo C1-4, acetilo, formilo, benzoílo o trifluoroacetilo; […]