METODOS DE ESCRUTINIO EMPLEANDO UN MODELO ESTRUCTURAL DE FIH.
Un método para identificar, explorar, caracterizar o diseñar una identidad química que se une a un factor inhibidor de HIF (FIH),
comprendiendo dicho método comparar un modelo estructural de FIH con un modelo estructural para dicha entidad química, procediendo dicho modelo estructural del FIH de los factores estructurales o coordenadas estructurales que se muestran en la Tabla 3
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/GB2003/004492.
Solicitante: ISIS INNOVATION LIMITED.
Nacionalidad solicitante: Reino Unido.
Dirección: EWERT HOUSE, EWERT PLACE,SUMMERTOWN, OXFORD OX2 7SG.
Inventor/es: RATCLIFFE,PETER JOHN,UNIVERSITY OF OXFORD, PUGH,CHRISTOPHER WILLIAM,UNIVERSITY OF OXFORD, SCHOFIELD,CHRISTOPHER JOSEPH,UNIV. OF OXFORD, HEWITSON,KIRSTY SARAH,UNIVERSITY OF OXFORD, ELKINS,JONATHAN MARK,UNIVERSITY OF OXFORD.
Fecha de Publicación: .
Fecha Concesión Europea: 16 de Diciembre de 2009.
Clasificación Internacional de Patentes:
- A61K31/16 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › Amidas, p. ej. ácidos hidroxámicos.
- A61K31/395 A61K 31/00 […] › que tienen el nitrógeno como heteroátomo de un ciclo, p. ej. guanetidina o rifamicina.
- G06F19/00D
Clasificación PCT:
- C12Q1/26 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12Q PROCESOS DE MEDIDA, INVESTIGACION O ANALISIS EN LOS QUE INTERVIENEN ENZIMAS, ÁCIDOS NUCLEICOS O MICROORGANISMOS (ensayos inmunológicos G01N 33/53 ); COMPOSICIONES O PAPELES REACTIVOS PARA ESTE FIN; PROCESOS PARA PREPARAR ESTAS COMPOSICIONES; PROCESOS DE CONTROL SENSIBLES A LAS CONDICIONES DEL MEDIO EN LOS PROCESOS MICROBIOLOGICOS O ENZIMOLOGICOS. › C12Q 1/00 Procesos de medida, investigación o análisis en los que intervienen enzimas, ácidos nucleicos o microorganismos (aparatos de medida, investigación o análisis con medios de medida o detección de las condiciones del medio, p. ej. contadores de colonias, C12M 1/34 ); Composiciones para este fin; Procesos para preparar estas composiciones. › en los que interviene una oxidorreductasa.
- G01N33/573 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › para enzimas o isoenzimas.
Clasificación antigua:
- C12Q1/26 C12Q 1/00 […] › en los que interviene una oxidorreductasa.
- G01N33/573 G01N 33/00 […] › para enzimas o isoenzimas.
Fragmento de la descripción:
Método de escrutinio empleando un modelo estructural de FIH.
Campo de la invención
La presente invención se refiere a métodos de diseño de inhibidores del FIH usando la estructura cristalina del FIH.
Antecedentes de la invención
En células de muchos organismos la exposición a un entorno en el que el oxígeno está reducido respecto a los niveles óptimos induce una respuesta hipóxica. En estas células hipóxicas, la activación de una cascada transcripcional que implica al factor inducible por hipoxia (HIF) dirige una serie de respuestas adaptativas que aumentan el suministro de oxígeno o limitan la demanda de oxígeno. La activación del HIF en el cáncer y en enfermedades vasculares hipóxicas isquémicas ha puesto de manifiesto su importante papel en la patología humana y demostró que la manipulación de la actividad del HIF tiene un potencial terapéutico importante.
El complejo transcripcional del HIF comprende un heterodímero aß, siendo HIF-ß una proteína nuclear constitutiva que se dimeriza con subunidades de HIF-a reguladas por oxígeno (Semenza, G. L. (2000) Genes Dev. 14, 1983-1991). La actividad de HIF-a se suprime por una modificación dependiente de oxígeno catalizada por una serie de dioxigenasas dependientes de Fe(II) y 2OG que hidroxilan restos de HIF-a específicos. En presencia de oxígeno en HIF-1a humano, la 4-hidroxilación de Pro402 o Pro564 por un conjunto de isozimas prolil hidroxilasas de HIF (PHD1-3) (Epstein et al. (2001) Cell 107, 4357; Bruick, R. K. y McKnight, S. L. (2001) Science 294, 1337-1340) media su reconocimiento por el complejo ubiquitina ligasa de von Hippel-Lindau (VHL) y su posterior direccionamiento para la destrucción del proteosoma (Ivan et al, (2001) Science 292, 464468; Jaakkola et al. (2001) Science 292, 468-472, WO 02/074981). En un mecanismo complementario el FIH cataliza la ß-hidroxilación de la Asn803 de HIF-1a (Lando et al, (2002) Science 295, 858-861) bloqueando la interacción con el coactivador de la transcripción p300 (Dames et al (2002) Proc. Natl. Acad. Sci. U. S. A. 99, 5271-5276; Freedman et al, (2002) Proc. Natl. Acad. Sci. U. S. A. 99, 5367-5372). En la hipoxia, la limitación de la actividad enzimática permite que el HIF-a escape a la destrucción y se vuelva transcripcionalmente activo.
La inhibición de hidroxilasas de HIF activa fuertemente la cascada transcripcional del HIF incluso en presencia de oxígeno (Epstein et al. (2001) Cell 107, 4354). Por lo tanto, la inhibición de las hidroxilasas de HIF da como resultado una respuesta proangiogénica que puede usarse en el tratamiento de enfermedades cardiovasculares/enfermedades vasculares hipóxicas isquémicas, incluyendo el infarto de miocardio y la anemia. Un problema con esta estrategia es que las células humanas contienen otras enzimas que pertenecen a la misma familia que las hidroxilasas de HIF, es decir, que utilizan dioxígeno (un cosustrato), 2-oxoglutarato (2OG) (un cosustrato) y Fe(II) (un cofactor). Dichas enzimas se ejemplifican por la fitanoíl coenzima A hidroxilasa, la procolágeno prolil-4-hidroxilasa, la procolágeno prolil-3-hidroxilasa, la gamma-butirobetaína hidroxilasa, Alk B (una enzima de reparación del ADN) y otras que incluyen 2OG oxigenasas predichas identificadas en base a los análisis de secuencia que incluyen una subfamilia relacionada con el FIH (Hewitson et al., J BIOL CHEM 277 (29): 26351-26355, 2002). Generalmente se está de acuerdo en que es deseable que los inhibidores de enzimas usados como agentes farmacéuticos sean selectivos para su diana deseada o las dianas implicadas en la producción del efecto deseado. Una ausencia de selectividad puede conducir a efectos secundarios tóxicos que hacen a los compuestos particulares inadecuados para el uso en terapia humana o animal. Una estrategia para identificar compuestos que sean selectivos para la diana deseada consiste en emprender análisis estructurales, mecánicos y de otro tipo sobre los agentes deseados y usar la información obtenida para contribuir a la preparación de compuestos selectivos, o de compuestos más selectivos (respecto a los previamente conocidos), para su uso como agentes farmacéuticos para el uso en seres humanos o animales. En la presente memoria se describen estudios estructurales y de otro tipo sobre las hidroxilasas de HIF que permiten el diseño de inhibidores selectivos del FIH y enzimas relacionadas.
Compendio de la invención
Los presentes inventores han identificado ahora el sitio de hidroxilación de la asparagina 803 de HIF-1a por FIH. Además, los inventores han obtenido la estructura cristalina para el FIH, incluyendo la identificación del sitio de unión y de los restos implicados en la interacción del FIH con el HIF.
Por consiguiente, la presente invención proporciona un método de identificación, exploración, caracterización o diseño de una entidad química que mimetiza a o se une al FIH, comprendiendo dicho método comparar un modelo estructural de FIH con un modelo estructural para dicha entidad química, obteniéndose dicho modelo estructural de FIH de factores estructurales o coordenadas estructurales que se muestran en la Tabla 3.
La invención también proporciona el uso de las coordenadas estructurales del FIH de la Tabla 3 que pueden obtenerse sometiendo a un cristal que comprende el FIH a mediciones de difracción con rayos X y deduciendo las coordenadas estructurales a partir de las mediciones de difracción para identificar, explorar, caracterizar, diseñar o modificar una entidad química.
Descripción de las figuras
Figura 1: sitio de unión a 2OG.
Figura 2: unión de Asn-803.
Figura 3: conformación de CAD en el sitio 1.
Figura 4: conformación de CAD en el sitio 2.
Figura 5: figura que indica el giro formado por 802-804 de HIF-CAD en el sitio activo del FIH.
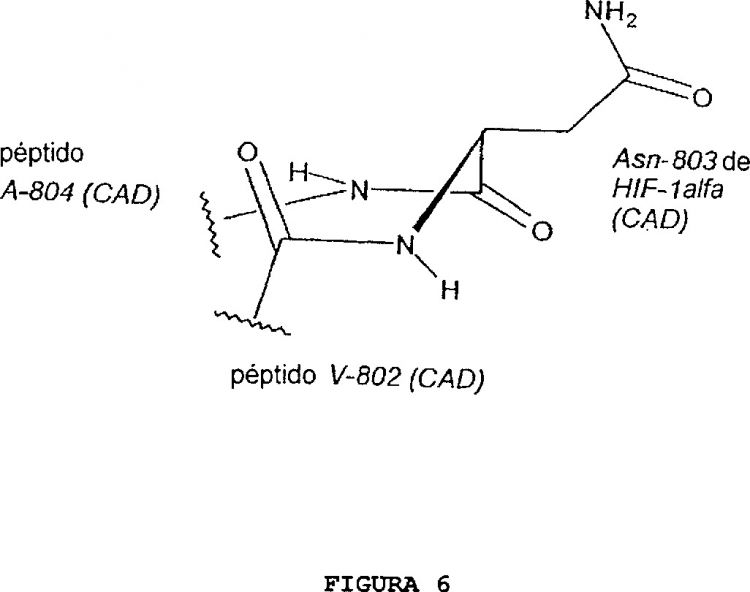
Figura 6: conformación del giro formado por los restos 802-804 de HIF-CAD en el sitio activo del FIH.
Descripción detallada de la invención
Los presentes inventores han identificado la posición de la asparagina 803 que se hidroxila por el FIH. Además, los inventores han identificado la estructura cristalina del FIH. Esta estructura permite por lo tanto la identificación de los restos aminoacídicos implicados en la unión del FIH al HIF.
La identificación de la interacción y de las estructuras permite la caracterización o identificación de las entidades químicas que pueden unirse y, en particular, que pueden inhibir al FIH. Pueden identificarse varios tipos diferentes de inhibidores como se analiza con más detalle a continuación.
Los inventores han cristalizado con éxito el FIH humano. Esta es la primera cristalización del FIH y ha permitido la determinación de la estructura cristalina. Las coordenadas del análisis cristalino se exponen en la Tabla 3 a continuación. Los estudios han permitido el análisis de la unión de la asparagina 803 del HIF y el análisis de la conformación del dominio de activación c-terminal (CAD) del HIF en los sitios de unión al FIH. La presente invención proporciona el uso de las coordenadas estructurales del FIH para identificar, caracterizar, diseñar o explorar entidades químicas. Las entidades químicas de interés son las que se unen al FIH y, en particular, que inhiben la actividad asparaginil hidroxilasa del FIH. Además, pueden identificarse, caracterizarse o diseñarse entidades químicas que sean asparagina hidroxilasas modificadas.
Típicamente, las coordenadas estructurales usadas pueden obtenerse sometiendo a un cristal que comprende el FIH o un fragmento del mismo a mediciones de difracción de rayos X y deduciendo las coordenadas estructurales a partir de las mediciones de difracción para identificar, explorar, caracterizar, diseñar o modificar una entidad química. Las coordenadas estructurales indican las posiciones de átomos individuales dentro del cristal y proporcionan una indicación del espacio disponible para ajustar la posición de átomos individuales cuando se diseña una entidad química.
El cristal sometido a métodos de difracción de rayos X comprende el FIH o un fragmento del mismo. El FIH puede ser de cualquier fuente pero preferiblemente es un FIH humano. El FIH puede ser una forma modificada. Por ejemplo, el FIH puede modificarse por inserción, deleción, adición N-terminal o C-terminal o sustitución de un aminoácido por otro aminoácido. Las sustituciones...
Reivindicaciones:
1. Un método para identificar, explorar, caracterizar o diseñar una identidad química que se une a un factor inhibidor de HIF (FIH), comprendiendo dicho método comparar un modelo estructural de FIH con un modelo estructural para dicha entidad química, procediendo dicho modelo estructural del FIH de los factores estructurales o coordenadas estructurales que se muestran en la Tabla 3.
2. Uso de las coordenadas estructurales del FIH de la Tabla 3 para identificar, explorar, caracterizar, diseñar o modificar una entidad química.
3. Un uso de acuerdo con la reivindicación 2, en el que dicha entidad química se une al FIH.
4. Un método o uso de acuerdo con una cualquiera de las reivindicaciones anteriores, en el que dicha entidad química se selecciona para inhibir la actividad asparaginil hidroxilasa del FIH.
5. Un método o uso de acuerdo con una cualquiera de las reivindicaciones anteriores, en el que dicha entidad química forma interacciones hidrófobas con cualquiera o todas las cadenas laterales de uno o más restos aminoacídicos de dicho polipéptido seleccionado de Leu186, Leu188, Thr196, Phe207 e Ile281.
6. Un método o uso de acuerdo con una cualquiera de las reivindicaciones 1 a 4, en el que dicha entidad química forma interacciones electrostáticas o de formación de enlaces de hidrógeno con uno o más restos aminoacídicos de dicho polipéptido seleccionado de Tyr145, Thr196 y Lys214.
7. Un método o uso de acuerdo con una cualquiera de las reivindicaciones anteriores que comprende además poner en contacto dicha entidad química in vitro con el HIF o un fragmento del mismo o un homólogo de cualquiera de los mismos que incorpore la asparagina 803, con el FIH o un homólogo del mismo que mantenga la actividad asparaginil hidroxilasa del FIH y controlar la hidroxilación de la asparagina 803.
Patentes similares o relacionadas:
Inhibidores de la replicación del virus de la inmunodeficiencia humana, del 13 de Mayo de 2020, de VIIV Healthcare UK (No.5) Limited: Un compuesto de fórmula I, incluyendo las sales farmacéuticamente aceptables del mismo: **(Ver fórmula)** en la que: cada uno de R1a y R1b se selecciona independientemente […]
Combinaciones y modos de administración de agentes terapéuticos y terapia combinada, del 8 de Abril de 2020, de ABRAXIS BIOSCIENCE, LLC: Una composición que comprende nanopartículas que comprenden paclitaxel y una albúmina, para uso en un método para el tratamiento de cáncer de pulmón en un individuo, en […]
Politerapia para el tratamiento de infecciones por VHB, del 25 de Marzo de 2020, de Novira Therapeutics Inc: rn inhibidor del ensamblaje de la cápside y peginterferón alfa-2a, siendo el inhibidor del ensamblaje de la cápside un compuesto de fórmula IVc: **(Ver fórmula)** o […]
Inhibidores de MCL1 macrocíclicos para tratar el cáncer, del 19 de Febrero de 2020, de ASTRAZENECA AB: Un compuesto que es acido 17-cloro-5,13,14,22-tetrametil-28-oxa-2,9-ditia-5,6,12,13,22- pentaazaheptaciclo[27.7.1.14,7.011,15.016,21.020,24.030,35]octatriaconta-1 ,4 ,6,11,14,16,18,20,23,29,31,33,35-tridecaeno- […]
Compuestos que comprenden restos de heteroarilo unidos y su uso como nuevos modificadores del sabor umami, saborizantes y potenciadores del sabor para composiciones comestibles, del 18 de Diciembre de 2019, de Firmenich Incorporated: Un compuesto de la Fórmula (IA), **(Ver fórmula)** o una sal comestiblemente aceptable del mismo; y en el que i) n' es cero, uno, dos o tres, y cada R20 se […]
Procedimientos de tratamiento de encefalopatía hepática, del 11 de Diciembre de 2019, de Salix Pharmaceuticals, Ltd: Rifaximina para su uso en la disminución del riesgo de un sujeto de episodios importantes de encefalopatía hepática (EH) en un sujeto que padece EH o en un sujeto con […]
Compuestos terapéuticamente activos y sus métodos de utilización, del 20 de Noviembre de 2019, de Agios Pharmaceuticals, Inc: Compuesto que presenta la fórmula Ia o una sal o hidrato farmacéuticamente aceptable del mismo, en el que: **(Ver fórmula)** el anillo A se selecciona de fenilo, […]
Uso de plerixafor para tratar y/o prevenir exacerbaciones agudas de la enfermedad pulmonar obstructiva crónica, del 9 de Octubre de 2019, de Université de Bordeaux: Una composición para su uso en un método para tratar y/o prevenir las EAEPOC, que comprende una cantidad terapéuticamente eficaz de plerixafor […]