Trastornos autoinmunitarios neurológicos.
Un método de diagnosticar en un mamífero un trastorno neurológico autoinmunitario seleccionado del grupo que comprende encefalitis límbica,
síndrome de Morvan, y neuromiotonía que comprende detectar, en una muestra de fluido corporal del mamífero, autoanticuerpos hacia un epítopo de al menos una proteína del complejo Kv1, en donde la proteína del complejo Kv1 comprende al menos una de CASPR2 (proteína asociada a contactina 2), Lgi1 (gen inactivado de glioma rico en leucina 1) y TAG1 (glicoproteína axonal transitoria 1); en donde el método comprende los pasos de a) poner en contacto el fluido corporal con la al menos una proteína del complejo Kv1; y b) detectar cualquier complejo autoanticuerpo-antígeno formado entre la al menos una proteína del complejo Kv1 y autoanticuerpos presentes en el fluido corporal, en donde la presencia de dicho complejo es indicativa de un trastorno neurológico autoinmunitario seleccionado del grupo que comprende encefalitis límbica, síndrome de Morvan y neuromiotonía.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/GB2009/051441.
Solicitante: ISIS INNOVATION LIMITED.
Nacionalidad solicitante: Reino Unido.
Dirección: University of Oxford Ewert House Ewert Place Summertown Oxford 0X2 7SG REINO UNIDO.
Inventor/es: VINCENT,ANGELA.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- G01N33/564 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › para complejos inmunológicos preexistentes o enfermedades autoinmunes.
PDF original: ES-2550880_T3.pdf


Fragmento de la descripción:
Trastornos autoinmunitarios neurológicos La presente invención se refiere a trastornos autoinmunitarios, y en particular a métodos de diagnosticar tales trastornos en mamíferos. La presente invención también proporciona kits para uso en dicho diagnóstico, y métodos y composiciones para detectar autoanticuerpos.
Los anticuerpos contra canales de potasio operados por voltaje (VGKC) se asocian con tres síndromes clínicos principales: neuromiotonía (MNT) , síndrome de Morvan (SMo) y encefalitis límbica (EL) . NMT describe síndromes de hiperexcitabilidad de nervios periféricos que producen calambres musculares y rigidez, y algunas veces dolor. El SMo describe NMT más características autonómicas, por ejemplo, sudoración excesiva, estreñimiento, irregularidades cardiacas y características del sistema nervioso central, particularmente confusión, alucinaciones e insomnio. La EL asociada con anticuerpos anti-VGKC incluye las características restringidas al sistema nervioso central (SNC) de amnesia, trastornos de la personalidad o psiquiátricos, y convulsiones (epilepsia) . Estas afecciones (particularmente el SMo) se pueden asociar con tumores tímicos u otros (carcinoma de pulmón, linfoma, neoplasias malignas ginecológicas) pero la EL asociada a anticuerpo anti-VGKC es principalmente no paraneoplásica. Los tres síndromes tienen un inicio subagudo y pueden responder a inmunoterapia. Además, hay reconocimiento de estos anticuerpos en algunos pacientes que presentan otros síndromes clínicos tal como epilepsia idiopática. La mayoría de los pacientes hasta ahora son adultos, pero se han identificado algunos niños con estos anticuerpos y EL o epilepsia. Como ya se ha demostrado in vivo con MNT [1], mucha evidencia apoya un papel patogénico de la inmunoglobulina G (IgG) en EL y SMo. En primer lugar, los pacientes con frecuencia experimentan una recuperación clínica rápida después del intercambio de plasma [2, 3]. En segundo lugar, los títulos del anticuerpo en un paciente individual se correlacionan bien con alteraciones en el estado clínico [2, 3]. En tercer lugar, la IgG del paciente se une al hipocampo, la región anatómica a la que se pueden localizar casi todas las características clínicas del SNC [2-4]. Aproximadamente 500 pacientes con anticuerpos anti-VGKC y características del SNC han sido diagnosticados en los últimos 5 años en el RU (A Vincent, observaciones sin publicar) .
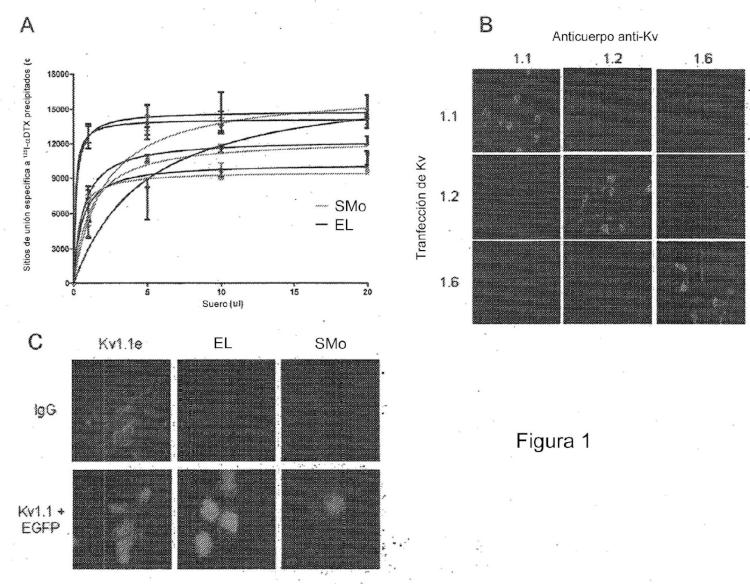
Los sueros de pacientes que inmunoprecipitan homogenizado de cerebro de mamífero solubilizado con digitonina marcado con alfa-dendrotoxina yodada (I125-αDTX) se designan como que contienen anticuerpos anti-VGKC [5, 6]. Los canales de potasio operados por voltaje consisten en un número de familias estructuralmente diferentes de canales incluyendo el subtipo Kv1 (Shaker) . Las subunidades de Kv1 alfa pueden homo-o heterotetramerizar exclusivamente con otras subunidades de Kv1 para formar canales activos. αDTX se une a canales Kv1.1, 1.2 y 1.6 que están todos presentes en tejido cerebral y Kv1.1 y 1.2 se encuentran en nervios periféricos. Estas 3 subunidades pueden tener su función y expresión de superficie modulada por Kv1.4 y por Kvβ1, 2 y 3, donde Kvβ2 es el miembro Kvβ más abundante en tejido cerebral.
Los pacientes con EL y SMo generalmente tienen títulos de anticuerpo anti-VGKC mayores que los pacientes de MNT. Las dianas antigénicas y efectos funcionales de anticuerpos anti-VGKC en MNT se han estudiado previamente en detalle y se ha mostrado que la IgG de MNT se une a Kv1 expresados y disminuye las corrientes de Kv1 [5-7] pero solo un estudio ha examinado los anticuerpos anti-VGKC de EL o SMo [8].
Recientemente, se ha descrito un número de proteínas novedosas que interaccionan con Kv1 [9, 10]. La presente invención muestra que proteínas del complejo Kv1, por ejemplo, las tres proteínas del complejo de Kv1 CASPR2 (proteína asociada a contactina 2) , Lgi1 (gen inactivado de glioma rico en leucina 1) , TAG1 (glicoproteína axonal transitoria 1, también conocida como contactina 2) , y no necesariamente las proteínas de Kv1 mismas, son las dianas para autoanticuerpos de algunos pacientes con EL y SMo.
Según un primer aspecto, la presente invención proporciona un método de diagnosticar un trastorno autoinmunitario neurológico seleccionado del grupo que comprende encefalitis límbica, síndrome de Morvan, y neuromiotonía en un mamífero, que comprende el paso de detectar, en una muestra de fluido corporal del mamífero, autoanticuerpos hacia un epítopo de al menos una proteína del complejo Kv1, en donde la proteína del complejo Kv1 comprende al menos una de CASPR2 (proteína asociada a contactina 2) , Lgi1 (gen inactivado de glioma rico en leucina 1) , TAG1 (glicoproteína axonal transitoria 1) ; en donde el método comprende los pasos de a) poner en contacto el fluido corporal con la al menos una proteína del complejo Kv1; y b) detectar cualquier complejo autoanticuerpo-antígeno formado entre la al menos una proteína del complejo Kv1 y autoanticuerpos presentes en el fluido corporal, en donde la presencia de dicho complejo es indicativa de un trastorno neurológico autoinmunitario; en donde el trastorno neurológico autoinmunitario se selecciona del grupo que comprende encefalitis límbica, síndrome de Morvan y neuromiotonía.
La al menos una proteína del complejo Kv1 puede estar acomplejada/unida con otras proteínas del complejo Kv1, o la al menos una proteína de Kv1 puede estar separada del complejo Kv1, por ejemplo, no colocalizada, o no físicamente unida al complejo. Los autoanticuerpos se pueden unir a las proteínas normalmente acomplejadas/unidas incluso cuando no están en estado acomplejado/unido.
La proteína del complejo Kv1 puede ser una proteína accesoria esencial o no esencial a Kv1. La proteína del complejo Kv1 comprende al menos una de CASPR2, Lgi1 y TAG1. En una forma de realización, las proteínas del complejo Kv1 pueden no comprender Kv1.
CASPR2, Lgi1 y TAG1 son proteínas que se ha mostrado que interaccionan o están físicamente unidas con Kv1. Por ejemplo, CASPR2 y Tag1 son necesarias para la localización de proteínas de Kv1 en los nódulos de Ranvier.
La proteína del complejo Kv1 puede comprender, o consistir esencialmente en, CASPR2. La proteína del complejo Kv1 puede comprender, o consistir esencialmente en, Lgi1. La proteína del complejo Kv1 puede comprender, o consistir esencialmente en, TAG1. La proteína del complejo Kv1 puede comprender, o consistir esencialmente en, una proteína del complejo Kv1 diferente de CASPR2, Tag1, Lgi1, y Kv1.
Preferiblemente el trastorno neurológico es encefalitis límbica o síndrome de Morvan, o neuromiotonía. Donde el trastorno neurológico es encefalitis límbica, la característica dominante del trastorno neurológico puede comprender convulsiones, por ejemplo, epilepsia, o amnesia, o trastorno psiquiátrico solo.
Donde el trastorno neurológico autoinmunitario es síndrome de Morvan y/o neuromiotonía, la proteína del complejo Kv1 puede comprender CASPR2. Los autoanticuerpos dirigidos contra CASPR2 pueden ser indicativos de, o estar asociados con, un riesgo aumentado de neoplasias malignas del timo y/o otras neoplasias malignas.
Donde el trastorno neurológico autoinmunitario es encefalitis límbica, la proteína del complejo Kv1 puede comprender Lgi1.
Donde el trastorno neurológico autoinmunitario es neuromiotonía y/o encefalitis límbica, la proteína del complejo Kv1 puede comprender TAG1.
Donde el trastorno neurológico autoinmunitario es encefalitis límbica, síndrome de Morvan o neuromiotonía la proteína del complejo Kv1 puede comprender CASPR2 y TAG1.
Preferiblemente, el método de la invención comprende además los pasos de a) poner en contacto el fluido corporal con la proteína del complejo Kv1 o un determinante antigénico de la misma; y b) detectar cualquier complejo anticuerpo-antígeno formado entre proteína del complejo Kv1 o un determinante antigénico de la misma y anticuerpos presentes en el fluido corporal, en donde la presencia de dicho complejo es indicativa de un trastorno neurológico autoinmunitario, preferiblemente de encefalitis límbica, síndrome de Morvan o neuromiotonía.
Preferiblemente, el método de la invención se realiza en combinación con una valoración de síntomas clínicos. La combinación del método de la invención y un análisis de los síntomas clínicos se puede usar para determinar el trastorno neurológico específico que tiene un individuo.
El autoanticuerpo se puede detectar por cualquier técnica de ensayo inmunológico, de las cuales muchas se conocen en la técnica. Los ejemplos de técnicas adecuadas incluyen ELISA, radioinmunoensayo, un ensayo de competición, un ensayo... [Seguir leyendo]
Reivindicaciones:
1. Un método de diagnosticar en un mamífero un trastorno neurológico autoinmunitario seleccionado del grupo que comprende encefalitis límbica, síndrome de Morvan, y neuromiotonía que comprende detectar, en una 5 muestra de fluido corporal del mamífero, autoanticuerpos hacia un epítopo de al menos una proteína del complejo Kv1, en donde la proteína del complejo Kv1 comprende al menos una de CASPR2 (proteína asociada a contactina 2) , Lgi1 (gen inactivado de glioma rico en leucina 1) y TAG1 (glicoproteína axonal transitoria 1) ; en donde el método comprende los pasos de a) poner en contacto el fluido corporal con la al menos una proteína del complejo Kv1; y b) detectar cualquier complejo autoanticuerpo-antígeno formado entre la al menos una proteína del complejo Kv1 y autoanticuerpos presentes en el fluido corporal, en donde la presencia de dicho complejo es indicativa de un trastorno neurológico autoinmunitario seleccionado del grupo que comprende encefalitis límbica, síndrome de Morvan y neuromiotonía.
2. Uso de un kit de ensayo para diagnosticar un trastorno neurológico autoinmunitario seleccionado del grupo que comprende encefalitis límbica, síndrome de Morvan y neuromiotonía en un mamífero según el método de la reivindicación 1, en donde el kit comprende al menos un epítopo de al menos una proteína del complejo Kv1, en donde la proteína del complejo Kv1 comprende al menos una de CASPR2, Lgi1 y TAG1 e instrucciones para usar el kit.
o un epítopo de las mismas, en donde un compuesto que previene la unión de dicho anticuerpo a al menos una proteína del complejo Kv1 o un epítopo de la misma es un candidato para tratar trastornos neurológicos autoinmunitarios, en donde el trastorno neurológico autoinmunitario se selecciona del grupo que comprende encefalitis límbica, síndrome de Morvan, y neuromiotonía.
5. El método o uso de un kit de cualquiera de las reivindicaciones precedentes en donde el mamífero es un ser 35 humano.
Figura 13
Hombres Mujeres Total Neg para Ac contraVGKC
Números totales 78 30 108 8
Edad mediana, intervalo 54, 19-78 60, 17-83 60, 17-83
Tumores no tímicos* 5 2 7 0
Timomas** 8 3 11 0
Encefalitis límbica oepilepsia 49 16 65 0
Síndrome de Morvan 11 1 12 0
Neuromiotonía 15 10 25 8
Epilepsia u otras 3 3 6 0
Figura 14
Todos los pacientes Lgi1 CASPR2 TAG-1 Proteína accesoria aúnno identificada
Número total 39 27 4 38
Neoplasias malignastímicas 0 10 0 1
Encefalitis límbica oepilepsia 36 7 1 21
Síndrome de Morvan 2 10 0 0
Neuromiotonía 0 8 3 14
Otro síndrome 1 2 0 3
negativo para Accontra VGKC 0 0 1 7
* La mayoría no estaban actualmente activos
Patentes similares o relacionadas:
Biomarcador de enfermedad autoinmunitaria, del 15 de Julio de 2020, de Tzartos, Socrates: Un método de diagnóstico o pronóstico de una enfermedad autoinmunitaria asociada con la formación de lesiones desmielinizadas del sistema nervioso central (SNC) […]
ANTICUERPO SÉRICO IGM-PC COMO BIOMARCADOR DE LA ESCLEROSIS MÚLTIPLE, Y NUEVA ELISA ULTRASENSIBLE PARA EL DIAGNÓSTICO DE ESTA ENFERMEDAD, del 2 de Julio de 2020, de FUNDACION UNIVERSITARIA SAN PABLO CEU: Anticuerpo sérico IgM frente a fosfatidilcolina (IgM-PC) para ser utilizado como biomarcador de la esclerosis múltiple (EM) y de las diferentes fases de esta enfermedad, […]
Ensayos para la detección de fármacos anti-TNF y autoanticuerpos, del 8 de Abril de 2020, de Prometheus Biosciences, Inc: Un método para determinar la presencia o el nivel de un fármaco anti-TNFa en una muestra biológica, en la que el fármaco anti-TNFa es un […]
Composiciones y métodos para el diagnóstico de la artritis reumatoide, del 4 de Marzo de 2020, de Inova Diagnostics, Inc: Un complejo que comprende un polipéptido purificado que comprende una alfa-1-antitripsina humana (hA1AT) carbamilada in vitro, o uno de sus fragmentos, y […]
Procedimientos y kits de supervisión de la nefropatía membranosa, del 15 de Enero de 2020, de uroimmun Medizinische Labordiagnostika AG: Un procedimiento in vitro para diagnosticar y/o pronosticar la nefropatía membranosa en un paciente, comprendiendo dicho procedimiento la etapa de detectar en una […]
Procedimiento de determinación de las concentraciones activas y/o de las constantes cinéticas de interacción en muestras biológicas complejas en resonancia de plasmón superficial, del 8 de Enero de 2020, de Université de Bordeaux: Método para determinar en muestras biológicas complejas en resonancia de plasmón superficial la concentración activa de un analito y, facultativamente, las constantes […]
Método para la medición de anticuerpos anti-fármaco, del 25 de Diciembre de 2019, de JIMRO CO., LTD: Un método para medir anticuerpos anti-fármaco (ADA) en un analito a medir, comprendiendo el método: una etapa de proporcionar una muestra […]
Procedimientos para determinar el riesgo de diabetes tipo 1 mediante biomarcadores de proteínas séricas, del 28 de Octubre de 2019, de TURUN YLIOPISTO: Un procedimiento para predecir, determinar y/o monitorizar un riesgo de y/o progresión hacia la diabetes tipo 1 (T1D) en un individuo, comprendiendo el procedimiento: a) determinar […]