METODO IN VITRO NO INVASIVO PARA DETECTAR CARCINOMA TRANSICIONAL DE VEJIGA.
Método in vitro no invasivo para detectar carcinoma transicional de vejiga.
La presente invención se refiere a un método in vitro no invasivo para detectar la presencia de carcinoma transicional de vejiga en un individuo mediante análisis de orina, para determinar el estadio o severidad de dicho cáncer o para monitorizar el efecto del tratamiento administrado a un individuo que padece dicho cáncer
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P200700945.
Solicitante: LABORATORIOS SALVAT, S.A..
Nacionalidad solicitante: España.
Provincia: BARCELONA.
Inventor/es: SIMON BUELA,LAUREANO, MARTINEZ MARTINEZ,ANTONIO, SOLOAGA VILLOCH,ANA, RAMOS RODRIGUEZ,INMA.
Fecha de Solicitud: 30 de Marzo de 2007.
Fecha de Publicación: .
Fecha de Concesión: 30 de Abril de 2010.
Clasificación Internacional de Patentes:
- G01N33/574 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › para el cáncer.
- G01N33/68 G01N 33/00 […] › en los que intervienen proteínas, péptidos o aminoácidos.
Clasificación PCT:
- G01N33/574 G01N 33/00 […] › para el cáncer.
- G01N33/68 G01N 33/00 […] › en los que intervienen proteínas, péptidos o aminoácidos.
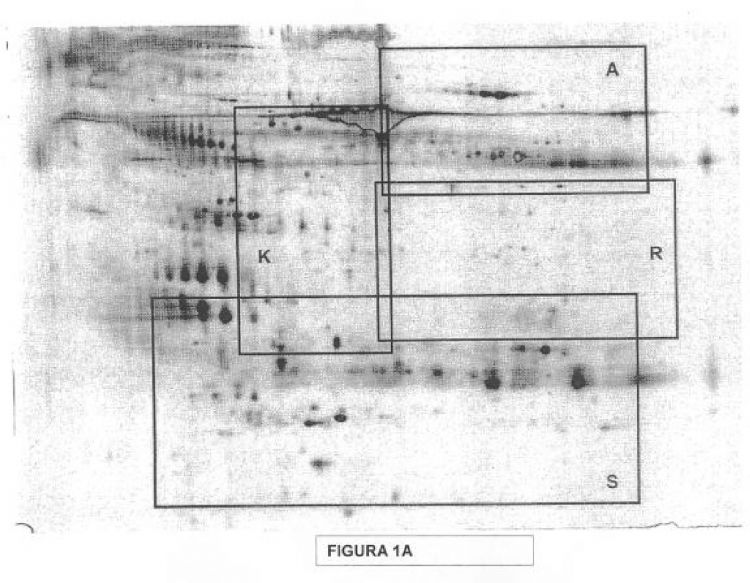
Fragmento de la descripción:
Método in vitro no invasivo para detectar carcinoma transicional de vejiga.
Sector de la técnica al cual se refiere la invención
La presente invención se refiere a un método in vitro no invasivo para detectar la presencia de carcinoma transicional de vejiga en un individuo mediante análisis de orina, así como al uso de secuencias peptídicas derivadas de proteínas seleccionadas y a un kit para llevar a cabo dicho método.
Estado de la técnica relativo a la invención
El cáncer de vejiga es el cáncer más común del tracto urinario; es también el cuarto cáncer más común en hombres y el octavo más común en mujeres. Incluye un amplio espectro de tumores de varios tipos histológicos como son carcinoma transicional de vejiga (BTCC, 90%), carcinoma de células escamosas (7%), adenocarcinoma (2%) y carcinoma no diferenciado (1%).
Los mejores indicadores del pronóstico de BTCC son el grado y estadio del tumor. Los tumores de vejiga se clasifican citomorfológicamente de G1 (grado bajo) a G3 (grado alto) en estado de diferenciación decreciente e incremento de la agresividad de la enfermedad según la Organización Mundial de la Salud (OMS). Con respecto al estadio o grado de invasividad, los BTCCs se clasifican como papilar superficial (Ta y T1), invasivo del músculo (T2 a T4), y carcinoma no común in situ o tumor in situ (TIS).
Los tumores de grado bajo normalmente están confinados a la mucosa o infiltran las capas superficiales (estadios Ta y T1). La mayoría de tumores de grado alto se detectan como mínimo en el estadio T1 (invadiendo la lamina propria). Aproximadamente un 75% de los casos diagnosticados de cáncer de vejiga son superficiales. El 25% restante son invasivos del músculo en el momento del diagnóstico. Los pacientes con BTCC superficial presentan un buen pronóstico aunque el riesgo de recidiva es del 70%. A pesar de este riesgo, los tumores Ta tienden a ser de grado bajo y solamente un 10-15% progresa con invasión del músculo en 2 años. Sin embargo, el porcentaje de cánceres T1 que progresa al estadio T2 es más elevado (30-50%).
Actualmente, el mejor diagnóstico para el cáncer de vejiga se establece o bien por cistoscopia y biopsia transuretral o por resección, siendo todos ellos métodos invasivos. El uso de cistoscopios flexibles convierte la técnica en menos agresiva, aunque sigue siendo invasiva y muy incómoda y requiere alguna forma de anestesia.
La técnica no invasiva predominante para el diagnóstico de BTCC es la identificación de células neoplásicas mediante examen morfológico de las células de la orina. Así, actualmente se utilizan citologías para controlar pacientes de cáncer de vejiga diagnosticados y tratados. Aunque la citología manual de la orina puede detectar tumores in situ que no son detectables mediante cistoscopia, así como también tumores localizados en la parte superior de la vejiga o en la parte superior del tracto urinario, por ejemplo uréter, pelvis y riñón; varios estudios han demostrado que la citología presenta muy baja sensibilidad para el diagnóstico de cáncer de vejiga, no detectando hasta el 50% de los tumores. Los resultados de las citologías son sutiles y pueden confundirse con procesos reactivos o degenerativos. Además, los estudios citológicos requieren la evaluación individual de un experto, lo cual retrasa la disponibilidad de los resultados y además introduce subjetividad y variación en los resultados finales. En realidad, no se dispone de ningún método no invasivo altamente sensible y específico para el diagnóstico del cáncer de vejiga (Boman, H., et al., J Urol 2002, 167:80-83).
Se han realizado muchos esfuerzos para mejorar la detección no invasiva del cáncer. Avances recientes en el perfil de expresión de células cancerosas mediante técnicas de proteómica, electroforesis bidimensional de alta resolución y espectrometría de masas han hecho posible la identificación de proteínas como marcadores de cáncer de vejiga, tales como la proteína matricial nuclear NMP22 (Soloway, M.S., et al., J Urol 1996, 156:363-367), el ácido hialurónico y la hialuronidasa (Pham HT, et al., Cancer Res 1997, 57:778-783), los complejos de membrana basal (BTA, Pode, D., et al., J Urol 1999, 161:443-446), el antígeno carcinoembrionario (CEA, Halim A.B., et al., Int J Biol Marcadores, 1992; 7:234-239), la uroplakina II (Wu X.R., et al., Cancer Res 1998; 58:1291-1297), el factor de dispersión/de crecimiento hepatocitario (SF/HGF, Gohji K, et al., J Clin Oncol 2000; 18:2963-2971), las proteínas de la familia queratina/citoqueratina tales como citoqueratina 20 (Buchumensky V, et al., J Urol 1998, 160:1971-1974), la citoqueratina 18 (Sánchez-Carbayo M, et al., Clin Cancer Res 2000, 6:3585-3594), la proteína del tumor mamario 8-Ka (MAT-8, Morrison BW, et al., J Biol Chem, 1995, 270:2176-2182) y la telomerasa (Lee DH, et al., Clinical Cancer Research, 1998, 4: 535-538).
Memon A. A. et al. (Cancer Detect Prev 2005, 29:249-255) identifican siete proteínas diferencialmente expresadas en líneas celulares y biopsias de cáncer de vejiga. Sin embargo, no utilizan ningún control para comparar.
Rasmussen H. H. et al. (J Urol 1996, 155 :2113-2119) describen una base de datos de las proteínas más abundantes presentes en la orina de pacientes de cáncer de vejiga. Celis J. E. et al (Electrophoresis 1999, 300-309) describen una base de datos de proteínas presentes en biopsias provinientes de pacientes con cáncer de vejiga. Sin embargo, no se identifican marcadores en ninguna de estas referencias, ya que los autores no muestran una cuantificaión del perfil diferencial de proteínas en muestras sanas versus muestras tumorales.
Por ahora, no se ha encontrado ningún marcador útil para para predecir la prognosis y la extensión del cáncer de vejiga en ensayos clínicos (Miyake, H., et al., J Urol 2002; 167:1282-1287).
Descripción de la invención
La presente invención proporciona un método in vitro no invasivo, altamente sensible, eficiente y rápido, relativo a proteínas asociadas con BTCC. También proporciona un método para el diagnóstico, pronóstico y monitorización de BTCC mediante análisis de muestras de orina. La presente invención proporciona sorprendentemente una combinación de biomarcadores de cáncer de vejiga para la detección de BTCC mediante análisis de orina, con valor significativo para el diagnóstico, pronóstico y/o monitorización de BTCC.
La alfa-amilasa (AMYS) carcinoide, la alfa-amilasa pancreática y la alfa amilasa IA pertenecen a la familia de las glicosil hidrolasas 13 e hidrolizan enlaces 1,4-alfa-glucosídicos en oligosacáridos y polisacáridos, y catalizan la primera etapa en la digestión del glicógeno y el almidón de la dieta. El genoma humano contiene un conjunto de genes que codifican amilasas y que se expresan en niveles elevados o bien en la glándula salival o en el páncreas.
La apolipoproteína A-I (APOA1) pertenece a la familia de las apolipoproteínas A1/A4/E y participa en el transporte inverso de colesterol desde los tejidos hasta el hígado para su excreción mediante la promoción del reflujo de colesterol desde los tejidos y la actuación como cofactor de la lecitina colesterol aciltransferasa (LCAT).
La catepsina D (CATD) es una proteasa ácida que pertenece a la familia de las peptidasas Al y que activa la degradación proteica intracelular. Está implicada en la patogénesis de diversas enfermedades tales como cáncer de vejiga (Ozer E., et al., Urology 1999, 54:50-5 y loachim E., et al., Anticancer Res 2002, 22:3383-8), cáncer de mama y posiblemente enfermedad de Alzheimer. La catepsina D se sintetiza como un precursor inactivo de 52 kDa, formado por dos polipéptidos de 14 kDa (CATD H) y 34 kDa (CATD K). El péptido inactivo se activa por proteólisis del extremo N-terminal resultando en la proteína enzimáticamente activa de 48 kDa.
La glutatión S-transferasa (GSTP1) pertenece a una familia de enzimas que juegan un papel importante en la detoxificación mediante catálisis de la conjugación de algunos compuestos hidrofóbicos y electrofílicos con glutatión reducido.
La peroxiredoxina 2 (PRDX2) pertenece a la familia de las ahpc/tsa y está implicada en la regulación redox de la célula. Reduce los peróxidos con equivalentes reductores obtenidos a través del sistema de tioredoxina. No tienen capacidad para recibir electrones de la glutaredoxina. Puede desempeñar un papel importante en la eliminación...
Reivindicaciones:
1. Una combinación de biomarcadores para la detección de BTCC que comprende los biomarcadores CATD (ID SEC 1, ID SEC 2), GSTP1 (ID SEC 3), RETBP (ID SEC 4) y STIP1 (ID SEC 5) o sus variantes transcripcionales o post-traduccionales.
2. Combinación según la reivindicación 1 que comprende además los biomarcadores AMYS (ID SEC 6), APOA1 (ID SEC 7) o sus variantes transcripcionales o post-traduccionales.
3. Combinación según la reivindicación 2 que comprende además el biomarcador PRDX2 (ID SEC 8) o sus variantes transcripcionales o post-traduccionales.
4. Combinación según la reivindicación 2 ó 3 que comprende además el biomarcador TTHY (ID SEC 9) o sus variantes transcripcionales o post-traduccionales.
5. Un método in vitro no invasivo que comprende: a) detectar y cuantificar la combinación de biomarcadores definida en la reivindicación 1 en una muestra test de orina de un individuo; y b) comparar el valor de expresión obtenido en a) en la muestra test de orina con el correspondiente valor estándar en orina normal, donde variaciones en el valor obtenido en a) respecto al valor estándar en orina normal son indicativas de carcinoma transicional de vejiga.
6. Método según la reivindicación 5, donde la etapa a) comprende detectar y cuantificar la combinación de biomarcadores definida en la reivindicación 2.
7. Método según la reivindicación 5, donde la etapa a) comprende detectar y cuantificar la combinación de biomarcadores definida en la reivindicación 3.
8. Método según la reivindicación 5, donde la etapa a) comprende detectar y cuantificar la combinación de biomarcadores definida en la reivindicación 4.
9. Método según cualquiera de las reivindicaciones 5 a 8, donde el método se emplea para detectar la presencia de BTCC, determinar el estadio o severidad de este cáncer, evaluar la ausencia de enfermedad después de resección quirúrgica, establecer un diagnóstico y/o pronóstico de este cáncer y/o monitorizar el efecto de la tratamiento administrado a un individuo que padece dicho cáncer.
10. Método según cualquiera de las reivindicaciones 5 a 9, donde la muestra de orina a analizar se obtiene de un individuo a quien no se le ha diagnosticado previamente carcinoma transicional de vejiga.
11. Método según cualquiera de las reivindicaciones 5 a 9, donde la muestra de orina a analizar se obtiene de un individuo a quien se le ha diagnosticado previamente carcinoma transicional de vejiga.
12. Método según cualquiera de las reivindicaciones 5 a 9, donde la muestra de orina a analizar se obtiene de un individuo que está recibiendo tratamiento en la actualidad contra carcinoma transicional de vejiga.
13. Método según cualquiera de las reivindicaciones 5 a 12, donde la detección y cuantificación de proteínas comprende una primera etapa, en la cual el extracto de proteína de la muestra se pone en contacto con una composición de anticuerpos específicos para uno o más epítopos de las proteínas de la reivindicación 1, y una segunda etapa, en la cual se cuantifican los complejos anticuerpo-proteína.
14. Método según la reivindicación 13, donde los anticuerpos son de origen humano, humanizados o de origen no humano y seleccionados entre anticuerpos monoclonales o policlonales, fragmentos de anticuerpos intactos o recombinantes, combibodies y fragmentos de anticuerpo Fab o scFv.
15. Método según la reivindicación 13 ó 14, donde la detección y cuantificación de los complejos anticuerpo-proteína, las técnicas utilizadas se seleccionan del grupo que comprende: western blot, ELISA (ensayo inmunoabsorbente unido a enzima), RIA (radioinmunoensayo), EIA competitivo (inmunoensayo enzimático competitivo), DAS-ELISA (ELISA sandwich de doble anticuerpo), técnicas inmunocitoquímicas o inmunohistoquímicas, técnicas basadas en el uso de biochips o microarrays de proteína que incluyen anticuerpos específicos, ensayos basados en la precipitación de oro coloidal en formatos tales como dipsticks; o por técnicas de afinidad cromatográfica, ensayos de unión a ligando y ensayos de unión a lectina.
16. Método según cualquiera de las reivindicaciones 5 a 15, donde el método se utiliza para monitorizar la eficacia del tratamiento farmacológico o quirúrgico.
17. Método según cualquiera de las reivindicaciones 5 a 16, donde el método se utiliza para determinar la progresión de la enfermedad cuando la misma proteína o proteínas se comparan en diferentes muestras obtenidas de un mismo paciente a diferentes tiempos durante la evolución del carcinoma transicional de vejiga.
18. Uso in vitro de las secuencias peptídicas derivadas de los biomarcadores de la combinación definida en la reivindicación 1 para detectar la presencia de BTCC mediante análisis de orina, determinar el estadio o severidad de este cáncer, evaluar la ausencia de enfermedad después de resección quirúrgica, establecer un diagnóstico y/o pronóstico de este cáncer y/o monitorizar el efecto de la tratamiento administrado a un individuo que padece dicho cáncer, donde los biomarcadores están presentes en orina.
19. Uso según la reivindicación 18 de las secuencias peptídicas derivadas de los biomarcadores de la combinación definida en la reivindicación 2.
20. Uso según la reivindicación 18 de las secuencias peptídicas derivadas de los biomarcadores de la combinación definida en la reivindicación 3.
21. Uso según la reivindicación 18 de las secuencias peptídicas derivadas de los biomarcadores de la combinación definida en la reivindicación 4.
22. Uso según cualquiera de las reivindicaciones 18 a 21, donde variaciones en el nivel de expresión de uno o más biomarcadores en una muestra test de orina respecto al correspondiente valor estándar en orina normal son indicativas de carcinoma transicional de vejiga.
23. Uso conjunto de los nucleótidos o secuencias peptídicas derivados de los biomarcadores de la combinación definida en la reivindicación 1, en métodos para cribar, identificar, desarrollar y evaluar la eficiencia de compuestos en el carcinoma transicional de vejiga.
24. Un kit para llevar a cabo el método previamente descrito en cualquiera de las reivindicaciones 5 a 17 que comprende 1) anticuerpos que reconocen específicamente la combinación de biomarcadores definida en la reivindicación 1 y 2) un soporte en un embalaje adecuado.
25. Un kit según la reivindicación 24 que se emplea para detectar la presencia de carcinoma transicional de vejiga, determinar el estadio o severidad de este cáncer, evaluar la falta de enfermedad después de resección quirúrgica, establecer un diagnóstico y/o pronóstico de este cáncer y/o monitorizar el efecto del tratamiento administrado a un individuo que padece dicho cáncer.
26. Un kit según la reivindicación 24 ó 25 que comprende un biochip.
27. Un kit según la reivindicación 26, donde el biochip comprende anticuerpos para la detección de proteínas de la combinación de biomarcadores definida en la reivindicación 1.
Patentes similares o relacionadas:
Métodos y composiciones para el diagnóstico y pronóstico de lesión renal e insuficiencia renal, del 29 de Julio de 2020, de Astute Medical, Inc: Un método para evaluar el estado renal en un sujeto, que comprende: realizar una pluralidad de ensayos configurados para detectar una […]
Neuregulina para tratar la insuficiencia cardíaca, del 29 de Julio de 2020, de Zensun (Shanghai) Science & Technology, Co., Ltd: Neuregulina para usar en un método para tratar la insuficiencia cardíaca crónica en un paciente, donde el paciente tiene un nivel plasmático de NT-proBNP […]
Inmunomoduladores, del 29 de Julio de 2020, de BRISTOL-MYERS SQUIBB COMPANY: Un compuesto de la fórmula (I) **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en donde: A se selecciona de **(Ver fórmula)** en donde: […]
Detección de interacciones proteína a proteína, del 15 de Julio de 2020, de THE GOVERNING COUNCIL OF THE UNIVERSITY OF TORONTO: Un método para medir cuantitativamente la fuerza y la afinidad de una interacción entre una primera proteína de membrana o parte de la misma y una […]
Método para llevar a cabo el seguimiento de la enfermedad de Gaucher, del 15 de Julio de 2020, de Centogene GmbH: Un método para determinar la evolución de la enfermedad de Gaucher en un sujeto, que comprende la etapa de determinar en varios puntos en el […]
Procedimiento para evaluación de la función hepática y el flujo sanguíneo portal, del 15 de Julio de 2020, de The Regents of the University of Colorado, a body corporate: Procedimiento in vitro para la estimación del flujo sanguíneo portal en un individuo a partir de una única muestra de sangre o suero, comprendiendo el procedimiento: […]
Biomarcadores de pronóstico y predictivos y aplicaciones biológicas de los mismos, del 1 de Julio de 2020, de INSTITUT GUSTAVE ROUSSY: Un método para evaluar la sensibilidad o la resistencia de un tumor frente a un agente antitumoral, que comprende evaluar la cantidad de complejo eiF4E-eiF4G (complejo Cap-ON) […]
Métodos de monitorización terapéutica de profármacos de ácido fenilacético, del 24 de Junio de 2020, de Immedica Pharma AB: Glicerilo tri-[4-fenilbutirato] (HPN-100) para su uso en un método para tratar un trastorno del ciclo de la urea en un sujeto que tiene discapacidad […]