PROCEDIMIENTO DE DIAGNOSTICO Y TRATAMIENTO DEL CANCER BASADO EN LA LAFORINA, ELEMENTOS BIOLOGICOS PARA LLEVARLOS A CABO Y SUS APLICACIONES.
Procedimiento de diagnóstico y tratamiento del cáncer basado en la laforina,
elementos biológicos para llevarlos a cabo y sus aplicaciones.
La presente invención describe un procedimiento de diagnóstico del cáncer basado en la identificación de la ausencia o disminución de la expresión de la proteína laforina, preferentemente cáncer de colon, mama y riñón. Igualmente, se ha establecido el papel de las proteínas laforina y malina humanas en la regulación de proteínas con actividad oncogénica, por lo que se describen varias aproximaciones terapéuticas basadas en su uso para la elaboración de composiciones farmacéuticas
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P200702757.
Solicitante: CONSEJO SUPERIOR DE INVESTIGACIONES CIENTIFICAS
HOSPITAL VALL D'HEBRON.
Nacionalidad solicitante: España.
Provincia: MADRID.
Inventor/es: RAMON Y CAJAL AGUERAS,SANTIAGO, RODRIGUEZ DE CORDOBA,SANTIAGO.
Fecha de Solicitud: 19 de Octubre de 2007.
Fecha de Publicación: .
Fecha de Concesión: 16 de Junio de 2010.
Clasificación Internacional de Patentes:
- A61K38/17A2
- A61K48/00 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › Preparaciones medicinales que contienen material genético que se introduce en las células del cuerpo vivo para tratar enfermedades genéticas; Terapia génica.
- C07H21/04 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07H AZUCARES; SUS DERIVADOS; NUCLEOSIDOS; NUCLEOTIDOS; ACIDOS NUCLEICOS (derivados de ácidos aldónicos o sacáricos C07C, C07D; ácidos aldónicos, ácidos sacáricos C07C 59/105, C07C 59/285; cianohidrinas C07C 255/16; glicales C07D; compuestos de constitución indeterminada C07G; polisacáridos, sus derivados C08B; ADN o ARN concerniente a la ingeniería genética, vectores, p. ej. plásmidos o su aislamiento, preparación o purificación C12N 15/00; industria del azúcar C13). › C07H 21/00 Compuestos que contienen al menos dos unidades mononucleótido que tienen cada una grupos fosfato o polifosfato distintos unidos a los radicales sacárido de los grupos nucleósido, p. ej. ácidos nucleicos. › con desoxirribosilo como radical sacárido.
- C12Q1/68B
Clasificación PCT:
- A61K38/17 A61K […] › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › que provienen de animales; que provienen de humanos.
- A61K48/00 A61K […] › Preparaciones medicinales que contienen material genético que se introduce en las células del cuerpo vivo para tratar enfermedades genéticas; Terapia génica.
- C07H21/04 C07H 21/00 […] › con desoxirribosilo como radical sacárido.
- C12Q1/68 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12Q PROCESOS DE MEDIDA, INVESTIGACION O ANALISIS EN LOS QUE INTERVIENEN ENZIMAS, ÁCIDOS NUCLEICOS O MICROORGANISMOS (ensayos inmunológicos G01N 33/53 ); COMPOSICIONES O PAPELES REACTIVOS PARA ESTE FIN; PROCESOS PARA PREPARAR ESTAS COMPOSICIONES; PROCESOS DE CONTROL SENSIBLES A LAS CONDICIONES DEL MEDIO EN LOS PROCESOS MICROBIOLOGICOS O ENZIMOLOGICOS. › C12Q 1/00 Procesos de medida, investigación o análisis en los que intervienen enzimas, ácidos nucleicos o microorganismos (aparatos de medida, investigación o análisis con medios de medida o detección de las condiciones del medio, p. ej. contadores de colonias, C12M 1/34 ); Composiciones para este fin; Procesos para preparar estas composiciones. › en los que intervienen ácidos nucleicos.
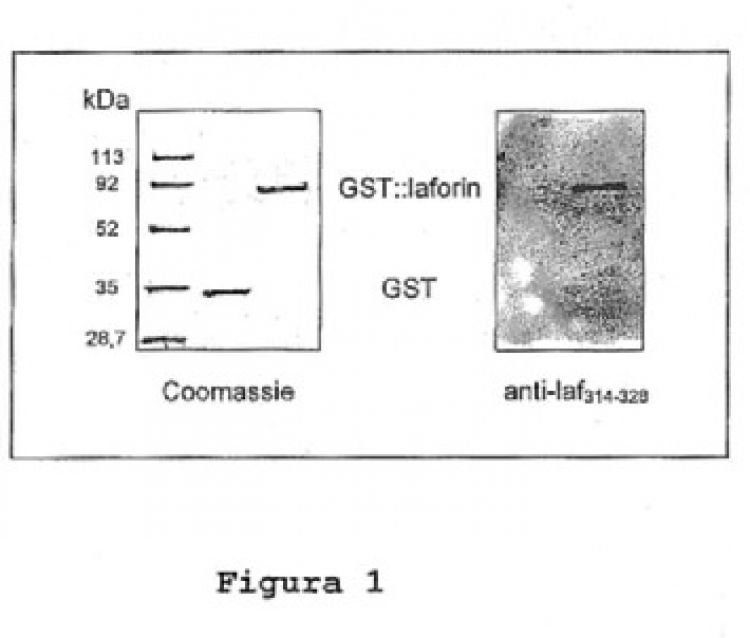
Fragmento de la descripción:
Procedimiento de diagnóstico y tratamiento del cáncer basado en la laforina, elementos biológicos para llevarlos a cabo y sus aplicaciones
Sector de la técnica
La presente invención se circunscribe al sector de la biomedicina y, concretamente, al sector del diagnóstico y tratamiento de pacientes con cáncer, y más concretamente, al diagnóstico mediante herramientas biotecnológicas.
Estado de la técnica
La proteína laforina está codificada por el gen EPM2A situado en el cromosoma 6q24 y fue identificada a finales de los 90 en dos estudios independientes como una proteína cuya ausencia causaba la epilepsia mioclónica progresiva (PME) del tipo Lafora (LD, MIM 254780) (1, 2, 3, 4). LD es una enfermedad grave caracterizada por un deterioro progresivo neurológico, mioclonía y epilepsia que se inicia durante la adolescencia (normalmente entre los 10 y 17 años de edad) y lleva al paciente a un estado vegetativo terminal en los 10 años siguientes al comienzo de la enfermedad (5). LD se caracteriza por la presencia de depósitos intracelulares de poliglucosanos en todos los tejidos, pero fundamentalmente en el sistema nervioso central y en el corazón (6, 7, 8, 9, 10, 11). La acumulación intracelular de poliglucosanos llevó a considerar la enfermedad como una alteración en los procesos de almacenaje celular. Datos recientes indican que LD es consecuencia de defectos en la regulación de proteínas implicadas en el metabolismo del glucógeno que llevan a una acumulación anormal de poliglucosanos en las neuronas alterando la fisiología celular y desencadenando procesos de muerte celular programada (apoptosis) (12).
Se han identificado dos genes asociados a esta enfermedad. Así, además de EPM2A, que codifica para la laforina y que se encuentra mutado en un 50-60% de los casos de LD, se ha identificado un segundo gen en el cromosoma 6p22.3 denominado EPM2B que codifica para la proteína malina (13) y que está mutado en el 30-40% de los enfermos con LD. La eliminación del gen EPM2A en ratones produce un fenotipo similar al que se observa en los pacientes de LD, incluyendo la presencia de cuerpos de Lafora, neurodegeneración y trastornos neurológicos graves (14). Se ha descrito una forma de LD en perros que está causada por mutaciones en EPM2B (15).
La laforina es una proteína de 331 aminoácidos con actividad fosfatasa de especificidad dual, que presenta un dominio funcional de unión a carbohidratos en el extremo amino-terminal (16, 17) e interacciona con varias proteínas, alguna de ellas implicada en el metabolismo del glucógeno como PTG (18), que es una de las subunidades reguladoras de la proteína fosfatasa 1 (PP1). La malina es una E3-ubicuitin ligasa de 395 aminoácidos que posee un dominio RING finger y seis dominios NHL (13, 19, 20).
Malina interacciona con laforina (19, 20) lo que indica que ambas proteínas actúan a través de una vía común y explica por qué los pacientes con mutaciones en laforina o malina son neurológica e histológicamente indistinguibles (21, 22).
Inicialmente, se sugirió que la interacción entre malina y laforina regulaba negativamente laforina mediante degradación vía proteosoma (20). Similarmente, se ha sugerido que laforina es una fosfatasa de GSK3 y que es a través de la activación de GSK3 (defosforilación) como laforina inactiva a la glucógeno sintasa y la síntesis de glucógeno (19). Sin embargo, otros resultados han cuestionado el papel de laforina en la regulación de GSK3 (23, 24). En este sentido, se ha demostrado que laforina y malina regulan la actividad de la glucógeno sintasa y de otras proteínas importantes en la síntesis del glucógeno, como PTG, mediante un mecanismo novedoso que implica la degradación vía proteosoma de estas proteínas (12). Este mecanismo es particularmente importante en el caso de las neuronas porque estas células disponen de la maquinaria enzimática para sintetizar glucógeno pero no pueden degradarlo ya que no expresan la glucógeno fosfatasa (12). Laforina y malina se encargan de silenciar la síntesis de glucógeno en neuronas, evitando la acumulación de poliglucosanos y la activación de mecanismos apoptóticos en las neuronas (12).
Recientemente, se ha descrito que el gen Epm2a es un gen que actuaría como supresor de tumores en una cepa de ratones inmunocomprometidos (línea TG-B de transgénicos para el receptor de células T) y se ha proporcionado evidencia experimental, utilizando líneas celulares de linfomas B y T humanas y murinas, de que el silenciamiento de Laforina juega un papel en el aumento de señalización a través de la vía de Wnt lo que es esencial para el desarrollo de tumores en un huésped inmunocomprometido (25). Además, la función de laforina como gen supresor de tumores se ha relacionado con la actividad de laforina de actuar como fosfatasa de GSK-3P (25). La relevancia de estos estudios en linfomas T humanos se ha extrapolado del estudio de un panel de líneas humanas de linfomas T en los que se analizó la expresión de laforina y la relación que existe entre niveles de expresión de laforina y acumulación de beta- catenina en el núcleo como un indicador de activación de la vía de señalización de Wnt. Así, en la las líneas CCRE-CEM, Jurkat y J45.01 no se detectó mRNA de Epm2a. En contraste, las lineas HH, H9 y MJ tienen mRNA de Epm2a y niveles muy bajos de beta-catenina nuclear. Estudios adicionales muestran una correlación entre la expresión del gen Epm2a y la reducción de beta-catenina, lo que sugiere que la represión epigenética de Emp2a podría jugar un papel en la activación de la vía de señalización de Wnt en linfomas T humanos. Sin embargo, estos resultados contrastan con el hecho de que los pacientes con LD, los portadores de mutaciones en EPM2A en heterocigosis, o los ratones genéticamente modificados que carecen de laforina o en los que se sopreexpresa una forma inactiva de laforina (14, 26), no muestran una mayor predisposición a tumores. Por todo ello, aunque los datos generados en el modelo de ratón y en las líneas de linfomas son sugerentes, está todavía por establecer si el silenciamiento de Laforina se asocia a la aparición de tumores en humanos y si es así, si el papel de laforina como supresor de tumores es extensible a otros cánceres ademas de los linfomas de células T o B o a individuos que no esten inmunocomprometidos.
Descripción de la invención
Un objeto de la invención lo constituye un procedimiento de diagnóstico y pronóstico de una muestra biológica tumoral, en adelante procedimiento de diagnóstico de la invención, basado en la determinación de los niveles de la presencia de laforina y que comprende las siguientes etapas:
a) identificación de los niveles de expresión de laforina,
b) comparación de los niveles de laforina observados en a) con una muestra biológica control, e
c) identificación de una muestra como tumoral cuando los niveles de laforina disminuyen con respecto a los obtenidos en la muestra control.
Un objeto particular de la invención lo constituye el procedimiento de identificación de un paciente con cáncer en el que la identificación de laforina se realiza conjuntamente con la identificación de malina en la misma muestra biológica. En este caso el término malina se refiere tanto al gen como a la proteína malina.
Otro objeto particular de la invención lo constituye el procedimiento de identificación de un paciente con cáncer en el que la identificación de laforina de se refiere a la forma proteica de la laforina humana (SEQ ID NO 2) y se lleva a cabo mediante el uso de un anticuerpo específico de la proteína laforina en técnicas inmunológicas. Los anticuerpos pueden ser monoclonales o policlonales, fragmentos o derivados de los mismos.
Así, otro objeto de la invención lo constituye el hibridoma LAF-A7 (depositado en la colección de cultivos ECACC -European Collection of Animal Cell Culture- el 18 de octubre de 2007 con la referencia Q7394) y el anticuerpo monoclonal LAF-A7, producido por dicho hibridoma, y desarrollados en la presente invención.
Otro objeto particular de la invención lo constituye el procedimiento de identificación de un paciente humano con cáncer en el que la identificación de laforina se lleva a cabo mediante la amplificación génica de un precursor génico de laforina perteneciente, a titulo ilustrativo y sin que limite el alcance de la invención, al siguiente grupo: PCR cuantitativa o en una PCR semi-cuantitativa con unos cebadores específicos de laforina humana.
Otra realización particular de la invención...
Reivindicaciones:
1. Procedimiento de diagnóstico y pronóstico de una muestra biológica tumoral caracterizado porque se basa en la determinación de los niveles de la presencia de laforina y que comprende las siguientes etapas:
2. Procedimiento de identificación según la reivindicación 1 caracterizado porque la identificación de laforina se realiza conjuntamente con la identificación de malina en la misma muestra biológica.
3. Procedimiento de identificación según las reivindicaciones 1 y 2 caracterizado porque la identificación de la laforina se refiere a la forma proteica de la laforina humana, preferentemente de SEQ ID NO 2 y se lleva a cabo mediante el uso de un anticuerpo específico de la proteína laforina en técnicas inmunológicas.
4. Procedimiento de identificación según la reivindicación 3 caracterizado porque el anticuerpo puede ser monoclonal o policlonal, fragmentos o derivados de los mismos.
5. Procedimiento de identificación según la reivindicación 3 caracterizado porque la técnica inmunológica pertenece al siguiente grupo: inmunohistoquímica y western blot o inmunoblot.
6. Procedimiento de identificación según las reivindicaciones 1 a la 5 caracterizado porque el anticuerpo utilizado es el anticuerpo monoclonal LAF-A7 producido por el hibridoma LAF-A7 depositado en ECACC Q7394.
7. Hibridoma LAF-A7 caracterizado porque produce el anticuerpo LAF-A7 y porque se encuentra depositado en la colección de cultivos ECACC - European Collection of Animal Cell Culture- el 18 de octubre de 2007 con la referencia Q7394.
8. Anticuerpo monoclonal LAF-A7 caracterizado porque es producido por el hibridoma según la reivindicación 7.
9. Uso de cualquier otro anticuerpo, monoclonal o policlonal, específico de la laforina para el diagnóstico del cáncer o para la elaboración de composiciones farmacéuticas de diagnóstico contra el cáncer.
10. Procedimiento de identificación según las reivindicaciones 1 y 2 caracterizado porque la identificación de la laforina se lleva a cabo mediante la amplificación génica de un precursor génico de la laforina, perteneciente al siguiente grupo: PCR cuantitativa o en una PCR semi-cuantitativa con unos cebadores específicos de laforina humana.
11. Procedimiento de identificación según las reivindicaciones 1 y 2 caracterizado porque la identificación de la laforina se lleva a cabo mediante la técnica de Northern blot con sondas de polinucleótidos específicas de laforina.
12. Procedimiento de identificación según las reivindicaciones 1 y 2 caracterizado porque la identificación de la laforina se lleva a cabo mediante hibridación in situ con un precursor de laforina.
13. Procedimiento de identificación según las reivindicaciones 1 a la 6 y 10 a la 12 caracterizado porque el tipo de cáncer que se diagnostica pertenece al siguiente grupo: colon, mama y riñón.
14. Uso de un compuesto o agente activador, inductor o agonista de la actividad antitumoral de la laforina/malina, en la elaboración de un medicamento o composición farmacéutica para la profilaxis y tratamiento de tumores en mamíferos, preferentemente seres humanos, y más preferentemente para el cáncer de colon, mama y riñón, caracterizado porque el compuesto está constituido por una proteína o péptido laforina/malina con actividad antitumoral en el interior de las células de un mamífero, preferentemente humanas, y que comprende una o varias proteínas o péptidos laforina/malina pertenecientes al siguiente grupo:
15. Uso de un compuesto según la reivindicación 14 caracterizado porque la secuencia de a) es la secuencia de aá. de la laforina humana (SEQ ID NO 2).
16. Uso de un compuesto según la reivindicación 14 caracterizado porque la secuencia de a) comprende la secuencia de aá. de la laforina y la malina humanas (SEQ ID NO 2 y SEQ ID NO 5).
17. Uso de un compuesto o agente activador, inductor o agonista de la actividad antitumoral de la laforina/malina, en la elaboración de un medicamento o composición farmacéutica para la profilaxis y tratamiento de tumores en mamíferos, preferentemente seres humanos, y más preferentemente para el cáncer de colon, mama y riñón, caracterizado porque comprende el compuesto que está constituido por una construcción genética que comprende una o varias secuencias de nucleótidos laforina o malina pertenecientes al siguiente grupo:
18. Uso de un compuesto según la reivindicación 17 caracterizado porque la secuencia de nucleótidos de a) es la secuencia de nucleótidos codificantes de la laforina humana (SEQ ID NO 1).
19. Uso de un compuesto según la reivindicación 17 caracterizado porque la secuencia de nucleótidos de a) comprende la secuencia de nucleótidos codificante de la laforina y la malina humanas (SEQ ID NO 1 y SEQ ID NO 4).
20. Uso de un compuesto según la reivindicación 17 caracterizado porque el compuesto está constituido por el vector de expresión génica que comprende una secuencia de nucleótidos laforina/malina (SEQ ID NO 1 ó 4, o ambas) o una construcción génica laforina/malina que las comprenda (SEQ ID NO 1 ó 4, o ambas) y que permite la expresión de una proteína o péptido con actividad antitumoral.
21. Composición farmacéutica útil para el tratamiento del cáncer caracterizada porque se ha obtenido según las reivindicaciones 14 a la 20.
Patentes similares o relacionadas:
Composiciones útiles en el tratamiento de la deficiencia de ornitina transcarbamilasa (OTC), del 8 de Julio de 2020, de THE TRUSTEES OF THE UNIVERSITY OF PENNSYLVANIA: Un vector vírico recombinante que comprende una secuencia de ácido nucleico que codifica la proteína ornitina transcarbamilasa humana (hOTC) y secuencias […]
Terapia génica para la diabetes, del 8 de Julio de 2020, de UCL Business Ltd: Una molécula de ácido nucleico que comprende una secuencia de nucleótidos que codifica una proteína preproinsulina funcional en donde la secuencia de nucleótidos tiene al menos […]
Vacuna de ADN que contiene un epítopo específico de VEGF y/o un epítopo específico de angiopoyetina-2, del 1 de Julio de 2020, de OSAKA UNIVERSITY: Un vector de expresión que codifica un polipéptido del antígeno del núcleo del virus de la hepatitis B quimérico con una inserción para uso en el tratamiento o la profilaxis […]
Composiciones para modular la expresión de SOD-1, del 24 de Junio de 2020, de Biogen MA Inc: Un compuesto antisentido según la siguiente fórmula: mCes Aeo Ges Geo Aes Tds Ads mCds Ads Tds Tds Tds mCds Tds Ads mCeo Aes Geo mCes Te (secuencia […]
Ácido nucleico antisentido, del 24 de Junio de 2020, de NIPPON SHINYAKU CO., LTD.: Un oligómero antisentido de 14 a 32 bases de longitud, que comprende dos unidades de oligómeros conectadas seleccionadas del grupo que consiste […]
Plekhg5 como diana farmacéutica para trastornos neurológicos, del 15 de Junio de 2020, de CONSEJO SUPERIOR DE INVESTIGACIONES CIENTIFICAS (CSIC): Plekhg5 como diana farmacéutica para trastornos neurológicos. La invención hace referencia al uso del gen Plekhg5 como diana farmacológica para el cribado, […]
Vectores de AAV dirigidos a oligodendrocitos, del 10 de Junio de 2020, de THE UNIVERSITY OF NORTH CAROLINA AT CHAPEL HILL: Un ácido nucleico que codifica una cápside de AAV, comprendiendo el ácido nucleico una secuencia codificante de la cápside de AAV que es al menos el 96 % idéntica […]
Método para activar células T auxiliares, del 10 de Junio de 2020, de OTSUKA PHARMACEUTICAL CO., LTD.: Una composición para su uso en el tratamiento o prevención del cáncer mediante la activación de células T auxiliares en un sujeto, en donde dicha composición […]