DERIVADOS DE N-2-ADAMANTIL-2-FENOXI-ACETAMIDA COMO INHIBIDORES DE 11-BETAHIDROXIESTEROIDE-DESHIDROGENASA.
Un compuesto para uso como medicamento que tiene la fórmula
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2005/054197.
Solicitante: JANSSEN PHARMACEUTICA NV.
Nacionalidad solicitante: Bélgica.
Dirección: TURNHOUTSEWEG 30,2340 BEERSE.
Inventor/es: JAROSKOVA,LIBUSE,JANSSEN PHARMACEUTICA N.V, LINDERS,JOANNES T.M.,JANSSEN PHARMACEUTICA N.V, VAN DER VEKEN,L. J.E.,JANSSEN PHARMACEUTICA N.V, WILLEMSENS,G. H. M.,JANSSEN PHARMACEUTICA N.V, BISCHOFF,FRANCOIS P.,JANSSEN PHARMACEUTICA N.V.
Fecha de Publicación: .
Fecha Concesión Europea: 23 de Diciembre de 2009.
Clasificación PCT:
- A61K31/165 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › teniendo ciclos aromáticos, p. ej. colchicina, atenolol, progabide.
- A61P19/10 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 19/00 Medicamentos para el tratamiento de problemas del esqueleto. › para la osteoporosis.
- A61P25/28 A61P […] › A61P 25/00 Medicamentos para el tratamiento de trastornos del sistema nervioso. › de los problemas neurodegenerativos del sistema nervioso central, p. ej. noótropos, activadores del conocimiento, medicamentos para el tratamiento del Alzheimer o de otras formas de demencia.
- A61P27/06 A61P […] › A61P 27/00 Medicamentos para tratar los trastornos de los sentidos. › Agentes antiglaucoma o mióticos.
- A61P3/04 A61P […] › A61P 3/00 Medicamentos para el tratamiento de trastornos del metabolismo (de la sangre o de fluido extracelular A61P 7/00). › Anorexiantes; Medicamentos para el tratamiento de la obesidad.
- A61P3/10 A61P 3/00 […] › para la hiperglucemia, p.ej. antidiabéticos.
- A61P9/00 A61P […] › Medicamentos para el tratamiento de trastornos en el aparato cardiovascular.
- C07C235/22 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07C COMPUESTOS ACICLICOS O CARBOCICLICOS (compuestos macromoleculares C08; producción de compuestos orgánicos por electrolisiso electroforesis C25B 3/00, C25B 7/00). › C07C 235/00 Amidas de ácidos carboxílicos, estando sustituida la estructura carbonada de la parte ácida por átomos de oxígeno. › con el átomo de nitrógeno de al menos uno de los grupos carboxamido unido a un átomo de carbono de un ciclo distinto de un ciclo aromático de seis miembros.
- C07D307/85 C07 […] › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 307/00 Compuestos heterocíclicos que contienen ciclos de cinco miembros que tienen un átomo de oxígeno como único heteroátomo del ciclo. › unidos en la posición 2.
- C07D311/66 C07D […] › C07D 311/00 Compuestos heterocíclicos que contienen ciclos de seis miembros que contienen un átomo de oxígeno como único heteroátomo, condensados con otros ciclos. › con átomos de carbono que tienen tres enlaces a heteroátomos con a lo más un enlace a halógeno, p. ej. radicales éster o nitrilo, unidos directamente en la posición 2.
- C07D319/20 C07D […] › C07D 319/00 Compuestos heterocíclicos que contienen ciclos de seis miembros que tienen dos átomos de oxígeno como únicos heteroátomos del ciclo. › con sustituyentes unidos al heterociclo.
Fragmento de la descripción:
Derivados de N-2-adamantil-2-fenoxi-acetamida como inhibidores de 11ß-hidroxiesteroide-deshidrogenasa.
El síndrome metabólico es una enfermedad con prevalencia creciente no sólo en el mundo occidental sino también en Asia y países en desarrollo. Se caracteriza por obesidad, en particular obesidad central o visceral, diabetes tipo 2, hiperlipidemia, hipertensión, arterioesclerosis, enfermedades cardiacas coronarias y insuficiencia renal finalmente crónica (C.T. Montague et al. (2000), Diabetes, 49, 883-888).
Se sabe que los glucocorticoides y 11ß-HSD1 son factores importantes en la diferenciación de las células adiposas estromales en adipocitos maduros. En las células viscerales estromales de los pacientes obesos, el nivel de mRNA de 11ß-HSD1 está incrementado comparado con el tejido subcutáneo. Adicionalmente, la sobre-expresión en el tejido adiposo de 11ß-HSD1 en ratones transgénicos está asociada con niveles incrementados de corticosterona en el tejido adiposo, obesidad visceral, sensibilidad a la insulina, diabetes tipo 2, hiperlipidemia e hiperfagia (H. Masuzaki et al. (2001), Science, 294, 2166-2170). Por consiguiente, la 11ß-HSD1 está implicada muy probablemente en el desarrollo de obesidad visceral y el síndrome metabólico.
La inhibición de 11ß-HSD1 da como resultado una disminución en la diferenciación y un aumento en la proliferación de células adiposas estromales. Además, la deficiencia de glucocorticoides (adrenalectomía) mejora la capacidad de insulina y leptina para promover anorexia y pérdida de peso, y este efecto es invertido por la administración de glucocorticoides (P.M. Stewart et al (2002), Trends Endocrin. Metabol. 13, 94-96). Estos datos sugieren que la reactivación mejorada de cortisona por 11ß-HSD1 puede exacerbar la obesidad y puede ser beneficioso inhibir esta enzima en el tejido adiposo de los pacientes obesos.
La obesidad está ligada también a riesgos cardiovasculares. Existe una relación significativa entre la tasa de excreción de cortisol y HDL colesterol tanto en hombres como en mujeres, lo que sugiere que los glucocorticoides regulan componentes clave del riesgo cardiovascular. Análogamente, la rigidez aórtica está asociada también con adiposidad visceral en los adultos de edad avanzada.
El impacto del efecto de la actividad reducida de 11ß-HSD1 se pone de relieve por el ratón desactivado en 11ß-HSD1 que tiene niveles incrementados en plasma de glucocorticoide endógeno activo, pero a pesar de esto sigue estando protegido contra la resistencia a la insulina inducida por el estrés y la obesidad. Adicionalmente, estos ratones silenciados presentan un perfil de lípidos plasmídicos anti-aterogénicos y beneficios del deterioro cognitivo reducido relacionado con la edad.
Glucocorticoides y glaucoma
Los glucocorticoides aumentan el riesgo de glaucoma por elevar la presión intraocular cuando se administran exógenamente y en ciertas condiciones de producción incrementada como en el síndrome de Cushing. El aumento de la presión intraocular inducido por los glucocorticosteroides está causado por una resistencia incrementada al flujo acuoso de salida debido a los cambios de glucocorticoides inducidos en la red trabecular y su matriz intracelular. Zhou et al. (Int J Mol Med (1998) 1, 339-346) han comunicado también que los corticosteroides aumentan las cantidades de fibronectina así como de colágeno tipo I y tipo IV en la red trabecular de los segmentos anteriores de bovino en cultivos de órganos.
11ß-HSD1 se expresa en las células basales del epitelio corneal y las células epiteliales no pigmentadas. El mRNA receptor de glucocorticoides fue detectado únicamente en la red trabecular, mientras que en las células epiteliales no pigmentadas estaba presente mRNA para el receptor glucocorticoide, mineralocorticoide y 11ß-HSD1. La administración de carbenoxolona a pacientes dio como resultado una disminución importante en la presión intraocular (S. Rauz et al. (2001), Invest. Ophtalmol. Vis. Science, 42, 2037-2042), lo que sugiere un papel para los inhibidores de HSD1 en el tratamiento del glaucoma.
De acuerdo con ello, el problema subyacente a resolver por la presente invención fue identificar inhibidores potentes de 11ß-HSD, con una selectividad alta para 11ß-HSD1, y el uso de los mismos en el tratamiento de patologías asociadas con la formación excesiva de cortisol, es decir trastornos en los cuales es deseable un nivel reducido de glucocorticoide activo, tales como el síndrome metabólico, diabetes tipo 2, tolerancia empeorada a la glucosa (IGT), glucosa empeorada en ayunas (IFG), dislipidemia, hipertensión, obesidad, diabetes, enfermedades cardiovasculares relacionadas con obesidad, arterioesclerosis, ateroesclerosis, miopatía, osteoporosis, trastornos neurodegenerativos y psiquiátricos, trastornos relacionados con el estrés y glaucoma. Como se muestra más adelante en esta memoria, se encontró que las 2-adamantanilacetamidas de fórmula (I) son útiles como medicamento, en particular en la fabricación de un medicamento para el tratamiento de patologías asociadas con el exceso de formación de cortisol.
Salim S.S. et al. (J. Chem. Eng. Data (1984), 29, 229-231) proporciona la síntesis de algunos N-(3-metil-2-quinoxaloil)-amino-alcoholes nuevos y describe en particular 2-quinoxalincarboxamida, 3-metil-N-triciclo[3.3.1.13,7]dec-2-ilo. Se demostró que los 1,4-dióxidos de dichas quinoxalinas tienen actividad antibacteriana, en donde las quinoxalinas originarias eran inactivas como agentes antibacterianos.
Masamune H. et al (Solicitud de Patente Internacional PCT WO 01/23399 describe N-2-adamantil-2-fenoxi-acetamidas como compuestos intermedios en la preparación de nucleósidos como receptores de adenosina, antidiabéticos, inhibidores de enzimas y para el tratamiento de la isquemia. Véanse en particular el esquema IV, p. 41 y los Ejemplos 70, 73, B32 y B35.
Sin embargo, en ninguno de los documentos arriba citados se ha descrito la aplicación terapéutica de los derivados de N-2-adamantil-acetamida de la presente invención.
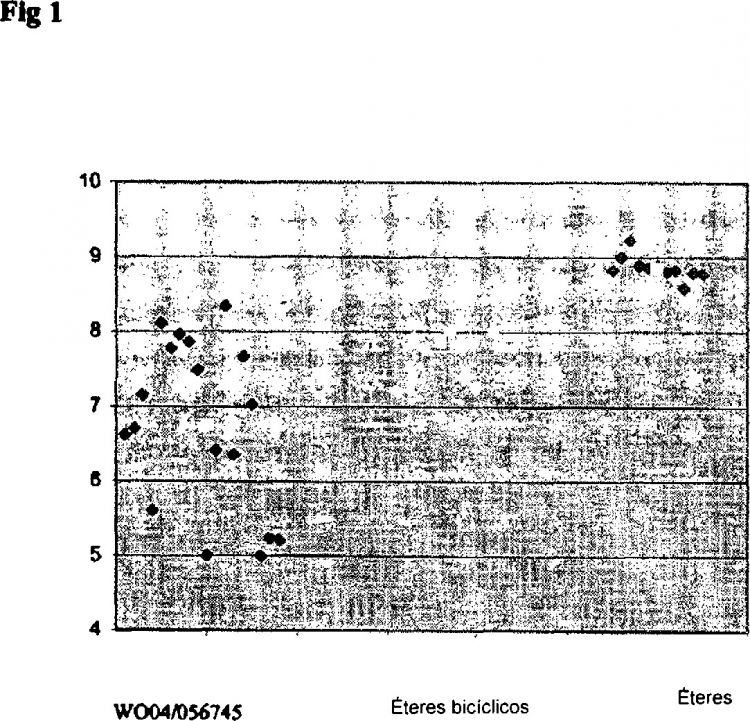
El uso de adamantil-acetamidas como inhibidores de la 11ß-hidroxiesteroide-deshidrogenasa se describió en Linders J. et al (Solicitud de Patente Internacional PCT WO 2004/056745). Comparados con los compuestos descritos en dicha publicación, los compuestos de la presente invención difieren en que comprenden un heteroátomo adicional, representado como -Z- en la fórmula (I) siguiente. La presencia de este heteroátomo adicional, junto con la configuración particular de la cadena principal (representada en negrilla más adelante), mejoraba significativamente la actividad global de las adamantil-acetamidas como inhibidores de la 11ß-hidroxiesteroide-deshidrogenasa (Figura 1).
La Figura 1 proporciona una comparación de la actividad de las células 3T3-L1 (valores pCI50 - véase el Ejemplo C más adelante en esta memoria) de las adamantil-acetamidas bicíclicas descritas en la Solicitud de Patente Internacional PCT WO 2004/056745 con los éteres bicíclicos de la presente solicitud y los éteres simples de la presente solicitud.
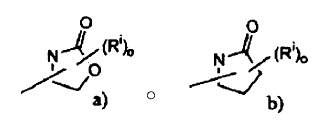
El uso farmacéutico de amidas sustituidas para modular la actividad de 11ß-HSD1, sea solas o en combinación con un agonista receptor de glucocorticoides o un agente antihipertensivo ha sido descrito en las Solicitudes de Patente Internacional PCT WO 2004/089470, WO 2004/089415 y WO 2004/089416. En dichas publicaciones de patente, solamente un compuesto, a saber N-adamantan-2-il-2-o-toliloxi-acetamida, dentro del alcance de la presente solicitud ha sido descrito y está, de acuerdo con ello, excluido de la principal y las ulteriores reivindicaciones de uso médico en la presente solicitud. Compuestos adicionales dentro del alcance de la presente solicitud, pero no descritos previamente para uso como medicamentos son:
Reivindicaciones:
1. Un compuesto para uso como medicamento que tiene la fórmula
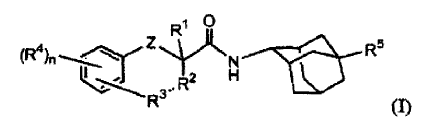
las formas de N-óxido, las sales de adición farmacéuticamente aceptables y las formas estereoquímicamente isómeras de aquéllos, en donde
R11 y R12 representan cada uno independientemente hidrógeno, alquilo C1-4, alquiloxicarbonilo C1-4 o alquilcarbonilo C1-4;
R13 y R14 representan cada uno independientemente hidrógeno, alquilo C1-4, alquil C1-6-SO2-, mono-o di(alquil C1-4)amino-SO2-, Ar1-SO2, mono-o di(alquil C1-4)aminocarbonilo, alquil C1-4-oxicarbonilo o alquilcarbonilo C1-4 en donde dicho alquil C1-6-SO2-, alquil C1-4-oxicarbonilo o alquilcarbonilo C1-4 están sustituidos cada uno independiente y opcionalmente con uno, dos o tres sustituyentes seleccionados de halo, alquiloxicarbonilo C1-4, NR19R20 y Het2;
R15 y R16 representan cada uno independientemente hidrógeno, alquilo C1-4, alquiloxicarbonilo C1-4 o alquilcarbonilo C1-4;
R17 y R18 representan cada uno independientemente hidrógeno, alquilo C1-4, alquiloxicarbonilo C1-4 o alquilcarbonilo C1-4;
R19 y R20 representan cada uno independientemente hidrógeno, alquilcarbonilo C1-4, alquiloxicarbonilo C1-4 o alquilo C1-4 sustituido opcionalmente con uno o más sustituyentes seleccionados de halo o hidroxi;
R21 y R22 representan cada uno independientemente hidrógeno, Ar2 o alquilo C1-4 sustituido opcionalmente con uno o más sustituyentes seleccionados de halo o hidroxi;
R23 y R24 representan cada uno independientemente hidrógeno, alquilcarbonilo C1-4, Het4 o alquilo C1-4 sustituido opcionalmente con uno o más sustituyentes seleccionados de halo o hidroxi;
2. Un compuesto para uso como medicamento de acuerdo con la reivindicación 1, en donde
R11 y R12 representan cada uno independientemente hidrógeno, alquilo C1-4 o alquilcarbonilo C1-4;
R13 y R14 representan cada uno independientemente hidrógeno, alquilo C1-4 o alquilcarbonilo C1-4;
R15 y R16 representan cada uno independientemente hidrógeno, alquilo C1-4, o alquilcarbonilo C1-4; y
R17 y R18 representan cada uno independientemente hidrógeno, alquilo C1-4 o alquilcarbonilo C1-4, con la condición, sin embargo, de que dicho compuesto es distinto de N-adamantan-2-il-2-o-toliloxi-acetamida.
3. Un compuesto de fórmula (I), las formas de N-óxido, las sales de adición farmacéuticamente aceptables y las formas estereoquímicamente isómeras del mismo, en donde
R11 y R12 representan cada uno independientemente hidrógeno, alquilo C1-4, o alquilcarbonilo C1-4;
R13 y R14 representan cada uno independientemente hidrógeno, alquilo C1-4, alquil C1-6-SO2, mono-o di(alquil C1-4)amino-SO2-, Ar1-SO2, mono-o di(alquil C1-4)amino-carbonil-, alquil C1-4-oxicarbonilo o alquilcarbonilo C1-4 en donde dicho alquil C1-6-SO2, alquil C1-4-oxicarbonilo o alquilcarbonilo C1-4 están cada uno independiente y opcionalmente sustituidos con uno, dos, o tres sustituyentes seleccionados de halo, alquiloxicarbonilo C1-4, NR19R20 y Het2;
R15 y R16 representan cada uno independientemente hidrógeno, alquilo C1-4, alquiloxicarbonilo C1-4 o alquilcarbonilo C1-4;
R17 y R18 representan cada uno independientemente hidrógeno, alquilo C1-4, alquiloxicarbonilo C1-4 o alquilcarbonilo C1-4;
R19 y R20 representan cada uno independientemente hidrógeno, alquilcarbonilo C1-4 o alquilo C1-4 sustituido opcionalmente con uno o más sustituyentes seleccionados de halo o hidroxi;
R21 y R22 representan cada uno independientemente hidrógeno, Ar2 o alquilo C1-4 sustituido opcionalmente con uno o más sustituyentes seleccionados de halo o hidroxi;
R23 y R24 representan cada uno independientemente hidrógeno, alquilcarbonilo C1-4, Het4 o alquilo C1-4 sustituido opcionalmente con hidroxi;
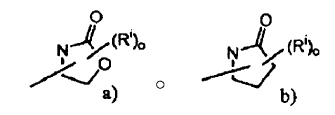
4. Un compuesto de acuerdo con la reivindicación 3, en donde
R11 y R12 representan cada uno independientemente hidrógeno, alquilo C1-4 o alquilcarbonilo C1-4;
R13 y R14 representan cada uno independientemente hidrógeno, alquilo C1-4 o alquilcarbonilo C1-4;
R15 y R16 representan cada uno independientemente hidrógeno, alquilo C1-4 o alquilcarbonilo C1-4; y
R17 y R18 representan cada uno independientemente hidrógeno, alquilo C1-4 o alquilcarbonilo C1-4.
5. Un compuesto de fórmula (Ii),
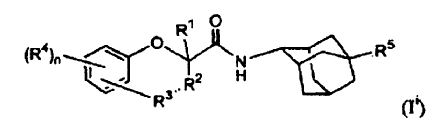
las formas de N-óxido, las sales de adición farmacéuticamente aceptables y las formas estereoquímicamente isómeras de los mismos, en donde
R11 y R12 representan cada uno independientemente hidrógeno, alquilo C1-4, alquiloxicarbonilo C1-4 o alquilcarbonilo C1-4;
R13 y R14 representan cada uno independientemente hidrógeno, alquilo C1-4, alquil C1-6-SO2-, mono- o di(alquil C1-4)amino-SO2-, Ar1-SO2, mono- o di(alquil C1-4)aminocarbonilo, alquil C1-4-oxicarbonilo o alquiloxicarbonilo C1-4 en donde dicho alquil C1-6-SO2, alquiloxicarbonilo C1-4 o alquilcarbonilo C1-4 están sustituidos cada uno independiente y opcionalmente con uno, dos o tres sustituyentes seleccionados de halo, alquiloxicarbonilo C1-4, NR19R20 y Het2;
R15 y R16 representan cada uno independientemente hidrógeno, alquilo C1-4, alquiloxicarbonilo C1-4 o alquilcarbonilo C1-4; en particular hidrógeno, alquilo C1-4 o alquilcarbonilo C1-4;
R17 y R18 representan cada uno independientemente hidrógeno, alquilo C1-4, alquiloxicarbonilo C1-4 o alquilcarbonilo C1-4; en particular hidrógeno, alquilo C1-4 o alquilcarbonilo C1-4;
R19 y R20 representan cada uno independientemente hidrógeno, alquiloxicarbonilo C1-4, alquilcarbonilo C1-4 o alquilo C1-4 sustituido opcionalmente con uno o más sustituyentes seleccionados de halo o hidroxi;
R21 y R22 representan cada uno independientemente hidrógeno, Ar2 o alquilo C1-4 sustituido opcionalmente con halo o hidroxi;
R23 y R24 representan cada uno independientemente hidrógeno, alquilcarbonilo C1-4, Het4 o alquilo C1-4 sustituido opcionalmente con halo o hidroxi;
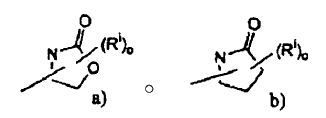
6. Un compuesto de acuerdo con la reivindicación 5, en donde
R11 y R12 representan cada uno independientemente hidrógeno, alquilo C1-4 o alquilcarbonilo C1-4;
R13 y R14 representan cada uno independientemente hidrógeno, alquilo C1-4 o alquilcarbonilo C1-4;
R15 y R16 representan cada uno independientemente hidrógeno, alquilo C1-4 o alquilcarbonilo C1-4; y
R17 y R18 representan cada uno independientemente hidrógeno, alquilo C1-4 o alquilcarbonilo C1-4; con la condición, sin embargo, de que cuando R5 representa hidrógeno en dicho compuesto de fórmula (Ii), entonces R1 y R2 representan alquilo C1-4.
7. Un compuesto para uso como medicamento de acuerdo con la reivindicación 1, en donde;
R11 y R12 representan cada uno independientemente hidrógeno, alquilo C1-4 o alquilcarbonilo C1-4;
R13 y R14 representan cada uno independientemente hidrógeno, alquilo C1-4, alquil C1-6-SO2-, mono-o di(alquil C1-4)amino-SO2-, Ar1-SO2, mono-o di(alquil C1-4)aminocarbonilo, alquil C1-4-oxicarbonilo o alquilcarbonilo C1-4 en donde dicho alquil C1-6-SO2-, alquil C1-4-oxicarbonilo o alquilcarbonilo C1-4 están sustituidos cada uno independiente y opcionalmente con uno, dos o tres sustituyentes seleccionados de halo, alquiloxicarbonilo C1-4, NR19R20 y Het2;
R17 y R18 representan cada uno independientemente alquilo C1-4;
R19 y R20 representan cada uno independientemente hidrógeno o alquilo C1-4 sustituido opcionalmente con hidroxi;
R21 y R22 representan cada uno independientemente hidrógeno o Ar2;
R23 y R24 representan cada uno independientemente hidrógeno o Het4;
Ar1 y Ar2 representan cada uno fenilo sustituido opcionalmente con alquilo C1-4 con la condición, sin embargo, de que dicho compuesto de fórmula (I) es distinto de N-adamantan-2-il-2-o-toliloxi-acetamida.
8. Un compuesto para uso como medicamento de acuerdo con la reivindicación 1, en donde;
R11 y R12 representan cada uno independientemente hidrógeno, alquilo C1-4 o alquilcarbonilo C1-4, con la condición, sin embargo, de que dicho compuesto de fórmula (I) es distinto de N-adamantan-2-il-2-o-toliloxi-acetamida.
9. Un compuesto de acuerdo con la reivindicación 5, en donde:
10. Un compuesto de acuerdo con la reivindicación 9, en donde:
11. Un compuesto de acuerdo con la reivindicación 5, en donde
R11 y R12 representan cada uno independientemente hidrógeno, alquilo C1-4 o alquilcarbonilo C1-4; en particular R11 y R12 representan metilo;
R13 y R14 representan cada uno independientemente hidrógeno, alquilo C1-4, alquil C1-6-SO2-, mono- o di(alquil C1-4)amino-SO2-, Ar1-SO2, mono- o di(alquil C1-4)aminocarbonilo, alquil C1-4-oxicarbonilo o alquiloxicarbonilo C1-4 en donde dicho alquil C1-6-SO2, alquil C1-4-oxicarbonilo o alquilcarbonilo C1-4 están sustituidos cada uno independiente y opcionalmente con uno, dos o tres sustituyentes seleccionados de halo, alquiloxicarbonilo C1-4, NR19R20 y Het2;
R17 y R18 representan cada uno independientemente hidrógeno o alquilo C1-4; en particular R17 y R18 representan metilo;
R19 y R20 representan cada uno independientemente hidrógeno o alquilo C1-4 sustituido opcionalmente con hidroxi; en particular R19 y R20 representan cada uno independientemente hidrógeno, metilo o hidroxietilo;
R21 y R22 representan cada uno independientemente hidrógeno o Ar2; en particular R21 y R22 representan cada uno independientemente hidrógeno o metilfenilo;
R23 y R24 representan cada uno independientemente hidrógeno o Het4; en particular R23 y R24 representan cada uno independientemente hidrógeno o piperidinilo;
12. Un compuesto de acuerdo con la reivindicación 11, en donde
R11 y R12 representan cada uno independientemente hidrógeno, alquilo C1-4 o alquilcarbonilo C1-4.
13. Un compuesto de acuerdo con la reivindicación 5, en donde el compuesto se selecciona del grupo constituido por
2,3-dihidro-N-[(1R,3S)-5-hidroxitriciclo[3.3.1.13,7]dec-2-il]-1,4-benzodioxin-2-carboxamida,
N-[(1R,3S)-5-hidroxitriciclo[3.3.1.13,7]dec-2-il]-2-metil-2-(2-metilfenoxi)-propanamida,
N-[(1R,3S)-5-hidroxitriciclo[3.3.1.13,7]dec-2-il]-2-metil-2-(4-metilfenoxi)-propanamida,
2-(3,5-dimetilfenoxi)-N-[(1R,3S)-5-hidroxitriciclo-[3.3.1.13,7]dec-2-il]-2-metil-propanamida,
3,4-dihidro-N-[(1R,3S)-5-hidroxitriciclo[3.3.1.13,7]dec-2-il]-2H-1-benzopiran-2-carboxamida,
2-(4-cloro-2-metilfenoxi)-N-[(1R,3S)-5-hidroxitriciclo-[3.3.1.13,7]dec-2-il]-2-metil-propanamida,
2-(4-cloro-2-metil-fenoxi)-N-[(1R,3S)-5-metanosulfonil-aminotriciclo[3.3.1.13,7]dec-2-il]-2-metil-propionamida,
2-(4-cloro-2-metil-fenoxi)-N-[(1R,3S)-5-(dimetilamino)-sulfonilaminotriciclo[3.3.1.13,7]dec-2-il]-2-metil-propionamida,
2-(4-cloro-fenoxi)-N-[(1R,3S)-5-hidroxitriciclo-[3.3.1.13,7]dec-2-il]-2-metil-propionamida,
N-[(1R,3S)-5-(dimetilamino)sulfonilaminotriciclo-[3.3.1.13,7]dec-2-il]-2-metil-2-(3-trifluorometilfenoxi)-propio- namida,
N-[(1R,3S)-5-metanosulfonilaminotriciclo[3.3.1.13,7]dec-2-il]-2-metil-2-(3-trifluorometilfenoxi)-propionamida,
N-[(1R,3S)-5-aminotriciclo[3.3.1.13,7]dec-2-il]-2-(2-cloro-fenoxi)-2-metilpropionamida,
N-[(1R,3S)-5-aminotriciclo[3.3.1.13,7]dec-2-il]-2-metil-2-(2-trifluorometilfenoxi)-propionamida,
N-[(1R,3S)-5-etanosulfonilaminotriciclo[3.3.1.13,7]dec-2-il]-2-metil-2-(3-trifluorometilfenoxi)-propionamida,
ácido (3R,5S)-4-[2-(4-cloro-2-metil-fenoxi)-2-metil-propionilamino]triciclo[3.3.1.13,7]decano-l-carboxílico,
N-[(1R,3S)-5-aminotriciclo[3.3.1.13,7]dec-2-il]-2-(4-cloro-2-metil-fenoxi)-2-metil-propionamida,
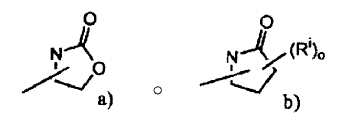
2-(4-cloro-2-metil-fenoxi)-2-metil-N-[(1R,3S)-5-(3-metil-2-oxopirrolidin-1-il)triciclo[3.3.1.13,7]dec-2-il]propio- namida,
2-(3-bromo-fenoxi)-2-metil-N-[(1R,3S)-5-(2-oxo-oxazolidin-3-il)-triciclo[3.3.1.13,7]dec-2-il]-propionamida,
2-(3-bromo-fenoxi)-N-[(1R,3S)-5-metanosulfonilaminotriciclo[3.3.1.13,7]dec-2-il]-2-metil-propionamida, o
2-(4-cloro-fenoxi)-N-[(1R,3S)-5-metanosulfonilaminotriciclo[3.3.1.13,7]dec-2-il]-2-metil-propionamida.
14. Un compuesto, las formas de N-óxido, las sales de adición farmacéuticamente aceptables y las formas estereoquímicamente isómeras del mismo, en el cual el compuesto se selecciona del grupo constituido por:
N-[(1R,3S)-5-hidroxitriciclo[3.3.1.13,7]dec-2-il]-3-metil-2-benzofurancarboxamida,
N-[(1R,3S)-5-hidroxitriciclo[3.3.1.13,7]dec-2-il]-2-benzofurancarboxamida, o
N-[(1R,3S)-5-hidroxitriciclo[3.3.1.13,7]dec-2-il]-7-metoxi-2-benzofurancarboxamida.
15. Una composición farmacéutica que comprende un vehículo o farmacéuticamente aceptable y, como ingrediente activo, una cantidad inhibidora eficaz de 11ß-HSD1 de un compuesto como se describe en una cualquiera de las reivindicaciones 1 a 14.
16. Un proceso de preparación de una composición farmacéutica como se define en la reivindicación 15, caracterizado porque un vehículo farmacéuticamente aceptable se mezcla íntimamente con una cantidad inhibidora eficaz de 11ß-HSD1 de un compuesto como se describe en una cualquiera de las reivindicaciones 1 a 14.
17. Un compuesto de acuerdo con una cualquiera de las reivindicaciones 3, 4, 5, 6, 9, 10, 11, 12, 13 ó 14 para uso como medicamento.
18. Uso de un compuesto de acuerdo con una cualquiera de las reivindicaciones 1 a 14 en la fabricación de un medicamento para el tratamiento de patologías asociadas con exceso de formación de cortisol tales como por ejemplo obesidad, diabetes, enfermedades cardiovasculares relacionadas con obesidad, demencia, cognición, osteoporosis, estrés y glaucoma.
19. Uso de un compuesto de acuerdo con una cualquiera de las reivindicaciones 1 a 14 en combinación con un agente antihipertensivo en la fabricación de un medicamento para el tratamiento de resistencia a la insulina, dislipidemia, obesidad e hipertensión.
20. Uso de un compuesto de acuerdo con una cualquiera de las reivindicaciones 1 a 14 en combinación con un agonista del receptor de glucocorticoides en la fabricación de un medicamento para la reducción de efectos secundarios indeseables que ocurren durante la terapia con agonistas de los receptores de glucocorticoides y para el tratamiento de algunas formas de cáncer, enfermedades y trastornos que tienen inflamación como componente.
Patentes similares o relacionadas:
Uso de principios activos refrescantes fisiológicos y agentes que contienen tales principios activos, del 17 de Junio de 2020, de Symrise AG: Procedimiento no terapéutico para la modulación in-vitro del receptor de mentol frío TRPM8, en el que se lleva a contacto el receptor con al menos un modulador, que se selecciona […]
Moléculas químicas que inhiben el mecanismo de corte para tratar enfermedades causadas por anomalías de empalme, del 17 de Junio de 2020, de CENTRE NATIONAL DE LA RECHERCHE SCIENTIFIQUE (C.N.R.S.): Un compuesto elegido entre el grupo que comprende: • N-(3-Dimetilamino-propil)-3-(4-trifluorometoxi-fenilamino)-benzamida; • 4-(4-Metoxi-fenilamino)-3-metil-N-(3-metil-butil)-benzamida; […]
Sales cristalinas de un profármaco de dextroanfetamina, del 6 de Mayo de 2020, de SANDOZ AG: Una sal cristalina de L-lisina-d-anfetamina representada por la estructura química como se representa en la fórmula (II) **(Ver fórmula)** […]
Composición farmacéutica inyectable estable de antagonista del receptor de neuroquinina-1 y procedimiento para su preparación, del 29 de Abril de 2020, de PHARMATHEN S.A.: Una composición farmacéutica de liberación controlada para administración intramuscular o subcutánea que comprende Aprepitant o Fosaprepitant […]
Combinaciones de moduladores duales de IRS/STAT3 y agentes anticancerígenos para el tratamiento del cáncer, del 29 de Abril de 2020, de TyrNovo Ltd: Una composición farmacéutica que comprende un inhibidor de EGFR y/o un anticuerpo EGFR en combinación con un compuesto representado por la estructura […]
Implantes intraoculares que contienen prostamida y métodos de uso de éstos, del 1 de Abril de 2020, de ALLERGAN, INC.: Implante intraocular biodegradable, comprendiendo el implante una matriz de polímero biodegradable, polietilen glicol 3350, y una prostamida como el […]
Formulaciones de 15-hidroxiestearato de macrogol, del 25 de Diciembre de 2019, de ALLERGAN, INC.: Composición oftálmica que comprende un principio activo farmacéutico en una cantidad suficiente para contribuir al tratamiento, la prevención o reducción […]
Inhibidores de benzimidazol del canal de sodio, del 18 de Diciembre de 2019, de Zalicus Pharmaceuticals Ltd: Un compuesto seleccionado del grupo que consiste en **(Ver fórmula)** o una sal o solvato farmacéuticamente aceptable del mismo.