DERIVADOS DE FENILGLICINAMIDA Y PIRIDILCLICINAMIDA UTILES COMO AGENTES ANTICOAGULANTES.
Un compuesto de Fórmula (III):
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2006/024345.
Solicitante: BRISTOL-MYERS SQUIBB COMPANY.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: ROUTE 206 AND PROVINCE LINE ROAD,PRINCETON NJ 08543-4000.
Inventor/es: ZHANG,XIAOJUN, NIRSCHL,ALEXANDRA A, ZOU,YAN, PRIESTLEY,ELDON SCOTT.
Fecha de Publicación: .
Fecha Concesión Europea: 13 de Enero de 2010.
Clasificación Internacional de Patentes:
- C07D217/22 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 217/00 Compuestos heterocíclicos que contienen isoquinoleína o isoquinoleína hidrogenada en el sistema cíclico. › con heteroátomos o con átomos de carbono que tienen tres enlaces a heteroátomos, con a lo sumo un enlace a halógeno, p. ej. radicales éster o nitrilo, directamente unidos a los átomos de carbono del ciclo que contiene nitrógeno.
- C07D237/34 C07D […] › C07D 237/00 Compuestos heterocíclicos que contienen ciclos de diazina-1,2 o diazina-1,2 hidrogenada. › con átomos de nitrógeno unidos directamente a los átomos de carbono del ciclo que contiene nitrógeno, p. ej. radicales de hidrazina.
- C07D401/12 C07D […] › C07D 401/00 Compuestos heterocíclicos que contienen dos o más heterociclos, que tienen átomos de nitrógeno como únicos heteroátomos del ciclo, siendo al menos un ciclo de seis miembros con solamente un átomo de nitrógeno. › unidos por una cadena que contiene heteroátomos como enlaces de cadena.
Clasificación PCT:
- A61K31/472 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › Isoquinoleínas no condensadas, p. ej. papaverina.
- A61K31/495 A61K 31/00 […] › que tienen ciclos con seis eslabones con dos nitrógenos como únicos heteroátomos de un ciclo, p. ej. piperazina (A61K 31/48 tiene prioridad).
- C07D217/22 C07D 217/00 […] › con heteroátomos o con átomos de carbono que tienen tres enlaces a heteroátomos, con a lo sumo un enlace a halógeno, p. ej. radicales éster o nitrilo, directamente unidos a los átomos de carbono del ciclo que contiene nitrógeno.
- C07D237/34 C07D 237/00 […] › con átomos de nitrógeno unidos directamente a los átomos de carbono del ciclo que contiene nitrógeno, p. ej. radicales de hidrazina.
- C07D401/12 C07D 401/00 […] › unidos por una cadena que contiene heteroátomos como enlaces de cadena.
Fragmento de la descripción:
Derivados de fenilglicinamida y piridilglicinamida útiles como anticoagulantes.
Campo de la invención
La presente invención proporciona nuevos derivados de fenilglicinamida y piridilglicinamida y análogos de los mismos, que son inhibidores selectivos de enzimas de serinproteasa de la cascada de coagulación y/o el sistema de activación de contacto; por ejemplo, factor VIIa, factor Xa, factor XIa, factor IXa, trombina y/o calicreína en plasma. En particular, se refiere a compuestos que son inhibidores del factor VIIa. Esta invención también se refiere a composiciones farmacéuticas que comprenden estos compuestos.
Antecedentes de la invención
El factor VIIa es una serinproteasa en plasma que interviene en el inicio de la cascada de coagulación. Está presente en la sangre humana en una concentración de aproximadamente 500 ng/ml, con aproximadamente el 1% de la cantidad total en el factor VIIa de forma proteolíticamente activa (Morrissey, J. H. y col. Blood 1993, 81, 734-744). El factor VIIa se une con alta afinidad con su cofactor, factor hístico, en presencia de iones de calcio para formar un complejo con actividad proteolítica mejorada (Carson, S.D. y Brozna, J.P. Blood Coag. Fibrinol. 1993, 4, 281-292). El factor hístico se expresa normalmente en células que rodean a la vasculatura y dentro de la pared del vaso, y se expone al factor VIIa en sangre por lesión en el vaso o ruptura de la placa aterosclerótica. Una vez formado, el complejo factor hístico/factor VIIa inicia la coagulación sanguínea por escisión proteolítica de factor X a factor Xa, factor IX a factor IXa y autoactivación de factor VII adicional a VIIa. El factor Xa, generado directamente por factor hístico/factor VIIa o indirectamente a través de la acción de factor IXa, cataliza la conversión de protrombina a trombina. La trombina convierte el fibrinógeno en fibrina, que se polimeriza para formar el marco estructural de un coágulo sanguíneo, y activa las plaquetas, que son un componente celular clave de coagulación (Hoffman, M. Blood Reviews 2003, 17, S1-S5). Además, existe evidencia de que el factor hístico está presente en la sangre, probablemente en una forma encriptada que se desencripta durante la formación de coágulos (Giesen, P. L. A. y col. Proc. Natl. Acad. Sci. 1999, 96, 2311-2315; Himber, J. y col. J. Tromb. Haemost. 2003, 1, 889-895). El complejo factor hístico/factor VIIa derivado de factor hístico transportado en sangre puede desempeñar un papel importante en la propagación de la cascada de coagulación (crecimiento de coágulos) y en formación de trombo en ausencia de lesión en las paredes de los vasos (es decir, trombosis venosa profunda o sepsis inducida por estasis). La fuente de factor hístico transportado por la sangre es un área de investigación activa (Morrissey, J. H. J. Tromb. Haemost. 2003, 1, 878-880).
Aunque la coagulación sanguínea es esencial para la regulación de la hemostasia de un organismo, también interviene en muchas dolencias patológicas. En trombosis, puede formarse un coágulo de sangre, o trombo, y obstruir la circulación localmente, causando isquemia y daño orgánico. Alternativamente, en un proceso conocido como embolia, el coágulo puede desalojarse y posteriormente quedar atrapado en un vaso distal, en el que de nuevo causa isquemia y daño orgánico. Las enfermedades que proceden de la formación de un trombo patológico se refieren colectivamente como trastornos trombóticos o tromboembólicos e incluyen síndrome coronario agudo, angina inestable, infarto de miocardio, accidente cerebrovascular isquémico, trombosis venosa profunda, enfermedad arterial oclusiva periférica, ataque isquémico transitorio y embolia pulmonar. Además, la trombosis se produce en superficies artificiales en contacto con sangre, lo que incluye catéteres y válvulas cardiacas artificiales. Por tanto, los fármacos que inhiben la coagulación sanguínea, o anticoagulantes, son "agentes centrales para la prevención y el tratamiento de trastornos tromboembólicos" (Hirsch, J. y col. Blood 2005, 105, 453-463).
Debido a su papel clave en la cascada de coagulación, los investigadores han postulado que la inhibición del factor VIIa podría usarse para tratar o prevenir enfermedad trombótica o tromboembólica. (Girard, T. J.; Nicholson, N. S. Curr. Opin. Pharmacol. 2001, 1, 159-163; Lazarus, R. A., y col. Curr. Med. Chem. 2004, 11, 2275-2290; Frederick, R. y col. Curr. Med. Chem. 2005, 12, 397-417). Varios estudios han confirmado que varios inhibidores biológicos y de moléculas pequeñas de factor VIIa tienen eficacia antitrombótica in vivo con una baja responsabilidad de hemorragia. Por ejemplo, se ha demostrado que un inhibidor de factor VIIa biológico XK1, que comprende un híbrido de primer dominio kunitz de inhibidor de ruta de factor hístico y cadena ligera de factor X, previene la formación de trombos en un modelo de rata de trombosis arterial, sin cambio en el tiempo de hemorragia o en la pérdida total de sangre (Szalony, J. A. y col. J. Thrombosis and Thrombolysis 2002, 14, 113-121). Además, los inhibidores de factor VIIa dirigidos a sitios activos de moléculas pequeñas han demostrado eficacia antitrombótica en modelos animales de trombosis arterial (Suleymanov, O., y col. J Pharmacology and Experimental Therapeutics 2003, 306, 1115-1121; Young, W. B., y col. Bioorg. Med. Chem. Lett. 2006, 16, 2037-2041) y trombosis venosa (Szalony, J. A., y col. Thrombosis Research 2003, 112, 167-174; Arnold, C. S., y col. Thrombosis Research 2006, 117, 343-349), con escaso impacto en el tiempo de hemorragia o pérdida de sangre. Por otra parte, actualmente se encuentra bajo investigación clínica la proteína anticoagulante de nematodos recombinante de inhibidor de factor VIIa biológico C2 (rNAPC2) para tratamiento de síndromes coronarios agudos. Los resultados de los ensayos clínicos iniciales demuestran que rNAPC2 reduce la generación de trombina sistémica en pacientes sometidos a angioplastia coronaria (Moons, A. H. M. J. Am. Coll. Cardiol. 2003, 41, 2147-2153) y que evita la trombosis venosa profunda en pacientes sometidos a sustitución de rodilla total (Lee, A., y col. Circulation 2001, 104, 74-78).
En consecuencia se han realizado trabajos para identificar y optimizar los inhibidores de factor VIIa. Por ejemplo, el documento US-5.866.542 describe proteínas anticoagulantes de nematodos recombinantes que inhiben el factor VIIa. El documento US-5.843.442 desvela anticuerpos monoclonales o fragmentos de anticuerpos que poseen actividad inhibidora de factor VIIa, y el documento US-5.023.236 presenta tripéptidos y derivados de tripéptidos que inhiben el factor VIIa.
La solicitud de patente internacional WO-2004/072.102 describe compuestos de bencenoacetamida que son útiles en el tratamiento de trastornos asociados con el factor VIIa.
Una forma alternativa de inicio de la coagulación está operativa cuando se expone la sangre a superficies artificiales (por ejemplo, durante hemodiálisis, cirugía cardiovascular "en bomba", injertos de vasos, sepsis bacteriana). Este procedimiento se denomina también activación de contacto. La absorción superficial de factor XII conduce a cambio conformacional en la molécula de factor XII, con lo que se facilita la activación para factor XII proteolíticamente activo (factor XIIa y factor XIIf). El factor XIIa (o XIIf) tiene una serie de proteínas objeto, que incluyen precalicreína en plasma y factor XI. La calicreína en plasma activa además el factor XII, llevando a una amplificación de la activación de contacto. El FXI activado actúa sobre FIX, que actúa a través de la cascada de coagulación para producir trombina. Así, sería de esperar que los inhibidores de calicreína en plasma ejercieran un efecto antitrombótico en condiciones de activación de contacto. La activación de contacto es un procedimiento mediado en superficie responsable en parte de la regulación de la trombosis y la inflamación, y está mediado, al menos en parte, por rutas fibrinolíticas, de complemento, de cininógeno/cinina y otras rutas humorales y celulares (para revisión, Coleman, R. Contact Activation Pathway, páginas 103-122 en Hemostasia and Thrombosis, Lippincott Williams & Wilkins 2001; Schmaier A.H. Contact Activation, páginas 105-128 en Thrombosis and Hemorrhage, 1998).
La calicreína en plasma es un zimógeno de una serinproteasa de tipo tripsina y está presente en plasma en de 35 a 50 µg/ml. La estructura génica es similar a la del factor XI; en conjunto, la secuencia de aminoácidos de calicreína en plasma tiene una homología del 58% con el factor XI. La activación proteolítica por factor XIIa en un enlace interno 1389-R390...
Reivindicaciones:
1. Un compuesto de Fórmula (III):
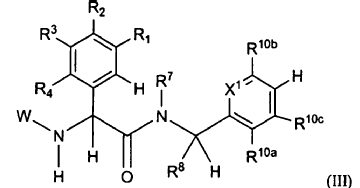
o un esteroisómero o sal farmacéuticamente aceptable, o solvato del mismo, en la que:
W es
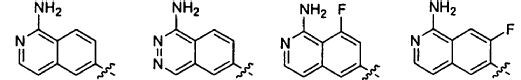
o

X1 es CH o N;
R1 es Cl, Br, Me, Et, OMe, OEt, OCHF2, o ciclopropilo;
R2 es H, F, Cl, OMe, O(i-Pr), u OCHF2;
R3 es H u OMe;
R4 es H, F, Cl, u OMe;
R7 es H, Me, -CH2CO2H, o -CH2CO2(alquilo C1-4);
R8 es H, Me, CO2H, CO2(alquilo C1-4), -CH2CO2H, o -CH2CO2(alquilo C1-4);
R10a es F, O(alquilo C1-4), CONRcRd, -S(alquilo C1-4), -SO2(alquilo C1-4), -SO2-ciclopropilo, -SO2-ciclobutilo, -SO2-ciclopentilo, -SO2-(pirrolidin-1-ilo), -SO2-(piperid-1-ilo), -SO2-(azepan-1-ilo), -SO2NRcRd, -SO2NH-ciclopropilo, morfolin-4-ilo, 3,5-dimetil-pirazol-1-ilo, o 3,5-dietil-pirazol-1-ilo;
R10b es OH, NH2, -NHCO(alquilo C1-4), -NHCO2(alquilo C1-4), -NHSO2NH2, -SO2NH2, o -NHCONRcRd;
R10c es H, Cl, o Me;
Rc y Rd son, independientemente en cada ocurrencia, H o alquilo C1-4; alternativamente, Rc y Rd, cuando están unidos al mismo átomo de nitrógeno, se combinan formando un heterociclo de 4 a 5 eslabones que comprende: átomos de carbono y de 0 a 2 heteroátomos adicionales seleccionados entre N, O y S(O)p; estando dicho heterociclo sustituido con 0 a 2 Rg; y
Rg es, independientemente en cada ocurrencia, =O, F, Cl, Br, CF3, OH, o alquilo C1-4.
2. Un compuesto según la reivindicación 1, en el que:
W es
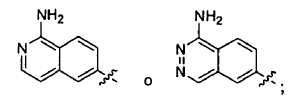
X1 es CH;
R7 es H, Me, o -CH2CO2H;
R8 es H, Me, CO2H, -CH2CO2H, o -CH2CO2Me;
R10a es F, O(i-Pr), -CONMe2, -CO-(pirrolidin-1-ilo), -CO-(piperid-1-ilo), -S(i-Pr), -SO2Et, -SO2Pr, -SO2(i-Pr), -SO2(t-Bu), -SO2-ciclopropilo, -SO2-ciclobutilo, -SO2-ciclopentilo, -SO2-(pirrolidin-1-ilo), -SO2-(piperid-1-ilo), -SO2-(azepan-1-ilo), -SO2NHMe, -SO2NMe2, -SO2NHEt, -SO2NH(i-Pr), -SO2NH-ciclopropilo, morfolin-4-ilo, 3,5-dimetil-pirazol-1-ilo, o 3,5-dietil-pirazol-1-ilo;
R10b es OH, NH2, -NHCOMe, -NHCOPr, -NHCO2Me, -NHCO2Et, -NHCO2(i-Pr), -NHCO2(i-Bu), -NHSO2NH2, -SO2NH2, -NHCON(Me)2, -NHCON(Me)(Et), -NHCON(Me)(i-Pr),
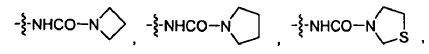
o
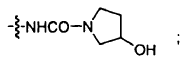
y
R10c es H.
3. Un compuesto según la reivindicación 1, seleccionándose el compuesto entre
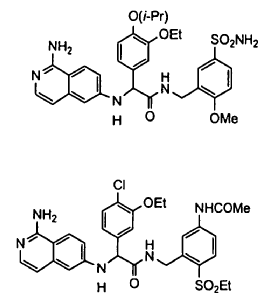
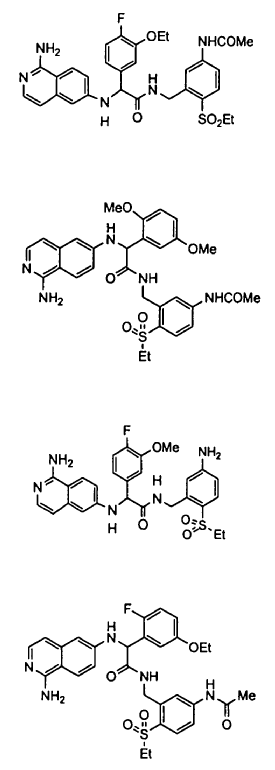
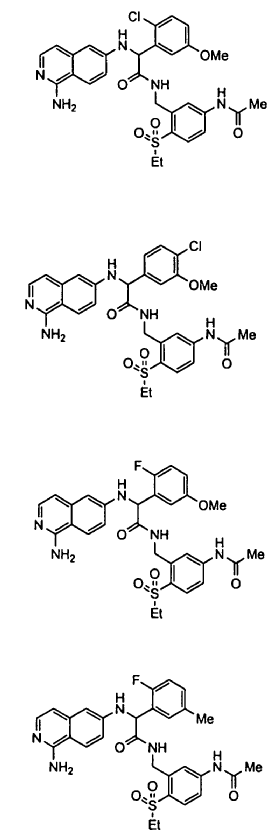
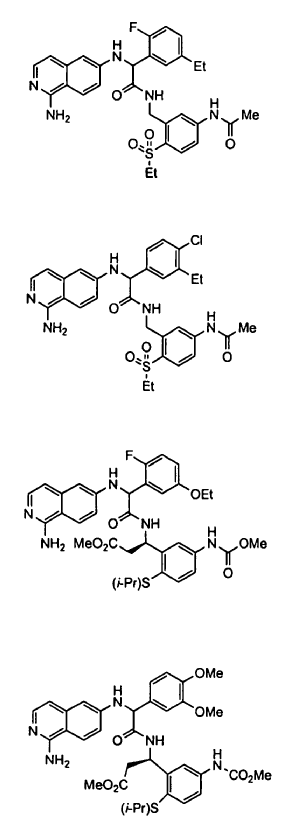
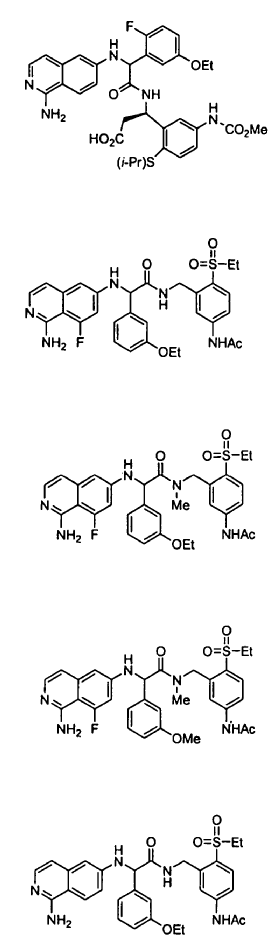
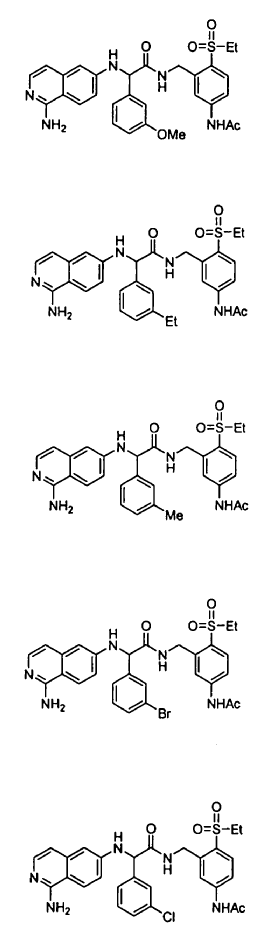
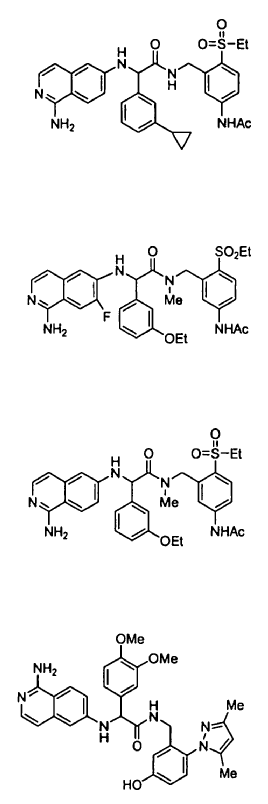
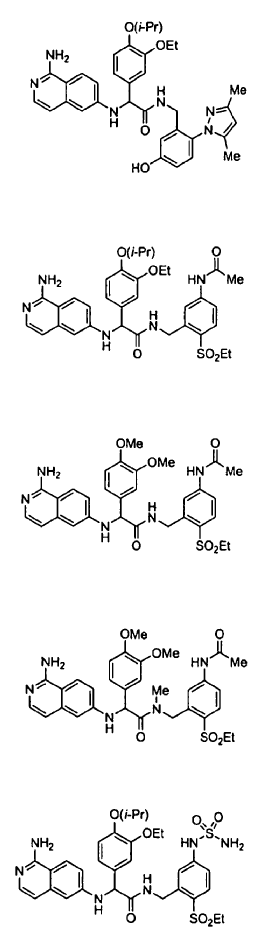
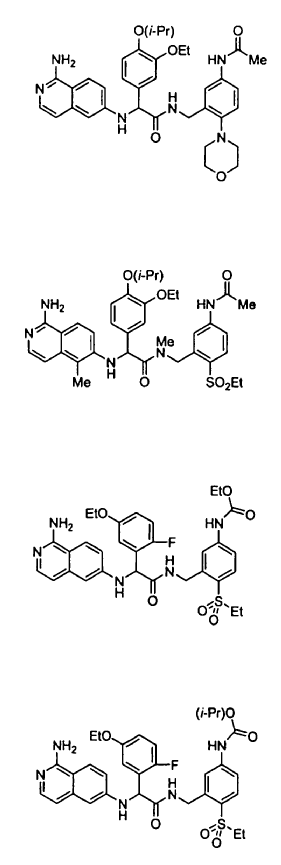
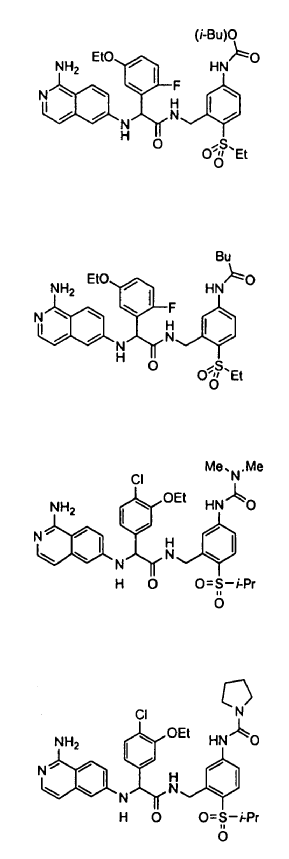
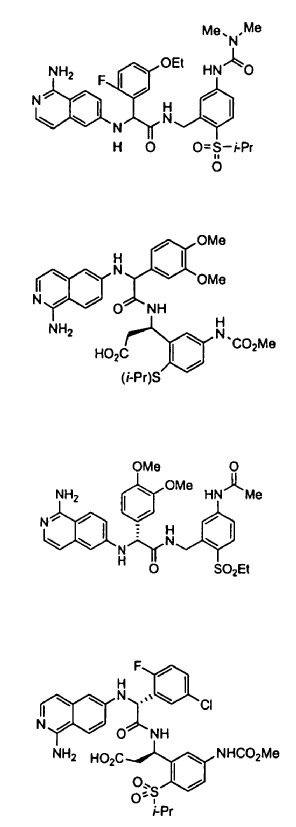

o un esteroisómero o sal farmacéuticamente aceptable, o solvato del mismo.
4. Una composición farmacéutica, que comprende: un vehículo farmacéuticamente aceptable y una cantidad terapéuticamente eficaz de un compuesto de una cualquiera de las reivindicaciones 1 a 3.
5. Un compuesto de una cualquiera de las reivindicaciones 1 a 3 para su uso en terapia.
6. El compuesto según la reivindicación 5 para su uso en el tratamiento de un trastorno tromboembólico.
7. El compuesto según la reivindicación 6, en el que el trastorno tromboembólico se selecciona entre el grupo constituido por trastornos tromboembólicos cardiovasculares arteriales, trastornos tromboembólicos cardiovasculares venosos y trastornos tromboembólicos en las cavidades cardiacas o en la circulación periférica.
8. El compuesto según la reivindicación 6, en el que el trastorno tromboembólico se selecciona entre angina inestable, un síndrome coronario agudo, fibrilación auricular, primer infarto de miocardio, infarto de miocardio recurrente, muerte súbita isquémica, ataque isquémico transitorio, accidente cerebrovascular, aterosclerosis, enfermedad arterial oclusiva periférica, trombosis venosa, trombosis venosa profunda, tromboflebitis, embolia arterial, trombosis arterial coronaria, trombosis arterial cerebral, embolia cerebral, embolia renal, embolia pulmonar, y trombosis resultante de implantes, dispositivos o procedimientos médicos en los que la sangre está expuesta a una superficie artificial que promueve la trombosis.
Patentes similares o relacionadas:
Compuestos y procedimientos de uso, del 29 de Julio de 2020, de Medivation Technologies LLC: Un compuesto de fórmula (Aa-1): **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en la que: A representa H, halógeno, amino, […]
Compuestos heterocíclicos que activan AMPK y métodos de uso de los mismos, del 29 de Julio de 2020, de RIGEL PHARMACEUTICALS, INC.: Un compuesto que es N-((cis)-1-(4-cianobencil)-3-fluoropiperidin-4-il)-6-(4-(4-metoxibenzoil)piperidin-1-carbonil)nicotinamida; N-((3S,4S)-1-(4-cianobencil)-3-fluoropiperidin-4-il)-6-(4-(4-metoxibenzoil)piperidin-1-carbonil)nicotinamida; […]
Compuestos de alquinilbenceno heterocíclicos, y composiciones médicas y usos de los mismos, del 29 de Julio de 2020, de Guangzhou Healthquest Pharma Co., Ltd: Un compuesto de alquinilbenceno heterocíclico que tiene la fórmula (I) y una sal farmacéuticamente aceptable, o estereoisómero del mismo, **(Ver […]
Derivados de piperidina 1,4 sustituidos, del 29 de Julio de 2020, de 89Bio Ltd: Un compuesto de acuerdo con la Fórmula I: **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en donde: A se selecciona de […]
Ureas asimétricas p-sustituidas y usos médicos de las mismas, del 22 de Julio de 2020, de Helsinn Healthcare SA: Un compuesto de Fórmula I: **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en donde: una línea discontinua indica un enlace opcional; X es CH; […]
Derivados de bencimidazol como inhibidores Nav 1.7 (subunidad alfa del canal de sodio, dependiente del voltaje, tipo IX (SCN9A)) para tratar el dolor, la disuria y la esclerosis múltiple, del 22 de Julio de 2020, de Sumitomo Dainippon Pharma Co., Ltd: Un compuesto de fórmula (I): **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, donde R1a, R1b, R1c, y R1d son independientemente hidrógeno, […]
Derivado de dihidropiridazin-3,5-diona, del 15 de Julio de 2020, de CHUGAI SEIYAKU KABUSHIKI KAISHA: Un compuesto representado por la fórmula (I) o una sal del mismo, o un solvato del compuesto o la sal: **(Ver fórmula)** en donde R1, R4 y R5 se definen […]
Inhibidores de btk de tipo nicotinimida sustituida y su preparación y uso en el tratamiento del cáncer, la inflamación y las enfermedades autoinmunitarias, del 15 de Julio de 2020, de Guangzhou InnoCare Pharma Tech Co., Ltd: Un compuesto seleccionado del grupo que consiste en: 6-(1-acriloilpiperidin-4-il)-2-(4-fenoxifenil)nicotinamida; **(Ver fórmula)** 6-(4-acriloilpiperazin-1-il)-2-(4-fenoxifenil)nicotinamida; […]