CONJUGADOS DE HEMOGLOBINA-POLISACARIDO.
Procedimiento para preparar un producto conjugado de hemoglobina-polisacárido que comprende:
(a) someter un polisacárido de partida seleccionado de entre almidón y derivados de almidón a apertura oxidativa del ciclo para producir un polisacárido de ciclo oxidativamente abierto portador de grupos aldehído;
(b) hacer reaccionar el polisacárido de ciclo oxidativamente abierto con una hemoglobina en condiciones adecuadas para formar enlaces de base de Schiff entre la hemoglobina y el polisacárido de ciclo abierto para formar un producto conjugado de hemoglobina-polisacárido inicial que contiene polisacárido oxidado;
(c) degradar el polisacárido de ciclo oxidativamente abierto manteniendo el producto conjugado en condiciones controladas de solución acuosa con un pH predeterminado durante un periodo de tiempo hasta que se forma otro producto conjugado de hemoglobina-polisacárido degradado con un peso molecular promedio reducido en comparación con el producto conjugado de hemoglobina-polisacárido inicial;
(d) reducir el otro producto conjugado de hemoglobina-polisacárido con un peso molecular promedio reducido para obtener un producto conjugado de hemoglobina-polisacárido reducido; y
(e) recuperar el producto conjugado de hemoglobina-polisacárido reducido
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/CA99/00260.
Solicitante: HEMOSOL INC..
Nacionalidad solicitante: Canadá.
Dirección: 115 SKYWAY AVENUE,ETOBICOKE, ONTARIO M9W 4Z4.
Inventor/es: ADAMSON,GORDON,W.
Fecha de Publicación: .
Fecha Concesión Europea: 9 de Diciembre de 2009.
Clasificación Internacional de Patentes:
- A61K47/48K8
Clasificación PCT:
- A61K47/48
Clasificación antigua:
- A61K47/48
Fragmento de la descripción:
Conjugados de hemoglobina-polisacárido.
Campo de la invención
La presente invención se refiere a portadores de oxígeno biocompatibles para la administración a pacientes como suplemento o sustitución parcial de sangre entera. Más específicamente, la presente invención se refiere a portadores de oxígeno basados en hemoglobina (HBOC) para la administración a mamíferos como sustituto o suplemento sanguíneo, y a procedimientos para su preparación.
Antecedentes de la invención
La hemoglobina, como componente transportador de oxígeno natural de la sangre, es un candidato evidente para formar la base de un sustituto sanguíneo, por ejemplo en forma de solución acuosa. Se han llevado a cabo y documentado extensos trabajos científicos para intentar conseguir una solución de hemoglobina satisfactoria que actúe como sustituto de la sangre. Sin embargo, las propiedades químicas de la hemoglobina fuera de los glóbulos rojos son marcadamente diferentes de sus propiedades dentro de los mismos, por ejemplo, en lo que se refiere a su afinidad por el oxígeno. La necesidad de alguna forma de modificación química de la hemoglobina para hacerla adecuada para su utilización como sustituto sanguíneo ha sido reconocida desde hace tiempo y ha sido investigada profusamente.
Es conocido el hecho de que la hemoglobina comprende un tetrámero de cuatro subunidades, concretamente dos subunidades a, cada una de las cuales presenta una cadena peptídica de globina, y dos subunidades ß, cada una de las cuales presenta una cadena peptídica de globina. El tetrámero presenta un peso molecular de aproximadamente 64 kilodaltons, y cada subunidad presenta aproximadamente el mismo peso molecular. La hemoglobina tetramérica en solución acuosa diluida se disocia fácilmente en dímeros a-ß, y en determinadas condiciones, en monómeros de subunidad a y monómeros de subunidad ß. Los dímeros y monómeros tienen un peso molecular demasiado bajo para su retención en el sistema circulatorio del cuerpo, y son filtrados por el riñón para su excreción con la orina. Este hecho conlleva una vida media inaceptablemente breve de un producto de este tipo en el cuerpo. Han sido reconocidos anteriormente los beneficios de la presencia de enlaces químicos entre las subunidades para asegurar el mantenimiento de la forma tetramérica (reticulación intramolecular
). Además, también se ha reconocido como deseable en muchos casos el enlazamiento de dos o más unidades tetraméricas para formar oligómeros y polímeros de hemoglobina de peso molecular mayor de 64 kilodaltons (reticulación intermolecular
).
En consecuencia, un enfoque para desarrollar un HBOC para uso clínico ha sido la reticulación intramolecular de unidades de hemoglobina, formando tetrámeros estabilizados con un peso molecular de aproximadamente 64 kilodaltons, y opcionalmente la formación a partir de dichos tetrámeros de oligómeros con 2-6 de dichos tetrámeros mediante reticulación intermolecular. Se han propuesto una gran variedad de reactivos reticulantes con este propósito, incluyendo sacáridos de ciclo oxidativamente abierto, tales como o-rafinosa (patente US nº 4.857.636 de Hsia y patente US nº 5.532.352 de Pliura et al, por ejemplo), imidatos bifuncionales, tales como hidrocloruro de dietil-malonimidato (patente US nº 3.925.344 de Muzur), triazinas halogenadas, divinilsulfonas, diisocianatos, glutaraldehído y otros dialdehídos (patente US nº 4.001.200 de Bonsen et al), ésteres de bis-diaspirina (patente US nº 5.529.719 de Tye), fosfatos bis- y trisacilo (patente US nº 5.250.665 de Kluger et al) y otros.
Otro enfoque para la preparación de un HBOC con un peso molecular adecuado para uso clínico ha consistido en el acoplamiento de hemoglobina a un polisacárido biocompatible. Dichos conjugados presentan la ventaja, en comparación con las hemoglobinas reticuladas y oligomerizadas, que consiste en requerir cantidades menores de hemoglobina por unidad de HBOC y, en consecuencia, resultan más económicos de preparar y presentan menores toxicidades relacionadas con la hemoglobina. La conjugación de un coloide con la hemoglobina en la preparación de un HBOC también permite el control de las propiedades de flujo, tales como la viscosidad y la presión osmótica coloidal, ajustando el tamaño de dicho coloide, su grado de modificación y la relación coloide/hemoglobina. Estos mismos parámetros pueden ser utilizados para controlar el peso molecular final y el tiempo de retención vascular del producto.
La patente US nº 4.064.118 de Wong propone la preparación de un sustituto sanguíneo o extensor sanguíneo acoplando químicamente hemoglobina con un material polisacárido seleccionado de entre dextrano e hidroxietil almidón con un peso molecular comprendido aproximadamente dentro del intervalo 5 kDa - 2.000 kDa. Sin embargo, en dicha patente solo se ejemplifica el uso de dextrano.
Baldwin et al, Tetrahedron
37, págs. 1723-1726 (1981) Synthesis of Polymer-Bound Hemoglobin Samples
describen la modificación química de dextrano e hidroxietil almidón (HES) para formar polímeros sustituidos con aldehído, y su posterior reacción con hemoglobina para formar hemoglobina soluble enlazada a polímero. Mientras que los productos formados de este modo pudieron enlazar oxígeno, los mismos fueron considerados inadecuados para su utilización como sustitutos sanguíneos, ya que sus curvas de enlace de oxígeno estaban considerablemente desplazadas hacia la izquierda, lo que indica que tienen una afinidad demasiado elevada por el oxígeno (P50 demasiado baja).
Sumario de la invención
Un objetivo de la presente invención consiste en proporcionar un HBOC nuevo.
Otro objeto de la presente invención consiste en dar a conocer un conjugado de polisacárido-hemoglobina nuevo útil como HBOC.
Otro objetivo de la presente invención consiste en proporcionar un procedimiento para preparar un conjugado de polisacárido-hemoglobina nuevo útil como HBOC.
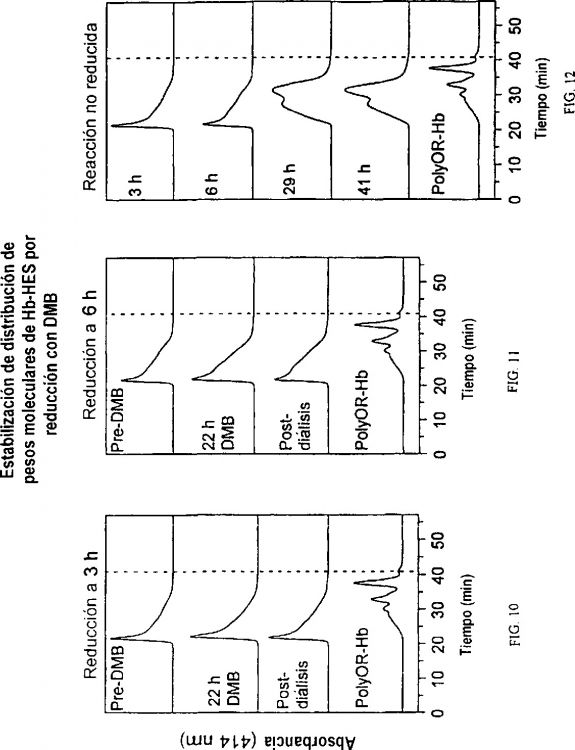
La presente invención proporciona por lo tanto en un primer aspecto el procedimiento según la reivindicación 1. En el procedimiento según la presente invención se utiliza un polisacárido seleccionado de entre almidón y derivados de almidón en una forma de ciclo oxidativamente abierto. En dicha forma oxidativa, por lo menos una parte de las unidades monoméricas de sacárido se oxidan para que presenten grupos aldehído. A continuación, el polisacárido oxidado así formado se hace reaccionar con hemoglobina extracelular, de tal modo que dicha hemoglobina, a través de los grupos amina primarios de las cadenas de globina que reaccionan con los grupos aldehído del polisacárido oxidado, se enlaza covalentemente con el polisacárido a través de enlaces de base de Schiff. Inicialmente, y muy rápidamente, se forma un producto que incluye especies con un peso molecular muy elevado, del orden de 500 kDa o mayor, en cantidades sustanciales y en una amplia distribución de pesos moleculares (128->500 kDa).
Manteniendo dicho producto en condiciones controladas, en solución acuosa y a un pH predeterminado, el mismo se puede transformar en una proporción controlada y a lo largo de un período de tiempo relativamente breve (por ejemplo de 4-48 horas en función de las condiciones) en un producto con un peso molecular mucho menor (90-200 kDa) con una distribución de pesos moleculares mucho más estrecha. Tras la reducción química para reducir los enlaces de base de Schiff entre la hemoglobina y el polisacárido a enlaces amina secundarios, dicho producto presenta propiedades tales como una afinidad por el oxígeno dentro del intervalo P50 = 4 a 50 mmHg 37ºC, en función del estado de ligando de la hemoglobina en el momento de la conjugación, lo que convierte a dicho producto en eminentemente adecuado como candidato para un portador de oxígeno basado en hemoglobina para uso clínico en mamíferos. El grado de transformación se puede controlar controlando el tiempo de aplicación de la etapa de reducción. Además, el producto resultante no contiene hemoglobina no reaccionada detectable, que, en caso de estar presente, se disociaría dando lugar a dímeros aß, de los que se sospecha que provocan lesiones renales, ni contiene cantidades detectables de productos con un peso molecular excesivamente elevado (superior a aproximadamente 500-600 kDa).
El producto del procedimiento según la presente invención es un conjugado de polisacárido-hemoglobina útil como portador de oxígeno basado en hemoglobina. De manera adecuada, el producto presenta una afinidad por el oxígeno, expresada como...
Reivindicaciones:
1. Procedimiento para preparar un producto conjugado de hemoglobina-polisacárido que comprende:
2. Procedimiento según la reivindicación 1, en el que el otro producto conjugado de hemoglobina-polisacárido con un peso molecular promedio reducido presenta asimismo una distribución de pesos moleculares más estrecha en comparación con el producto conjugado de hemoglobina-polisacárido inicial.
3. Procedimiento según la reivindicación 1 ó 2, en el que no existe hemoglobina no reaccionada detectable ni conjugado detectable de peso molecular superior a aproximadamente 500 kDa en el producto conjugado de hemoglobina-polisacárido reducido.
4. Procedimiento según cualquiera de las reivindicaciones 1 a 3, en el que el polisacárido de partida es el hidroxietil almidón.
5. Procedimiento según la reivindicación 4, en el que el hidroxietil almidón presenta un peso molecular comprendido de entre 70-1.000 kDa.
6. Procedimiento según la reivindicación 4 ó 5, en el que el hidroxietil almidón presenta un índice de sustitución de 0,5-0,7.
7. Procedimiento según cualquiera de las reivindicaciones 4 a 6, en el que la relación de masa entre la hemoglobina y el hidroxietil almidón oxidado del producto conjugado de hemoglobina-hidroxietil almidón reducido es 0,25:1-5:1.
8. Procedimiento según la reivindicación 7, en el que la relación de masa entre la hemoglobina y el hidroxietil almidón oxidado es 0,5:1-3:1.
9. Procedimiento según cualquiera de las reivindicaciones anteriores, en el que el conjugado inicial se mantiene en la etapa (c) en solución acuosa a un pH de desde aproximadamente 7,2-10, a una temperatura de 15-30 grados Celsius, para reducir el peso molecular promedio del producto conjugado inicial.
10. Procedimiento según cualquiera de las reivindicaciones anteriores, en el que el conjugado inicial se mantiene en solución acuosa durante 4-48 horas.
11. Procedimiento según cualquiera de las reivindicaciones anteriores, en el que el peso molecular del conjugado de la etapa (c) es de 90-200 kDa.
12. Procedimiento según cualquiera de las reivindicaciones anteriores, en el que la etapa de reducción (d) es una única etapa de reducción para realizar la reducción de la base de Schiff y de manera sustancialmente simultánea para reducir los grupos aldehído.
13. Procedimiento según la reivindicación 12, en el que la reducción se lleva a cabo con un agente reductor a base de boro.
14. Procedimiento según la reivindicación 13, en el que el agente reductor a base de boro es el dimetilamino borano.
15. Procedimiento según cualquiera de las reivindicaciones 1 a 14, en el que la etapa de reducción (d) se lleva a cabo en dos etapas sucesivas de reducción, la primera para llevar a cabo la reducción de la base de Schiff, y la segunda para reducir los grupos aldehído.
16. Procedimiento según cualquiera de las reivindicaciones anteriores, en el que la hemoglobina se obtiene de cultivo celular.
17. Procedimiento según cualquiera de las reivindicaciones anteriores, en el que la hemoglobina es la hemoglobina animal.
18. Procedimiento según cualquiera de las reivindicaciones 1 a 16, en el que la hemoglobina es la hemoglobina humana.
19. Procedimiento según cualquiera de las reivindicaciones anteriores, en el que la hemoglobina es la desoxihemoglobina.
20. Procedimiento según cualquiera de las reivindicaciones 1 a 18, en el que la hemoglobina es la hemoglobina-monóxido de carbono.
21. Procedimiento según cualquiera de las reivindicaciones anteriores, en el que la hemoglobina está reticulada.
22. Procedimiento según cualquiera de las reivindicaciones anteriores, en el que el producto conjugado de hemoglobina-polisacárido reducido presenta una P50 de 4-50 mmHg a 37ºC.
23. Procedimiento según la reivindicación 5, en el que el producto conjugado de hemoglobina-polisacárido reducido presenta una P50 intermedia entre los estados R y T de la hemoglobina natural.
24. Producto conjugado de hemoglobina-polisacárido producido mediante un procedimiento según cualquiera de las reivindicaciones anteriores.
25. Producto conjugado de hemoglobina-polisacárido producido mediante un procedimiento según la reivindicación 1.
26. Producto conjugado de hemoglobina-polisacárido producido mediante un procedimiento según cualquiera de las reivindicaciones 2 a 23.
27. Producto conjugado de hemoglobina-polisacárido según cualquiera de las reivindicaciones 24 a 26, que comprende un polisacárido de ciclo oxidativamente abierto que se ha degradado a un pH entre 7,2-10.
28. Producto conjugado de hemoglobina-polisacárido según la reivindicación 27, en el que el polisacárido es el hidroxietil almidón.
29. Producto conjugado de hemoglobina-polisacárido según cualquiera de las reivindicaciones 26, 27 ó 28, en el que el polisacárido es hidroxietil almidón que presenta un peso molecular de 70 a 1.000 kDa.
30. Producto conjugado de hemoglobina-polisacárido según cualquiera de las reivindicaciones 26 a 29, en el que el hidroxietil almidón presenta un índice de sustitución de desde 0,5-0,7.
31. Producto conjugado de hemoglobina-polisacárido según cualquiera de las reivindicaciones 26 a 30, en el que la hemoglobina se obtiene de cultivo celular.
32. Producto conjugado de hemoglobina-polisacárido según cualquiera de las reivindicaciones 26 a 31, en el que la hemoglobina es la hemoglobina animal.
33. Producto conjugado de hemoglobina-polisacárido según cualquiera de las reivindicaciones 26 a 31, en el que la hemoglobina es la hemoglobina humana.
34. Producto conjugado de hemoglobina-polisacárido según cualquiera de las reivindicaciones 26 a 33, en el que la hemoglobina es la desoxihemoglobina.
35. Producto conjugado de hemoglobina-polisacárido según cualquiera de las reivindicaciones 26 a 33, en el que la hemoglobina es la hemoglobina-monóxido de carbono.
36. Producto conjugado de hemoglobina-polisacárido según cualquiera de las reivindicaciones 26 a 35, en el que la hemoglobina está reticulada.
37. Producto conjugado de hemoglobina-polisacárido según cualquiera de las reivindicaciones 26 a 36, en el que el producto conjugado de hemoglobina-polisacárido presenta una P50 de 4-50 mmHg a 37ºC.
38. Producto conjugado de hemoglobina-polisacárido según la reivindicación 28, en el que el producto conjugado de hemoglobina-polisacárido presenta una P50 intermedia entre los estados R y T de la hemoglobina natural.
Patentes similares o relacionadas:
CONJUGADOS DE HIDROXIALQUILALMIDÓN-PRINCIPIO ACTIVO, del 10 de Enero de 2012, de FRESENIUS KABI DEUTSCHLAND GMBH: Procedimiento para la preparación de un conjugado covalente de HAS-principio activo en el que el HAS y un principio activo se hacen reaccionar selectivamente […]
TEJIDOS DE UNIÓN Y PROTEÍNAS DE RETICULACIÓN CON COMPUESTOS DE NAFTALIMIDA, del 3 de Enero de 2012, de PHOTOBIOMED CORPORATION: Un compuesto 4-amino-1,8-naftalimida para usar en un procedimiento para estabilizar la pared de una arteria que tiene proteínas en la pared […]
COMPLEJOS DE CARBOHIDRATO-HIERRO SOLUBLES EN AGUA, PREPARACIÓN DE LOS MISMOS Y MEDICAMENTOS QUE LOS CONTIENEN, del 25 de Agosto de 2011, de VIFOR (INTERNATIONAL) AG: Complejo de carbohidrato-hierro soluble en agua con un peso molecular medio Mw de 80 kDa hasta 400 kDa, que se puede obtener a partir de una solución acuosa de una sal de […]
 INHIBIDORES DUALES ANTITROMBÓTICOS QUE COMPRENDEN UN RESIDUO DE BIOTINA, del 24 de Junio de 2011, de N. V. ORGANON: un compuesto antitrombotico de formula (I) **Fórmula** oligosacarido-espaciador-A (I), donde el oligosacarido es un residuo de pentasacarido cargado […]
INHIBIDORES DUALES ANTITROMBÓTICOS QUE COMPRENDEN UN RESIDUO DE BIOTINA, del 24 de Junio de 2011, de N. V. ORGANON: un compuesto antitrombotico de formula (I) **Fórmula** oligosacarido-espaciador-A (I), donde el oligosacarido es un residuo de pentasacarido cargado […]
 COMPOSICIONES Y MÉTODOS PARA LA DETECCIÓN DE DIROLIMUS, del 11 de Mayo de 2011, de SIEMENS HEALTHCARE DIAGNOSTICS INC.: Compuesto que comprende un resto, seleccionado del grupo que consiste en restos de marcador de poli(aminoácido), restos de marcador que no son de poli(aminoácido), […]
COMPOSICIONES Y MÉTODOS PARA LA DETECCIÓN DE DIROLIMUS, del 11 de Mayo de 2011, de SIEMENS HEALTHCARE DIAGNOSTICS INC.: Compuesto que comprende un resto, seleccionado del grupo que consiste en restos de marcador de poli(aminoácido), restos de marcador que no son de poli(aminoácido), […]
 MEDICAMENTOS PARA ENFERMEDADES ARTICULARES, del 3 de Septiembre de 2010, de TAKATA SEIYAKU KABUSHIKI KAISHA
RICHTER GEDEON VEGYESZETI GY R R.T: Complejo de ácido hialurónico y zinc para su utilización en el tratamiento de enfermedades artríticas
MEDICAMENTOS PARA ENFERMEDADES ARTICULARES, del 3 de Septiembre de 2010, de TAKATA SEIYAKU KABUSHIKI KAISHA
RICHTER GEDEON VEGYESZETI GY R R.T: Complejo de ácido hialurónico y zinc para su utilización en el tratamiento de enfermedades artríticas
DERIVATIZACION DEL FACTOR ESTIMULANTE DE COLONIAS GRANULOCITICAS (GCSF), del 2 de Septiembre de 2010, de LIPOXEN TECHNOLOGIES LIMITED: Un compuesto que es un derivado polisacárido N-terminal del GCSF, o de una proteína parecida al GCSF, en el que el polisacárido es el ácido polisiálico […]
COMPLEJOS HIDROSOLUBLES DE SUSTANCIAS MEDICAMENTOSAS CON DERIVADOS DE ALMIDON DE ALTO PESO MOLECULAR, del 22 de Julio de 2010, de SUPRAMOL PARENTERAL COLLOIDS GMBH: Complejo molecular constituido por una sustancia vehículo de alto peso molecular y una sustancia medicamentosa, presentando la sustancia vehículo grupos funcionales, […]