COMPOSICIONES DE LIBERACION CONTROLADA Y NANOPARTICULADAS QUE COMPRENDEN DERIVADOS DE PROSTAGLANDINA.
Composiciones de liberación controlada y nanopartículadas que comprenden derivados de prostaglandina preferentemente limaprost o una sal o derivado de ella,
teniendo biodisponibilidad mejorada. Las partículas tienen un tamaño medio efectivo de alrededor de 2000 nm y son útiles en el tratamiento de síntomas de isquemia. La invención también se refiere a una composición de liberación controlada que incluye un derivado de la prostaglandina, como limaprost alfadex o una nanopartícula, que en operación libera una droga de una manera pulsada o bimodal para el tratamiento de síntomas de isquemia
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2006/013784.
Solicitante: ELAN PHARMA INTERNATIONAL LIMITED.
Nacionalidad solicitante: Irlanda.
Dirección: MONKSLAND ATHLONE,COUNTY WESTMEATH.
Inventor/es: LIVERSIDGE, GARY, JENKINS,SCOTT.
Fecha de Publicación: .
Fecha de Concesión: 25 de Junio de 2010.
Clasificación Internacional de Patentes:
- A61K9/16H4
- A61K9/16K
- A61K9/20H4
- A61K9/20K2B
- A61K9/50M
Clasificación PCT:
- A61K31/5575 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › teniendo un ciclo ciclopentano, p. ej. prostaglandina E 2 , prostaglandina F 2-alpha.
- A61K9/16 A61K […] › A61K 9/00 Preparaciones medicinales caracterizadas por un aspecto particular. › Aglomerados; Granulados; Microbolitas.
- A61K9/50 A61K 9/00 […] › Microcápsulas (A61K 9/52 tiene prioridad).
- A61P9/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Medicamentos para el tratamiento de trastornos en el aparato cardiovascular.
Fragmento de la descripción:
Composiciones de liberación controlada y nanoparticuladas que comprenden derivados de prostaglandina.
Campo de la invención
La presente invención se refiere a un método novedoso para tratar pacientes que tienen síntomas isquémicos. En particular, la presente invención se refiere a formas farmacéuticas novedosas para la administración controlada de un derivado de prostaglandina, tal como limaprost alfadex. La presente invención se refiere además a un derivado de prostaglandina nanoparticulado, preferiblemente limaprost, o sales o derivados del mismo, composición que tiene un tamaño medio de partícula eficaz inferior a aproximadamente 2000 nm de diámetro. La presente invención se refiere también a formas farmacéuticas novedosas para la administración controlada de un derivado de prostaglandina nanoparticulado, tal como limaprost o una sal o derivado del mismo, composición para el tratamiento de síntomas isquémicos en un paciente.
Antecedentes de la invención
A. Antecedentes con respecto a derivados de prostaglandina
Las prostaglandinas (PG) son sustancias producidas en la membrana celular que son responsables de provocar una reacción biofiláctica a diversos estímulos. Se ha determinado que la alteración en el equilibrio de las PG en el organismo está asociada con enfermedad. Debido a que las PG muestran diversos efectos biológicos importantes en una cantidad de trazas, se han investigado la síntesis y actividad biológica de las PG naturales y un gran número de derivados de PG para determinar su uso terapéutico.
La prostaglandina E2 (PGE2) es la más común y la más activa biológicamente de las PG de mamífero; ésta muestra la mayoría de las actividades biológicas características de las PG incluyendo vasodilatación, efectos inmunomoduladores, contracción o relajación del músculo liso, inhibición de la secreción gástrica e inhibición de la reabsorción de sodio y se ha usado mucho como un agente oxitócico y presenta un efecto protector en la mucosa intestinal.
La prostaglandina E1 (PGE1) tiene muchas propiedades iguales a las de PGE2 e inhibe también la agregación plaquetaria. La PGE1 es un metabolito del ácido dihomogammalinolénico (DGLA) y es una PG que se produce de manera natural en el ser humano. La PGE1 es un potente agente vasodilatador que aumenta el flujo sanguíneo periférico. La PGE1 tiene también muchos otros efectos biológicos tales como broncodilatación y mediación de la inflamación.
Sin embargo, debido a que PGE2 y PGE1 son químicamente inestables, son malas para conservar sus efectos farmacológicos y es difícil aplicarlas al uso práctico. La diligencia en el desarrollo de PG nativas y sus derivados y análogos estructurales para el tratamiento de seres humanos, ha dado como resultado la formulación de varios fármacos basados en derivados de PG que se comercializan en la actualidad. Por ejemplo, limaprost es un derivado de PGE1 con modificaciones estructurales destinadas a proporcionarle una semivida prolongada y una potencia superior.
Limaprost se ofrece con la marca comercial registrada OPALMON® por Ono Pharmaceutical Co., Ltd. de Japón. El nombre químico para OPALMON® es compuesto de inclusión de a-ciclodextrina de ácido (E)-7-{(1R,2R,3R)-3-hidroxi-2-[(3S,5S)-E-3-hidroxi-5-metil-1-nonenil]-5-oxociclopentil}-2-heptanoico. OPALMON® contiene limaprost como un clatrato de ciclodextrina (limaprost) que tiene la fórmula molecular C22H36O5aC36H60O30 y la siguiente fórmula estructural:
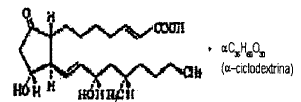
Limaprost se encuentra en forma de un polvo blanco. Es muy soluble en agua, muy ligeramente soluble en etanol y prácticamente insoluble en acetato de etilo y dietil éter. Es higroscópico.
Los comprimidos de OPALMON® son un derivado de PGE1 administrado por vía oral. Una dosificación típica en adultos de limaprost es de 15-30 µg al día en tres dosis divididas administradas como un comprimido oral.
Siendo una forma modificada de PGE1, limaprost es 10-1.000 veces más potente que PGE1 como inhibidor de la adhesividad plaquetaria, tal como se mide in vitro. La inyección intracoronaria (100 ng/kg) o inyección intravenosa (3 µg/kg) en perros anestesiados produce vasodilatación y aumenta el flujo sanguíneo coronario en un 60-80%. Se observaron efectos hipotensores significativos a 100 y 300 µg/kg por vía oral en ratas. Limaprost ejerce efectos potentes sobre la vasodilatación, aumento del flujo sanguíneo e inhibición de la agregación plaquetaria, y de este modo ha demostrado efectos clínicos sobre diversos síntomas isquémicos tales como úlcera, dolor y sensación de frío asociados con tromboangitis obliterante, así como aquellos sobre síntomas subjetivos (dolor y entumecimiento de piernas) y capacidad de andar asociada con estenosis de la columna lumbar adquirida.
El hecho de que los derivados de PG, preferiblemente la PGE1, tienen el efecto de aumentar el flujo sanguíneo, los hace útiles para la prevención y/o el tratamiento de una variedad de síntomas isquémicos. La isquemia se produce como un resultado de un suministro insuficiente de sangre a un órgano, normalmente, pero no siempre, debido a una arteria bloqueada. La isquemia miocárdica es un estado intermedio en la enfermedad de la arteria coronaria durante el - que el tejido cardiaco se ve privado lenta o - repentinamente de oxígeno y otros nutrientes. Finalmente, el tejido cardiaco afectado morirá. Cuando el flujo sanguíneo está completamente bloqueado al corazón, la isquemia puede conducir a un infarto de miocardio. La isquemia puede producirse también en las arterias del cerebro, en las que los bloqueos pueden conducir a un accidente cerebrovascular. Aproximadamente el 80-85% de todos los accidentes cerebrovasculares son isquémicos. La mayoría de los bloqueos en las arterias cerebrales se deben a un coágulo sanguíneo, con frecuencia en una arteria estrechada por placa. La isquemia puede producir también disfunción eréctil bloqueando el flujo sanguíneo rico en oxígeno a través de los vasos sanguíneos hasta el pene. La administración de la PGE1 vasodilatadora o derivados de la misma se ha considerado un tratamiento eficaz para éstos y otros síntomas isquémicos.
Se describen derivados de PG, por ejemplo, en la patente estadounidense número 5.690.957 para "Prostaglandin Derivatives". Esta patente describe derivados de éster de PGE1 o clatratos de ciclodextrina de los mismos, formulaciones de liposomas que los contienen, composiciones farmacéuticas que los contienen y método para usar derivados de PGE1 para la prevención y el tratamiento del trastorno de la circulación periférica, úlcera de decúbito, úlceras de piel o para el mantenimiento del flujo sanguíneo después de una cirugía vascular reparadora.
Los derivados de PG son de alto valor terapéutico para el tratamiento de síntomas isquémicos. Sin embargo, dado que los derivados de PG, por ejemplo, limaprost alfadex, requieren la administración oral tres veces al día, el cumplimiento estricto del paciente es un factor critico en la eficacia de los derivados de PG en el tratamiento de síntomas isquémicos. Además, tal administración frecuente requiere con frecuencia la atención de profesionales sanitarios y contribuye al coste elevado asociado con los tratamientos que implican derivados de PG tales como limaprost alfadex. Por tanto, en la técnica existe una necesidad de composiciones de derivado de PG que superen éstos y otros problemas asociados con su uso en el tratamiento de síntomas isquémicos.
Entonces, la presente invención se refiere a una composición para la liberación controlada de un derivado de PG, preferiblemente limaprost alfadex. La presente invención se refiere también a una formulación nanoparticulada de limaprost o una sal o derivado del misma que tiene una biodisponibilidad mejorada. La presente invención se refiere también a una composición para la liberación controlada de un derivado de PG nanoparticulado, por ejemplo limaprost nanoparticulado o una sal o derivado del mismo, tal como se describe en detalle en el presente documento. En particular, la presente invención se refiere a composiciones de liberación controlada que en funcionamiento suministran un derivado de PG o un derivado de PG nanoparticulado en una manera de liberación pulsátil o de orden cero constante o una composición nanoparticulada de liberación inmediata con biodisponibilidad mejorada. La presente invención...
Reivindicaciones:
1. Composición de derivado de prostaglandina nanoparticulada estable que comprende:
2. Composición según la reivindicación 1, en la que dicha partícula de derivado de prostaglandina se selecciona del grupo que consiste en una fase cristalina, una fase amorfa, una fase semicristalina y mezclas de las mismas.
3. Composición según la reivindicación 1, en la que la composición se formula para la administración seleccionada del grupo que consiste en comprimidos, cápsulas, sobres, soluciones, dispersiones orales y mezclas de los mismos.
4. Composición según la reivindicación 1, en la que la composición comprende además uno o varios excipientes, vehículos farmacéuticamente aceptables o una combinación de los mismos.
5. Composición según la reivindicación 1, en la que dicho derivado de prostaglandina está presente en una cantidad que consiste en desde aproximadamente el 99,5% hasta aproximadamente el 0,001%, desde aproximadamente el 95% hasta aproximadamente el 0,1% y desde aproximadamente el 90% hasta aproximadamente el 0,5% en peso, basado en el peso combinado total del derivado de prostaglandina y al menos un estabilizador de superficie, que no incluye otros excipientes.
6. Composición según la reivindicación 1, en la que el al menos un estabilizador de superficie está presente en una cantidad de desde aproximadamente el 0,5% hasta aproximadamente el 99,999% en peso, desde aproximadamente el 5,0% hasta aproximadamente el 99,9% en peso y desde aproximadamente el 10% hasta aproximadamente el 99,5% en peso, basado en el peso en seco combinado total del derivado de prostaglandina y al menos un estabilizador de superficie, que no incluye otros excipientes.
7. Composición según la reivindicación 1, en la que el estabilizador de superficie se selecciona del grupo que consiste en un estabilizador de superficie aniónico, un estabilizador de superficie catiónico, un estabilizador de superficie zwitteriónico y un estabilizador de superficie iónico.
8. Composición según la reivindicación 1, en la que dicho derivado de prostaglandina es limaprost y que comprende:
9. Composición según la reivindicación 8, que comprende además un agente de recubrimiento.
10. Composición según la reivindicación 1, en la que dicho derivado de prostaglandina es limaprost y que comprende:
11. Composición según la reivindicación 10, que comprende además un agente de recubrimiento.
12. Composición según la reivindicación 1, formulado en una forma farmacéutica seleccionada del grupo que consiste en dispersiones líquidas, geles, aerosoles, pomadas, cremas, formulaciones de liberación controlada, formulaciones de fusión rápida, formulaciones liofilizadas, comprimidos, cápsulas, formulaciones de liberación retardada, formulaciones de liberación prolongada, formulaciones de liberación pulsátil y formulaciones mixtas de liberación inmediata y de liberación controlada.
13. Composición según la reivindicación 1, que comprende adicionalmente uno o varios principios activos útiles para el tratamiento de síntomas isquémicos.
14. Composición según la reivindicación 1, en la que dicho(s) uno o varios principio(s) activo(s) es/son útil(es) en el tratamiento de enfermedades seleccionadas del grupo que consiste en úlcera, dolor y sensación de frío asociados con tromboangitis obliterante, dolor y entumecimiento de piernas, capacidad de andar asociada con estenosis de la columna lumbar adquirida, isquemia miocárdica, accidente cerebrovascular, disfunción eréctil, trastorno de la circulación periférica o úlcera de decúbito.
15. Método de preparación de un derivado de prostaglandina nanoparticulado que comprende poner en contacto partículas de dicho derivado de prostaglandina con al menos un estabilizador de superficie durante un tiempo y en condiciones suficientes para proporcionar una composición de derivado de prostaglandina nanoparticulada que tiene un tamaño medio de partícula eficaz inferior a aproximadamente 2000 nm de diámetro.
16. Método según la reivindicación 15, en el que dicha puesta en contacto comprende:
17. Uso de un derivado de prostaglandina nanoparticulado oral que comprende partículas de dicho derivado de prostaglandina que tiene al menos un estabilizador de superficie asociado con la superficie de las mismas, en el que las partículas tienen un tamaño de partícula eficaz inferior a aproximadamente 2000 nm de diámetro, en la preparación de un medicamento para el tratamiento de síntomas isquémicos.
18. Composición de liberación controlada que comprende: (A) una primera población de partículas que contienen derivado de prostaglandina que permite la liberación inmediata o inmediata retardada de dicho derivado de prostaglandina de la misma; y (B) al menos una población posterior de partículas que contienen prostaglandina que permite la liberación modificada de dicho derivado de prostaglandina de la misma; permitiendo dicha composición la administración del derivado de prostaglandina de una manera pulsátil o de orden cero.
19. Composición según la reivindicación 18, en la que dicha liberación modificada se consigue usando un recubrimiento de liberación modificada, un material de matriz de liberación modificada o ambos.
20. Composición según la reivindicación 18, en la que la cantidad de principio activo contenida es de desde aproximadamente 0,1 mg hasta 500 mg.
21. Composición según cualquiera de las reivindicaciones 18-20, en la que la composición está contenida en una cápsula de gelatina dura o de gelatina blanda.
22. Uso de una composición según la reivindicación 18, en la preparación de un medicamento para el tratamiento de síntomas isquémicos
23. Composición que comprende: (A) partículas que contienen derivado de prostaglandina que permite la liberación modificada de derivado de prostaglandina de las mismas; y (B) una capa de derivado de prostaglandina recubierta sobre la parte superior de dichas partículas que permite la liberación inmediata de dicho derivado de prostaglandina.
24. Composición según la reivindicación 1, que permite la liberación modificada de dicho derivado de prostaglandina.
25. Composición según la reivindicación 24, en la que dicha liberación modificada se consigue usando un recubrimiento de liberación modificada, un material de matriz de liberación modificada o ambos.
26. Composición según la reivindicación 1, en la que dicha composición comprende partículas de liberación inmediata.
Patentes similares o relacionadas:
PREPARADO FARMACÉUTICO QUE COMPRENDE UN INGREDIENTE ACTIVO DISPERSADO SOBRE UNA MATRIZ, del 27 de Diciembre de 2011, de NYCOMED GMBH: Un preparado, en el que un ingrediente activo seleccionado del grupo de N-(3,5-dicloropirid-4-il)-3ciclopropilmetoxi-4-difluorometoxibenzamida (INN: roflumilast), el […]
COMPOSICIONES FARMACÉUTICAS ESTABILIZADAS QUE COMPRENDEN FESOTERODINA, del 23 de Diciembre de 2011, de UCB PHARMA GMBH: Una composición farmacéutica que comprende fesoterodina o una sal o solvato farmacéuticamente aceptable de la misma y un estabilizante farmacéuticamente […]
GRANULADO QUE CONTIENE UNA SUSTANCIA FARMACÉUTICAMENTE ACTIVA Y UN EMULSIONANTE Y MÉTODO PARA SU PRODUCCIÓN, del 12 de Diciembre de 2011, de ECHO PHARMACEUTICALS B.V: Un granulado con un diámetro medio ponderado en volumen de 1-200 µm y que contiene: - al menos 0,1 % en peso de una sustancia farmacéuticamente activa; - al menos 10 […]
ADMINISTRACIÓN PULMONAR DE AMINOGLUCÓSIDOS, del 8 de Septiembre de 2011, de NOVARTIS AG: Una composición de polvo seco dispersable para la administración localizada a los pulmones, para utilizar en el tratamiento o prevención de infecciones respiratorias, […]
NUEVA FORMA DE SUPOSITORIO QUE COMPRENDE UN COMPUESTO ACTIVO ÁCIDO-LÁBIL, del 5 de Julio de 2011, de NYCOMED GMBH: Un supositorio para compuestos activos ácido-lábiles, en donde el compuesto ácido-lábil es un inhibidor de la bomba de protones ácido-lábil, una sal […]
FORMULACIÓN FARMACEÚTICA QUE COMPRENDE ATORVASTANINA CÁLCICA, del 20 de Junio de 2011, de LEK PHARMACEUTICALS D.D.: Una formulación farmacéutica que comprende atorvastatina cálcica como ingrediente activo y una sustancia de ajuste del pH, caracterizada porque […]
 PROCEDIMIENTO PARA LA PREPARACIÓN DE MICROPARTÍCULAS, del 7 de Junio de 2011, de EVONIK ROHM GMBH: Procedimiento para la preparación de micropartículas, que comprende las etapas a) preparar una masa fundida de polímero que comprende al menos un polímero de soporte y […]
PROCEDIMIENTO PARA LA PREPARACIÓN DE MICROPARTÍCULAS, del 7 de Junio de 2011, de EVONIK ROHM GMBH: Procedimiento para la preparación de micropartículas, que comprende las etapas a) preparar una masa fundida de polímero que comprende al menos un polímero de soporte y […]
COMPOSICIÓN FARMACÉUTICA QUE COMPRENDE LOS DERIVADOS DE 2,3-DIHIDRO-6-NITROIMIDAZO[2,1-B]OXAZOL, del 28 de Marzo de 2011, de OTSUKA PHARMACEUTICAL CO., LTD.: Composición farmacéutica que comprende: (I) por lo menos un compuesto oxazol seleccionado de entre el grupo constituido por compuestos de 2,3-dihidro-6-nitroimidazo[2,1-b]oxazol […]