ANALOGOS PEPTIDICOS DE PACAP.
Un péptido de fórmula (I),
(I),(R1R2) A1-A2-A3-A4-A5-A6-A7-A8-A9-A10-A11-A12-A13-A14-A15-A16-A17-A18-A19
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP99/03020.
Solicitante: SOCIETE DE CONSEILS DE RECHERCHES ET D'APPLICATIONS SCIENTIFIQUES S.A.S..
Nacionalidad solicitante: Francia.
Dirección: 51-53 RUE DU DOCTEUR BLANCHE,75016 PARIS.
Inventor/es: DONG,ZHENG,X.
Fecha de Publicación: .
Fecha Concesión Europea: 25 de Noviembre de 2009.
Clasificación Internacional de Patentes:
- C07K14/575L
Clasificación PCT:
- A61K38/22 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Hormonas (derivados de pro-opiomelanocortina, pro-encefalina o pro-dinorfina A61K 38/33, p. ej. corticotropina A61K 38/35).
- C07K14/575 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › Hormonas.
Clasificación antigua:
- A61K38/22 A61K 38/00 […] › Hormonas (derivados de pro-opiomelanocortina, pro-encefalina o pro-dinorfina A61K 38/33, p. ej. corticotropina A61K 38/35).
- C07K14/575 C07K 14/00 […] › Hormonas.
Fragmento de la descripción:
Análogos peptídicos de PACAP.
Antecedentes de la invención
La presente Invención se dirige a nuevos análogos de PACAP (polipéptido activador de la adenilato ciclasa hipofisaria) y a su uso para tratar afecciones y/o enfermedades descritas en el presente documento.
Se resume una revisión del PACAP y de su función fisiológica en Christophe, J., Biochimica et Biophysica Acta, 1154, 183-199(1993), como sigue.
El PACAP es un miembro de una superfamilia que ya incluye varios péptidos reguladores, p. ej., VIP, PHI, PHV, secretina, helodermina, helospectina I y II, glucagón, GIP y GRF. Este péptido biológicamente activo existe en dos formas amidadas: PACAP(1-38)-NH2 (PACAP-38) y PACAP(1-27)-NH2 (PACAP-27). La secuencia de aminoácidos deducida de PACAP-38 en el hombre (Kimura, C, y col., Biochem. Biophys. Res. Commun., 166, 81-89, (1990)) y la rata (Ogi, K., y col., Biochem. Biophys. Res. Commun., 173, 1271-1279, (1990)) es idéntica a la del PACAP-38 ovino aislado.
Se han descrito al menos dos clases de receptores de PACAP en tejidos mamíferos y lineas celulares: los receptores de tipo I que prefieren PACAP y los receptores de tipo II que se unen a PACAP-27, PACAP-38 y VIP (péptido intestinal vasoactivo) (Cauvin, A., y col., Peptides, 11, 773-777 (1990) y Shivers, B.D., y col., Endocrinology, 128, 3055-3065 (1991)). Además, el primer tipo es capaz de presentar dos subtipos, y el segundo tipo se puede dividir provisionalmente en 3 subtipos.
El tipo I es muy selectivo en cuanto que reconoce PACAP-27 y PACAP-38 de forma mucho más potente que VIP. Por lo tanto PACAP-27 y PACAP-38 pueden activar la adenilato ciclasa con la misma alta potencia y eficacia. Sin embargo, los receptores de tipo I pueden estar presentes como dos subtipos (o estados) que coexisten, basándose en la unión de radioligandos. En las membranas de cerebro de rata (Cauvin, A., y col., Regul. Pept. 35, 161-173, (1991)), el subtipo PACAP-A no presenta prácticamente ninguna preferencia por PACAP-38 frente a PACAP-27, mientras que el subtipo PACAP-B reconoce PACAP-38 con una alta afinidad y PACAP-27 con baja afinidad.
El receptor de tipo II es el receptor VIP clásico. Basándose en la afinidad de unión y activación de la adenilato ciclasa, ahora parece que el receptor de tipo II no es selectivo, puesto que muestra una afinidad alta similar por PACAP-27, PACAP-38 y VIP.
Ya se ha establecido un espectro relativamente integral de las actividades farmacológicas para las funciones fisiológicas de PACAP.
En relación con el eje hipotálamo-hipofisario, el PACAP reduce la ingestión de alimento en ratones y eleva la arginina vasopresina en el plasma en ratas, probablemente a través de las neuronas PACAP-ir (ir = inmunorreactivo) en los núcleos paraventricular y supraóptico que se proyectan a la neurohipófisis. El PACAP que se origina en el hipotálamo también puede ser transportado a la pituitaria anterior a través de los vasos portales. Los datos sobre la antehipófisis sugieren una función en la reproducción y crecimiento. El PACAP estimula la adenilato ciclasa y aumenta el [Ca2+] en células gonadotrópicas, somatotrópicas y folículoestrelladas. Aumenta la secreción de a-MSH de melanotropos y la de interleuquina-6 de las células folículoestrelladas hipofisarias. El PACAP potencia los efectos de la LHRH (o GnRH, hormona liberadora de gonadotropina) en la secreción de LH (hormona luteinizante) y FSH. De forma quizás más clara, el PACAP aumenta la síntesis de LH, GH (hormona de crecimiento), PRL (prolactina) y ACTH después de 1-2 días En patología humana, PACAP-27 y PACAP-38 estimulan la actividad de la adenilato ciclasa en membranas de adenomas hipofisarios no productores
, que producen gonadotropina, GH y ACTH.
En el cerebro, y fuera del hipotálamo, el PACAP estimula la síntesis de melatonina de los pinealocitos y puede tener una función en la integración de entradas visuales y en la memoria. La amplia distribución de receptores de PACAP de tipo I contrasta con la localización más concentrada de los receptores de VIP-PACAP de tipo II. Los tipos de receptores en el ojo del conejo pueden contribuir a la fisiología de la retina y coroide. En general, el aumento neuronal de AMPc y Ca2+ puede contribuir al desarrollo cerebral precoz, reparación y modificación de los circuitos, con la ayuda de factores neurotrópicos de los astrocitos que también son estimulados por el PACAP.
Los receptores de tipo I representan una minoría (20%) comparado con los receptores de tipo II en el hígado de rata. El PACAP relaja directamente la motilidad del tracto digestivo por activación de los canales de K+ activados por calcio sensibles a apamina y es un neuropéptido secretor de aniones en la mucosa yeyunal de rata, posiblemente a través de las neuronas submucosas. El PACAP contrae la vesícula biliar en perros conscientes por un mecanismo pregangliónico. In vivo aumenta la secreción de amilasa por un mecanismo colinérgico en el perro y libera glucagón en la rata.
El PACAP provoca la hipersecreción y síntesis de catecolaminas de las glándulas suprarrenales de rata y facilita la mitosis, génesis de neuritas y supervivencia de neuroblastos simpatéticos de rata cultivados. Una inyección i.v. de bolo de PACAP induce un cambio bifásico en la presión sanguínea (disminución seguida de aumento) que va acompañado de un cambio bifásico en la resistencia del sistema vascular. La respuesta de subida de la presión sanguínea se debe a la liberación de catecolaminas de la glándula suprarrenal. La acción relajante del PACAP en el los anillos aórticos precontraídos aislados de conejo es 100 veces más potente que la de VIP, sorprendentemente duradera e independiente del endotelio. El PACAP también es un potente microvasodilatador en la piel humana y aquí su acción es de nuevo de larga duración. El PACAP-38 produce un aumento de la velocidad de latido en los cardiomiocitos de rata neonatal y estimula la adenilato ciclasa en membranas de sarcolema de ventrículos porcino y canino. El PACAP relaja el músculo liso vascular y de las vías aéreas en el pulmón de cobaya, rata y gato. El PACAP-ir es abundante en testículos de rata y los receptores de tipo I en espermatozoides pueden tener una función en la movilidad del esperma.
Además, el PACAP puede intervenir en procesos ontogenéticos en el sistema nervioso y modular la mitogénesis y diferenciación (p. ej., extensión de las neuritas) en varias lineas celulares en las que el tumor maligno a veces está en el origen del surgimiento del receptor de tipo I.
Por lo tanto, hay un gran interés en encontrar análogos del PACAP que sean más activos que el PACAP-27 y/o PACAP-38 y/o que tengan una semivida más larga en el paciente.
La patente de Estados Unidos nº 5.208.320 describe algunos péptidos que producen actividad de AMPc. Robberecht, P-, y col., Molecular Pharmacology 42:347-355, (1992) describen una serie de análogos de PACAP-27 y PACAP-38. La publicación PCT WO 96/09064 describe una serie de análogos de PACAP para usar para prevenir o tratar el daño cerebral.
Resumen de la invención
Esta invención se dirige a un péptido de fórmula (I),
o una sal del mismo farmacéuticamente aceptable, indicado grupo A, en el que,
A1 es His o Pal;
A2 es Ser, Thr o hSer;
A3 es Asp o Glu; o
A4 es Gly, ß-Ala, Gaba, Ava, Aib o Acc;
A5 es Ile, Leu, Cha, Nle, Val, Tle, Abu, Aib, Acc o Nva;
A6 es Phe, ß-Nal, Tyr o Trp;
A7 es Thr, Ser o Val;
A8 es Asp o Glu;
A9 es Ser, Thr o hSer;
A10 es Tyr, Phe, Amp, ß-Nal o Trp;
A11...
Reivindicaciones:
1. Un péptido de fórmula (I),
o una sal del mismo farmacéuticamente aceptable, en el que,
A1 es His o Pal;
A2 es Ser, Thr o hSer;
A3 es Asp o Glu; o
A4 es Gly, ß-Ala, Gaba, Ava, Aib o Acc;
A5 es Ile, Leu, Cha, Nle, Val, Tle, Abu, Aib, Acc o Nva;
A6 es Phe, p-Nal, Tyr o Trp;
A7 es Thr, Ser o Val;
A8 es Asp o Glu;
A9 es Ser, Thr o hSer;
A10 es Tyr, Phe, Amp, ß-Nal o Trp;
A11 es Ser, Thr o hSer;
A12, A14 y A15 se selecciona cada uno independientemente del grupo que consiste en Arg, Lys, Orn y hArg;
A13 es Tyr, Phe, Amp, ß-Nal o Trp;
A16 es Gln, Glu, Asp o Asn;
A17 es Met, Leu, Nle, Abu, Tle, Val, Ile, Cha, Ala, Aib, Acc o Nva;
A18 es Ala, Aib o Acc;
A19 es Val, Leu, Ile, Ala, Abu, Tle, Cha, Aib, Acc, Nle o Nva;
A20, A21, A29, A30, A32, A34, A36 y A38 se selecciona cada uno independientemente del grupo que consiste en Lys, Arg, Orn y hArg;
A22 es Tyr, Phe, Amp, ß-Nal o Trp;
A23 es Leu, Ile, Nle, Tle, Met, Val, Ala, Aib, Acc, Cha, Abu o Nva;
A24 es Ala, Aib; Val, Abu, Acc, Ile, Leu, Nle, Tle o Nva;
A25 es Ala, Aib, Val, Abu, Acc, Ile, Leu, Nle, Nva o Tle;
A26 es Val, Leu, Ile, Ala, Abu, Tle, Cha, Aib, Acc, Nva o Nle;
A27 es Leu, Ile, Nle, Tle, Met, Val, Ala, Aib, Acc, Nva, Cha, o Abu;
A28 es Gly, Aib, Acc, ß-Ala, Gaba o Ava;
A31 es Tyr, Phe, Amp, ß-Nal o Trp;
A33 es Gln, Asn, Glu o Asp;
A35 es Val, Leu, Ile, Ala, Abu, Tle, Cha, Aib, Nva, Acc o Nle;
A37 es Asn, Gln, Asp, Glu, Ala, Aib o Acc;
R1 y R2 se selecciona cada uno independientemente del grupo que consiste en H;
R3 es OH o NH2
caracterizado porque al menos uno de A2, A17, A18, A19, A23, A27, A28 y A35 es Acc, o una sal del mismo farmacéuticamente aceptable.
2. Un péptido de acuerdo con la reivindicación 1, de fórmula (I),
o una sal del mismo farmacéuticamente aceptable, en el que,
A1 es His;
A2 es Ser;
A3 es Asp;
A4 es Gly o ß-Ala;
A5 es Ile o Acc;
A6 es Phe;
A7 es Thr;
A8 es Asp;
A9 es Ser;
A10 es Tyr;
A11 es Ser;
A12 es Arg;
A13 es Tyr;
A14 es Arg;
A15 es Lys;
A16 es Gln o Glu;
A17 es Met, Leu, Nle o Acc;
A18 es Ala, Aib o Acc;
A19 es Val o Acc;
A20 es Lys;
A21 es Lys;
A22 es Tyr;
A23 es Leu o Acc;
A24 es Ala o Aib;
A25 es Ala, Glu, o Aib;
A26 es Val;
A27 es Leu o Acc;
A28 es Gly, Acc, ß-Ala, Gaba o Ava;
A29 es Lys;
A30 es Arg;
A31 es Tyr;
A32 es Lys;
A33 es Gln o Glu;
A34 es Arg;
A35 es Val o Acc;
A36 es Lys;
A37 es Asn o Aib;
A38 es Lys;
R1 y R2 se selecciona cada uno independientemente del grupo que consiste en H
R3 es OH o NH2.
3. Un péptido de acuerdo con la reivindicación 1 ó 2, en el que al menos uno de A5, A17, A18, A19, A23, A27, A28 y A35 es A6c o A5c, o una sal del mismo farmacéuticamente aceptable.
4. Un péptido de acuerdo con la reivindicación 3, en el que al menos uno de A5, A18 y A19 es A5c, o una sal del mismo farmacéuticamente aceptable.
5. Un péptido de acuerdo con la reivindicación 3, en el que al menos uno de A17, A19, A23, A27, A28 y A35 es A6c, o una sal del mismo farmacéuticamente aceptable.
6. Un péptido de acuerdo con la reivindicación 4, en el que dicho péptido es [A5c5]hPACAP(1-38)NH2, [A5c19]hPACAP(1-38)NH2, [Leu17, A5c19]hPACAP(1-38)NH2, [Nle17, A5c19]hPACAP(1-38)NH2, [N-a-octadecanoil-His1, A5c19]hPACAP(1-38)NH2, [A5c19, (Lys-N-
7. Un péptido de acuerdo con la reivindicación 5, en el que dicho péptido es [A6c23'27]hPACAP(1-38)NH2, [A6c17]hPACAP(1-38)NH2, [A6c19,23]hPACAP(1-38)NH2, [A6c23]hPACAP(1-38)NH2, [A6c27]hPACAP(1-38)NH2, [A6c28]hPACAP(1-38)NH2, [A6c35]hPACAP(1-38)NH2 o [A6c19]hPACAP(1-38)NH2.
8. Un péptido de acuerdo con la reivindicación 1 ó 2, en el que A28 es ß-Ala, Gaba o Ava, o una sal del mismo farmacéuticamente aceptable.
9. Un péptido de acuerdo con la reivindicación 1 ó 2, en el que al menos uno de A4 y A28 es ß-Ala, o una sal del mismo farmacéuticamente aceptable.
10. Un péptido de acuerdo con la reivindicación 8, en el que A28 es Gaba o Ava, o una sal del mismo farmacéuticamente aceptable.
11. Un péptido de acuerdo con la reivindicación 1 ó 2, en el que al menos uno de A18, A24, A25 y A37 es Aib, o una sal del mismo farmacéuticamente aceptable.
12. Un péptido de acuerdo con la reivindicación 1 ó 2, en el que al menos uno de A18, A25 y A33 son Glu, o una sal del mismo farmacéuticamente aceptable.
13. Un péptido de acuerdo con la reivindicación 1 ó 2, en el que dicho péptido es [A5c19, ß-Ala28]hPACAP(1-38)NH2.
14. Un péptido de acuerdo con la reivindicación 1 ó 2, en el que dicho péptido es [Aib24, A6c27]hPACAP(1-38)NH2, [Aib18, A6c23]hPACAP(1-38)NH2, [Aib18'25, A6c23]hPACAP(1-38)NH2 o [A6c23, Aib25]hPACAP(1-38)NH2.
15.Un péptido de acuerdo con la reivindicación 1 ó 2, en el que dicho péptido es [Glu33, A6c35]hPACAP(1-38)NH2.
16. Una composición farmacéutica que comprende una cantidad eficaz de un péptido de acuerdo con la reivindicación 1 ó 2, o una sal del mismo farmacéuticamente aceptable, y un vehículo farmacéuticamente aceptable.
Patentes similares o relacionadas:
PÉPTIDOS CON PROPIEDADES MEJORADAS QUE TIENEN LA ACTIVIDAD BIOLÓGICA DEL PÉPTIDO INTESTINAL VASOACTIVO (PIV) Y SU USO PARA EL TRATAMIENTO DE ENFERMEDADES PULMONARES, del 9 de Febrero de 2012, de RES INTERNATIONAL SARL: Péptido sintético que tiene la actividad biológica del péptido intestinal vasoactivo (PIV), donde dicho péptido presenta propiedades farmacológicas y/o físicas mejoradas […]
PROCEDIMIENTO PARA LA AMIDACIÓN DE POLIPÉPTIDOS CON AMINOÁCIDOS BÁSICOS C-TERMINALES UTILIZANDO ENDOPROTEASAS ESPECÍFICAS, del 1 de Febrero de 2012, de SANOFI-AVENTIS DEUTSCHLAND GMBH: Procedimiento para la fabricación de péptidos di o polibásicos amidados C-terminales de la fórmula general I en la que (AS)-X-NH2 (I) AS significa […]
PROTEÍNAS DE FUSIÓN DE EXENDINA, del 3 de Enero de 2012, de BIOREXIS PHARMACEUTICAL CORPORATION: Una proteína de fusión que comprende una exendina-4 fusionada con una transferrina modificada (mTf) mediante un polipéptido enlazante, comprendiendo dicha […]
PÉPTIDOS Y COMPOSICIONES MEDICINALES QUE CONTIENEN LOS MISMOS, del 18 de Noviembre de 2011, de ILS INC: Un péptido que consiste en la secuencia de aminoácidos representada por fórmula (I) o una sal farmacéuticamente aceptable de la misma: en la que A representa […]
 COMPOSICIÓN FARMACÉUTICA QUE COMPRENDE UN PÉPTIDO DE EXENDINA-4, del 17 de Mayo de 2011, de AMYLIN PHARMACEUTICALS, INC.: Composición farmacéutica que comprende un péptido de exendina-4 que presenta la secuencia de aminoácidos HGEGTFTSDL SKQMEEEAVR LFIEWLKNGG PSSGAPPPS […]
COMPOSICIÓN FARMACÉUTICA QUE COMPRENDE UN PÉPTIDO DE EXENDINA-4, del 17 de Mayo de 2011, de AMYLIN PHARMACEUTICALS, INC.: Composición farmacéutica que comprende un péptido de exendina-4 que presenta la secuencia de aminoácidos HGEGTFTSDL SKQMEEEAVR LFIEWLKNGG PSSGAPPPS […]
NEUROPÉPTIDOS PARA EL CULTIVO DE ORGANISMOS ACUÁTICOS, del 16 de Febrero de 2011, de CENTRO DE INGENIERIA GENETICA Y BIOTECNOLOGIA (CIGB): La presente invención esta relacionada con la utilización de variantes del Péptido Activador de la Adenilato Ciclasa de Pituitariapara estimular el crecimiento y mejorar […]
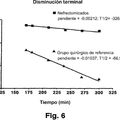 EXENDINA PARA LA SUPRESION DEL GLUCAGON, del 22 de Julio de 2010, de AMYLIN PHARMACEUTICALS, INC.: Compuesto que es una exendina, agonista de la exendina, o exendina modificada o agonista modificado de la exendina para utilizar en la disminución […]
EXENDINA PARA LA SUPRESION DEL GLUCAGON, del 22 de Julio de 2010, de AMYLIN PHARMACEUTICALS, INC.: Compuesto que es una exendina, agonista de la exendina, o exendina modificada o agonista modificado de la exendina para utilizar en la disminución […]
Composiciones que comprenden una proteína de fusión de VIP-ELP para su uso en el tratamiento de fibrosis quística, del 29 de Julio de 2020, de Phasebio Pharmaceuticals, Inc: Una composición farmacéutica que comprende una proteína de fusión que comprende un péptido intestinal vasoactivo (VIP) y uno o más péptidos de tipo elastina (ELP), que […]