Uso de ARN para reprogramar células somáticas.
Un método para producir células que tienen características de célula madre que comprende las etapas de
(i) proporcionar una población de células que comprende células somáticas,
(ii) introducir ARN en al menos una porción de dichas células somáticas, dicho ARN que codifica los factores que inducen el desarrollo de las características de la célula madre en dichas células somáticas, y (iii) permitir el desarrollo de las células que tienen características de célula madre,
en donde el ARN se obtiene por transcripción in vitro o síntesis química.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2008/010593.
Solicitante: BioNTech AG.
Nacionalidad solicitante: Alemania.
Dirección: An der Goldgrube 12 55131 Mainz ALEMANIA.
Inventor/es: SAHIN, UGUR, POLEGANOV,MARCO, BEISSERT,TIM.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C12N15/00 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K).
- C12N5/16 C12N […] › C12N 5/00 Células no diferenciadas humanas, animales o vegetales, p. ej. líneas celulares; Tejidos; Su cultivo o conservación; Medios de cultivo para este fin (reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00). › Células animales.
PDF original: ES-2532125_T3.pdf
Fragmento de la descripción:
Uso de ARN para reprogramar células somáticas Campo de la invención La presente invención proporciona los métodos para desdiferenciar células somáticas en células de tipo madre sin generar embriones o fetos. Más específicamente, la presente invención proporciona los métodos para efectuar la desdiferenciación de células somáticas a células que tienen características de célula madre, particularmente, pluripotencia, mediante la introducción de ARN que codifica factores que inducen la desdiferenciación de las células somáticas en células somáticas y cultivar la células somáticas permitiendo desdiferenciar las células. Después que se desdiferencian, las células se pueden inducir para re-diferenciar en la misma o un tipo de célula somática diferente, tal como neuronal, hematopoyética, muscular, epitelial, y otros tipos de células. Las células-madre derivadas por la presente invención tienen aplicaciones médicas para el tratamiento de enfermedades degenerativas mediante "terapia celular" y se pueden usar en nuevas estrategias terapéuticas en el tratamiento de trastornos cardíacos, neurológicos, endocrinológicos, vasculares, de la retina, dermatológicos, musculatura-esquelética, y otras enfermedades.
Antecedentes de la invención Las células madre denominadas además células progenitoras son células con capacidades para auto renovarse, permanecer indiferenciadas, y para volverse diferenciadas en uno o más tipos de células especializadas con fenotipos maduros. Las células madre no son terminalmente diferenciadas y no están en el final de una vía de diferenciación.
Las células totipotentes contienen toda la información genética necesaria para crear todas las células del cuerpo, que incluyen las células de la placenta. Las células humanas tienen esta capacidad totipotente sólo durante las primeras divisiones de un óvulo fecundado. Después de tres a cuatro divisiones de células totipotentes, sigue una serie de etapas en las que las células se vuelven cada vez más especializadas. La siguiente etapa de división resulta en células pluripotentes, que son muy versátiles y pueden dar lugar a cualquier tipo de célula, excepto las células de la placenta u otros tejidos de soporte del útero. En la etapa siguiente, las células se vuelven multipotentes, lo que significa que pueden dar lugar a varios otros tipos de células, pero esos tipos son limitados en número. Al final de la cadena larga de divisiones celulares que componen el embrión estan las células "terminalmente diferenciadas" que se consideran estar comprometidas permanentemente a una función específica.
Existen tres grupos principales de células madre: (i) células madre somáticas o adultas (células post-natal) , que existen en todos los organismos post-natales, (ii) células madre embrionarias, que se pueden derivar de una etapa de desarrollo pre-embrionario o embrionario y (iii) células madre fetales (pre-natal) , que se pueden aislar del feto en desarrollo.
Las tecnologías de células madre que implican el aislamiento y uso de células madre embrionarias humanas se han vuelto en un tema importante de la investigación médica. Las células madre embrionarias humanas tienen un potencial para diferenciarse en cualquiera de los tipos de células en el cuerpo humano, que incluyen los tejidos complejos. Se espera que muchas enfermedades que resultan de la disfunción de las células pueden ser susceptibles al tratamiento mediante la administración de células madre embrionarias humanas o células derivadas de células madre embrionarias humanas. La capacidad de las células madre embrionarias pluripotentes para diferenciarse y dar lugar a una pluralidad de células maduras especializadas revela la aplicación potencial de estas células como un medio para sustituir, restaurar o complementar las células dañadas o enfermas, tejidos y órganos. Sin embargo, consideraciones científicas y éticas han frenado el progreso de la investigación que usa células madre embrionarias recuperadas de embriones abortados o embriones formados usando técnicas de fertilización in vitro.
Las células madre adultas están presentes sólo en frecuencias bajas y exhiben potencial de diferenciación restringido y un crecimiento pobre. Un problema adicional asociado con el uso de células madres adultas es que estas células no son inmunológicamente privilegiadas, o pueden perder su privilegio inmunológico después del trasplante, en donde el término "inmunológicamente privilegiada" se usa para denotar un estado donde el sistema inmunitario del receptor no reconoce las células como extrañas. Así, sólo los trasplantes autólogos son posibles en la mayoría de los casos cuando se usan células madre adultas. La mayoría de las formas de terapia de célula madre actualmente previstas son procedimientos médicos personalizados prácticamente y por lo tanto, factores económicos asociados con tales procedimientos limitan su potencial de amplio alcance.
La restauración de la expresión de al menos algunos genes embrionarios específicos medidos se ha observado en células somáticas a continuación de la fusión con células madre embrionarias. Sin embargo, las células resultantes son
híbridas, frecuentemente con un genotipo tetraploide, y por lo tanto no son adecuadas como células normales o histocompatibles para propósitos de trasplante.
El uso de la transferencia nuclear de la célula somática ha demostrado reprogramar adecuadamente el contenido nuclear de la célula somática para adoptar la pluripotencia, sin embargo, plantea un conjunto de preocupaciones además de la posición moral. Las tensiones colocadas tanto en el óvulo como el núcleo introducido son enormes, lo que conduce a una alta pérdida en las células resultantes. Además, el procedimiento se tiene que realizar manualmente bajo un microscopio, y por lo tanto, la transferencia nuclear de la célula somática es muy intensiva en recursos. Adicionalmente, no toda la información genética de las células donadoras se transfiere, se quedan atrás como la mitocondria de la célula donadora que contienen su propio ADN mitocondrial. Las células híbridas resultantes conservan esas estructuras mitocondriales que originalmente pertenecieron al huevo. Como consecuencia, los clones no son copias perfectas del donador del núcleo.
Una etapa importante para las células pluripotentes derivadas del paciente se logró por Takahashi y otros en 2006. Se demostró que la sobreexpresión de factores de transcripción definidos (TFs) que son conocidos para regular y mantener la pluripotencia de células madre (Takahasi y otros, 2006, Cell 126, 663-676; Schulz & Hoffmann, 2007, Epigenetics 2, 37-42) pueden inducir un estado pluripotente de fibroblastos somáticos murinos, denominado células madre pluripotentes inducidas (iPS) . En este estudio los autores identificaron OCT3/4, SOX2, KLF4 y c-MYC que se requieren para la generación de la célula iPS (Takahasi y otros, 2006) . En un estudio posterior los autores demostraron que los mismos TFs son capaces de reprogramar fibroblastos humanos adultos (Takahasi y otros, 2007, Cell 131, 861-872) , mientras que otros atribuyen esta actividad a un cóctel TF modificado compuesto de OCT3/4, SOX2, NANOG y LIN28 respecto fibroblastos humanos (Yu y otros, 2007, Science 318, 1917) o murino (Wernig y otros, 2007, Nature 448, 318324) . Para los estudios iniciales, así como la mayoría de los estudios posteriores los TFs de reprogramación se sobreexpresaron usando vectores retrovirales o lentivirales. Debido al silenciamiento de los promotores virales estos estudios reproduciblemente muestran que la expresión de TFs exógenos se suspende durante el proceso de reprogramación (revisado por Hotta & Ellis, 2008, J. Cell Biochem. 105, 940-948) . En consecuencia, el estado pluripotente se mantiene por los factores de transcripción endógenos activados. Además, el silenciamiento de TFs expresados viralmente es requisito previo para la posterior re-diferenciación de las células iPS a precursores específicos a tejido (Yu y otros, 2007) . Una desventaja importante de la entrega viral es la reactivación estocástica de los retrovirus integrados que codifican oncogenes potentes, que en el caso de c-MYC conduce a la inducción de tumores en ratones quiméricos (Okita y otros, 2007, Nature 448, 313-317) . Mientras tanto se ha demostrado que la generación de células iPS es posible en ausencia de MYC (Nakagawa y otros, 2008, Nat. Biotechnol., 26 (1) , 101 -106) . En general, sólo OCT4 y SOX2 se reportaron ser esencial para la reprogramación, los oncogenes como MYC y KLF4 parecen actuar como potenciadores (McDevitt & Palecek, 2008, Curr. Opin. Biotechnol. 19, 527-33) . En consecuencia se demostró que otros productos génicos transformantes como... [Seguir leyendo]
Reivindicaciones:
1. Un método para producir células que tienen características de célula madre que comprende las etapas de (i) proporcionar una población de células que comprende células somáticas, (ii) introducir ARN en al menos una porción de dichas células somáticas, dicho ARN que codifica los factores que inducen el desarrollo de las características de la célula madre en dichas células somáticas, y (iii) permitir el desarrollo de las células que tienen características de célula madre,
en donde el ARN se obtiene por transcripción in vitro o síntesis química.
2. El método de la reivindicación 1, en donde dicho ARN es el ARN capaz de expresar OCT4 y el ARN capaz de expresar SOX2.
3. El método de la reivindicación 2 en donde el método comprende además introducir el ARN capaz de expresar NANOG y/o ARN capaz de expresar LIN28.
4. El método de la reivindicación 2 o 3 en donde el método comprende además introducir el ARN capaz de expresar KLF4 y/o el ARN capaz de expresar c-MYC.
5. El método de cualquier una de las reivindicaciones 1 a 4, en donde las células que tienen características de célula madre presentan un estado pluripotente.
6. El método de cualquier una de las reivindicaciones 1 a 5, en donde dichas células somáticas son fibroblastos, 25 preferentemente fibroblastos de pulmón, fibroblastos de prepucio o fibroblastos dérmicos.
7. El método de cualquier una de las reivindicaciones 1 a 6, en donde dicho ARN se introduce en dicha al menos una porción de células somáticas por electroporación.
Patentes similares o relacionadas:
Métodos mejorados para producir terapias celulares adoptivas, del 22 de Abril de 2020, de Bluebird Bio, Inc: Un método in vitro para producir un producto terapéutico de células T que comprende: a) proporcionar una población de células mononucleares […]
Anticuerpos anti-ricina y sus usos, del 8 de Abril de 2020, de HER MAJESTY THE QUEEN IN RIGHT OF CANADA AS REPRESENTED BY THE MINISTER OF NATIONAL DEFENCE: Un anticuerpo, aislado o purificado, o fragmento de este, que comprende una cadena ligera variable que comprende una CDR L1 de secuencia KASQDINNYLR […]
Usos de anticuerpos IL-1 alfa, del 18 de Marzo de 2020, de XBIOTECH, INC: Un método para cuantificar la cantidad de IL-1α en una muestra biológica, el método comprendiendo las etapas de: (a) separar una muestra biológica […]
Uso de moléculas inhibidoras de semaforina-4D en combinación con una terapia inmunomoduladora para inhibir el crecimiento tumoral y la metástasis, del 8 de Enero de 2020, de Vaccinex, Inc: Un anticuerpo aislado o fragmento de unión a un antígeno del mismo que se une específicamente a semaforina-4D (SEMA4D) para su uso en la inhibición, el retraso o la reducción […]
Sistemas y procedimientos de anticuerpos anti-SOX10, del 11 de Diciembre de 2019, de Biocare Medical, LLC: Preparación aislada de un anticuerpo monoclonal de ratón que se une específicamente a una proteína SOX10, en la que dicho anticuerpo monoclonal de […]
 Producción de células provenientes de líneas neurales a partir de sangre, del 25 de Septiembre de 2019, de KWALATA TRADING LIMITED: Una composición de materia, derivada por la estimulación in vitro de una población de células centrales (CCP) derivada de la sangre de al menos 5 millones […]
Producción de células provenientes de líneas neurales a partir de sangre, del 25 de Septiembre de 2019, de KWALATA TRADING LIMITED: Una composición de materia, derivada por la estimulación in vitro de una población de células centrales (CCP) derivada de la sangre de al menos 5 millones […]
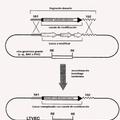 Producción de anticuerpos híbridos que contienen regiones variables humanas y regiones constantes de roedor, del 26 de Junio de 2019, de REGENERON PHARMACEUTICALS, INC.: Un procedimiento para modificar genéticamente un locus génico endógeno de la región variable de cadena pesada de inmunoglobulina en una célula madre embrionaria (ES) de […]
Producción de anticuerpos híbridos que contienen regiones variables humanas y regiones constantes de roedor, del 26 de Junio de 2019, de REGENERON PHARMACEUTICALS, INC.: Un procedimiento para modificar genéticamente un locus génico endógeno de la región variable de cadena pesada de inmunoglobulina en una célula madre embrionaria (ES) de […]
Producción de polipéptidos recombinantes, del 12 de Junio de 2019, de MEDIMMUNE, LLC: Un método para producir un polipéptido recombinante en un cultivo celular de ovario de hámster chino (CHO), comprendiendo el método: (a) cultivar células CHO que tienen […]