Vacunas recombinantes y utilización de las mismas.
Molécula de fusión que comprende un antígeno, una región transmembranaria y la región citoplásmica de unacadena de una molécula de MHC,
en la que la molécula de fusión no comprende ninguno de los siguientes: (i)dominios α1, α2 y α3 de la cadena α de una molécula de MHC de clase I, (ii) ß2-microglobulina de una molécula deMHC de clase I, (iii) dominios α1 y α2 de la cadena α de una molécula de MHC de clase II y (iv) dominios ß1 y ß2 dela cadena ß de una molécula de MHC de clase II.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2004/011512.
Solicitante: BioNTech AG.
Nacionalidad solicitante: Alemania.
Dirección: Hölderlinstrasse 8 55131 Mainz ALEMANIA.
Inventor/es: TURECI, OZLEM, SAHIN, UGUR, KREITER,SEBASTIAN.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/7088 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › Compuestos que tienen al menos tres nucleósidos o nucleótidos.
- A61K38/17 A61K […] › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › que provienen de animales; que provienen de humanos.
- C07K14/47 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › de mamíferos.
- C07K14/705 C07K 14/00 […] › Receptores; Antígenos celulares de superficie; Determinantes celulares de superficie.
- C12N15/62 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Secuencias de ADN que codifican proteínas de fusión.
PDF original: ES-2400249_T3.pdf
Fragmento de la descripción:
Vacunas recombinantes y utilización de las mismas.
La presente invención se refiere a moléculas de fusión de antígenos, a los ácidos nucleicos que las codifican y a la utilización de dichas moléculas de fusión y ácidos nucleicos.
Las moléculas de fusión según la presente invención se pueden utilizar en un gran número de aplicaciones, entre las que se incluye la inducción de una respuesta inmunitaria en un mamífero.
Las reacciones de linfocitos T específicas de antígeno son desencadenadas por péptidos antigénicos unidos a la hendidura de unión de las glucoproteínas del complejo principal de histocompatibilidad (MHC) como parte del mecanismo del sistema inmunitario, en el que se identifican los antígenos extraños y se induce una respuesta a los mismos. Los péptidos antigénicos enlazados interactúan con los receptores de los linfocitos T y de este modo modulan una respuesta inmunitaria. Los péptidos antigénicos están unidos de forma no covalente a determinados “bolsillos de unión” formados por residuos polimórficos de la hendidura de unión de la proteína MHC.
Las moléculas de MHC de clase II son glucoproteínas heterodiméricas formadas por cadenas a y º. Los dominios a1 y º1 de estas moléculas se pliegan y forman una hendidura de unión al péptido. Los péptidos antigénicos se unen a la molécula de MHC mediante la interacción entre los aminoácidos de anclaje del péptido y los dominios a1 y º1. La estructura cristalina del complejo HLA DR1 humano de clase II con un péptido de virus de la gripe pone de manifiesto que los extremos N y C del péptido unido se prolongan fuera de la hendidura de unión, de modo que el extremo C del péptido se encuentra cerca del extremo N de la cadena º. [Brown, J.H. et al, 1993, Nature 364:33-39; Stern, L. J. et al, 1994, Nature 368:215-221]. Las moléculas de MHC de clase I presentan una organización de los dominios distinta de la de las moléculas de MHC de clase II, pero en general se trata de una estructura parecida con un sitio o hendidura de unión al péptido alejado de los dominios de membrana. [Véase, por ejemplo, Rudensky, A.Y. et al, 1991, Nature 353:622-627].
La etapa inicial en la presentación de un antígeno de una proteína extraña es la unión del antígeno nativo a una célula presentadora de antígeno (APC) . Tras unirse a las APC, los antígenos penetran en las células, ya sea por fagocitosis, por endocitosis mediada por receptor o por pinocitosis. Estos antígenos internalizados se encuentran en unas vesículas intracelulares unidas a la membrana llamadas endosomas. Tras la fusión endosoma-lisosoma, los antígenos son procesados por las proteasas celulares presentes en los lisosomas hasta obtenerse péptidos pequeños. Los péptidos se asocian con las cadenas a y º de las moléculas de MHC de clase II dentro de estos lisosomas. Estas moléculas de MHC de clase II, previamente sintetizadas en el retículo endoplasmático rugoso, se transportan sucesivamente a los complejos de Golgi y al compartimento lisosómico. El complejo péptido-MHC se presenta en la superficie de las APC para la activación de los linfocitos T y B. Por consiguiente, la accesibilidad de los sitios de procesamiento proteolítico del antígeno, la estabilidad de los péptidos resultantes en los lisosomas y la afinidad de los péptidos por las moléculas de MHC son factores determinantes para la inmunogenia de un epítopo específico.
Las vacunas recombinantes tienen una importancia particular en la medicina humana y veterinaria como agentes y medicamentos para la profilaxis y el tratamiento de enfermedades infecciosas y cánceres. El objetivo de la vacunación con una vacuna recombinante es inducir una respuesta inmunitaria específica a un antígeno determinado, teniendo dicha respuesta una actividad preventiva o terapéutica contra determinadas enfermedades.
Un factor esencial para la eficacia de una vacuna recombinante es una estimulación óptima de los linfocitos T del organismo inmunizado. Así, una serie de investigaciones experimentales con animales han demostrado que es necesaria una estimulación óptima tanto de los linfocitos CD8+ como de los linfocitos CD4+ para una inmunoterapia efectiva de los tumores. Los principales tipos conocidos de vacunas recombinantes se basan en proteínas recombinantes, fragmentos peptídicos sintéticos, virus recombinantes y vacunas de ácidos nucleicos basadas en ADN o ARN. En años recientes, las vacunas basadas en ácidos nucleicos ADN y ARN han adquirido cada vez más importancia. Sin embargo, se consigue una estimulación muy baja o nula de los linfocitos CD4+ con vacunas recombinantes basadas en ácidos nucleicos para muchos fines, entre otros para antígenos tumorales. Por este motivo, se han desarrollado una serie de modificaciones genéticas con la intención de aumentar la inmunogenia de las vacunas recombinantes. Hasta el momento, se han ensayado diversos métodos en este sentido, entre otros la heterogeneización de inmunógenos mediante la modificación de la secuencia primaria o por fusión a epítopos extraños, por ejemplo, de bacterias o virus [Lowenadler, B. et al, 1990, Eur. J. Immunol. 20: 1541-45; Clarke, B.E. et al, 1987, Nature 330: 381-84] y la preparación de productos quiméricos que consisten en el antígeno real y proteínas inmunomoduladoras, tales como citocinas [Ruckert, R. et al, 1998, Eur. J. Immunol. 28: 3312-20; Harvill, E. T., J. M. Fleming, y S. L. Morrison, 1996, J. Immunol. 157: 3165-70]. Aunque las vacunas basadas en la heterogeneización inducen mejores respuestas inmunitarias, tienen el gran inconveniente de que la inmunoestimulación contra el epítopo extraño predomina y de que, en algunos casos, las respuestas inmunitarias contra el objetivo de la vacuna son sólo moderadas.
Otra posibilidad atractiva es la fusión a secuencias de proteínas destinadas a permitir la translocación de la proteína en los compartimentos celulares que se degradan. Sin embargo, en la actualidad se sabe que estas modificaciones conducen únicamente a una mejora moderada de la estimulación de los linfocitos CD4+ y apenas ninguna mejora de las respuestas inmunitarias de los linfocitos CD8+ [Wu, T.C. et al, 1995, Proc. Natl. Acad. Sci. U.S.A. 92: 1167111675; Bonini, C. et al, 2001, J. Immunol. 166: 5250-57, Su, Z. et al, 2002, Cancer Res. 62: 5041-5048].
Por consiguiente, sería deseable disponer de vacunas que aumentaran significativamente la presentación de antígenos y, por lo tanto, la inmunogenia frente a un antígeno particular. Además, sería deseable que fuera posible modificar sistemáticamente las vacunas de tal modo que se obtuviera la máxima respuesta inmunitaria por parte de los linfocitos CD4+ y CD8+ sin tener que introducir epítopos extraños.
Este objeto se alcanza, según la presente invención, mediante el objeto de las reivindicaciones.
Según la presente invención, se ha podido determinar que las moléculas de fusión que comprenden moléculas de antígeno y partes de antígenos de histocompatibilidad, cuando se utilizan como vacunas, muestran una inmunogenia aumentada en un factor de > 100 en comparación con los antígenos no modificados, y que, sorprendentemente, las respuestas inmunitarias de los linfocitos T CD4+ y CD8+ aumentan de un modo no descrito hasta el momento.
La presente invención se refiere en general a moléculas de fusión de moléculas de antígeno y a la utilización de dichas moléculas de fusión.
En un aspecto, la presente invención se refiere a una molécula de fusión que comprende un antígeno, una región transmembranaria y la región citoplásmica de una cadena de una molécula de MHC, en la que la molécula de fusión no comprende ninguno de los siguientes fragmentos: (i) dominios a1, a2 y a3 de la cadena a de una molécula de MHC de clase I, (ii) 2-microglobulina de una molécula de MHC de clase I, (iii) dominios a1 y a2 de la cadena a de una molécula de MHC de clase II y (iv) dominios 1 y 2 de la cadena de una molécula de MHC de clase II. Resulta preferido que tanto la región transmembranaria como la región citoplásmica se deriven de una molécula de MHC.
De este modo, se da a conocer, en particular, una molécula de fusión que comprende un antígeno y una parte de una cadena de una molécula de MHC, la cual corresponde esencialmente a la secuencia de la región transmembranaria unida a la región citoplásmica de una molécula de MHC, donde la expresión “región transmembranaria unida a la región citoplásmica” se refiere al segmento de una cadena de una molécula de MHC que comienza con el extremo N de la región transmembranaria y termina con el extremo C de la región citoplásmica, en particular, el extremo C de la cadena completa de la molécula de MHC. En esta forma... [Seguir leyendo]
Reivindicaciones:
1. Molécula de fusión que comprende un antígeno, una región transmembranaria y la región citoplásmica de una cadena de una molécula de MHC, en la que la molécula de fusión no comprende ninguno de los siguientes: (i) dominios a1, a2 y a3 de la cadena a de una molécula de MHC de clase I, (ii) 2-microglobulina de una molécula de MHC de clase I, (iii) dominios a1 y a2 de la cadena a de una molécula de MHC de clase II y (iv) dominios 1 y 2 de la cadena de una molécula de MHC de clase II.
2. Molécula de fusión según la reivindicación 1, en la que la región transmembranaria es una región transmembranaria de una molécula de MHC.
3. Molécula de fusión según la reivindicación 1 o 2, en la que la región transmembranaria y la región citoplásmica comprenden una secuencia que corresponde a la región transmembranaria unida a la región citoplásmica de una molécula de MHC.
4. Molécula de fusión según cualquiera de las reivindicaciones 1 a 3, en la que la molécula de fusión comprende además una secuencia líder que puede controlar la translocación de una proteína o péptido a través de una membrana.
5. Molécula de fusión según la reivindicación 4, en la que la secuencia líder es una secuencia líder de una molécula de MHC.
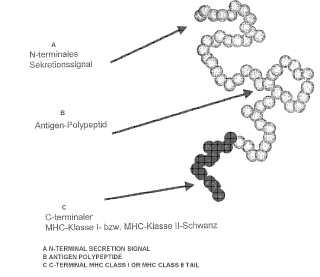
6. Molécula de fusión según la reivindicación 4 o 5, en la que la molécula de fusión presenta la disposición siguiente: extremo N - secuencia líder/antígeno/región transmembranaria/región citoplásmica - extremo C, en la que las regiones individuales pueden estar separadas opcionalmente entre sí mediante secuencias conectoras.
7. Ácido nucleico que codifica una molécula de fusión según cualquiera de las reivindicaciones 1 a 6.
8. Célula hospedadora que comprende un ácido nucleico según la reivindicación 7.
9. Composición farmacéutica que comprende una o más moléculas de fusión según cualquiera de las reivindicaciones 1 a 6 y/o uno o más ácidos nucleicos según la reivindicación 7 y/o una o más células hospedadoras según la reivindicación 8.
10. Composición farmacéutica según la reivindicación 9 en forma de vacuna.
11. Método in vitro para aumentar la cantidad de complejos MHC/péptido en una célula, en el que el método comprende la provisión de una o más moléculas de fusión según cualquiera de las reivindicaciones 1 a 6 y/o de uno
o más ácidos nucleicos según la reivindicación 7 para la célula.
12. Utilización de una o más moléculas de fusión según cualquiera de las reivindicaciones 1 a 6 y/o de uno o más ácidos nucleicos según la reivindicación 7 para la preparación de una composición farmacéutica para aumentar la cantidad de complejos MHC/péptido en una célula.
13. Método in vitro para aumentar la presentación de moléculas de superficie celular sobre las células que pueden presentar antígenos, particularmente linfocitos B y macrófagos, en el que el método comprende la provisión de una o más moléculas de fusión según cualquiera de las reivindicaciones 1 a 6 y/o de uno o más ácidos nucleicos según la reivindicación 7 para las células.
14. Utilización de una o más moléculas de fusión según cualquiera de las reivindicaciones 1 a 6 y/o de uno o más ácidos nucleicos según la reivindicación 7 para la preparación de una composición farmacéutica para aumentar la presentación de moléculas de superficie celular sobre las células que pueden presentar antígenos, particularmente linfocitos B y macrófagos.
15. Método según la reivindicación 11 o 13, o utilización según la reivindicación 12 o 14, en los que el aumento de la cantidad de complejos MHC/péptido o el aumento de la presentación de moléculas de superficie celular incrementa, a su vez, la activación primaria de los linfocitos T, particularmente de los linfocitos CD4+ y CD8+, que responden al antígeno.
16. Utilización de una o más moléculas de fusión según cualquiera de las reivindicaciones 1 a 6 y/o de uno o más ácidos nucleicos según la reivindicación 7 y/o de una o más células hospedadoras según la reivindicación 8 para la preparación de una composición farmacéutica para inducir una respuesta inmunitaria en un ser vivo.
17. Método in vitro para estimular o activar los linfocitos T, particularmente los linfocitos CD4+ y CD8+, en el que el método comprende la provisión para los linfocitos T de una o más moléculas de fusión según cualquiera de las reivindicaciones 1 a 6 y/o de uno o más ácidos nucleicos según la reivindicación 7 y/o de una o más células
hospedadoras según la reivindicación 8.
18. Utilización de una o más moléculas de fusión según cualquiera de las reivindicaciones 1 a 6 y/o de uno o más ácidos nucleicos según la reivindicación 7 y/o de una o más células hospedadoras según la reivindicación 8 para la
preparación de una composición farmacéutica para estimular o activar los linfocitos T, particularmente los linfocitos CD4+ y CD8+, en un ser vivo.
19. Utilización de una o más moléculas de fusión según cualquiera de las reivindicaciones 1 a 6 y/o de uno o más ácidos nucleicos según la reivindicación 7 y/o de una o más células hospedadoras según la reivindicación 8 para la 10 preparación de una composición farmacéutica para el tratamiento, la vacunación o la inmunización de un ser vivo.
Patentes similares o relacionadas:
Cadena ligera de enteroquinasa modificada, del 22 de Julio de 2020, de NOVO NORDISK A/S: Un análogo de la cadena ligera de la enteroquinasa bovina que comprende una secuencia de aminoácidos establecida en la SEQ ID NO: 1, en donde dicho análogo comprende […]
Detección de interacciones proteína a proteína, del 15 de Julio de 2020, de THE GOVERNING COUNCIL OF THE UNIVERSITY OF TORONTO: Un método para medir cuantitativamente la fuerza y la afinidad de una interacción entre una primera proteína de membrana o parte de la misma y una […]
Métodos y composiciones para ingeniería genómica, del 3 de Junio de 2020, de Sangamo Therapeutics, Inc: Una pareja de nucleasas de dedo de zinc (ZFN) que comprende una ZFN izquierda y una ZFN derecha, comprendiendo cada ZFN un dominio de escisión […]
Métodos y composiciones para escisión dirigida y recombinación, del 20 de Mayo de 2020, de Sangamo Therapeutics, Inc: Un método in vitro para la escisión selectiva de un gen HLA clase I, un gen HLA que codifica una proteína de clase 1 del Complejo de Histocompatibilidad Mayor (MHC) […]
Antígenos de coagulasa estafilocócica y métodos para su uso, del 13 de Mayo de 2020, de UNIVERSITY OF CHICAGO: Una composición inmunógena que comprende al menos dos dominios 1-2 de coagulasa estafilocócica diferentes, en donde cada uno de los al menos dos dominios […]
Reconocimiento de unión a diana celular mediante un agente bioactivo usando transferencia de energía de resonancia de bioluminiscencia intracelular, del 6 de Mayo de 2020, de PROMEGA CORPORATION: Un sistema de ensayo que comprende: (a) una biblioteca de agentes bioactivos, cada uno de los cuales está fijado a un fluoróforo; (b) una diana celular fusionada a […]
Etiqueta de epítopo y método de detección, captura y/o purificación de polipéptidos etiquetados, del 15 de Abril de 2020, de ChromoTek GmbH: Péptido epítopo aislado que tiene de 12 a 25 aminoácidos, en donde la secuencia de aminoácidos comprende una secuencia según se define en SEQ ID NO: 32 (X1X2RX4X5AX7SX9WX11X12), […]
Utilización diagnóstica de un polipéptido de fusión que comprende una proteína vírica y un enzima MGMT, del 15 de Abril de 2020, de INSTITUT PASTEUR: Utilización in vitro de un polipéptido de fusión que comprende una proteína vírica y i) el enzima 6-metilguanina-ADN-metiltransferasa (MGMT, EC 2.1.1.63) o un homólogo […]