Construcción de expresión de ADN.
Una construcción de ADN para expresión génica, en la que la construcción es una doble cadena de ADN lineal y de cadena abierta que comprende una secuencia promotora,
una secuencia de codificación y una señal de terminación, en donde la construcción comprende al menos un nucleótido L-ADN y en la que al menos un nucleótido L-ADN está comprendido en el interior de los cinco últimos nucleótidos de un extremo 5' y/o 3'.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2011/073984.
Solicitante: MOLOGEN AG.
Nacionalidad solicitante: Alemania.
Dirección: FABECKSTRASSE 30 14195 BERLIN ALEMANIA.
Inventor/es: SCHROFF, MATTHIAS, KLEUSS,CHRISTIANE, KAPP,KERSTIN.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C12N15/09 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Tecnología del ADN recombinante.
- C12N15/11 C12N 15/00 […] › Fragmentos de ADN o de ARN; sus formas modificadas (ADN o ARN no empleado en tecnología de recombinación C07H 21/00).
- C12N15/85 C12N 15/00 […] › para células animales.
PDF original: ES-2549192_T3.pdf



Fragmento de la descripción:
Construcción de expresión de ADN Campo de la invención
La invención se refiere a una construcción de expresión génica minimalista, a su transferencia en células y a su uso para la expresión génica en aplicaciones de medicina molecular.
Antecedentes de la invención
Las construcciones de expresión génica que pueden transferirse al interior de en una célula de interés se están usando frecuentemente para vacunación con ADN, terapia tumoral y prevención. Las construcciones de vectores para estos propósitos han de garantizar la transfección satisfactoria y un máximo de seguridad para el paciente. Las denominadas construcciones basadas en plásmidos de una doble cadena de ADN cerrada circular que se transfectan física o químicamente en células son relativamente seguras. Sin embargo, dependiendo del tipo de célula de interés, la eficacia de la transfección normalmente no es satisfactoria. Por lo tanto, los plásmidos no son aplicables en protocolos clínicos. Además, incluyen normalmente diversas proteínas procariotas (por ejemplo, genes de resistencia a antibióticos) que se transfieren conjuntamente en la célula. Los promotores procariotas no son absolutamente silenciosos en las células eucariotas lo que puede producir efectos inmunitarios no deseados. El sistema inmunitario del hospedador también puede eliminar las células transfectadas. Adicionalmente, los motivos CG no metilados en los vectores plasmídicos pueden ser inmunoestimuladores y justificar al menos alguna de la inmunotoxicidad observada en protocolos de terapia génica.
Los vectores retrovirales o adenovirales con replicación defectuosa a menudo se emplean en protocolos clínicos debido a su eficacia de transfección mucho más alta en comparación con los plásmidos. Sin embargo, albergan el riesgo sustancial de recombinación con virus de tipo silvestre o de activación de oncogenes. Además, la necesidad de usar altas titulaciones virales puede producir inflamación.
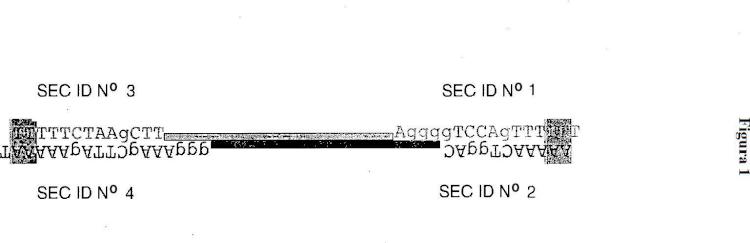
Por lo tanto, el desarrollo de construcciones de expresión génica mejoradas es esencial para superar los efectos secundarios no deseados de los plásmidos y vectores virales. El documento EP 0 941 318 desvela un nuevo tipo de vector, pequeño, lineal, cerrado de manera covalente, con forma de mancuerna, para la expresión génica minimalista, definida inmunológicamente, (MIDGE, Minimalistic Immunologically Defined Gene Expression). La MIDGE es una unidad de transferencia génica de tamaño mínimo; solo contiene el mínimo de secuencias necesarias: el casete de expresión, incluyendo el promotor, el gen y la secuencia estabilizadora de ARN, flanqueada por dos secuencias oligonucleotídicas de horquilla pequeña. Además, el diseño de MIDGE proporciona medios para el transporte eficaz en una célula de interés.
Las moléculas MIDGE son mucho más pequeñas que los plásmidos o los vectores virales usados convencionalmente y son por tanto más fáciles de transferir al interior de las células y permiten tasas de expresión elevadas. Estas incluyen horquillas cortas en ambos extremos para proteger el casete de expresión contra la degradación por nucleasas.
Breve sumario de la invención
Con respecto al estado de la técnica es un objetivo de la presente invención proporcionar una construcción de ADN eficaz para la expresión génica en una célula eucariota, que esté protegida contra la degradación por nucleasas.
De acuerdo con la divulgación se proporciona una construcción de ADN para la expresión génica, en la que la construcción es una doble cadena de ADN lineal y de cadena abierta que comprende un secuencia promotora, una secuencia codificante y una señal de terminación, en la que la construcción comprende al menos un nucleótido L- ADN en el interior de los cinco últimos nucleótidos de un extremo 5 y/o 3. También se incluye dentro del ámbito de la presente divulgación una construcción de ADN lineal, parcialmente monocatenario, con forma de mancuerna, que comprende al menos un nucleótido L-ADN.
Adicionalmente se proporciona una construcción de ADN, en la que al menos un nucleótido L-ADN se localiza en el extremo 5 y/o 3. Un bucle monocatenario puede localizarse en el extremo 5 y/o 3, también en combinación con al menos un nucleótido L-ADN, que se localiza dentro de los 5 últimos nucleótidos del extremo 5 y/o 3.
Una construcción de acuerdo con la divulgación puede comprender una cadena de ADN parcial o completamente bicatenaria. Adicionalmente se pretende que al menos un nucleótido L- o D-ADN se modifique con un grupo funcional seleccionado del grupo que comprende grupos carboxilo, amina, amida, aldimina, cetal, acetal, éster, éter, disulfuro, tiol y aldehido.
El nucleótido puede unirse a un compuesto seleccionado del grupo que comprende péptidos, proteínas, carbohidratos, lípidos, vesículas, anticuerpos, moléculas sintéticas, polímeros, microproyectiles, partículas metálicas,
nanopartículas o una fase sólida.
Se pretende que una construcción de acuerdo con la presente divulgación comprenda un promotor, que se seleccione del grupo que comprenda secuencias promotoras, que sean operativas en células de seres humanos, de animales o eucariotas. La construcción puede codificar proteínas, péptidos, anticuerpos, hormonas, citocinas u otras sustancias biológicamente activas, tales como ARN inhibidores, reguladores o estimuladores o inmunomoduladores.
Un objeto adicional de la presente divulgación es la construcción de ADN descrita anteriormente para la transfección estable o transitoria de células de seres humanos, de animales o eucariotas así como para terapia génica o vacunación con ADN. La expresión "terapia génica" incluye estrategias in vivo o ex vivo así como autólogas o alogénicas.
Un objeto adicional de la presente divulgación es la construcción de ADN descrita anteriormente para la vacunación profiláctica o terapéutica contra enfermedades infecciosas o parásitos.
Un objeto adicional es la construcción de ADN de acuerdo con la presente divulgación para el tratamiento de cáncer o de enfermedades autoinmunitarias, opcionalmente junto con el uso de una construcción de ADN inmunomoduladora no codificante.
Es un objetivo adicional de la presente invención proporcionar una composición farmacéutica que comprenda una construcción de ADN como la desvelada anteriormente. Dicha composición farmacéutica puede comprender adicionalmente un agente quimioterapéutico. Como alternativa, puede contener un antígeno adicional de origen bacteriano, fúngico, parasitario o viral.
Descripción detallada de la invención
Dentro del significado de la presente divulgación, una secuencia de ADN lineal, de cadena abierta lineal, se denomina construcción de ADN. Dicha secuencia de ADN puede ser monocatenaria o parcial o completamente bicatenaria. Las expresiones, construcción de ADN, molécula de ADN y construcción de expresión se usan de manera sinónima y no indican una limitación de la longitud de la secuencia de ADN correspondiente. Los componentes monoméricos de las construcciones de ADN son nucleótidos.
Una construcción de ADN puede fabricarse sintéticamente o puede tener un origen parcial o completamente biológico, en el que el origen biológico incluye métodos de fabricación de secuencias de ADN basados en procedimientos genéticos.
El L-ADN o nucleótidos en conformación L se refiere a nucleótidos que comprenden L-desoxirribosa como el resto de azúcar en lugar de la D-desoxirribosa de origen natural. La L-desoxirribosa es el enantiómero (imagen especular) de la D-desoxirribosa. Las construcciones de ADN que consisten, parcial o completamente, en nucleótidos en conformación L pueden ser, parcial o completamente, monocatenarias o bicatenarias; sin embargo, los nucleótidos en conformación L no pueden hibridar con nucleótidos en conformación D (Hauser et al., Nucleic Acid Res. 2006 34: 5101-11). El L-ADN es igualmente soluble y selectivo que el D-ADN. Incluso, el L-ADN es resistente frente a la degradación enzimática por enzimas de origen natural, especialmente exonucleasas, por tanto el L-ADN está protegido contra la degradación biológica (Urata et al., Nucleic Acids Res. 1992 20: 3325-32). Por lo tanto, el L-ADN es muy ampliamente aplicable.
Un "tallo" de acuerdo con la presente divulgación deberá entenderá como una doble cadena de ADN formada por emparejamiento de bases bien dentro de la misma molécula de ADN (que es entonces parcialmente auto- complementaria) o dentro de moléculas de ADN diferentes (que son parcial o completamente auto- complementarias). El emparejamiento de bases intramolecular designa el emparejamiento de bases dentro de la misma molécula de ADN y el emparejamiento de... [Seguir leyendo]
Reivindicaciones:
1. Una construcción de ADN para expresión génica, en la que la construcción es una doble cadena de ADN lineal y de cadena abierta que comprende una secuencia promotora, una secuencia de codificación y una señal de terminación, en donde la construcción comprende al menos un nucleótldo L-ADN y en la que al menos un nucleótldo L-ADN está comprendido en el interior de los cinco últimos nucleótldos de un extremo 5 y/o 3.
2. La construcción de acuerdo con la reivindicación 1, en la que al menos un extremo de la construcción de ADN comprende un bucle monocatenario.
3 La construcción de acuerdo con cualquiera de las reivindicaciones anteriores, en donde dicha construcción es parcialmente o completamente bicatenaria.
4 La construcción de acuerdo con cualquiera de las reivindicaciones anteriores, en la que al menos un nucleótldo L- ADN o D-ADN se modifica con un grupo funcional seleccionado del grupo que comprende grupos carboxllo, amina, amida, aldimina, cetal, acetal, áster, éter, disulfuro, tiol y aldehido.
5. La construcción de acuerdo con la reivindicación 4, en la que un nucleótldo modificado se liga a un compuesto seleccionado del grupo que comprende péptidos, proteínas, carbohidratos, anticuerpos, moléculas sintéticas, polímeros, microproyectiles, partículas metálicas, nanopartículas, lípidos o una fase sólida.
6. La construcción de acuerdo con cualquiera de las reivindicaciones anteriores, en la que el promotor se selecciona del grupo que comprende secuencias promotoras, que son operativas en células de seres humanos, de animales o eucariotas.
7. La construcción de acuerdo con al menos una de las reivindicaciones anteriores, en la que dicha construcción codifica proteínas, péptidos, anticuerpos, hormonas, citocinas u otras sustancias biológicamente activas.
8. La construcción de acuerdo con la reivindicación 7, en la que las sustancias biológicamente activas son inmunomoduladores.
9. Una composición farmacéutica que comprende la construcción de ADN de acuerdo con cualquiera de las reivindicaciones 1 a 8.
10. La composición farmacéutica de acuerdo con la reivindicación 9, que comprende adicionalmente un agente quimioterapéutico.
11. La construcción de ADN de acuerdo con una cualquiera de las reivindicaciones 1 a 8 o la composición farmacéutica de acuerdo con las reivindicaciones 9 o 10 para la transfección in vitro estable o transitoria de una célula humana, animal o eucarlota.
12 La construcción de ADN de acuerdo con una cualquiera de las reivindicaciones 1 a 8 o la composición farmacéutica de acuerdo con las reivindicaciones 9 o 10 para terapia génica ex-vivo o vacunación con ADN.
13 La construcción de ADN de acuerdo con una cualquiera de las reivindicaciones 1 a 8 o la composición farmacéutica de acuerdo con las reivindicaciones 9 o 10 para su uso en un método para el tratamiento de cáncer o de enfermedades autoinmunitarias.
14. Una combinación de la construcción de ADN de acuerdo con una cualquiera de las reivindicaciones 1 a 8 o la composición farmacéutica de acuerdo con las reivindicaciones 9 o 10 con una construcción de ADN ¡nmunomoduladora no codificante.
Patentes similares o relacionadas:
 Animales no humanos que tienen un locus de cadena ligera lambda de inmunoglobulina modificado por ingeniería, del 29 de Julio de 2020, de REGENERON PHARMACEUTICALS, INC.: Un roedor cuyo genoma de la línea germinal comprende un locus de cadena ligera λ de inmunoglobulina endógeno que comprende:
(a) uno o más segmentos […]
Animales no humanos que tienen un locus de cadena ligera lambda de inmunoglobulina modificado por ingeniería, del 29 de Julio de 2020, de REGENERON PHARMACEUTICALS, INC.: Un roedor cuyo genoma de la línea germinal comprende un locus de cadena ligera λ de inmunoglobulina endógeno que comprende:
(a) uno o más segmentos […]
 Procedimiento para la producción de polipéptidos, del 29 de Julio de 2020, de F. HOFFMANN-LA ROCHE AG: Promotor que tiene la secuencia de ácido nucleico de SEQ ID NO: 02.
Procedimiento para la producción de polipéptidos, del 29 de Julio de 2020, de F. HOFFMANN-LA ROCHE AG: Promotor que tiene la secuencia de ácido nucleico de SEQ ID NO: 02.
Ratones con un sistema inmunitario humanizado con células dendríticas reforzadas, del 22 de Julio de 2020, de INSERM (INSTITUT NATIONAL DE LA SANTE ET DE LA RECHERCHE MEDICALE): Un ratón Rag-/-, γc-/-, Flk2-/- deficiente para el gen activador de recombinación 2 (Rag2) y/o el gen activador de recombinación 1 (Rag1), cadena gamma […]
Detección de interacciones proteína a proteína, del 15 de Julio de 2020, de THE GOVERNING COUNCIL OF THE UNIVERSITY OF TORONTO: Un método para medir cuantitativamente la fuerza y la afinidad de una interacción entre una primera proteína de membrana o parte de la misma y una […]
Procedimientos y composiciones para el tratamiento de una afección genética, del 24 de Junio de 2020, de Sangamo Therapeutics, Inc: Una célula precursora de glóbulos rojos genomanipulada caracterizada por una modificación genómica dentro del exón 2 o el exón 4 de BCL11A o dentro de BCL11A-XL […]
Estructuras artificiales de poliepítopos para uso en inmunoterapia, del 17 de Junio de 2020, de Invectys: Un vector de expresión de ADN o una mezcla de vectores de expresión de ADN que codifica al menos dos epítopos de CD4 de la transcriptasa inversa de la telomerasa […]
Expresión de proteína biotecnológica mejorada que usa un activador CHEF1 híbrido, del 17 de Junio de 2020, de AGC Biologics, Inc: Un vector de expresión que comprende ADN regulador de la transcripción del factor 1α de elongación de hámster chino (CHEF1) 5' y un activador de citomegalovirus (CMV) que […]
Roedores con alelos mutantes de Acvr1 condicionales, del 10 de Junio de 2020, de REGENERON PHARMACEUTICALS, INC.: Una construcción de ácido nucleico que comprende: (i) un exón 5 de Acvr1 que codifica una secuencia de tipo silvestre a nivel de proteína, […]