Anticuerpo anti-IL-3Ralfa para su utilización en el tratamiento de un tumor de la sangre.
Anticuerpo contra una cadena de IL-3Rα humana, que no inhibe la señalización de IL-3,
y que se une al dominio B de la cadena de IL-3Rα humana pero no se une al dominio C de la cadena de IL-3Rα humana.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/JP2010/057510.
Solicitante: KYOWA HAKKO KIRIN CO., LTD..
Nacionalidad solicitante: Japón.
Dirección: 1-6-1, OHTEMACHI CHIYODA-KU TOKYO 100-8185 JAPON.
Inventor/es: TAWARA,TOMONORI, TAKAYANAGI,SHINICHIRO, INAGAKI,YOSHIMASA.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K39/395 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 39/00 Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53). › Anticuerpos (aglutininas A61K 38/36 ); Inmunoglobulinas; Inmunosuero, p. ej. suero antilinfocitario.
- A61P35/02 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 35/00 Agentes antineoplásicos. › específicos para la leucemia.
- C07K16/28 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 16/00 Inmunoglobulinas, p. ej. anticuerpos mono o policlonales. › contra receptores, antígenos celulares de superficie o determinantes celulares de superficie.
- C07K16/46 C07K 16/00 […] › Inmoglobulinas híbridas (híbridos de una inmunoglobulina con un péptido distinto de una inmunoglobulina C07K 19/00).
- C12N15/02 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Preparación de células híbridas por fusión de dos o más células, p. ej. fusión de protoplastos.
- C12N15/09 C12N 15/00 […] › Tecnología del ADN recombinante.
- C12P21/08 C12 […] › C12P PROCESOS DE FERMENTACION O PROCESOS QUE UTILIZAN ENZIMAS PARA LA SINTESIS DE UN COMPUESTO QUIMICO DADO O DE UNA COMPOSICION DADA, O PARA LA SEPARACION DE ISOMEROS OPTICOS A PARTIR DE UNA MEZCLA RACEMICA. › C12P 21/00 Preparación de péptidos o de proteínas (proteína monocelular C12N 1/00). › Anticuerpos monoclonales.
- C12R1/91 C12 […] › C12R SISTEMA DE INDEXACION ASOCIADO A LAS SUBCLASES C12C - C12Q, RELATIVO A LOS MICROORGANISMOS. › C12R 1/00 Microorganismos. › Líneas celulares.
- G01N33/53 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › Ensayos inmunológicos; Ensayos en los que interviene la formación de uniones bioespecíficas; Materiales a este efecto.
- G01N33/574 G01N 33/00 […] › para el cáncer.
- G01N33/577 G01N 33/00 […] › en los que interviene anticuerpos monoclonados.
PDF original: ES-2550639_T3.pdf




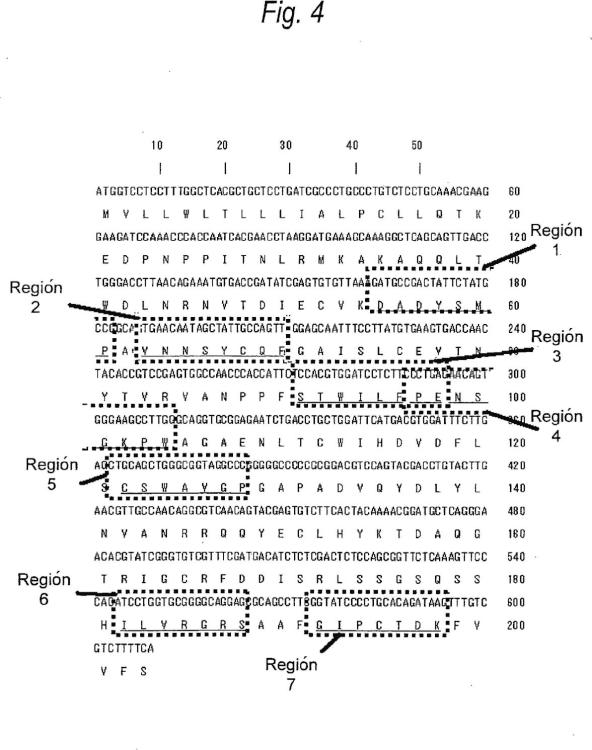
Fragmento de la descripción:
Anticuerpo anti-IL-3Ra para su utilización en el tratamiento de un tumor de la sangre.
Campo técnico
La presente invención se refiere a un anticuerpo contra la proteína IL-3Ra humana (por otro nombre: CD123 humana) . También se describen en la presente memoria un agente terapéutico y un agente de diagnóstico para tumores malignos mielociticos, particularmente leucemia mieloide aguda (AML) , que comprende como principio activo un anticuerpo anti-IL-3Ra humana.
Antecedentes de la invención Con respecto a tumor ma ligno:
Un tumor maligno (cáncer) es la primera causa principal de muerte en Japón, y el número de pacientes crece cada año, y se desea vivamente el desarrollo de un fármaco y un método terapéutico que tenga eficacia y seguridad elevadas. Como la causa que forma un tumor maligno, están una mutación del ADN por radiación, rayos ultravioletas y diversas sustancias carcinogénicas. Los estudios sobre tumores malignos se han centrado en la identificación biológica molecular de estos cambios genéticos. Como resultado, se considera que la transformación tumOfigénica es inducida por la acumulación de un gran número de mutaciooes, y similares. Se ha demostrado mediante un modelo de estirpe celular y similar que algunas mutaciones decisivas están conectadas directamente con la transformación tumorigénica. Con respecto a la leucemia como una de las enfermedades diana de la invención, se han identificado y clasificado muchas anormalidades cromosómicas. En muchos de los casos, se encuentra translocación del cromosoma, y en las principales translocaciones cromosómicas ya se han identificado algunos genes asociados con la translocación cromosómica. Analizando las funciones de los genes relacionados con la translocación, se ha encontrado que estos genes están implicados en el inicio de la leucemia.
Con respecto a las células troncales cancerosas:
Por otro lado, desde hace tiempo, desde el punto de vista de la biología celular, se ha propuesto la denominada hipótesis de células troncales cancerosas, que señala que la célula troncal es el origen de un tumor maligno similar al tejido normal. La célula troncal se define como una célula que tiene capacidad de replicación autónoma y pluripotencia, y generalmente se divide aproximadamente en célula troncal totipotente y célula troncal tisular. Las células troncales tisulares se originan a partir de tejidos y órganos específicos tales como el sistema sanguíneo, hígado, sistema nervioso, y similar, y presentan una frecuencia extremadamente baja. Entre ellas, se ha estudiado muy frecuentemente la célula troncal hematopoyética. Se ha dado a conocer que un sistema hematopoyético se puede reconstruir durante un período de tiempo prolongado transplantando una célula troncal hematopoyética en un ratón en el que se destruyó el sistema hematopoyético mediante una dosis letal de irradiación (documento 1 no de patente) . A diferencia de la célula troncal normal, los estudios sobre células troncales cancerosas se han retrasado durante un período de tiempo prolongado puesto que no se pudo encontrar su naturaleza exacta. Sin embargo, se ha identificado por primera vez una célula troncal cancerosa en leucemia mieloide aguda, en 1997 por Dick el al. Después, se ha dado a conocer la presencia de células troncales cancerosas en diversos tumores malignos Resumiendo, las células troncales cancerosas están presentes a una frecuencia de varios % o menos de todas las células troncales tanto tumorales y raras como normales. Se considera que las células restantes que forman el tumor SOfl células precursoras tumorales en las que la capacidad de proliferación está limitada, o células tumorales Mediante estos informes, se mostró que existe una jerarquía incluso en el tumor similar al tejido normal, y la célula troncal cancerosa que reside en este pico (origen) tiene una fuerte capacidad formadora de tumores Características y problemas terapéuticos de célu las tronca les cancerosas:
Resumiendo muchos informes, se considera que las células troncales cancerosas mantienen diversas características que poseen las células troncales normales. Los ejemplos de similitudes incluyen la rareza de las células, un microentorno (nicho) en el que existe la célula, la expresión de un gen de multirresistencia, la detención del ciclo celular, y similares.
Particularmente, las características de que expresan un grupo de genes de multirresistencia y de que están en la interfase del ciclo celular similar a células troncales normales podría convertirse en un problema terapéuticamente enorme. Un gen de multirresistencia BCRP es una bomba que afecta a la eficacia del fármaco al eliminar diversos agentes antitumorales fuera de las células, y se ha dado a conocer un método para recoger células troncales haciendo uso de la actividad (documento 2 no de patente) . Además, su presencia en la interfase del ciclo celular
bajo el estado de ~detención" (documento 3 no de patente) provoca una reducción de la sensibilidad a muchos agentes antitumorales y radiaciooes que atacan el crecimiento celular rápido del cáncer (documentos 4 y 5 no de patente) .
Basándose en las características anteriores, se considera que la célula troncal cancerosa que presenta resistencia a la terapia es una causa de regeneración tumoral
Con respecto al fármaco diana molecular
Las tres vías principales de tratamiento de un tumor maligno incluyen la terapia con agentes antitumorales, la terapia de radiación y la extirpación quirúrgica. El tumor de la sangre está limitado a la terapia con agentes antitumorales y a la terapia de radiación, y como se describe en lo anterior, la célula troncal cancerosa puede tener una resistencia a estos tratamientos. Otro problema es que los efectos secundarios son grandes, puesto que estos dos tratamientos afectan a todo el cuerpo. Como medio para resolver este problema, es de esperar un fármaco diana molecular Tienen la posibilidad de reducir los efectos secundarios al presentar su eficacia farmacéutica solamente en la célula que expresa la molécula diana.
Los ejemplos de fármacos típicos del fármaco diana molecular en el campo de enfermedades sanguíneas incluyen imatinib y rituximab. Imatinib se dirige contra un factor que provoca la leucemia, denominado Bcr-Abl, producido por una anormalidad cromosómica (cromosoma de Filadelfia) , que se obselVa en el 95% de los pacientes con CML Este es un fármaco de bajo peso molecular que induce el suicidio de células leucémicas al inhibir la función de BcrAbL Rituximab es un anticuerpo terapéutico que reconoce CD20 como una molécula de la superficie en una célula B, y tiene un efecto antitumoral sobre un tumor maligno de célula B (Iinfoma no de Hodgkin y similar) . Por otro lado, los fármacos diana moleculares para AML son pocos, y solamente hay un agente gemtuzumabozogamicina (Mylotarg) en el que un antibiótico, calicheamicina, está enlazado a un anticuerpo monoclonal para CD33, conocido como un antígeno de la superficie celular de AML. Sin embargo, actualmente el uso de Mylotarg está limitado debido a su fuerte toxicidad, que se considera derivada de la calicheamicina, además del problema de que el intelValo terapéutico es estrecho. Basándose en lo expuesto anteriormente, se puede afirmar que el descubrimiento de un nuevo gen diana y el desarrollo de un agente terapéutico para éste soo invenciones importantes que conducen directamente a la posibilidad de terapia y expansión de las elecciones de la terapia Como la realización de fármacos diana moleculares, se han estudiado y desarrollado diversas sustancias tales como un anticuerpo terapéutico y un fármaco de bajo peso molecular, así como un fármaco peptídico, una preparación proteica biológica tal como citocina, un ARNpi, aptámero, y similar. Cuando se usa un anticuerpo como agente terapéutico, debido a su especificidad, es útil en el tratamiento de patologías en las que la célula trastornada expresa un antígeno específico. El anticuerpo se une a una proteína que se expresa sobre la superficie celular como su antígeno, y actúa eficazmente al unirse a la célula. El anticuerpo tiene una característica de una semivida prolongada en la sangre y una elevada especificidad por su antígeno, y también es notablemente útil como agente antitumoraL Por ejemplo, cuando un anticuerpo se dirige a un antígeno específico de tumor, se puede esperar que el anticuerpo administrado se acumule en el tumor y ataque de ese modo a la célula tumoral vía la citotoxicidad dependiente del complemento (CDC) y la citotoxicidad celular dependiente del anticuerpo (ADCC) . Además, al unir una sustancia radioactiva, una sustancia citotóxica y similar a un anticuerpo, es posible transferir eficientemente un... [Seguir leyendo]
Reivindicaciones:
1. Anticuerpo contra una cadena de IL-3Ra humana, que no inhibe la seña lización de IL-3, y que se une al dominio B de la cadena de IL-3Ra humana pero no se une al dominio C de la cadena de IL-3Ra humana
2. Anticuerpo según la reivindicación 1, que presenta además una cilotoxicidad celular dependiente de anticuerpos (ADCC) elevada.
3. Anticuerpo según la reivindicación 1 o 2, en el que la citoloxicidad celular dependiente de anticuerpos (AOCC)
elevada muestra un porcentaje de lisis específica de 10% a una concentración de anticuerpo de 0, 01 , Ig/ml, medianle un mélodo de ensayo de AOCC de Colon-26fhC0123 que utiliza PBMC cultivadas con IL-2
4. Anlicuerpo según cualquiera de las reivindicaciones 1 a 3, que comprende unas secuencias de aminoácidos de CDR de cadena pesada y CDR de cadena ligera seleccionadas de entre el grupo que consiste en los (a) a (e) siguientes:
(a) CDR 1 a 3 de la cadena pesada son las secuencias de aminoácidos de SEC ID nO: 113 a 115, respectivamente, y COR 1 a 3 de la cadena ligera son las secuencias de aminoácidos de SEC ID nO. 131 a 133, respectivamente ,
(b) CDR 1 a 3 de la cadena pesada son las secuencias de aminoácidos de SEC ID nO: 116 a 118, respectivamente, y COR 1 a 3 de la cadena ligera son las secuencias de aminoácidos de SEC ID nO. 134 a 136, respectivamente ,
(c) CDR 1 a 3 de la cadena pesada son las secuencias de aminoácidos de SEC ID nO: 119 a 121 , respectivamente, y COR 1 a 3 de la cadena ligera son las secuencias de aminoácidos de SEC ID nO: 137 a 139, respectivamente ,
(d) CDR 1 a 3 de la cadena pesada son las secuencias de aminoácidos de SEC ID nO: 122 a 124, respectivamente, y CDR 1 a 3 de la cadena ligera son las secuencias de aminoácidos de SEC ID nO: 140 a 142, respectivamente , y
(e) CDR 1 a 3 de la cadena pesada son las secuencias de aminoácidos de SEC ID nO: 125 a 127, respectivamente, y COR 1 a 3 de la cadena ligera son las secuencias de aminoácidos de SEC ID nO. 143 a 145, respectivamente
5. Anticuerpo según cualquiera de las reivindicaciooes 1 a 4, que comprende una región variable de cadena pesada y una región variable de cadena ligera selecciooadas de entre el grupo que consiste en los (a) a (e) siguientes:
(a) una región variable de cadena pesada que comprende una secuencia de aminoácidos de glutamina (Q) en la posición 20 a serina (S) en la posición 139 en la secuencia de aminoácidos de SEC ID nO: 53 y una región variable de cadena ligera que comprende una secuencia de aminoácidos de valina (V) en la posición 23 a lisina (K) en la posición 129 en la secuencia de aminoácidos de SEC ID nO. 55;
(b) una región variable de cadena pesada que comprende una secuencia de aminoácidos de glutamina (O) en la
posición 20 a serina (S) en la posición 139 en la secuencia de aminoácidos de SEC ID nO. 57 y una región variable de cadena ligera que comprende una secuencia de aminoácidos de valina (V) en la posiciórJ 23 a lisina (K) en la posición 129 en la secuencia de aminoácidos de SEC ID nO: 59;
(c) una región variable de cadena pesada que comprende una secuencia de aminoácidos de glutamina (Q) en la posición 20 a serina (S) en la posición 139 en la secuencia de aminoácidos de SEC ID nO: 61 y una región variable de cadena ligera que comprende una secuencia de aminoácidos de ácido aspártico (O) en la posición 23 a lisina (K) en la posición 129 en la secuencia de aminoácidos de SEC ID nO: 63;
(d) una región variable de cadena pesada que comprende una secuencia de aminoácidos de glutamina (O) en la posición 20 a serina (S) en la posición 139 en la secuencia de aminoácidos de SEC ID nO: 65, y una región variable de cadena ligera que comprende una secuencia de aminoácidos de ácido aspártico (O) en la posición 23 a lisina (K) en la posición 129 en la secuencia de aminoácidos de SEC ID nO. 67; y
(e) una región variable de cadena pesada que comprende una secuencia de aminoácidos de glutamina (O) en la posición 20 a serina (S) en la posición 138 en la secuencia de aminoácidos de SEC ID nO: 69 y una región variable de cadena ligera que comprende una secuencia de aminoácidos de ácido aspártico (O) en la posición 23 a lisina (K) en la posición 129 en la secuencia de aminoácidos de SEC ID nO. 71
Composición farmacéutica que comprende el anticuerpo de IL-3Ra según cualquiera de las reivindicaciones 1 a 5, para su utilización en un método para prevenir o tratar un tumor de la sangre en el que una célula que expresa IL3Ru se encuentra en la médula ósea o la sangre periférica de un sujeto.
7. Anticuerpo de IL-3Ru según cualquiera de las reivindicaciones 1 a 5, para su utilización en un método para tratar
un tumor de la sangre en el que una célula que expresa IL-3Ru se encuentra en la médula ósea o la sangre 5 periférica 8. Utilización del anticuerpo de IL-3Ru según cualquiera de las reivindicaciones 1 a 5, para detectar en una muestra biológica de un sujeto un tumor de la sangre en el que una célula que expresa IL-3Ru se encuentra en la médula ósea o la sangre periférica.
9. Composición farmacéutica para su utilización según la reivindicación 6, anticuerpo de IL-3Ru para su utilización según la reivindicación 7, o utilización del anticuerpo de IL-3Ru según la reivindicación 8, en la/el que el tumor de la sangre es la leucemia mieloide aguda (AML) .
Patentes similares o relacionadas:
 Métodos para producir proteínas bicatenarias en bacterias, del 29 de Julio de 2020, de GENENTECH, INC.: Un método para producir un receptor de linfocitos T monoclonal de movilización inmunitaria contra el cáncer (ImmTAC) que comprende una cadena alfa del receptor de linfocitos […]
Métodos para producir proteínas bicatenarias en bacterias, del 29 de Julio de 2020, de GENENTECH, INC.: Un método para producir un receptor de linfocitos T monoclonal de movilización inmunitaria contra el cáncer (ImmTAC) que comprende una cadena alfa del receptor de linfocitos […]
Anticuerpos anti-alfa-sinucleína y procedimientos de uso, del 29 de Julio de 2020, de F. HOFFMANN-LA ROCHE AG: Un anticuerpo anti-alfa-sinucleína humana que comprende (a) HVR-H1 que comprende la secuencia de aminoácidos de SEQ ID NO: 21; (b) HVR-H2 que […]
Formulaciones estabilizadas que contienen anticuerpos anti-receptor de interleucina 4 (IL-4R), del 29 de Julio de 2020, de REGENERON PHARMACEUTICALS, INC.: Una jeringuilla precargada que contiene una formulación farmacéutica líquida estable, en la que la formulación farmacéutica líquida comprende: […]
Métodos y composiciones para tratar y prevenir enfermedades asociadas con la integrina AVB8, del 29 de Julio de 2020, de THE REGENTS OF THE UNIVERSITY OF CALIFORNIA: Un anticuerpo aislado que se une específicamente a la integrina β8 humana e inhibe la adhesión del péptido asociado a latencia (LAP) a ανβ8, en donde el […]
Anticuerpos anti-PD-L1 y usos de los mismos, del 22 de Julio de 2020, de MERCK PATENT GMBH: Un anticuerpo anti-PD-L1 aislado o su fragmento de union a antigeno que comprende una secuencia de region variable de cadena pesada y de cadena ligera, en donde: […]
Utilización de anticuerpos optimizados en ADCC para tratar a los pacientes con bajo nivel de respuesta, del 22 de Julio de 2020, de LABORATOIRE FRANCAIS DU FRACTIONNEMENT ET DES BIOTECHNOLOGIES: Utilización de una composición de anticuerpo monoclonal quimérico, humanizado o humano de isotipo IgG1 anti- Rhesus del glóbulo rojo humano cuya […]
Proteínas de unión al antígeno ST2, del 22 de Julio de 2020, de AMGEN INC.: Un anticuerpo aislado que se une a un antígeno ST2 que tiene la secuencia de aminoácidos 19-556 del SEQ ID NO: 1, comprendiendo dicho anticuerpo una secuencia de […]
Método para producir inmunoconjugados de anticuerpo-SN-38 con un enlazador CL2A, del 22 de Julio de 2020, de IMMUNOMEDICS, INC.: Un método para producir un compuesto, CL2A-SN-38, que presenta la estructura, **(Ver fórmula)** que comprende realizar un esquema de reacción como el que se muestra: **(Ver […]