Terapia de combinación antibacteriana para el tratamiento de infecciones por bacterias Gram-positivas.
Una composición que comprende miconazol, y sales farmacéuticamente aceptables del mismo,
y nisina, y sales farmacéuticamente aceptables de la misma, para su uso en el tratamiento de una infección a la que contribuyen o producida por bacterias Gram-positivas.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/GB2009/001772.
Solicitante: e-Therapeutics plc.
Nacionalidad solicitante: Reino Unido.
Dirección: 17 Blenheim Office Park, Long Hanborough Oxfordshire OX29 8LN REINO UNIDO.
Inventor/es: YOUNG,MALCOLM PHILIP, THOMAS,CATHERINE MARY.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/336 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › teniendo ciclos de tres eslabones, p. ej. oxirano, fumagilina.
- A61K31/4174 A61K 31/00 […] › Arilalquilimidazoles, p. ej. oximetazolina, nafazolina, miconazol.
- A61K31/42 A61K 31/00 […] › Oxazoles.
- A61K38/12 A61K […] › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Péptidos cíclicos.
- A61K38/16 A61K 38/00 […] › Péptidos que tienen más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados.
- A61P31/04 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 31/00 Antiinfecciosos, es decir antibióticos, antisépticos, quimioterápicos. › Agentes antibacterianos.
PDF original: ES-2523968_T3.pdf
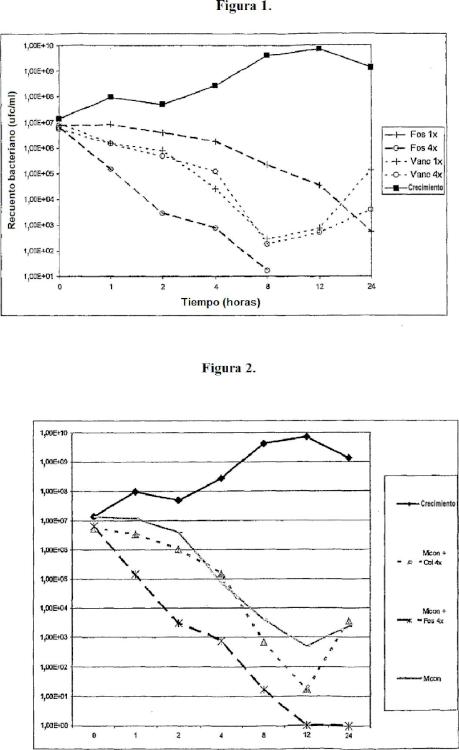
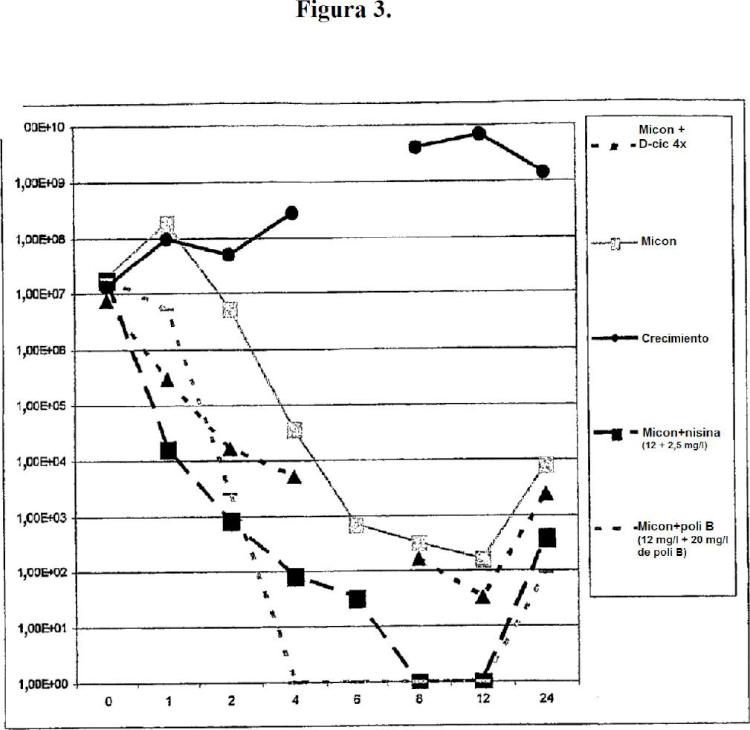
Fragmento de la descripción:
Terapia de combinación antibacteriana para el tratamiento de infecciones por bacterias Gram-positivas Campo de la invención
La presente invención proporciona un producto que comprende una combinación sinérgica de un imidazol terapéuticamente activo y una membrana de la célula bacteriana o agente activo de la pared celular, o un derivado o un metabolito del mismo, como preparación combinada para el tratamiento de infecciones causadas por o a las que contribuyen bacterias Gram-positivas.
Antecedentes
Las bacterias Gram-positivas, tales como estafilococos, enterococos y clostridios, son patógenos extremadamente importantes tanto en medicina humana como en veterinaria. En los Estados Unidos, entre 1995 y 1998, en el 6 % de las infecciones sanguíneas hospitalarias participaron bacterias Gram-positivas. Este porcentaje continúa aumentando. El desarrollo de resistencia a antibióticos entre bacterias Gram-positivas complica el tratamiento y puede conducir a elevada morbilidad y mortalidad.
La resistencia a antibióticos en bacterias se ha seleccionado por medio del uso prolífico de estos fármacos tanto en medicina humana como en la cria de animales, prácticas indiscriminadas de recetar y falta de conformidad del paciente con las pautas de tratamiento. La opciones terapéuticas para el tratamiento de tales microorganismos resistentes a fármacos, especialmente bacterias Gram-positivas, están siendo cada vez más limitadas. El problema de la resistencia a antibióticos se agrava por la propagación de los organismos resistentes a fármacos, y la diseminación de genes de resistencia entre las bacterias. La amenaza para el tratamiento satisfactorio de infecciones bacterianas propuesta por el desarrollo y propagación de la resistencia a antibióticos es uno de los problemas más significativos dentro del cuidado sanitario y la medicina veterinaria.
Estafilococos
Los estafilococos son causas Importantes de infección grave asociada al cuidado sanitario (HAI). Entre ellas destacan las cepas de Staphylococcus que han desarrollado u obtenido niveles variables de resistencia a antibióticos tales como la meticilina. Estos organismos difíciles de tratar son comúnmente conocidos como Staphylococcus aureus resistente a meticilina (MRSA) y Staphylococcus epidermidis resistente a meticilina (MRSE). Aproximadamente el 8 % de las cepas aisladas de S. epidermidis de infecciones asociadas a dispositivos son resistentes a meticilina (MRSE), además de ser multirresistentes. La resistencia a múltiples antibióticos y la capacidad de S. epidermidis para formar biopelículas sobre superficies inertes agravan los retos de tratar infecciones producidas por estos organismos.
En los EE.UU., más del 5 % de las cepas aisladas clínicas de S. aureus son resistentes a la (3-lactama meticilina (NNIS, 24). Simllarmente, informes de S. aureus resistente a meticilina (MRSA) en animales se han convertido en más frecuentes en los últimos años (O'Mahony y col., 25); MRSA se ha aislado de perros, gatos, ganado vacuno, ovejas, pollos, conejos y caballos (Devriese y Hommez, 1975, Hartmann y col., 1997, Pakycol., 1999, Tomlin y col., 1999, Lee, 23, Goni y col., 24, y Weese 24).
En tanto la medicina humana como en la veterinaria, son un problema significativo las biopelículas bacterianas (comunidades estructuradas de células bacterianas encerradas en una matriz polimérica auto-producida y adherente a una superficie inerte o viva (Costerton y col., 1999)). En la cria de animales, las biopelículas bacterianas pueden desarrollarse sobre la instrumentación de procesamiento de aves de corral (Arnold y Silvers, 2) y puede producir el fallo del tratamiento de mastitis en vacas infectadas por S. aureus (Melchior y col., 26). En el cuidado sanitario humano, se ha mostrado que biopelículas de bacterias colonizan muchos dispositivos médicos, que incluyen implantes ortopédicos (Bahna y col., 27). En el RU, el 35 % de la infección de las prótesis de cadera es atribuible a S. aureus, que produce aflojamiento séptico, falta de unión de la fractura y osteomielitis (Sanderson, 1991). La asociación de MRSA con el uso de dispositivos ortopédicos es extremadamente problemática debido al elevado espectro de resistencia de este organismo, además de la protección del sistema inmunitario dada por la fase de crecimiento de la biopelícula, que frecuentemente necesita la eliminación de un dispositivo contaminado, causando adicionalmente traumatismo al paciente y aumentando los costes médicos. La colonización con MRSA es el precursor general al desarrollo de una infección por MRSA, por lo que las intervenciones que reducen los niveles de colonización humana o la colonización de superficies tales como dispositivos médicos reducirán la propagación de infecciones en centros sanitarios.
La adquisición de resistencia a la meticilina entre especies estafilocócicas no solo descarta el uso de todos los antibióticos (3-lactámicos actualmente disponibles, sino que también se asocia comúnmente a resistencia a múltiples clases de fármacos.
La resistencia a la meticilina en estafilococos se desarrolla por la alteración de la diana del fármaco. Los antibióticos p-lactámicos, tales como la meticilina, actúan sobre cepas sensibles uniéndose a e inhibiendo proteínas llamadas proteínas de unión a penicilina. La resistencia a la meticilina en estafilococos se produce por la alteración de una de estas proteínas, PBP2', de manera que las p-lactamas se unen poco a ella. Esto hace que la bacteria se vuelva resistente a todos los fármacos p-lactámicos actualmente disponibles. Las infecciones por MRSA y MRSE pueden tratarse con fármacos de glicopéptido, tales como vancomicina. El aumento en la prevalencia de MRSA y MRSE, además de altos niveles emergentes de resistencia a aminoglucósidos y ampicilina en enterococos, ha producido un aumento en la dependencia de la vancomicina. Esto ha conducido a la posterior aparición de patógenos resistentes a vancomicina. Entre ellos están cepas comúnmente conocidas como Staphylococcus aureus de sensibilidad intermedia a vancomicina (VISA) y Staphylococcus aureus resistente a vancomicina (VRSA), todas las cuales son resistentes a múltiples fármacos y difíciles de tratar. La aparición de VISA y VRSA significa que los antibióticos actuales pueden llegar a ser ineficaces para el tratamiento de infecciones humanas tales como endocarditis, bacteremia y osteomielitis.
La administración de vancomicina a pacientes con infecciones por MRSA recurrentes produce un elevado riesgo de aparición de cepas de VISA o VRSA. La gran mayoría de las infecciones por VISA en los EE.UU. se producen en pacientes con MRSA recurrente tratados con vancomicina (Appelbaum, 26). Aunque una espectacular reducción en el uso de glicopéptidos tales como vancomicina reduciría la aparición y propagación de VISA y VRSA, esto no es práctico sin el uso de compuestos alternativos que no promueven la aparición de multirresistencia.
Clostridios
Los clostridios son bacterias Gram-positivas resistentes a múltiples fármacos que se están convirtiendo en una de las infecciones asociadas al cuidado sanitario más difíciles de tratar hasta la fecha. La administración de antibióticos de amplio espectro, tales como ampicilina, amoxicilina y las cefalosporinas, desempeña una función clave en el desarrollo de diarrea asociada a Clostridium diffícile (CDAD). Se cree que la presencia de un gran número de elementos genéticos móviles dentro del genoma de C. diffícile es responsable de la resistencia a múltiples fármacos observada en esta especie. El uso de antibióticos de amplio espectro reduce la colonización bacteriana en el intestino, permitiendo el crecimiento en exceso de C. diffícile. Clostridium diffícile es extremadamente resistente; formando esporas, puede sobrevivir extremos de temperatura, etanol y antibióticos, y así es muy difícil de tratar. Uno de los retos clave en el tratamiento de C. diffícile es el hecho de que puede formar estas esporas altamente resistentes. Como tal, el tratamiento con antibióticos produce comúnmente la inhibición de las células de Clostridium que crecen activamente, pero no de las esporas vegetativas. Las esporas permanecen en el intestino de un mamífero después del tratamiento y pueden entonces germinar produciendo una nueva infección por C. diffícile. Actualmente, los antibióticos de elección para el tratamiento de C. difficile son metronidazol y luego vancomicina si el metronidazol es ineficaz. Sin embargo, ninguno de estos fármacos puede inhibir el crecimiento de esporas de Clostridium, y como tal la prevalencia de recaídas en infección por C. difficile después del tratamiento se estima en aproximadamente el 55 % de todos los casos.
Inicialmente, se usó vancomicina... [Seguir leyendo]
Reivindicaciones:
1. Una composición que comprende miconazol, y sales farmacéuticamente aceptables del mismo, y nisina, y sales farmacéuticamente aceptables de la misma, para su uso en el tratamiento de una infección a la que contribuyen o
producida por bacterias Gram-positivas.
2. Una composición para su uso según la reivindicación 1, en la que la sal de miconazol es una sal de nitrato.
3. Una composición para su uso según la reivindicación 1, en la que las bacterias Gram-positivas se seleccionan del 1 grupo que consiste en estafilococos, enterococos y clostridios.
4. Una composición para su uso según la reivindicación 3, en la que las bacterias Gram-positivas difíciles de tratar se seleccionan del grupo que consiste en MRSA, MRSE, VISA, VRSA, VRE y clostridios.
5. Una composición para su uso según las reivindicaciones 3 o 4, en la que los organismos Gram-positivos
resistentes a múltiples fármacos del género Clostridium son C. diffícile.
6. Una composición para su uso según la reivindicación 1 para administración por vía oral.
Patentes similares o relacionadas:
Composiciones farmacéuticas que contienen una leucocidina E mutada, del 22 de Julio de 2020, de NEW YORK UNIVERSITY: Una composición que comprende: una proteína Leucocidina E (LukE) aislada que comprende la secuencia de aminoácidos de la SEQ ID NO: 4, o un polipéptido […]
Tratamiento o prevención de infecciones asociadas a biopelículas con agua con cloro libre disponible, del 15 de Julio de 2020, de Sonoma Pharmaceuticals, Inc: Agua con cloro libre disponible (FAC) para su uso en el tratamiento o reducción de la incidencia de una infección en un mamífero provocada por una biopelícula que contiene […]
Formulaciones de azalida acuosas concentradas, del 8 de Julio de 2020, de Sun Pharma Global FZE: Una composición farmacéutica tópica para su uso en el tratamiento de una infección ocular que comprende administrar a un paciente en necesidad del mismo, una cantidad […]
Composición tópica que comprende extractos de boldo y de reina de los prados, destinada a un animal, y sus aplicaciones, del 6 de Julio de 2020, de Virbac SA: Composición tópica para animales, caracterizada por que comprende en un medio fisiológicamente aceptable extractos de boldo Peumus boldus y extractos de reina […]
DERIVADOS DE OLIGOSACÁRIDOS SINTÉTICOS COMO VACUNA CONTRA BORDETELLA PERTUSSIS, del 2 de Julio de 2020, de INSTITUTO FINLAY DE VACUNAS: La presente invención proporciona fragmentos de oligosacáridos sintéticos provenientes del pentasacárido terminal del lipooligosacárido de Bordetella pertussis, un método […]
Inhibidores de lisina gingipaína, del 1 de Julio de 2020, de Cortexyme, Inc: Un compuesto de acuerdo con la Fórmula I: **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en donde Z es ariloximetil-carbonilo sustituido con halógeno; […]
Vacuna de ADN contra pseudotuberculosis en peces marinos, del 1 de Julio de 2020, de NATIONAL UNIVERSITY CORPORATION TOKYO UNIVERSITY OF MARINE SCIENCE AND TECHNOLOGY: Una vacuna de ADN para peces, caracterizada por: - impartir inmunidad contra la pseudotuberculosis causada por Photobacterium damselae subsp. piscicida - que comprende, […]
Vacuna subunitaria contra Mycoplasma spp., del 1 de Julio de 2020, de Agricultural Technology Research Institute: Una composición para prevenir una infección por Mycoplasma spp., que comprende: un principio activo, que comprende una proteína de PdhA; y un adyuvante […]