Proceso para la producción simultánea de sulfato de potasio, sulfato de amonio, hidróxido de magnesio y/o óxido de magnesio a partir de una sal mixta de kainita y amoníaco.
Un método para la producción simultánea de sulfato de potasio (SOP),
sulfato de amonio, hidróxido de magnesiomodificado en superficie y/o óxido de magnesio caracterizado por la cogeneración de dichos productos utilizandosal mixta de kainita, en la que la kainita es una sal doble de KCl y MgSO4 acompañada de agua de cristalización ycontiene, además, NaCl y MgCl2.6H2O como impurezas, y amoníaco como materias primas consumibles. Dichoproceso comprende las siguientes fases:
a) La conversión, en una primera zona de reacción, de la sal mixta de kainita en schoenita mediante elproceso de lixiviación acuosa, en la que dicho proceso comprende la reacción de la sal mixta con agua yun licor final de SOP de la fase (e) seguida de la separación de la schoenita pura y de un licor final deschoenita (SEL).
b) El tratamiento del licor final de schoenita claro obtenido en la fase (a) con CaCl2 acuoso para separar elsulfato en forma de yeso, seguido de la filtración de la torta para recuperar el yeso y un licor final deschoenita desulfatada.
c) La exposición del licor final de schoenita desulfatada obtenido en la fase (b) a una evaporación paraobtener una carnalita sólida y un licor rico en MgCl2.
d) La descomposición de la carnalita obtenida en la fase (c) con agua para recuperar el KCl y un licordescompuesto de carnalita (CDL) que contiene MgCl2 y KCl residual.
e) El tratamiento de la schoenita pura de la fase (a) con KCl obtenido en la fase (d) para producir sulfato depotasio (SOP) a la vez que se recicla el licor final de SOP en el proceso de la fase (a).
f) El lavado del yeso recuperado en la fase (b) para minimizar las impurezas adherentes.
g) El contacto, en una segunda zona de reacción, del yeso obtenido en la fase (f) con un licor de amoníaco oun licor madre de sulfato de amonio obtenido en la fase (i) y dióxido de carbono obtenido en la fase (k)para producir una solución de sulfato de amonio y el subproducto CaCO3 mediante la reacción deMerseberg.
h) La filtración de CaCO3 a partir de los productos de la fase (g), seguida de la neutralización del filtrado conácido sulfúrico para convertir el amoníaco residual en sulfato de amonio.
i) La evaporación del filtrado neutralizado obtenido en la fase (h) con el fin de recuperar el sulfato de amonioa la vez que se recicla el licor madre de la fase (g).
j) El lavado del CaCO3 obtenido en la fase (h) con agua para minimizar el yeso no reaccionado y lasimpurezas solubles adherentes, seguido de calcinaciones para obtener CO2 y cal viva de alta pureza.
k) El envasado del CO2 y el reciclaje en la fase (g).
l) La extinción de la cal generada en la fase (j) con agua descarbonatada y el tratamiento con CDLgenerado en la fase (d) y/o licor rico en MgCl2 obtenido en la fase (c) para producir una dispersión deMg(OH)2 y CaCl2 acuoso.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/IN2010/000194.
Solicitante: COUNCIL OF SCIENTIFIC & INDUSTRIAL RESEARCH.
Nacionalidad solicitante: India.
Dirección: ANUSANDHAN BHAWAN, 2 RAFI MARG NEW DELHI 110 001 INDIA.
Inventor/es: GHOSH, PUSHPITO KUMAR, MODY,HARESH MAHIPATLAL, CHUNAWALA,JATIN RAMESHCHANDRA, GANDHI,MAHESHKUMAR RAMNIKLAL, BAJAJ,HARI CHAND, MAITI,PRATYUSH, JOSHI,HIMANSHU LABHSHANKER, DERAIYA,HASINA HAJIBHAI, SARAIYA,UPENDRA PADMAKANT.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C01C1/24 QUIMICA; METALURGIA. › C01 QUIMICA INORGANICA. › C01C AMMONIA; CYANOGEN; SUS COMPUESTOS (sales de oxácidos de halógenos C01B 11/00; peróxidos, sales de los perácidos C01B 15/00; tiosulfatos, ditionitos, politionatos C01B 17/64; compuestos de selenio o teluro C01B 19/00; azidas C01B 21/08; amidas metálicas C01B 21/092; nitritos C01B 21/50; fosfuros C01B 25/08; sales de los oxácidos del fósforo C01B 25/16; compuestos que contienen silicio C01B 33/00; compuestos que contienen boro C01B 35/00; procesos de fermentación o procesos que utilizan enzimas para la preparación de elementos o de compuestos inorgánicos excepto anhídrido carbónico C12P 3/00; producción de elementos no metálicos o de compuestos inorgánicos por electrólisis o electroforesis C25B). › C01C 1/00 Amoniaco; Sus compuestos. › Sulfatos de amonio (C01C 1/14 tiene prioridad).
- C01D5/00 C01 […] › C01D COMPUESTOS DE LOS METALES ALCALINOS, es decir, DE LITIO, SODIO, POTASIO, RUBIDIO, CESIO O FRANCIO (hidruros metálicos C01B 6/00; sales de oxácidos de halógenos C01B 11/00; peróxidos, sales de los perácidos C01B 15/00; sulfuros o polisulfuros C01B 17/22; tiosulfatos, ditionitos, politionatos C01B 17/64; compuestos que contienen selenio o teluro C01B 19/00; compuestos binarios del nitrógeno con metales C01B 21/06; azidas C01B 21/08; amidas metálicas C01B 21/092; nitritos C01B 21/50; fosfuros C01B 25/08; sales de los oxácidos del fósforo C01B 25/16; carburos C01B 32/90; compuestos que contienen silicio C01B 33/00; compuestos que contienen boro C01B 35/00; cianuros C01C 3/08; sales del ácido ciánico C01C 3/14; sales de cianamida C01C 3/16; tiocianatos C01C 3/20; procesos de fermentación o procesos que utilizan enzimas para la preparación de elementos o de compuestos inorgánicos excepto anhídrido carbónico C12P 3/00; obtención a partir de mezclas, p. ej. a partir de minerales, de compuestos metálicos que son los compuestos intermedios de un proceso metalúrgico para la obtención de un metal libre C22B; producción de elementos no metálicos o de compuestos inorgánicos por electrólisis o electroforesis C25B). › Sulfatos o sulfitos de sodio, potasio o metales alcalinos en general.
- C01D5/06 C01D […] › C01D 5/00 Sulfatos o sulfitos de sodio, potasio o metales alcalinos en general. › Preparación de sulfatos por doble descomposición.
- C01F5/08 C01 […] › C01F COMPUESTOS DE BERILIO, MAGNESIO, ALUMINIO, CALCIO, ESTRONCIO, BARIO, RADIO, TORIO O COMPUESTOS DE LOS METALES DE LAS TIERRAS RARAS (hidruros metálicos C01B 6/00; sales de oxácidos de halógenos C01B 11/00; peróxidos, sales de los perácidos C01B 15/00; sulfuros o polisulfuros de magnesio, calcio, estroncio o bario C01B 17/42; tiosulfatos, ditionitos, politionatos C01B 17/64; compuestos que contienen selenio o teluro C01B 19/00; compuestos binarios del nitrógeno con metales C01B 21/06; azidas C01B 21/08; amidas metálicas C01B 21/092; nitritos C01B 21/50; fosfuros C01B 25/08; sales de los oxácidos del fósforo C01B 25/16; carburos C01B 32/90; compuestos que contienen silicio C01B 33/00; compuestos que contienen boro C01B 35/00; compuestos que tienen propiedades de tamices moleculares pero que no tienen propiedades de cambiadores de base C01B 37/00; compuestos que tienen propiedades de tamices moleculares y de cambiadores de base, p. ej. zeolitas cristalinas, C01B 39/00; cianuros C01C 3/08; sales del ácido ciánico C01C 3/14; sales de cianamida C01C 3/16; tiocianatos C01C 3/20; procesos de fermentación o procesos que utilizan enzimas para la preparación de elementos o de compuestos inorgánicos excepto anhídrido carbónico C12P 3/00; obtención a partir de mezclas, p. ej. a partir de minerales, de compuestos metálicos que son los compuestos intermedios de un proceso metalúrgico para la obtención de un metal libre C22B; producción de elementos no metálicos o de compuestos inorgánicos por electrólisis o electroforesis C25B). › C01F 5/00 Compuestos de magnesio. › por calcinación de hidróxido de magnesio.
PDF original: ES-2435008_T3.pdf
Fragmento de la descripción:
Proceso para la producción simultánea de sulfato de potasio, sulfato de amonio, hidróxido de magnesio y/o óxido de magnesio a partir de una sal mixta de kainita y amoníaco
Campo de la invención [0001] La presente invención hace referencia a un proceso para la producción simultánea de sulfato de potasio (SOP) , sulfato de amonio, hidróxido de magnesio modificado en superficie y/o óxido de magnesio que se caracteriza por la cogeneración de dichos productos mediante el uso de sal mixta de kainita y amoníaco como únicas materias primas consumibles.
Antecedentes de la invención [0002] La sal mixta de kainita se obtiene a partir de salmueras residuales. En su forma pura se trata de una sal doble de
KCl.MgSO4.3H2O aunque, dado que se obtiene de las salmueras residuales, contiene normalmente impurezas de NaCl y MgCl2.6H2O. [0003] El sulfato de potasio es un fertilizante doble que contiene un 50 % de K2O y un 18 % de azufre. Tiene además
otras aplicaciones tal y como se ha documentado en invenciones previas. [0004] El hidróxido de magnesio tiene un uso comercial en la industria de la pulpa y del papel y también como antiácido,
retardante de fuego, base blanda y como intermediario en la producción de fertilizantes, magnesia y varios productos químicos de magnesio. [0005] El sulfato de amonio se emplea como fertilizante doble y contiene un 21, 5 % de N y un 24, 6 % de S. También se
emplea como materia prima en la producción de diversos productos químicos. [0006] Cabe citar la patente US 7.041.268 del 8 de mayo de 2006 de Ghosh et al. que trata ampliamente la técnica
anterior relacionada con el sulfato potásico (también conocido como sulfato de potasio o SOP) derivada de fuentes de salmuera residual. [0007] Cabe también citar la misma patente que revela la preparación de sulfato de potasio y magnesia de manera
integrada a partir de sal mixta de kainita y cal. Se obtiene yeso como producto secundario. La sal de kainita cruda obtenida a partir de salmueras salinas mediante evaporación solar se trata con agua y con un flujo de residuos del proceso para convertirlo en schoenita (K2SO4.MgSO4.6H2O) filtrando al mismo tiempo impurezas no deseadas presentes en la kainita cruda. El lixiviado, que contiene K+, Na+, Mg2+, Cl- y SO42- se desulfata con CaCl2 y se permite que se evapore más para recuperar la sal doble de carnalita (KCl.MgCl2.6H2O) que se descompone con agua y se filtra caliente para obtener KCI en estado puro. Mientras tanto, el licor madre rico en Mg2+ se trata con cal para producir Mg (OH) 2 a la vez que se produce el CaCl2 necesario para la desulfatación. La schoenita y el KCI se tratan con agua para recuperar K2SO4 en estado sólido mientras se recicla el licor madre en la fase de descomposición de la kainita. El mayor inconveniente de este proceso es que la calidad de la cal puede variar y, con ella, la calidad del hidróxido de magnesio. Otro inconveniente es la eliminación del subproducto de yeso para el que en ocasiones es difícil encontrar un mercado.
Cabe hacer referencia a la patente US 4.504.458 del 12 de marzo de 1985 de Knudsen que revela un método para convertir yeso en sulfato de potasio o sulfato de sodio sometiendo la lechada acuosa de yeso a un intercambiador
de aniones (en forma de cloruro) en un medio ácido, lo que ofrece como resultado una solución de cloruro de calcio y resina en forma de sulfato. La resina intercambiadora de aniones se pone en contacto posteriormente con cloruro potásico o cloruro de sodio regenerando, así, la resina cargada de sulfato para formar una resina cargada de cloruro y un sulfato de potasio o una solución de sulfato de sodio.
Cabe citar a E. Sacher, ISMA Tech. Conf. 1968 que describe el proceso de Merseberg para la producción de sulfato de amonio a partir de yeso natural. [0010] También cabe hacer referencia al artículo “Disposal or use of gypsum in production of ammonium sulfate” de N.
D. Gopinath en Phosphoric Acid, Vol. 1, Parte II, (ed. A. V. Slack) , Marcel Dekker, Nueva York, 541-566 (1968) que trata la conversión de yeso en sulfato de amonio al reaccionar con carbonato amónico. No se aportan unos parámetros detallados del proceso ni se menciona la utilidad del subproducto de carbonato de calcio.
Durante la elaboración mediante un procedimiento húmedo de ácido fosfórico, la materia prima básica de la que están hechos la mayoría de fertilizantes fosfatados, se reacciona el fosfato natural concentrado con ácido sulfúrico, lo que da como resultado la producción de cantidades sustanciales del subproducto de yeso conocido como “fosfoyeso”. Se han presentado diversas propuestas para convertir el fosfoyeso y el yeso en productos útiles y económicos por medios químicos. En todos los casos, a pesar de que es técnicamente factible, el coste de los productos químicos necesarios para llevar a cabo la conversión ha superado el valor del producto resultante. Un ejemplo sería la reacción de yeso con amoníaco y dióxido de carbono para formar sulfato de amonio y carbonato de calcio. Debido a su baja pureza comparada con el yeso natural, el uso del fosfoyeso no ha resultado económico en estas circunstancias.
Cabe citar el artículo de M. Chou et al. en www.anl.gov/PCS/acsfuel/preprint%20archive/Files/40_4_CHICAGO_08-95_0896.pdf
Dicho artículo nos enseña la producción de sulfato de amonio y carbonato de calcio a partir de yeso. La reacción produce carbonato de calcio insoluble y una solución de sulfato de amonio. Los autores manifiestan en el mismo que la técnica, aunque en principio resultaba atractiva, no es viable comercialmente debido a algunos problemas con el precio y la calidad del yeso natural y la falta de disponibilidad de una fuente económica de dióxido de carbono.
Cabe hacer referencia al proceso de Solvey que nos muestra la preparación de ceniza de sosa a partir de NaCl, NH3 y CO2 con la cogeneración de NH4Cl. Se obtiene CO2 mediante la calcinación de piedra caliza (CaCO3) mientras que la cal obtenida se reacciona con NH4Cl para reciclar el amoníaco con la coproducción de CaCl2 residual que se libera como efluente.
El óxido de magnesio es un importante compuesto que se emplea en diversas industrias. El óxido de magnesio tiene el punto de fusión más elevado de entre los óxidos con un precio moderado y es, por tanto, una importante materia prima para los ladrillos refractarios y otros materiales. Es el único material, además del ZrO2, que puede soportar un calentamiento durante largos periodos por encima de los 2000ºC.
Cabe citar la solicitud de patente US 20007019121 de Ghosh et al. que revela un método para la preparación de MgO a partir de la reacción de sal de magnesio con sosa cáustica o cal. El Mg (OH) 2 crudo se calcina directamente y posteriormente se trata con agua para desintegrar la masa espontáneamente y así generar una lechada y disolver las sales solubles. Esta lechada es mucho más fácil de filtrar y de lavar que la lechada original de Mg (OH) 2. No se menciona ningún método para acelerar la filtración de la propia lechada de Mg (OH) 2.
Objeto de la invención [0017] El principal objetivo de la presente invención es diseñar un proceso integral para la producción simultánea de
sulfato de potasio, sulfato de amonio, hidróxido de magnesio y/o óxido de magnesio a partir de sal mixta de kainita y amoníaco. [0018] Otro objetivo es convertir el subproducto de yeso generado en el proceso SOP/MgO de la patente US 7.041.268
en un fertilizante de sulfato de amonio más valioso mediante las técnicas anteriores del proceso de Merseberg a la vez
que se utiliza el subproducto de carbonato de calcio en el propio proceso integrado. [0019] Otro objetivo es someter el carbonato de calcio a calcinación y utilizar el dióxido de carbono en la producción de sulfato de amonio.
Otro objetivo es utilizar la cal obtenida de la calcinación del carbonato de calcio para la preparación de Mg (OH) 2
junto con el subproducto CaCl2 necesario para la desulfatación del licor final de schoenita. [0021] Otro objetivo de la invención es generar cal de calidad alta constante en el mismo proceso de modo que el Mg (OH) 2 obtenido de él tenga también una calidad alta constante.
Otro objetivo es modificar el Mg (OH) 2 en superficie para mejorar su filtrabilidad durante el proceso.
Otro objetivo es emplear dicho Mg (OH) 2 modificado en superficie en otras aplicaciones en las que dicha modificación sea deseable. [0024] Otro objetivo es someter el Mg (OH) 2 modificado en superficie a calcinación para producir MgO que se libera del
modificador de superficie y que posee una pureza º97 %.... [Seguir leyendo]
Reivindicaciones:
1. Un método para la producción simultánea de sulfato de potasio (SOP) , sulfato de amonio, hidróxido de magnesio modificado en superficie y/o óxido de magnesio caracterizado por la cogeneración de dichos productos utilizando sal mixta de kainita, en la que la kainita es una sal doble de KCl y MgSO4 acompañada de agua de cristalización y contiene, además, NaCl y MgCl2.6H2O como impurezas, y amoníaco como materias primas consumibles. Dicho proceso comprende las siguientes fases:
a) La conversión, en una primera zona de reacción, de la sal mixta de kainita en schoenita mediante el proceso de lixiviación acuosa, en la que dicho proceso comprende la reacción de la sal mixta con agua y un licor final de SOP de la fase (e) seguida de la separación de la schoenita pura y de un licor final de schoenita (SEL) .
b) El tratamiento del licor final de schoenita claro obtenido en la fase (a) con CaCl2 acuoso para separar el sulfato en forma de yeso, seguido de la filtración de la torta para recuperar el yeso y un licor final de schoenita desulfatada.
c) La exposición del licor final de schoenita desulfatada obtenido en la fase (b) a una evaporación para obtener una carnalita sólida y un licor rico en MgCl2.
d) La descomposición de la carnalita obtenida en la fase (c) con agua para recuperar el KCl y un licor descompuesto de carnalita (CDL) que contiene MgCl2 y KCl residual.
e) El tratamiento de la schoenita pura de la fase (a) con KCl obtenido en la fase (d) para producir sulfato de potasio (SOP) a la vez que se recicla el licor final de SOP en el proceso de la fase (a) .
f) El lavado del yeso recuperado en la fase (b) para minimizar las impurezas adherentes.
g) El contacto, en una segunda zona de reacción, del yeso obtenido en la fase (f) con un licor de amoníaco o un licor madre de sulfato de amonio obtenido en la fase (i) y dióxido de carbono obtenido en la fase (k) para producir una solución de sulfato de amonio y el subproducto CaCO3 mediante la reacción de Merseberg.
h) La filtración de CaCO3 a partir de los productos de la fase (g) , seguida de la neutralización del filtrado con ácido sulfúrico para convertir el amoníaco residual en sulfato de amonio.
i) La evaporación del filtrado neutralizado obtenido en la fase (h) con el fin de recuperar el sulfato de amonio a la vez que se recicla el licor madre de la fase (g) .
j) El lavado del CaCO3 obtenido en la fase (h) con agua para minimizar el yeso no reaccionado y las impurezas solubles adherentes, seguido de calcinaciones para obtener CO2 y cal viva de alta pureza.
k) El envasado del CO2 y el reciclaje en la fase (g) .
l) La extinción de la cal generada en la fase (j) con agua descarbonatada y el tratamiento con CDL generado en la fase (d) y/o licor rico en MgCl2 obtenido en la fase (c) para producir una dispersión de Mg (OH) 2 y CaCl2 acuoso.
m) La adición de un agente modificador de superficie para facilitar la filtración de Mg (OH) 2 a la vez que se obtiene simultáneamente Mg (OH) 2 modificado en superficie necesario para aplicaciones de composiciones especiales.
n) La separación del Mg (OH) 2 modificado en superficie a partir de la lechada obtenida en la fase (m) mediante cualquier proceso conocido, y la recuperación de un filtrado que contiene CaCl2 seguida de su reciclaje para el proceso de desulfatación de la fase (b) .
o) La calcinación del Mg (OH) 2 obtenido en la fase (n) para recuperar MgO de alta pureza que quema simultáneamente el modificador de superficie.
2. Un método según la reivindicación 1, en el que la sal mixta de kainita está compuesta por 15-22 % de KCl; 15-22 % de NaCl.
2. 40 % de MgSO4 y 5-10 % de MgCl2.
3. Un método según la reivindicación 1, en el que la operación de lixiviación acuosa de la fase (a) según la reivindicación 1 se realiza empleando agua dulce o agua subterránea salobre o incluso agua de mar junto con el licor final de SOP.
4. Un método según la reivindicación 1, en el que la proporción de K+ en forma de schoenita pura y de SEL de la fase
(a) es de 0, 8-1, 2 dependiendo de la cantidad de agua añadida y el contenido de sulfato de SEL oscila entre el 5-12 % (p/v) .
5. Un método según la reivindicación 1, en el que el yeso obtenido en la fase (b) tiene una pureza que oscila entre e.
9. 99 % (p/p) .
6. Un método según la reivindicación 1, en el que el CaCO3 obtenido en la fase (h) tiene una pureza que oscila entre e.
9. 97 %.
7. Un método según la reivindicación 1, en el que la calcinación del CaCO3 en la fase (j) se lleva a cabo en un intervalo de temperatura d.
80. 900ºC durante un período de 1 a 3 horas.
8. Un método según la reivindicación 1, en el que el agua descarbonatada empleada en la preparación de la lechada de cal (cal apagada) de la fase (1) se obtiene mediante el tratamiento del agua con cal y la eliminación de la materia en suspensión.
9. Un método según la reivindicación 1, en el que el cloruro de magnesio en el licor descompuesto de carnalita se complementa con el licor rico en MgCl2 de la fase (c) , si fuera necesario, para la preparación de CaCl2 y Mg (OH) 2 según el método de la fase (1) .
10. Un método según la reivindicación 1, en el que la proporción molar de la cal sobre MgCl2 oscila entre 0, 8:1 y 0, 95:1 en la reacción de la fase (1) .
11. Un método según la reivindicación 1, en el que el agente modificador de superficie en un ácido graso libre y, más 5 concretamente, un ácido esteárico y la proporción del agente modificador de superficie sobre el Mg (OH) 2 en la fase (m) oscila entre 0, 01:1 y 0, 05:1 (p/p) .
12. Un método según la reivindicación 1, en el que el índice de filtración de Mg (OH) 2 es 2-3 veces más rápido en una prensa de filtro y la torta húmeda de Mg (OH) 2 tiene un contenido de humedad un 8-15 % más bajo que aquel en el 10 que no se usa un agente modificador de superficie.
13. Un método según la reivindicación 1, en el que la pureza del MgO obtenida en la fase (o) oscila entre e.
9. 99, 59 % (expresada en peso seco) .
Patentes similares o relacionadas:
Procedimiento para la preparación de granulados de sulfato de potasio y el granulado de sulfato de potasio obtenido a partir del mismo, así como su uso, del 8 de Enero de 2020, de K+S Minerals and Agriculture GmbH: Procedimiento para la preparación de granulados de sulfato de potasio, caracterizado porque se añade una sal de sodio seleccionada a partir […]
Procedimiento para la preparación de granulados de sulfato de potasio y el granulado de sulfato de potasio obtenido por dicho procedimiento, así como su uso, del 17 de Abril de 2019, de K+S KALI GMBH: Procedimiento para la preparación de granulados de sulfato de potasio, caracterizado por que al sulfato de potasio se le añade durante la […]
Procedimiento de preparación cíclica para producir boruro de titanio a partir de una mezcla de carga de alimentación intermedia de sales de titanio-boro-flúor con base de sodio y para producir criolita de sodio como subproducto, del 18 de Mayo de 2016, de Shenzhen Sunxing Light Alloys Materials Co., Ltd: Un procedimiento de preparación cíclica para producir boruro de titanio a partir de una carga de alimentación intermedia que es una mezcla de fluoroborato […]
Procedimiento cíclico de preparación para la producción de boruro de titanio a partir de una materia prima intermedia basada en potasio de una mezcla salina de titanio-boro-flúor y la producción de criolita de potasio como subproducto, del 18 de Mayo de 2016, de Shenzhen Sunxing Light Alloys Materials Co., Ltd: Un procedimiento cíclico de preparación para la producción de boruro de titanio a partir de una materia prima intermedia que es una mezcla de fluoborato […]
MÉTODO PARA LA PRODUCCIÓN DE PARTÍCULAS DE PERCARBONATO DE SODIO RECUBIERTAS, del 26 de Abril de 2011, de EVONIK DEGUSSA GMBH: Proceso para la producción de partículas de percarbonato de sodio recubiertas por pulverización de una solución acuosa que contiene sulfato de sodio sobre partículas de […]
PROCESO MEJORADO PARA LA RECUPERACION DE SULFATO DE POTASA (SOP) A PARTIR DE UN AGUA MADRE RICA EN SULFATO, del 3 de Noviembre de 2010, de COUNCIL OF SCIENTIFIC AND INDUSTRIAL RESEARCH: Un proceso integrado para la producción de sulfato de potasa (SOP) a partir de un agua madre rica en sulfato, a partir de una sal mixta de tipo kainita, comprendiendo dicho […]
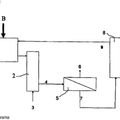 METODO PARA CRISTALIZAR SALES SOLUBLES DE ANIONES DIVALENTES A PARTIR DE SALMUERA, del 16 de Abril de 2010, de AKZO NOBEL N.V.: Un método para retirar al menos parcialmente una sal soluble de metal alcalino o de amonio, de un anión divalente, de una disolución acuosa de […]
METODO PARA CRISTALIZAR SALES SOLUBLES DE ANIONES DIVALENTES A PARTIR DE SALMUERA, del 16 de Abril de 2010, de AKZO NOBEL N.V.: Un método para retirar al menos parcialmente una sal soluble de metal alcalino o de amonio, de un anión divalente, de una disolución acuosa de […]
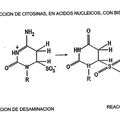 PROCEDIMIENTO MEJORADO PARA TRATAMIENTO DE BISULFITO, del 1 de Abril de 2008, de ROCHE DIAGNOSTICS GMBH F.HOFFMANN-LA ROCHE AG: Procedimiento para la conversión de una base de citosina, en un ácido nucleico, a una base de uracilo, que comprende las etapas de a) incubar una solución que comprende el […]
PROCEDIMIENTO MEJORADO PARA TRATAMIENTO DE BISULFITO, del 1 de Abril de 2008, de ROCHE DIAGNOSTICS GMBH F.HOFFMANN-LA ROCHE AG: Procedimiento para la conversión de una base de citosina, en un ácido nucleico, a una base de uracilo, que comprende las etapas de a) incubar una solución que comprende el […]