Método de purificación de anticuerpos terapéuticos y método de uso.
Un método de preparación de una inmunoglobulina anti-ß amiloide que consiste en tratar una inmunoglobulinaanti-ß amiloide a un pH de 11.
25 a 11.75 suficiente para disociar la proteína ß amiloide, o uno de sus fragmentos, dedicha inmunoglobulina anti-ß amiloide.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/AU2008/001466.
Solicitante: CSL LIMITED.
Nacionalidad solicitante: Australia.
Dirección: 45 POPLAR ROAD PARKVILLE VIC 3052 AUSTRALIA.
Inventor/es: COX,JOHN.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K38/17 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › que provienen de animales; que provienen de humanos.
- A61K39/395 A61K […] › A61K 39/00 Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53). › Anticuerpos (aglutininas A61K 38/36 ); Inmunoglobulinas; Inmunosuero, p. ej. suero antilinfocitario.
- A61P25/28 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 25/00 Medicamentos para el tratamiento de trastornos del sistema nervioso. › de los problemas neurodegenerativos del sistema nervioso central, p. ej. noótropos, activadores del conocimiento, medicamentos para el tratamiento del Alzheimer o de otras formas de demencia.
- C07K16/18 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 16/00 Inmunoglobulinas, p. ej. anticuerpos mono o policlonales. › contra materiales animales o humanos.
PDF original: ES-2442500_T3.pdf
Fragmento de la descripción:
Método de purificación de anticuerpos terapéuticos y método de uso Campo técnico Esta invención se refiere a la preparación de inmunoglobulina. Más concretamente, esta invención se refiere a la preparación de una inmunoglobulina anti-β amiloide que puede ser adecuada para la inmunoterapia de la enfermedad de Alzheimer.
La invención se expone en las reivindicaciones.
Antecedentes La enfermedad de Alzheimer es una enfermedad neurodegenerativa que, en su forma más común, se encuentra en personas mayores de 65 años. Aproximadamente 15 millones de personas en todo el mundo tienen la enfermedad de Alzheimer.
Los signos clínicos de la enfermedad de Alzheimer se caracterizan por deterioro cognitivo progresivo, junto con 20 disminución de las actividades relacionadas con la vida diaria y por síntomas neuropsiquiátricos o cambios de comportamiento.
La enfermedad de Alzheimer se caracteriza por la acumulación de placa en los tejidos cerebrales que está compuesta de péptidos β amiloides. La administración de anticuerpos anti-β amiloide en un modelo de la 25 enfermedad de Alzheimer en ratón parece reducir los depósitos de β amiloide en el cerebro del ratón y restaurar o aumentar la función cognitiva o al menos reducir la velocidad del deterioro cognitivo.
Hay anticuerpos naturales contra péptidos β amiloides presentes en el suero humano. La administración a seres humanos de preparados de inmunoglobulina humana obtenidos del suero humano se asocia a una disminución en los niveles de péptido β amiloide en el líquido cefalorraquídeo. [US2002/0009445.] Datos de un ensayo clínico reciente muestran resultados beneficiosos tanto en el comportamiento como en la cognición en pacientes con enfermedad de Alzheimer tratados con inmunoglobulina intravenosa ("IgIV") (http://www.news-medical.net/?id= 40383) .
Sin embargo, estos preparados de IgIV contienen cantidades significativas de péptidos β amiloides neurotóxicos y exhiben una variación significativa en la afinidad y el título del anticuerpo.
Previamente Duy et al., 2003, Brain, 126 1935 dieron a conocer la purificación de anticuerpos anti-β amiloide de inmunoglobulinas intravenosas humanas (IgIV) a pH 2.5. Estos anticuerpos se unieron a la proteína β amiloide y 40 protegieron de la neurotoxicidad a neuronas del hipocampo de ratas.
Li et al., 2004, BMC Neurosci., 5 21 dieron a conocer varios métodos para disociar anticuerpos anti-β amiloide de la proteína β amiloide, incluidos el uso de DTT 100 mM, betamercaptoetanol al 0.5% y pH 2.5.
Li et al., 2007, BMC Neurosci., 8 22 dieron a conocer que la incubación a pH 3.5 puede disociar complejos β amiloide-anticuerpo.
US 2006/099211 dio a conocer un método para la preparación de anticuerpos específicos para β amiloide que comprende la disociación ácida de complejos de beta amiloide-anticuerpo a pH 2.5.
Chung et al., 1967, J. Lipid Res. 8 631 describieron la purificación de anticuerpos anti-LDL de complejos anticuerpo-LDL por ultracentrifugación a pH alcalino. El pH óptimo fue el pH 11, ya que a mayor pH (por ej. pH 11.5) , el rendimiento se redujo debido a la agregación de la inmunoglobulina.
Resumen Se proporcionan preparaciones de inmunoglobulina anti-β amiloide en condiciones alcalinas donde la proteína β amiloide es escasamente soluble y por lo tanto, menos capaz de volver a unirse a la inmunoglobulina anti-β amiloide. La invención se expone en las reivindicaciones.
En un aspecto, un método de preparación de una inmunoglobulina anti-β amiloide consiste en tratar una inmunoglobulina anti-β amiloide inicial en condiciones alcalinas, suficientes para disociar la proteína β amiloide, o uno de sus fragmentos, de dicha inmunoglobulina anti-β amiloide inicial.
Convenientemente, la inmunoglobulina anti-β amiloide preparada según el método está sustancialmente exenta de proteína β amiloide unida.
En otro aspecto, un método de preparación de una composición implica preparar una inmunoglobulina anti-β amiloide tratando una inmunoglobulina anti-β amiloide inicial en condiciones alcalinas suficientes para disociar la proteína β amiloide, o uno de sus fragmentos, de dicha inmunoglobulina anti-β amiloide inicial y combinar la inmunoglobulina anti-β amiloide con un vehículo, diluyente o excipiente aceptable.
Aún en otro aspecto, se proporciona una inmunoglobulina anti-β amiloide aislada o purificada, preparada tratando una inmunoglobulina anti-β amiloide inicial en condiciones alcalinas suficientes para disociar la proteína β amiloide, o uno de sus fragmentos, de dicha inmunoglobulina anti-β amiloide inicial.
Se proporciona un método de preparación de una composición que comprende una inmunoglobulina anti-β amiloide, donde dicho método incluye tratar una inmunoglobulina anti-β amiloide inicial en condiciones alcalinas suficientes para disociar la proteína β amiloide, o uno de sus fragmentos, de dicha inmunoglobulina anti-β amiloide inicial; y un vehículo, diluyente o excipiente aceptable.
La composición preparada por el método es adecuada para tratar una enfermedad o afección asociada a placas de β amiloide, tales como la enfermedad de Alzheimer.
Un método para tratar una enfermedad o afección asociada a placas de β amiloide en un mamífero, puede implicar administrar a dicho mamífero una inmunoglobulina anti-β amiloide preparada tratando una inmunoglobulina anti-β amiloide inicial en condiciones alcalinas para disociar la proteína β amiloide, o uno de sus fragmentos, de dicha inmunoglobulina anti-β amiloide inicial y de ese modo tratar dicha enfermedad o afección en dicho mamífero.
En una realización, la enfermedad o afección asociada a placas de β amiloide es la enfermedad de Alzheimer.
En toda esta memoria, a menos que el contexto requiera algo diferente, las palabras "comprender" "comprende" o "que comprende", se entenderá que implican la inclusión de un número entero o grupo de números enteros establecidos, pero no la exclusión de ningún otro número entero ni grupo de números enteros.
Breve descripción de las figuras
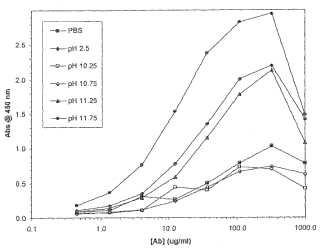
Figura 1: ELISA comparando la preparación de inmunoglobulina anti-β amiloide en presencia de (A) tampones de glicina:glicina HCl pH 2.5; glicina NaOH pH 10.25; glicina NaOH pH 10.75; glicina NaOH pH 11.25; y glicina NaOH pH 11.75. Figura 2: ELISA comparando la preparación de inmunoglobulina anti-β amiloide en presencia de tampones de dietilamina HCl: pH 10.25; pH 10.75; pH 11.25; y pH 11.75 con un control de glicina HCl pH 2.5.
Descripción detallada La proteína β amiloide unida específicamente se puede extraer de preparaciones de inmunoglobulinas anti-β amiloide en condiciones alcalinas. La purificación de inmunoglobulina anti-β amiloide IgIV en condiciones ácidas (por ejemplo aproximadamente pH 2) da como resultado proteína β amiloide soluble, que se puede volver a unir a la inmunoglobulina anti-β amiloide, particularmente cuando comienza la retroneutralización.
El tratamiento alcalino de la inmunoglobulina anti-β amiloide , incluso a un pH tan bajo como aproximadamente 10.5, disocia la proteína β amiloide de la inmunoglobulina anti-β amiloide, en las condiciones bajo las cuales la proteína βamiloide sigue siendo sustancialmente insoluble e incapaz de volver a ser unida por la inmunoglobulina anti-β amiloide. El método es particularmente adecuado para la elaboración a gran escala o industrial de la inmunoglobulina anti-β amiloide a partir de IgIV humana.
La mayor eficiencia de la inmunoglobulina anti-β amiloide después del tratamiento en condiciones alcalinas a escala industrial proporciona un proceso más viable desde el punto de vista comercial para la producción de inmunoglobulina anti-β amiloide.
Un método de preparación de una inmunoglobulina anti-β amiloide consiste en tratar una inmunoglobulina anti-β amiloide inicial en condiciones alcalinas suficientes para disociar la proteína β amiloide unida a inmunoglobulina, o uno de sus fragmentos, de dicha inmunoglobulina anti-β amiloide.
Inmunoglobulina anti-β amiloide aislada o purificada preparada por el método descrito más arriba.
Por "aislada" se entiende presente en un ambiente fuera de un estado natural o de lo contrario sometida a manipulación humana. El material aislado puede estar sustancialmente o esencialmente exento de componentes que normalmente lo acompañan en su estado natural, o puede ser manipulado para... [Seguir leyendo]
Reivindicaciones:
1. Un método de preparación de una inmunoglobulina anti-β amiloide que consiste en tratar una inmunoglobulina anti-β amiloide a un pH de 11.25 a 11.75 suficiente para disociar la proteína β amiloide, o uno de sus fragmentos, de 5 dicha inmunoglobulina anti-β amiloide.
2. El método de la reivindicación 1 donde la inmunoglobulina anti-β amiloide se obtiene del plasma humano.
3. El método de cualquiera de las reivindicaciones precedentes, que comprende además el paso de neutralizar al 10 menos parcialmente hasta un pH menor sin formar proteína β amiloide soluble.
4. El método de la reivindicación 3, que comprende además el paso de eliminar la proteína β amiloide insoluble por filtración, cromatografía o centrifugación.
6. Un método para preparar una inmunoglobulina anti-β amiloide de acuerdo con la reivindicación 1 que comprende:
(i) tratar una inmunoglobulina anti-β amiloide con un tampón de dietilamina HCl a un pH en el rango de 11.25-11.75 20 para disociar así sustancialmente la proteína β amiloide unida de dicha inmunoglobulina anti-β amiloide;
(ii) neutralizar parcialmente el pH de (i) a pH 9;
(iii) eliminar la proteína β amiloide;
(iv) neutralizar el pH de (ii) a un pH en el rango de pH 4.0-7.4; y
(v) recoger la inmunoglobulina anti-β amiloide. 25
7. El método de cualquiera de las reivindicaciones precedentes, donde (i) la inmunoglobulina anti-β amiloide preparada según el método está sustancialmente exenta de proteína β amiloide, (ii) la inmunoglobulina anti-βamiloide tiene actividad terapéutica con respecto a una enfermedad o afección asociada a placas de β amiloide y/o (iii) el método comprende además un paso de inactivación viral. 30
8. Un método de preparación de una composición de una inmunoglobulina anti-β amiloide, donde dicho método consiste en tratar una inmunoglobulina anti-β amiloide a un pH de 11.25 a 11.75 suficiente para disociar la proteína β amiloide, o uno de sus fragmentos, de dicha inmunoglobulina anti-β amiloide; y combinar la inmunoglobulina anti-β amiloide con un vehículo, diluyente o excipiente aceptable.
9. El método de la reivindicación 8, donde la composición es adecuada para tratar una enfermedad o afección asociada a placas de β amiloide en un mamífero.
10. El método de acuerdo con la reivindicación 9, donde dicho mamífero es un ser humano. 40
11. El método de acuerdo con la reivindicación 9, donde la enfermedad o afección es la enfermedad de Alzheimer.
Patentes similares o relacionadas:
Formulaciones estabilizadas que contienen anticuerpos anti-receptor de interleucina 4 (IL-4R), del 29 de Julio de 2020, de REGENERON PHARMACEUTICALS, INC.: Una jeringuilla precargada que contiene una formulación farmacéutica líquida estable, en la que la formulación farmacéutica líquida comprende: […]
Composición de anticuerpos monoclonales dirigidos contra BDCA-2, del 22 de Julio de 2020, de LABORATOIRE FRANCAIS DU FRACTIONNEMENT ET DES BIOTECHNOLOGIES: Composición de anticuerpos monoclonales dirigidos contra la proteína BDCA-2, presentando dichos anticuerpos un porcentaje de fucosilación inferior al 60% […]
Anticuerpos anti-PD-L1 y usos de los mismos, del 22 de Julio de 2020, de MERCK PATENT GMBH: Un anticuerpo anti-PD-L1 aislado o su fragmento de union a antigeno que comprende una secuencia de region variable de cadena pesada y de cadena ligera, en donde: […]
Composición para el tratamiento de enfermedades isquémicas o trastornos inflamatorios neurogénicos, que contienen el secretoma de células progenitoras neurales como ingrediente activo, del 22 de Julio de 2020, de S-BIOMEDICS: Una composición para uso en el tratamiento de enfermedad cerebrovascular isquémica, cardiopatía isquémica, infarto de miocardio, enfermedad de Alzheimer, enfermedad […]
Utilización de anticuerpos optimizados en ADCC para tratar a los pacientes con bajo nivel de respuesta, del 22 de Julio de 2020, de LABORATOIRE FRANCAIS DU FRACTIONNEMENT ET DES BIOTECHNOLOGIES: Utilización de una composición de anticuerpo monoclonal quimérico, humanizado o humano de isotipo IgG1 anti- Rhesus del glóbulo rojo humano cuya […]
Composiciones farmacéuticas que contienen una leucocidina E mutada, del 22 de Julio de 2020, de NEW YORK UNIVERSITY: Una composición que comprende: una proteína Leucocidina E (LukE) aislada que comprende la secuencia de aminoácidos de la SEQ ID NO: 4, o un polipéptido […]
Método para producir inmunoconjugados de anticuerpo-SN-38 con un enlazador CL2A, del 22 de Julio de 2020, de IMMUNOMEDICS, INC.: Un método para producir un compuesto, CL2A-SN-38, que presenta la estructura, **(Ver fórmula)** que comprende realizar un esquema de reacción como el que se muestra: **(Ver […]
Métodos de tratamiento y prevención de infecciones por staphylococcus aureus y afecciones asociadas, del 15 de Julio de 2020, de NEW YORK UNIVERSITY: Una composición para uso en un método de inmunización de un sujeto contra la infección por S. aureus, comprendiendo dicha composición: (i) un fragmento de polipéptido […]