Procedimiento para la desprotonación selectiva y funcionalización de 1-fluoro-2-substituido-3-clorobencenos.
Un procedimiento para la preparación de un litiobenceno de Fórmula I **Fórmula**
en la que
X representa F,
OR1 o NR2R3;
Y representa H o F; y
R1, R2 y R3 independientemente representan un grupo alquilo de C1-C4;
que comprende poner en contacto un fluorobenceno substituido de Fórmula II **Fórmula**
en la que X, Y, R1, R2 y R3 son como se define previamente
con un alquillitio en un disolvente orgánico inerte
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2009/030372.
Solicitante: DOW AGROSCIENCES LLC.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 9330 ZIONSVILLE ROAD INDIANAPOLIS, IN 46268-1054 ESTADOS UNIDOS DE AMERICA.
Inventor/es: RENGA,JAMES, ARNDT,KIM, EMONDS,MARK, OPPENHEIMER,JOSSIAN.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07F1/02 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07F COMPUESTOS ACICLICOS, CARBOCICLICOS O HETEROCICLICOS QUE CONTIENEN ELEMENTOS DISTINTOS DEL CARBONO, HIDROGENO, HALOGENOS, OXIGENO, NITROGENO, AZUFRE, SELENIO O TELURO (porfirinas que contienen metal C07D 487/22; compuestos macromoleculares C08). › C07F 1/00 Compuestos que contienen elementos de los grupos 1 o 11 del sistema periódico. › Compuestos de litio.
PDF original: ES-2424981_T3.pdf
Fragmento de la descripción:
Procedimiento para la desprotonación selectiva y funcionalización de 1-fluoro-2-substituido-3-clorobencenos Esta solicitud reivindica el beneficio de la solicitud provisional de los EE.UU. número de serie 61/010.918 presentada el 11 de enero de 2008. La presente invención se refiere a un procedimiento para la desprotonación selectiva y funcionalización en la posición adyacente al substituyente fluoro de ciertos 1-fluoro-2-substituido-3-clorobencenos.
Las patentes de EE.UU. 7.314.849 y 7.300.907 describen respectivamente ciertos compuestos de 6- (arilo polisubstituido) -4-aminopicolinato y ácido 2- (arilo poli-substituido) -6-amino-4-pirimidinocarboxílico y su uso como herbicidas. Los derivados de ácido 2-fluoro-3-substituido-4-clorofenilborónico son intermedios útiles para la preparación de estos herbicidas.
En las patentes 7.314.849 y 7.300.907, por ejemplo, los derivados de ácido 2-fluoro-3-substituido-4clorofenilborónico se preparan por intercambio halógeno-metal de 1-bromo-2-fluoro-3-substituido-4-clorobencenos con n-butillitio seguido enfriamiento rápido con un éster de ácido borónico.
Sería ventajoso producir estos materiales por desprotonación directa en lugar de por intercambio halógeno-metal. Esto permite el uso, por ejemplo, de materiales de partida menos complejos y evita la formación de una corriente de desecho bromada. Schlosser et al.: “Organometallics in Synthesis, A Manual” XX, (2002) , páginas 223-247 describen la preparación de 1, 2, 4-trifluoro-3-litiobenceno de 1, 2, 4-trifluorobenceno y LiCH (CH3) C2H5 en THF a -75ºC (página 223 entrada 6) .
La presente invención se refiere a la desprotonación altamente selectiva de 1-fluoro-2-substituido-3-clorobencenos en la posición adyacente al substituyente fluoro con compuestos de alquillitio. Los litiobencenos resultantes se derivan o funcionalizan adicionalmente por reacción con reactivos electrófilos. Más particularmente, la presente invención se refiere a un procedimiento para la preparación de un litiobenceno de Fórmula I
en la que X representa F, OR1 o NR2R3; Y representa H o F; y R1, R2 y R3 independientemente representan un grupo alquilo de C1-C4; que comprende poner en contacto un fluorobenceno substituido de Fórmula II
en la que X, Y, R1, R2 y R3 son como se define previamente con un alquillitio en un disolvente orgánico inerte. En otro aspecto de la presente invención, los litiobencenos se ponen en contacto adicionalmente con un reactivo electrófilo. Los reactivos electrófilos preferidos incluyen ésteres de ácido borónico, dióxido de carbono, N, N-dialquilformamidas y formiatos de alquilo.
El término alquilo y términos derivados tales como alcoxi, tal como se usan aquí, incluyen grupos de cadena lineal, de cadena ramificada y cíclica. De este modo, los grupos alquilo típicos son metilo, etilo, 1-metiletilo, propilo, ciclopropilo, butilo, 1, 1-dimetiletilo, ciclobutilo y 1-metilpropilo. Son a menudo preferidos metilo y etilo. Los grupos alquilo se denominan a veces normal (n) , iso (i) , secundario (s) , o terciario (t) .
Las materiales de partida de 1-fluoro-2-substituido-3-clorobenceno son compuestos conocidos y se pueden preparar por procedimientos bien conocidos por los expertos en la técnica.
La desprotonación selectiva en la posición adyacente al substituyente fluoro se consigue poniendo en contacto el 5 material de partida 1-fluoro-2-substituido-3-clorobenceno con un alquillitio en un disolvente orgánico inerte.
El compuesto de alquillitio sirve como base fuerte. Se puede emplear cualquier compuesto de alquillitio; se prefieren compuestos de alquillitio comercialmente disponibles como metillitio, n-butillitio y s-butillitio. Aunque la conversión completa requeriría un equivalente de la base alquillitio, a menudo es más beneficioso efectuar la reacción con un ligero exceso del alquillitio.
Típicamente se prefiere un exceso de un 1 a 10 por ciento molar de alquillitio siendo más preferido un exceso de un 2 a 5 por ciento molar.
La reacción se efectúa en condiciones anhidras en un disolvente orgánico inerte, es decir, un material orgánico en el que los reactantes son por lo menos parcialmente solubles y que es químicamente inerte a los reactantes. Ser químicamente inerte a los reactantes significa que el disolvente es por lo menos menos reactivo que lo que lo son 15 los 1-fluoro-2-substituido-3-clorobencenos con la base fuerte de alquillitio. Los disolventes orgánicos inertes apropiados incluyen hidrocarburos de C5-C8 de cadena lineal, ramificada o cíclica, tales como pentanos, hexanos, ciclohexano e iso-octano, y éteres, tales como éter dietílico, tetrahidrofurano, dioxano y éteres de glicol. Son generalmente preferidos los éteres. Son a menudo preferidas las mezclas de hidrocarburos y éteres, siendo las más preferidas las mezclas de tetrahidrofurano o 1, 2-dimetoxietano y las mezclas comerciales de octanos. La desprotonación se efectúa a una temperatura de -100ºC a 0ºC dependiendo de la naturaleza del substituyente X, del disolvente y del alquillitio empleado. La temperatura óptima se puede determinar fácilmente por optimización de rutina. Por ejemplo, cuando X es F o Cl, la temperatura preferida para la desprotonación es de -100ºC a 50ºC. Cuando X es OR1 o NR2R3, la temperatura preferida para la desprotonación es de -70ºC a -50ºC.
El procedimiento no es sensible a la presión y se lleva a cabo usualmente a presión atmosférica o ligeramente por 25 encima de presión atmosférica. El procedimiento se efectúa preferentemente en una atmósfera inerte seca tal como la proporcionada por una capa de nitrógeno.
Los litiobencenos de Fórmula I no se aíslan típicamente sino que se hacen reaccionar con un reactivo electrófilo. Un reactivo electrófilo se define como un reactivo que busca un par de electrones. Los reactivos electrófilos apropiados incluyen pero no están limitados a bromo, yodo, azufre, disulfuros, dióxido de azufre, ésteres de ácido borónico, 30 dióxido de carbono, haluros de sulfurilo, haluros de fosforilo, aldehídos, amidas y haluros de alquilo o acilo. Los ésteres de ácido borónico, dióxido de carbono, N, N-dialquilformamidas y formiatos de alquilo son reactivos electrófilos particularmente preferidos. Se puede enfriar la mezcla de reacción de litiobenceno y añadir el reactivo electrófilo a la disolución de reacción. Alternativamente, el litiobenceno se puede añadir al reactivo electrófilo a de 70ºC a -50ºC cuando X representa OR1 o NR2R3 y a de -100ºC a -60ºC cuando X representa F o Cl. El producto final, cuyas propiedades dependerán de la naturaleza del reactivo electrófilo, se puede aislar y recuperar por procedimientos convencionales bien conocidos por los expertos en la técnica.
En una reacción típica, se disuelve un material de partida de 1-fluoro-2-substituido-3-clorobenceno en un disolvente etéreo seco en atmósfera de nitrógeno. Se enfría la mezcla de reacción y se añade el compuesto de alquillitio; la mezcla de reacción se deja agitar hasta que la desprontonación es completa. La mezcla de reacción se enfría de nuevo y a continuación se trata con un reactivo electrófilo. Después de que se enfría completamente el litiobenceno, se trata la mezcla de reacción para recuperar el producto.
Se presentan los siguientes ejemplos para ilustrar la invención.
Ejemplos 1. Preparación de 2- (4-cloro-2-fluoro-3-metoxi-fenil) -[1, 3, 2]-dioxaborinano A una disolución de 2-cloro-6-fluoroanisol (100 g) en 1 litro (l) de 1, 2-dimetoxietano (DME) seco, enfriada a -70ºC, se añadieron 274 mililitros (ml) de n-BuLi 2, 5M en hexano durante 12 minutos (min) con buena agitación magnética. Durante la adición la reacción se calentó hasta -58ºC. Se retiró el baño de hielo seco y se dejó calentar la reacción hasta -50ºC durante 20 minutos para permitir que se disolviera una pequeña cantidad de un sólido blanco. Se retiró
una pequeña muestra directamente en una jeringuilla de 1 ml que contiene 0, 15 ml de MeSSMe. La muestra se diluyó con éter y se extrajo con agua. Se analizó la fase orgánica por GC. Solo estaba presente el 4% del material de partida en el barrido.
La disolución se enfrió a -70ºC, antes de añadir 74, 4 gramos (g) de borato de trimetilo gota a gota. La adición tardó 15 minutos y la temperatura se mantuvo por debajo de -45ºC. La disolución incolora se calentó a 0ºC con un baño de agua caliente antes de que se añadieran 140 g de HCl ac. al 37% casi de una vez. La disolución casi incolora desprendió un gas y llegó a 27ºC y se agitó durante 20 min antes de transferir la mezcla de dos fases a un embudo de separación. La capa acuosa viscosa inferior (285 ml) se separó y reservó. La fase orgánica... [Seguir leyendo]
Reivindicaciones:
1. Un procedimiento para la preparación de un litiobenceno de Fórmula I
en la que X representa F, OR1 o NR2R3; Y representa H o F; y R1, R2 y R3 independientemente representan un grupo alquilo de C1-C4; que comprende poner en contacto un fluorobenceno substituido de Fórmula II
en la que X, Y, R1, R2 y R3 son como se define previamente con un alquillitio en un disolvente orgánico inerte.
2. El procedimiento de la reivindicación 1, en el que el alquillitio es n-butillitio.
3. El procedimiento de la reivindicación 1, en el que el disolvente orgánico inerte es un hidrocarburo, un éter o sus mezclas.
5. El procedimiento de la reivindicación 1, en el que la mezcla de reacción se pone en contacto adicionalmente con un reactivo electrófilo.
6. El procedimiento de la reivindicación 5, en el que el reactivo electrófilo es ésteres de ácido borónico, dióxido de carbono, N, N-dialquilformamidas o formiatos de alquilo.
en la que X representa OR1 o NR2R3; Y representa H o F;
Z representa –CO2H o –CHO; y R1, R2 y R3 independientemente representan un grupo alquilo de C1-C4.
8. Los compuestos de la reivindicación 7, en los que X representa OCH3 e Y representa H.
Patentes similares o relacionadas:
Iniciadores de polimerización aniónica y procesos, del 26 de Abril de 2017, de BRIDGESTONE CORPORATION: Un método para fabricar un polímero funcionalizado en un recipiente de reacción, comprendiendo dicho método iniciar la polimerización de uno o más tipos de monómeros […]
Iniciador bifuncional de organolitio y copolímeros de dieno conjugado preparados utilizando el mismo, del 18 de Marzo de 2015, de LG CHEM LTD.: Compuesto de organolitio representado por la fórmula 1:**Fórmula** en la que R1 y R2, que pueden ser iguales o distintos representan, cada uno de ellos […]
 Procedimiento de preparación de metil litio, del 6 de Agosto de 2014, de Rockwood Lithium Inc: Una disolución de metil litio que comprende metil litio;
un disolvente aromático;
y de 2 a 4 equivalentes de MeTHF por mol de metil litio.
Procedimiento de preparación de metil litio, del 6 de Agosto de 2014, de Rockwood Lithium Inc: Una disolución de metil litio que comprende metil litio;
un disolvente aromático;
y de 2 a 4 equivalentes de MeTHF por mol de metil litio.
Proceso para la preparación de carbonato de litio de alta pureza, del 26 de Marzo de 2014, de Simbol, Inc: Un método para producir carbonato de litio de alta pureza, que comprende los siguientes pasos: hacer reaccionar con CO2 una primera solución acuosa que comprende un Li2CO3 […]
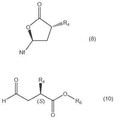
 Derivados de 3-alquil-5-(4-alquil-5-oxo-tetrahidrofuran-2-il)-pirrolidin-2-ona como productos intermedios en la síntesis de inhibidores de renina, del 28 de Octubre de 2013, de NOVARTIS AG: Compuesto de fórmula (II) **Fórmula**
en la que
R3 es alquilo C1-7 o cicloalquilo C3-8; y
R4 es alquilo C1-7, alquenilo C2-7, cicloalquilo C3-8, fenil o naftilalquilo […]
Derivados de 3-alquil-5-(4-alquil-5-oxo-tetrahidrofuran-2-il)-pirrolidin-2-ona como productos intermedios en la síntesis de inhibidores de renina, del 28 de Octubre de 2013, de NOVARTIS AG: Compuesto de fórmula (II) **Fórmula**
en la que
R3 es alquilo C1-7 o cicloalquilo C3-8; y
R4 es alquilo C1-7, alquenilo C2-7, cicloalquilo C3-8, fenil o naftilalquilo […]
 Síntesis convergente de inhibidores de renina y compuestos intermedios útiles en la misma, del 16 de Octubre de 2013, de DSM IP ASSETS B.V.: Un método para la preparación de un compuesto que satisface la fórmula o una sal farmacéuticamenteaceptable del mismo,**Fórmula**
seleccionándose R1 del […]
Síntesis convergente de inhibidores de renina y compuestos intermedios útiles en la misma, del 16 de Octubre de 2013, de DSM IP ASSETS B.V.: Un método para la preparación de un compuesto que satisface la fórmula o una sal farmacéuticamenteaceptable del mismo,**Fórmula**
seleccionándose R1 del […]
Composición organométalica de activación para la (co)polimerización de alfa-olefinas, que comprenden compuestos ciclopentadienilo fluorados, del 13 de Mayo de 2013, de versalis S.p.A: Composición organometálica que se puede usar como componente de activación en un catalizador metaloceno para la (co)polimerización de α-olefinas, caracterizada […]
NUEVO INICIADOR DICARBANIÓNICO, UN PROCEDIMIENTO PARA SU PREPARACIÓN Y USO DEL MISMO, del 9 de Mayo de 2011, de COUNCIL OF SCIENTIFIC AND INDUSTRIAL RESEARCH: Un nuevo iniciador dicarbanionico, de formula (I):** Fórmula**