Ensayos para el nt-pro-péptido natriurético de tipo b humano, el pro-péptido natriurético de tipo b humano y el péptido natriurético de tipo b humano.
Un inmunoensayo para cuantificar la cantidad de NT-pro-péptido natriurético de tipo B humano ("NT-proBNPhumano"),
de pro-péptido natriurético de tipo B humano ("proBNP humano") y de péptido natriurético cerebral5 humano ("hBNP") en una muestra de prueba que se está ensayando o que se sospecha que contiene el NT-proBNPhumano, el proBNP humano y el hBNP, comprendiendo el procedimiento las etapas de:
(a) poner en contacto una muestra de prueba con (i) un primer anticuerpo de captura que se une al NT-proBNPhumano y que ha sido inmovilizado sobre una fase sólida para producir un primer anticuerpo inmovilizado yformar una primera mezcla que comprende un complejo del primer anticuerpo de captura-NT-proBNP humano;
(ii) un segundo anticuerpo de captura que se une al proBNP humano y que ha sido inmovilizado sobre una fasesólida para producir un segundo anticuerpo inmovilizado y formar una segunda mezcla que comprende uncomplejo del segundo anticuerpo de captura-proBNP humano; y (iii) el segundo anticuerpo de captura, queademás de unirse al proBNP humano también se une al hBNP y que ha sido inmovilizado sobre una fase sólidapara producir un tercer anticuerpo inmovilizado y formar una tercera mezcla que comprende un complejo delsegundo anticuerpo de captura-hBNP humano, en el que dicho primer anticuerpo de captura comprende elanticuerpo 15F11 y el segundo anticuerpo de captura comprende el anticuerpo 8.1;
(b) poner en contacto dicha primera mezcla que comprende el complejo del primer anticuerpo de captura-NTproBNP humano con un primer anticuerpo de detección que se une al NT-proBNP humano y que ha sidoconjugado con un marcador detectable para formar una tercera mezcla que comprende un complejo del primeranticuerpo de captura-NT-proBNP humano-primer anticuerpo de detección, en el que el primer anticuerpo dedetección es el anticuerpo 15C4;
(c) poner en contacto dicha según la mezcla que comprende el complejo del segundo anticuerpo de capturaproBNPhumano con el primer anticuerpo de detección que, además de unirse al NT-proBNP humano, tambiénse une al proBNP humano, y que ha sido conjugado con un marcador detectable para formar una quinta mezclaque comprende un complejo del segundo anticuerpo de captura-proBNP humano-primer anticuerpo de detección,en el que el primer anticuerpo de detección es el anticuerpo 15C4;
(d) poner en contacto la tercera mezcla que comprende el complejo del segundo anticuerpo de captura- hBNPhumano con un segundo anticuerpo de detección que se une al hBNP y que ha sido conjugado con un marcadordetectable para formar una sexta mezcla que comprende un complejo del segundo anticuerpo de captura-hBNPsegundoanticuerpo de detección, en el que el segundo anticuerpo de detección es el anticuerpo 201.3; y
(e) determinar la cantidad de (i) el complejo del primer anticuerpo de captura-NT-proBNP humano-primeranticuerpo de detección formado en la etapa (b) mediante la detección del marcador detectable como unamedida de la cantidad de NT-proBNP humano contenido en la muestra de prueba; (ii) el complejo segundo deanticuerpo de captura-proBNP humano-primer anticuerpo de detección formado en la etapa (c) mediante ladetección del marcador detectable como una medida de la cantidad de proBNP humano contenido en la muestrade prueba; y (iii) el complejo del segundo anticuerpo de captura-hBNP-segundo anticuerpo de detección formadoen la etapa (d) mediante la detección del marcador detectable como una medida de la cantidad de hBNPcontenido en la muestra de prueba.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2010/056932.
Solicitante: AbbVie Inc.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 1 North Waukegan Road North Chicago, IL 60064 ESTADOS UNIDOS DE AMERICA.
Inventor/es: KONRATH,John,G, MOORE,JEFF A.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- G01N33/50 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › Análisis químico de material biológico, p. ej. de sangre o de orina; Ensayos mediante métodos en los que interviene la formación de uniones bioespecíficas con grupos coordinadores; Ensayos inmunológicos (procedimientos de medida o ensayos diferentes de los procedimientos inmunológicos en los que intervienen enzimas o microorganismos, composiciones o papeles reactivos a este efecto, procedimientos para preparar estas composiciones, procedimientos de control sensibles a las condiciones del medio en los procedimientos microbiológicos o enzimáticos C12Q).
- G01N33/53 G01N 33/00 […] › Ensayos inmunológicos; Ensayos en los que interviene la formación de uniones bioespecíficas; Materiales a este efecto.
PDF original: ES-2436867_T3.pdf
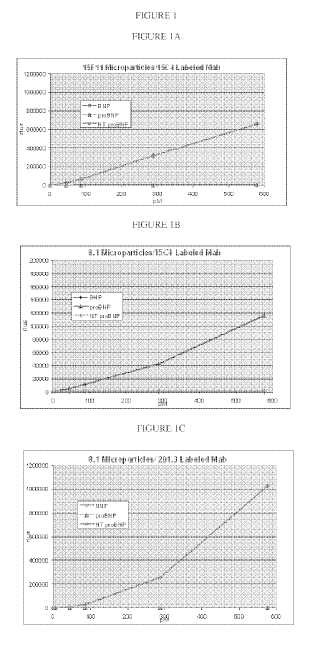
Fragmento de la descripción:
Ensayos para el nt-pro-péptido natriurético de tipo b humano, el pro-péptido natriurético de tipo b humano y el péptido natriurético de tipo b humano 5
Campo técnico En un aspecto, la presente desvelación se refiere a ensayos para detectar y/o cuantificar la cantidad de nt-propéptido natriurético de tipo B humano, de pro-péptido natriurético de tipo B humano y de péptido natriurético de tipo B humano en alícuotas obtenidas a partir de una muestra de prueba. En otro aspecto, la presente desvelación se refiere a reactivos inmunodiagnósticos para su uso en un ensayo para detectar y/o cuantificar la cantidad de nt-propéptido natriurético de tipo b humano, de pro-péptido natriurético de tipo b humano y de péptido natriurético de tipo b humano en una muestra de prueba. Aun en otro aspecto más, la presente desvelación se refiere a kits para su uso en la realización de un ensayo para detectar y/o cuantificar la cantidad de nt-pro-péptido natriurético de tipo b
humano, de pro-péptido natriurético de tipo b humano y de péptido natriurético de tipo b humano en una muestra de prueba.
Antecedentes El péptido natriurético atrial (en lo sucesivo "ANP") , el péptido natriurético de tipo B (en lo sucesivo "BNP") , el péptido natriurético de tipo C (en lo sucesivo "CNP") y el péptido natriurético Dendroaspis (en lo sucesivo "DNP") son cada uno miembros de una familia de hormonas conocidas como "péptidos natriuréticos". El ANP y el BNP comparten un amplio espectro de propiedades biológicas y pertenecen al sistema natriurético cardíaco. Tanto el ANP como el BNP tienen su origen en las células miocárdicas, mientras que el CNP tiene su origen en las células endoteliales. El DNP se aisló del veneno de la serpiente mamba verde y posee una similitud estructural con el ANP, el BNP y el CNP.
El ANP es secretado por el corazón en las aurículas. El ANP tiene un anillo de 17 aminoácidos cerrado por un puente de disulfuro entre dos residuos de cisteína. Once de los diecisiete aminoácidos del anillo están conservados en el ANP, el BNP, el CNP y el DNP. Además de la estructura anular de 17 aminoácidos, el ANP tiene una cola amino-terminal de 6 aminoácidos y una cola carboxi-terminal de 5 aminoácidos. El ANP es producido en forma de un pro-ANP de 126 aminoácidos que es la principal forma de almacenamiento del ANP. Después de la escisión proteolítica entre los aminoácidos 98 y 99, el péptido maduro de ANP de 28 aminoácidos se encuentra en el plasma sinusal coronario (Véase Yandle, J. Internal Med., 235: 561 -576 (1994) ) .
El BNP recibe su nombre debido a que se aisló por primera vez a partir de cerebro porcino, por lo que inicialmente, "BNP" significaba "péptido natriurético cerebral". Sin embargo, debido a que se averiguó que el BNP pertenecía al sistema natriurético cardiaco, la palabra "cerebral" se modificó por "de tipo B". Por lo tanto, "BNP" se refiere ahora a "péptido natriurético de tipo B". En los seres humanos, el BNP es secretado por el corazón a través del seno coronario, predominantemente desde los ventrículos cardíacos. El precursor pre-pro-péptido del BNP humano (en lo sucesivo, "pre-proBNP humano") tiene 134 aminoácidos de longitud (ID. SEC. Nº: 1) que comprende un péptido de señalización corto, que es escindido enzimáticamente para liberar el pro-péptido humano del BNP (en lo sucesivo "proBNP humano") que tiene 108 aminoácidos de longitud (ID. SEC. Nº: 2) . El proBNP humano es adicionalmente escindido en un pro-péptido N-terminal del BNP humano (en lo sucesivo "NT-proBNP humano") que tiene 76
aminoácidos de longitud (ID. SEC. Nº: 3) y la hormona activa, el BNP humano (en lo sucesivo "hBNP" o "hBNP-32") , que tiene 32 aminoácidos de longitud (ID. SEC. Nº: 4) . Se ha sugerido que cada uno de los NT-pro-BNP, hBNP-32 y proBNP humanos pueden circular en el plasma humano (véase, Tateyama y col., Biochem. Biophys. Res. Commun.
185: 760 -7 (1992) ; Hunt y col., Biochem. Biophys. Res. Commun. 214: 1175 -83 (1995) ) .
El CNP se encontró por primera vez en el cerebro, sin embargo, en su mayor parte se origina en las células endoteliales y renales. Está ampliamente distribuido en la vasculatura, el cerebro, el hueso y el endotelio. Hay poco, si lo hay, CNP presente en el corazón. El pro-CNP es un péptido de 103 aminoácidos que es procesado bien en el CNP-53 (aminoácidos 51 a 103) o bien en el CNP-22 (aminoácidos 82 a 103) , que son los péptidos activos. Al igual que el ANP, el CNP tiene un anillo de 17 aminoácidos cerrado por un puente de disulfuro entre residuos de cisteína.
Además de esta estructura anular de 17 aminoácidos, el CNP-22 tiene una cola amino-terminal de 5 aminoácidos y no contiene una cola carboxi-terminal. El CNP-53 es idéntico al CNP-22 excepto por una extensión de 31 aminoácidos en el extremo amino-terminal.
Como se ha mencionado previamente, el DNP se aisló a partir del veneno de la serpiente mamba verde. La forma madura del DNP está formada por 38 aminoácidos. Se ha informado de una inmunorreactividad de tipo DNP (DNP-LI) en plasma humano, y se ha averiguado que la concentración plasmática de DNP-LI está elevada en pacientes con insuficiencia cardiaca congestiva (véase, Cataliotti, y col., Mayo Clin. Proc., 76: 111 -1119 (2001) ) . Adicionalmente, también se sabe que la infusión de DNP sintético da como resultado una notable natriuresis y diuresis en asociación con un aumento del monofosfato de guanosina cíclico en plasma y orina. Id.
En los seres humanos, una cardiopatía puede estimular la secreción de ANP y de BNP. De hecho, la secreción de ANP y de BNP en seres humanos refleja típicamente un cambio en la función cardíaca. Específicamente, la secreción de ANP está típicamente acelerada cuando la aurícula sufre una carga, mientras que la biosíntesis y la secreción de BNP se estimulan cuando el ventrículo sufre una carga. Por consiguiente, tanto el ANP como el BNP son útiles como indicadores en el diagnóstico de cardiopatía. Sin embargo, a pesar de esto y con el tiempo, el BNP
se ha reconocido como un indicador útil en el diagnóstico de cardiopatía, más que el ANP. Por ejemplo, la concentración sanguínea del BNP es sólo de 1/6 de la del ANP en un sujeto normal, pero llega a ser superior a la del ANP en pacientes con insuficiencia cardiaca. Además, la concentración sanguínea del BNP aumenta en el caso de insuficiencia cardiaca, al igual que la del ANP, la concentración plasmática del BNP a menudo excede la del ANP, reflejando así de forma más precisa la gravedad de la alteración cardiaca. Además, el nivel de BNP en pacientes con insuficiencia cardiaca aumenta a menudo entre varias decenas hasta varias centenas el de los sujetos sanos normales.
Se sabe que el proBNP humano, el NT-proBNP humano y el hBNP pueden circular y pueden ser detectados en muestras de prueba de pacientes que padecen una patología cardiovascular, particularmente insuficiencia cardiaca.
Tanto el hBNP como el NT-proBNP humano se usan frecuentemente como marcadores para detectar una insuficiencia cardiaca y para evaluar el riesgo de la misma en pacientes. Sin embargo, la cantidad real de cada una de las formas individuales del BNP (es decir, el proBNP humano, el NT-proBNP humano y el BNP humano) que circula es dudosa debido a las reactividades cruzadas de los ensayos comerciales actuales para estas diversas formas (véase, Liang F., y col., J. American College of Cardiology, 49 (10) : 1071 -1078 (2007) ) .
Adicionalmente, se sabe que el proBNP humano y el NT-proBNP humano pueden estar glucosilados (véase, Schellenberger, U. y col., Archives of Biochemistr y and Biophysics, 451: 160 -166 (2006) ) , y estas formas glucosiladas han sido aisladas a partir de muestras humanos (véase, Hammerer-Lercher A., y col., Clinical Chemistr y , 54 (5) : 858 -865 (2008) y Seferian, K. y col., Clinical Chemistr y , 54 (5) : 866 -873 (2008) ) . Existen siete posibles sitios de glucosilación confinados en una región de 36 aminoácidos dentro de la porción N-terminal del péptido (desde el aminoácido 36 hasta el 71) . Los anticuerpos generados contra esta región pueden unirse o no a las muestras que contienen el analito proBNP o NT-proBNP humanos, dependiendo de: 1) el inmunógeno usado para crear el anticuerpo; y 2) si el analito está o no glucosilado. Los ensayos funcionales para el proBNP y el NTproBNP humanos deberían usar anticuerpos que eviten estas regiones.
En vista de lo cual, existe una necesidad de la técnica de nuevos ensayos que sean capaces de cuantificar simultáneamente la cantidad de NT-proBNP humano, de proBNP humano y de BNP humano en una muestra de prueba. La presente desvelación persigue proporcionar nuevos ensayos y procedimientos. La presente desvelación... [Seguir leyendo]
Reivindicaciones:
1. Un inmunoensayo para cuantificar la cantidad de NT-pro-péptido natriurético de tipo B humano ("NT-proBNP humano") , de pro-péptido natriurético de tipo B humano ("proBNP humano") y de péptido natriurético cerebral
humano ("hBNP") en una muestra de prueba que se está ensayando o que se sospecha que contiene el NT-proBNP humano, el proBNP humano y el hBNP, comprendiendo el procedimiento las etapas de:
(a) poner en contacto una muestra de prueba con (i) un primer anticuerpo de captura que se une al NT-proBNP humano y que ha sido inmovilizado sobre una fase sólida para producir un primer anticuerpo inmovilizado y formar una primera mezcla que comprende un complejo del primer anticuerpo de captura-NT-proBNP humano;
(ii) un segundo anticuerpo de captura que se une al proBNP humano y que ha sido inmovilizado sobre una fase sólida para producir un segundo anticuerpo inmovilizado y formar una segunda mezcla que comprende un complejo del segundo anticuerpo de captura-proBNP humano; y (iii) el segundo anticuerpo de captura, que además de unirse al proBNP humano también se une al hBNP y que ha sido inmovilizado sobre una fase sólida
para producir un tercer anticuerpo inmovilizado y formar una tercera mezcla que comprende un complejo del segundo anticuerpo de captura-hBNP humano, en el que dicho primer anticuerpo de captura comprende el anticuerpo 15F11 y el segundo anticuerpo de captura comprende el anticuerpo 8.1;
(b) poner en contacto dicha primera mezcla que comprende el complejo del primer anticuerpo de captura-NTproBNP humano con un primer anticuerpo de detección que se une al NT-proBNP humano y que ha sido conjugado con un marcador detectable para formar una tercera mezcla que comprende un complejo del primer anticuerpo de captura-NT-proBNP humano-primer anticuerpo de detección, en el que el primer anticuerpo de detección es el anticuerpo 15C4;
(c) poner en contacto dicha según la mezcla que comprende el complejo del segundo anticuerpo de capturaproBNP humano con el primer anticuerpo de detección que, además de unirse al NT-proBNP humano, también
se une al proBNP humano, y que ha sido conjugado con un marcador detectable para formar una quinta mezcla que comprende un complejo del segundo anticuerpo de captura-proBNP humano-primer anticuerpo de detección, en el que el primer anticuerpo de detección es el anticuerpo 15C4;
(d) poner en contacto la tercera mezcla que comprende el complejo del segundo anticuerpo de captura-hBNP humano con un segundo anticuerpo de detección que se une al hBNP y que ha sido conjugado con un marcador detectable para formar una sexta mezcla que comprende un complejo del segundo anticuerpo de captura-hBNPsegundo anticuerpo de detección, en el que el segundo anticuerpo de detección es el anticuerpo 201.3; y
(e) determinar la cantidad de (i) el complejo del primer anticuerpo de captura-NT-proBNP humano-primer anticuerpo de detección formado en la etapa (b) mediante la detección del marcador detectable como una medida de la cantidad de NT-proBNP humano contenido en la muestra de prueba; (ii) el complejo segundo de
anticuerpo de captura-proBNP humano-primer anticuerpo de detección formado en la etapa (c) mediante la detección del marcador detectable como una medida de la cantidad de proBNP humano contenido en la muestra de prueba; y (iii) el complejo del segundo anticuerpo de captura-hBNP-segundo anticuerpo de detección formado en la etapa (d) mediante la detección del marcador detectable como una medida de la cantidad de hBNP contenido en la muestra de prueba.
2. El inmunoensayo de la reivindicación 1, en el que la fase sólida se elige de entre el grupo que consiste en una partícula magnética, una microesfera, un tubo de ensayo, una placa de microtitulación, una cubeta, una membrana, una molécula estructural, una película, un papel de filtro, un disco y un chip.
4. El inmunoensayo de la reivindicación 1, en el que el marcador detectable del segundo anticuerpo de detección se elige de entre el grupo que consiste en un marcador radioactivo, un marcador enzimático, un marcador quimioluminiscente, un marcador fluorescente, un marcador termométrico y un inmunomarcador de reacción en cadena de la polimerasa.
(a) poner en contacto una muestra de prueba con (i) un primer anticuerpo de detección que se une al NT-proBNP humano y que ha sido con un marcador detectable para formar una primera mezcla que comprende un complejo de NT-proBNP-primer anticuerpo de detección; (ii) el primer anticuerpo de detección que, además de unirse al NT-proBNP humano, también se une al proBNP humano y que ha sido conjugado con un marcador detectable para formar una segunda mezcla que comprende un complejo de proBNP humano-primer detección; y (iii) un 65 segundo anticuerpo de detección que se une al hBNP y que ha sido conjugado con un marcador detectable para formar adicionalmente en la tercera mezcla que comprende un complejo de hBNP-segundo anticuerpo de detección, en los que el primer anticuerpo de detección es el anticuerpo 15C4 y el segundo anticuerpo de detección es el anticuerpo 201.3;
(b) poner en contacto dicha primera mezcla que comprende el complejo NT-proBNP humano-primer anticuerpo de detección con un primer anticuerpo de captura que se une al NT-proBNP humano y que ha sido inmovilizado sobre una fase sólida para producir un primer anticuerpo inmovilizado para formar una cuarta mezcla que comprende un complejo del primer anticuerpo de captura-NT-proBNP humano-primer anticuerpo de detección, en el primer anticuerpo de captura es 15F11;
(c) poner en contacto dicha segunda mezcla que comprende el complejo proBNP humano-primer anticuerpo de detección con un segundo anticuerpo de captura que se une al proBNP humano y que ha sido inmovilizado sobre una fase sólida para producir un segundo anticuerpo inmovilizado para formar una quinta mezcla que comprende un complejo del segundo anticuerpo de captura-proBNP humano-primer anticuerpo de detección, en el que el segundo anticuerpo de captura es 8.1;
(d) poner en contacto la tercera mezcla que comprende el complejo hBNP-segundo anticuerpo de detección con
el segundo anticuerpo de captura que, además de unirse al proBNP humano también se une al hBNP, y que ha sido inmovilizado sobre una fase sólida para producir un segundo anticuerpo inmovilizado para formar una sexta mezcla que comprende un complejo del segundo anticuerpo de captura-hBNP-segundo anticuerpo de detección, en el que el segundo anticuerpo de captura es 8.1; y
(e) determinar la cantidad de (i) el complejo del primer anticuerpo de captura-NT-proBNP humano-primer anticuerpo de detección formado en la etapa (b) mediante la detección del marcador detectable como una medida de la cantidad de NT-proBNP humano contenido en la muestra de prueba; (ii) el complejo del segundo anticuerpo de captura-proBNP humano-primer anticuerpo de detección formado en la etapa (c) mediante la detección del marcador detectable como una medida de la cantidad de proBNP humano contenido en la muestra de prueba; y (iii) el complejo del segundo anticuerpo de captura-hBNP-segundo anticuerpo de detección formado en la etapa (d) mediante la detección del marcador detectable como una medida de la cantidad de hBNP contenido en la muestra de prueba.
6. El inmunoensayo de la reivindicación 5, en el que la fase sólida se elige de entre el grupo que consiste en una partícula magnética, una microesfera, un tubo de ensayo, una placa de microtitulación, una cubeta, una membrana, una molécula estructural, una película, un papel de filtro, un disco y un chip.
7. El inmunoensayo de la reivindicación 5, en el que el marcador detectable del primer anticuerpo de detección se elige de entre el grupo que consiste en un marcador radioactivo, un marcador enzimático, un marcador quimioluminiscente, un marcador fluorescente, un marcador termométrico y un inmunomarcador de reacción en
cadena de la polimerasa.
8. El inmunoensayo de la reivindicación 5, en el que el marcador detectable del segundo anticuerpo de detección se elige de entre el grupo que consiste en un marcador radioactivo, un marcador enzimático, un marcador quimioluminiscente, un marcador fluorescente, un marcador termométrico y un inmunomarcador de reacción en cadena de la polimerasa.
9. Reactivos inmunodiagnósticos que comprenden:
(a) un primer anticuerpo de captura específico para el NT-pro-péptido natriurético de tipo B humano ("NT-proBNP 45 humano") ;
(b) un segundo anticuerpo de captura que es específico para cada uno del pro-péptido natriurético de tipo B humano ("proBNP humano") y del péptido natriurético cerebral humano ("hBNP") ;
(c) un primer anticuerpo de detección que es específico para cada uno del NT-proBNP humano y del proBNP humano; y
(d) un segundo anticuerpo de detección que es específico para el hBNP.
10. Los reactivos inmunodiagnósticos de la reivindicación 9, en los que el primer anticuerpo de captura es el anticuerpo 15F11.
11. Los reactivos inmunodiagnósticos de la reivindicación 9, en los que el segundo anticuerpo de captura es el anticuerpo 8.1.
12. Los reactivos inmunodiagnósticos de la reivindicación 9, en los que el primer anticuerpo de detección es el anticuerpo 15C4.
13. Los reactivos inmunodiagnósticos de la reivindicación 9, en los que el segundo anticuerpo de detección es el anticuerpo 201.3.
14. Un kit para detectar la cantidad de NT-pro-péptido natriurético de tipo B humano ("NT-proBNP humano") , de pro65 péptido natriurético de tipo B humano ("proBNP humano") y de péptido natriurético cerebral humano ("hBNP") en una muestra de prueba, comprendiendo dicho kit:
(a) instrucciones para realizar el ensayo de la muestra de prueba; y
(b) reactivos inmunodiagnósticos que comprenden: 5
(i) un primer anticuerpo de captura específico para el NT-proBNP humano;
(ii) un segundo anticuerpo de captura que es específico para cada uno del proBNP humano y del hBNP;
(iii) un primer anticuerpo de detección que es específico para cada uno del NT-proBNP humano y del proBNP
humano; y 10 (iv) un segundo anticuerpo de detección que es específico para el hBNP.
15. El kit de la reivindicación 14, en el que el primer anticuerpo de captura es el anticuerpo 15F11; el segundo anticuerpo de captura es el anticuerpo 8.1;
el primer anticuerpo de detección es el anticuerpo 15C4; o el segundo anticuerpo de detección es el anticuerpo 201.3.
Patentes similares o relacionadas:
Dispositivos modulares para puntos de atención y usos de los mismos, del 29 de Julio de 2020, de Labrador Diagnostics LLC: Un sistema para la detección automatizada de un analito a partir de una muestra de fluido corporal, que comprende: un dispositivo de fluidos que comprende: […]
Detección de interacciones proteína a proteína, del 15 de Julio de 2020, de THE GOVERNING COUNCIL OF THE UNIVERSITY OF TORONTO: Un método para medir cuantitativamente la fuerza y la afinidad de una interacción entre una primera proteína de membrana o parte de la misma y una […]
Anticuerpos del OPGL, del 15 de Julio de 2020, de AMGEN FREMONT INC.: Un anticuerpo, que comprende una cadena pesada y una cadena ligera, donde: a) la cadena pesada comprende: 1) una secuencia de aminoácidos recogida […]
ANTICUERPO MONOCLONAL O UNA PORCIÓN DE UNIÓN A ANTÍGENO DEL MISMO QUE SE UNE A LA PROTEÍNA L DEL VIRUS PARAINFLUENZA HUMANO (PIV); MÉTODO Y KIT PARA DETECTAR AL VIRUS PIV, del 2 de Julio de 2020, de PONTIFICIA UNIVERSIDAD CATÓLICA DE CHILE: La invención presenta la generación de anticuerpos monoclonales, o fragmentos de los mismos, que reconocen la proteína L del virus parainfluenza humano (PIV), donde dichos […]
ANTICUERPOS MONOCLONALES ESPECÍFICOS PARA EL ANTÍGENO PB2 DEL VIRUS DE LA INFLUENZA HUMANA (FLU), SECUENCIAS NUCLEOTÍDICAS; MÉTODO Y KIT DE DIAGNÓSTICO DE INFECCIÓN PRODUCIDA POR FLU, del 2 de Julio de 2020, de PONTIFICIA UNIVERSIDAD CATÓLICA DE CHILE: La invención presenta la generación de anticuerpos monoclonales, o fragmentos de los mismos, que reconocen la proteína PB2 del virus de la influenza humana (Flu), […]
Dispositivo para la detección de analitos, del 1 de Julio de 2020, de TECHLAB, INC.: Un dispositivo para detectar por lo menos una sustancia de interés en una muestra líquida, comprendiendo el dispositivo: (a) una unidad que […]
Un ensayo de la respuesta inmunológica mediada por células, del 17 de Junio de 2020, de Cellestis Limited: Un método para medir una actividad de respuesta inmunológica mediada por células, comprendiendo dicho método: (a) proporcionar una composición de incubación […]
Método de deducción de un valor de positividad de biomarcador en porcentaje para células seleccionadas presentes en un campo de visión, del 10 de Junio de 2020, de NOVARTIS AG: Método de deducción de un valor para el % de positividad de biomarcador (PBP) para todas las células u, opcionalmente, uno o más subconjuntos de las […]