Anticuerpos enteramente humanos contra 4-1BB humano (CD137).
Un anticuerpo monoclonal enteramente humano o una parte de unión a antígeno del mismo que se uneespecíficamente a 4-1BB,
que comprende una región variable de cadena ligera y una región variable de cadenapesada, en el que:
5 dicha región variable de cadena ligera comprende una CDR1 que consiste en los restos aminoacídicos 44-54 deSEC ID Nº: 6, una CDR2 que consiste en los restos aminoacídicos 70-76 de SEC ID Nº: 6, una CDR3 queconsiste en los restos aminoacídicos 109-119 de SEC ID Nº: 6; y
dicha región variable de cadena pesada comprende una CDR1 que consiste en los restos aminoacídicos 50-54de SEC ID Nº: 3, una CDR2 que consiste en los restos aminoacídicos 69-84 de SEC ID Nº: 3 y una CDR3 queconsiste en los restos aminoacídicos 117-129 de SEC ID Nº: 3.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2004/033587.
Solicitante: BRISTOL-MYERS SQUIBB COMPANY.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: Route 206 & Province Line Road Princeton, NJ 08543-4000 ESTADOS UNIDOS DE AMERICA.
Inventor/es: HALK,EDWARD,L, JURE-KUNKEL,MARIA, HEFTA,LAURA J, SANTORO,MARC, GANGULY,SUBINAY.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K39/00 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53).
- C07K16/28 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 16/00 Inmunoglobulinas, p. ej. anticuerpos mono o policlonales. › contra receptores, antígenos celulares de superficie o determinantes celulares de superficie.
PDF original: ES-2432357_T3.pdf
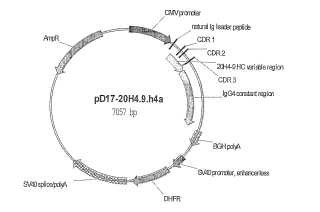
Fragmento de la descripción:
Anticuerpos enteramente humanos contra 4-1BB humano (CD137)
Campo de la invención La invención está dirigida a anticuerpos enteramente humanos y, más específicamente, a los anticuerpos enteramente humanos frente a 4-1BB humano (CD137) .
Antecedentes de la invención Un amplio cuerpo de evidencias ha demostrado de forma inequívoca que existe cierto grado de respuesta inmune contra el cáncer en seres humanos y en animales. En los pacientes de cáncer, los componentes celulares del sistema inmune son capaces de reconocer los antígenos expresados por las células tumorales, tales como diferenciación de antígenos oncofetales o productos génicos mutados (S. Rosenberg, Nature, 411: 380-4 (2001) ; P. van der Bruggen y col., Immunological Rev., 188: 51-64 (2002) ) . Un número de estudios clínicos ha mostrado que la infiltración de linfocitos en el tumor tiene un significado de pronóstico favorable (E. Halapi, Med. Oncol., 15 (4) : 20311 (1998) ; Y. Naito y col., Cancer Res., 58 (16) : 3491-4 (1998) ; L. Zhang y col., N.E. J. Med., 348 (3) : 203-13 (2003) ) . Además, el tratamiento con inmunomoduladores, tales como las citoquinas o productos bacterianos, vacunas contra el cáncer o inmunoterapia adoptiva ha llevado a la regresión del tumor en un némero de pacientes (S. Rosenberg, Cancer J. Sci. Am. 6 (S) : 2 (2000) ; P. Bassi, Surg. Oncol., 11 (1-2) : 77-83 (2002) ; S. Antonia y col., Current Opinion in Immunol., 16: 130-6 (2004) ) . A pesar de estas respuestas, la inmunidad contra el cáncer fracasa frecuentemente en la eliminación eficaz de las células tumorales. Las causas de este fracaso se pueden agrupar en tres categorías principales: (i) incapacidad de reconocimiento del tumor por parte de las células inmunes, bien por la expresión variable de los antígenos tumorales o por la expresión reducida del complejo mayor de histocompatibilidad de clase I (CMH) ; (ii) microentorno tumoral inmunosupresor, como resultado de la secreción de citoquinas inhibidoras por las células tumorales (por ejemplo, TGF-β) ; y (iii) inmunogenicidad tumoral escasa debido a la falta de expresión de moléculas coestimuladoras en las células tumorales, lo que da lugar a la incapacidad de las células tumorales de estimular eficazmente a las células T. Los avances en nuestra comprensión de las necesidades para el reconocimiento de los antígenos tumorales y la función efectora inmune indican que una estrategia potencial para aumentar una respuesta inmune antitumoral es proporcionar una coestimulación por medio de una molécula auxiliar. Las células T específicas contra los antígenos tumorales necesitan la coestimulación para iniciar y mantener las funciones efectoras. Por tanto, pueden aplicarse terapias que dirigen moléculas coestimuladoras para modular y mejorar la respuesta inmune contra los tumores.
El modelo actual de activación de las células T postula que las células T intactas necesitan dos señales para activarse plenamente: (i) una señal proporcionada a través de la unión de los antígenos procesados presentados al receptor de la célula T por moléculas del complejo mayor de histocompatibilidad de clase I (CMH) ; y (ii) una señal adicional proporcionada por la interacción de moléculas coestimuladoras sobre la superficie de las células T y sus ligandos sobre las células presentadoras de antígeno. El reconocimiento de un antígeno por una célula T intacta es insuficiente por sí mismo para desencadenar la activación de la célula T. Sin una señal coestimuladora, las células T pueden eliminarse bien sea por muerte o por inducción de anergia. La señalización por medio de la molécula coestimuladora CD28 parece ser la clave para el inicio de las respuestas de la célula T. Sin embargo, la señalización de CD137 (4-1BB) ha demostrado ser primordial para el mantenimiento y la expansión de la respuesta inmune frente antígenos, así como también para la generación de la memoria de las células T.
CD137 (4-1BB) es un miembro de la familia génica del receptor de necrosis tumoral (TNF-R) , que incluye proteínas que están implicadas en la regulación de la proliferación celular, la diferenciación y la muerte celular programada. CD137 es una glucoproteína de membrana de tipo I de 30 kDa que se expresa como un homodímero de 55 kDa. El receptor se describió inicialmente en ratones (B. Kwon y col., P.N.A.S. EE.UU., 86: 1963-7 (1989) ) y más tarde se identificó en seres humanos (M. Alderson y col., Eur. J. Immunol., 24: 2219-27 (1994) ; Z. Zhou y col., Immunol. Lett.,
45: 67 (1995) ) (Véanse también, las solicitudes PCT publicadas WO95/07984 y WO96/29348 y la Patente de Estados Unidos Nº 6.569.997, (Véase, SEC ID Nº: 2.) ) . Las formas humana y murina de CD137 son idénticas en el 60% a nivel de aminoácidos. Las secuencias conservadas aparecen en el dominio citoplasmático, así como otras 5 regiones de la molécula, lo que indica que estos restos pueden ser importantes para la función de la molécula de CD137 (Z. Zhou y col., Immunol. Lett., 45: 67 (1995) ) . La expresión de CD137 ha mostrado estar predominantemente en las células de linaje linfoide tales como las células T activadas, los linfocitos citolíticos naturales activados (NK) , células NKT, células T reguladoras de CD4CD25 y también en timocitos activados y linfocitos intraepiteliales. Además, CD137 ha mostrado que se expresa en las células de origen mieloide como las células dendríticas, monocitos, neutrófilos y eosinófilos. Aunque la expresión de CD137 está limitada principalmente a las células inmunitarias/inflamatorias, existen informes que describen su expresión en células endoteliales asociadas con un pequeño número de tejidos de sitios inflamatorios y tumores.
Las actividades funcionales de CD137 en las células T se han caracterizado ampliamente. La señalización por medio de CD137 en presencia de dosis subóptimas de anti-CD3 ha mostrado que induce la proliferación de células T y la síntesis de citoquinas (principalmente IFN-!) , e inhibe la muerte de las células activadas. Estos efectos se han observado en células T tanto humanas como murinas (W. Shuford y col., J. Exp. Med., 186 (1) : 47-55 (1997) ; D.
Vinay y col., Semin. Immunol., 10 (6) : 481-9 (1998) ; D. Laderach y col., Int. Immunol., 14 (10) : 1155-67 (2002) ) . Tanto en seres humanos como en ratones, la coestimulación aumenta las funciones efectoras, tales como la producción de IFN-! y la citotoxicidad, mediante el aumento del número de células T específicas de antígeno y efectoras CD8+. En ausencia de la señalización anti-CD3, la estimulación por medio de CD137 no altera la función de las células T, lo que indica que CD137 es una molécula coestimuladora.
Los acontecimientos fisiológicos que se observan a continuación de la estimulación de CD137 sobre las células T están mediados por señales de NF-∀B y PI3K/ERK1/2 con funciones fisiológicas separadas. Las señales de NF-∀B desencadenan la expresión de Bcl-XL, una molécula antiapoptótica, resultando así en un aumento de la supervivencia, mientras que las señales de PI3K y ERK1/2 son responsables específicamente de la progresión del ciclo celular mediado por CD137 (H. Lee y col., J. Immunol., 169 (9) : 4882-8 (2002) ) . El efecto de la activación de CD137 sobre la inhibición de muerte celular inducida por activación se ha demostrado in vitro por Hurtado y col. (J. Hurtado y col., J. Immunol., 158 (6) : 2600-9 (1997) ) y en un sistema in vivo en el que se ha demostrado que los anticuerpos monoclonales anti-CD137 (mab) daban lugar a la supervivencia a largo plazo de las células T CD8+ activadas por superantígeno previniendo la supresión clónica (C. Takahashi y col., J. Immunol., 162: 5037 (1999) ) . Posteriormente, dos informes demostraron, en diferentes condiciones experimentales, que la señal de CD137 regulaba tanto la expansión clónica como la supervivencia de las células T CD8+ (D. Cooper y col., Eur. J. Immunol., 32 (2) : 521-9 (2002) ; M. Maus y col., Nat. Biotechnol., 20: 143 (2002) ) . La reducción de la apoptosis que se observó tras la coestimulación estaba correlacionada con el aumento de los niveles de Bcl-XL en células T CD8+, mientras que la expresión de Bcl-2 permanecía sin cambios. Se demostró que la regulación positiva de los genes antiapoptóticos Bcl-XL y bfl-1 por medio de 4-1BB estaba mediada por la activación de NF-∀B, ya que PDTC, un bloqueante específico de NF-∀B inhibía la regulación positiva de Bcl-XL mediada por 4-1BB (H. Lee y col., J. Immunol., 169 (9) : 4882-8 (2002) ) . Por otro lado, la expansión clónica de las células T activadas parece que está mediada por el aumento de la expresión de ciclinas D2, D3 y E y la regulación negativa de la proteína p27kip1. Este efecto ocurre tanto de manera dependiente... [Seguir leyendo]
Reivindicaciones:
1. Un anticuerpo monoclonal enteramente humano o una parte de unión a antígeno del mismo que se une específicamente a 4-1BB, que comprende una región variable de cadena ligera y una región variable de cadena pesada, en el que:
dicha región variable de cadena ligera comprende una CDR1 que consiste en los restos aminoacídico.
4. 54 de SEC ID Nº: 6, una CDR2 que consiste en los restos aminoacídico.
7. 76 de SEC ID Nº: 6, una CDR3 que consiste en los restos aminoacídico.
10. 119 de SEC ID Nº: 6; y dicha región variable de cadena pesada comprende una CDR1 que consiste en los restos aminoacídico.
5. 54 de SEC ID Nº: 3, una CDR2 que consiste en los restos aminoacídico.
6. 84 de SEC ID Nº: 3 y una CDR3 que consiste en los restos aminoacídico.
11. 129 de SEC ID Nº: 3.
2. El anticuerpo monoclonal enteramente humano o una parte de unión a antígeno del mismo de la reivindicación 1, en el que:
dicha cadena ligera comprende una región variable que consiste en los restos aminoacídico.
2. 129 de SEC ID Nº: 6; y dicha cadena pesada comprende una región variable que consiste en los restos aminoacídico.
2. 140 de SEC ID Nº: 3.
3. Un anticuerpo monoclonal enteramente humano que comprende una cadena ligera y una cadena pesada, en el que dicha cadena ligera comprende los restos aminoacídico.
2. 236 de SEC ID Nº: 6 y dicha cadena pesada comprende los restos aminoacídico.
2. 467 de SEC ID Nº: 3.
4. Una composición farmacéutica que comprende:
el anticuerpo monoclonal enteramente humano o una parte de unión a antígeno del mismo de la reivindicación 1 o 2; y un vehículo farmacéuticamente aceptable.
5. Una composición farmacéutica que comprende:
el anticuerpo monoclonal enteramente humano de la reivindicación 3; y un vehículo farmacéuticamente aceptable.
6. El anticuerpo monoclonal enteramente humano o una parte de unión a antígeno del mismo de una cualquiera de las reivindicaciones 1 a 3 para su uso en el tratamiento de un cáncer.
7. Uso de un polinucleótido aislado que comprende una secuencia de nucleótidos que codifica la secuencia de aminoácidos de los restos aminoacídico.
2. 467 de SEC ID Nº: 3 y un polinucleótido aislado que comprende una secuencia de nucleótidos que codifica la secuencia de aminoácidos de los restos aminoacídico.
2. 236 de SEC ID Nº: 6 para producir un anticuerpo monoclonal enteramente humano o una parte de unión a antígeno del mismo que comprende una región variable de cadena ligera y una región variable de cadena pesada como se define en una cualquiera de las reivindicaciones 1 a 3.
8. Uso de un polinucleótido que comprende la secuencia de nucleótidos de SEC ID Nº: 1 y un polinucleótido que comprende la secuencia de nucleótidos de SEC ID Nº: 4 para producir un anticuerpo monoclonal enteramente humano o una parte de unión a antígeno del mismo que comprende una región variable de cadena ligera codificada por la secuencia de nucleótidos de SEC ID Nº: 4 y una región variable de cadena pesada codificada por la secuencia de nucleótidos de SEC ID Nº: 1.
Patentes similares o relacionadas:
Eliminación de impurezas de cultivos celulares residuales, del 29 de Julio de 2020, de NOVARTIS AG: Un método para eliminar la Proteína Nuclear (NP) de la Gripe de una preparación que comprende proteínas del virus de la gripe de interés que incluyen hemaglutinina […]
 Cepas de Bordetella vivas atenuadas como vacuna de dosis única contra la tos ferina, del 29 de Julio de 2020, de INSTITUT PASTEUR DE LILLE: Una vacuna que comprende una cepa viva, atenuada y mutada de Bordetella pertussis que comprende al menos una mutación del gen (ptx) de la toxina […]
Cepas de Bordetella vivas atenuadas como vacuna de dosis única contra la tos ferina, del 29 de Julio de 2020, de INSTITUT PASTEUR DE LILLE: Una vacuna que comprende una cepa viva, atenuada y mutada de Bordetella pertussis que comprende al menos una mutación del gen (ptx) de la toxina […]
Composición de vacuna que contiene un adyuvante sintético, del 22 de Julio de 2020, de INFECTIOUS DISEASE RESEARCH INSTITUTE: Una composición farmacéutica que comprende: un adyuvante lípido de glucopiranosilo (GLA), que tiene la fórmula: **(Ver fórmula)** en la que: […]
Arenavirus trisegmentados como vectores de vacunas, del 22 de Julio de 2020, de UNIVERSITE DE GENEVE: Una partícula de arenavirus trisegmentada infecciosa y competente para la replicación que comprende un segmento L y dos segmentos S, en donde uno de los dos segmentos […]
Inmunoterapia novedosa contra diversos tumores, entre ellos tumores cerebrales y neuronales, del 22 de Julio de 2020, de IMMATICS BIOTECHNOLOGIES GMBH: Péptido que comprende una secuencia de aminoácidos acorde con la SEQ ID N.º 19, en que dicho péptido tiene una longitud total de entre 9 y 16 aminoácidos.
Método para producir inmunoconjugados de anticuerpo-SN-38 con un enlazador CL2A, del 22 de Julio de 2020, de IMMUNOMEDICS, INC.: Un método para producir un compuesto, CL2A-SN-38, que presenta la estructura, **(Ver fórmula)** que comprende realizar un esquema de reacción como el que se muestra: **(Ver […]
Métodos mejorados para la preparación de escualeno, del 15 de Julio de 2020, de NOVARTIS AG: Un procedimiento para la preparación de escualeno a partir de una composición que comprende escualeno a partir de una fuente animal, dicho procedimiento comprendiendo […]
Formulaciones estables que contienen anticuerpos anti-PCSK9, del 15 de Julio de 2020, de AMGEN INC.: Una formulación estable que comprende un anticuerpo monoclonal que se une específicamente a PCSK9, en donde PCSK9 comprende los aminoácidos de la SEQ ID NO: […]