Ácidos grasos de longitud de cadena media, glicéridos y análogos como factores de supervivencia y activación de neutrófilos.
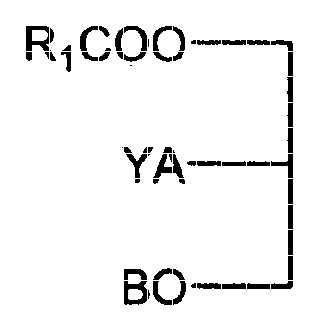
Compuesto de fórmula I
en la que:
A y B son iguales o diferentes y son cada uno H o R1CO,
R1 es alquilo C7 o C9,
Y es O o NH;
para uso en el trasplante de médula ósea o para uso en el tratamiento de un estado seleccionado de neutropenia, heridas y mielosupresión originada por quimioterapia o radioterapia.
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E07116425.
Solicitante: PROMETIC BIOSCIENCES INC..
Nacionalidad solicitante: Canadá.
Dirección: 8168 Montview Mont-Royal Québec H4P 2L7 CANADA.
Inventor/es: ZACHARIE, BOULOS, PENNEY,CHRISTOPHER, GAGNON,LYNE, BARABE,JEAN, LAURIN,PIERRE.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/18 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › Sulfamidas (compuestos que contienen un grupo para N-benceno-sulfonil-N A61K 31/63).
- A61K31/194 A61K 31/00 […] › que tienen dos o más grupos carboxilo, p. ej. ácidos succínico, maléico o ftálico.
- A61K31/20 A61K 31/00 […] › que tienen un grupo carboxilo unido a una cadena acíclica de al menos siete átomos de carbono, p. ej. ácidos esteárico, palmítico o araquídico.
- A61K31/23 A61K 31/00 […] › de ácidos que tienen un grupo carboxilo unido a una cadena de al menos siete átomos de carbono.
- A61K31/255 A61K 31/00 […] › de ácidos oxigenados del azufre o sus tio-análogos.
- A61K31/7024 A61K 31/00 […] › Esteres de sacáridos.
- A61K38/19 A61K […] › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Citoquinas; Linfoquinas; Interferones.
- A61K38/20 A61K 38/00 […] › Interleuquinas.
- A61P7/06 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 7/00 Medicamentos para el tratamiento de trastornos de la sangre o del fluido extracelular. › Antianémicos.
- C07C233/18 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07C COMPUESTOS ACICLICOS O CARBOCICLICOS (compuestos macromoleculares C08; producción de compuestos orgánicos por electrolisiso electroforesis C25B 3/00, C25B 7/00). › C07C 233/00 Amidas de ácidos carboxílicos. › con el átomo de carbono del grupo carboxamido unido a un átomo de hidrógeno o a un átomo de carbono de una estructura carbonada acíclica saturada.
- C07C233/47 C07C 233/00 […] › con el átomo de carbono del grupo carboxamido unido a un átomo de hidrógeno o a un átomo de carbono de una estructura carbonada acíclica saturada.
- C07C235/06 C07C […] › C07C 235/00 Amidas de ácidos carboxílicos, estando sustituida la estructura carbonada de la parte ácida por átomos de oxígeno. › con los átomos de nitrógeno de los grupos carboxamido unidos a átomos de hidrógeno o a átomos de carbono acíclicos.
- C07C235/08 C07C 235/00 […] › con el átomo de nitrógeno de al menos uno de los grupos carboxamido unido a un átomo de carbono acíclico de un radical hidrocarbonado sustituido por átomos de oxígeno unidos por enlaces sencillos.
- C07C237/22 C07C […] › C07C 237/00 Amidas de ácidos carboxílicos, estando sustituida la estructura carbonada de la parte ácida por grupos amino. › con átomos de nitrógeno de grupos amino unidos a la estructura carbonada de la parte ácida, acilados.
- C07H15/04 C07 […] › C07H AZUCARES; SUS DERIVADOS; NUCLEOSIDOS; NUCLEOTIDOS; ACIDOS NUCLEICOS (derivados de ácidos aldónicos o sacáricos C07C, C07D; ácidos aldónicos, ácidos sacáricos C07C 59/105, C07C 59/285; cianohidrinas C07C 255/16; glicales C07D; compuestos de constitución indeterminada C07G; polisacáridos, sus derivados C08B; ADN o ARN concerniente a la ingeniería genética, vectores, p. ej. plásmidos o su aislamiento, preparación o purificación C12N 15/00; industria del azúcar C13). › C07H 15/00 Compuestos que contienen radicales hidrocarbonados o hidrocarbonados sustituidos, unidos directamente a los heteroátomos de los radicales sacárido. › unidos a un átomo de oxígeno de un radical sacárido.
- C11C3/00 C […] › C11 ACEITES, GRASAS, MATERIAS GRASAS O CERAS ANIMALES O VEGETALES; SUS ACIDOS GRASOS; DETERGENTES; VELAS. › C11C ACIDOS GRASOS OBTENIDOS A PARTIR DE GRASAS, ACEITES O CERAS; VELAS; GRASAS, ACEITES O ACIDOS GRASOS OBTENIDOS POR MODIFICACION QUIMICA DE GRASAS, ACEITES O ACIDOS GRASOS. › Grasas, aceites o ácidos grasos obtenidos por modificación química de grasas, aceites o ácidos grasos, p. ej. por ozonólisis (grasas o aceites sulfonados C07C 309/62; grasas epoxidadas C07D 303/42; aceites vulcanizados, p.ej. pseudocaucho C08H 3/00).
- C11C3/02 C11C […] › C11C 3/00 Grasas, aceites o ácidos grasos obtenidos por modificación química de grasas, aceites o ácidos grasos, p. ej. por ozonólisis (grasas o aceites sulfonados C07C 309/62; grasas epoxidadas C07D 303/42; aceites vulcanizados, p.ej. pseudocaucho C08H 3/00). › por esterificación de ácidos grasos con glicerina.
PDF original: ES-2439738_T3.pdf
Fragmento de la descripción:
Ácidos grasos de longitud de cadena media, glicéridos y análogos como factores de supervivencia y activación de neutrófilos
Campo de la invención La presente invención se refiere a la prevención y/o al tratamiento de la neutropenia. Esto incluye el tratamiento de la neutropenia asociada al uso de quimioterapia y radioterapia así como también al tratamiento de la neutropenia originada por infecciones, enfermedades hematológicas y deficiencias nutricionales. La presente invención también se refiere generalmente a reducir la toxicidad de los fármacos y aumentar la eficacia de los fármacos. En particular, la presente invención se refiere al uso de ácidos grasos de longitud de cadena media como factor de supervivencia y de activación de neutrófilos o factor de proliferación de las células madre de la médula ósea.
Antecedentes de la invención El término quimioterapia se refiere al uso de agentes citotóxicos tales como ciclofosfamida, doxorubicina, daunorubicina, vinblastina, vincristina, bleomicina, etopósido, topotecán, irinotecán, taxotere, taxol, 5-fluorouracilo, metotrexato, gemcitabina, cisplatino, carboplatino o clorambucilo con el fin de erradicar células cancerosas y tumores. Sin embargo, estos agentes no son específicos y, particularmente a dosis altas, son tóxicos para las células normales y las células en división rápida. A menudo, esto conduce a diversos efectos secundarios en pacientes sometidos a quimioterapia y terapia de radiación. La mielosupresión, una reducción grave de la producción de células sanguíneas en la médula ósea, es uno de tales efectos secundarios. Se caracteriza por leucopenia, neutropenia y trombocitopenia. La neutropenia crónica grave (idiopática, cíclica y congénita) se caracteriza también por una disminución selectiva en el número de neutrófilos circulantes y por una susceptibilidad potenciada a las infecciones bacterianas.
La esencia del tratamiento del cáncer con fármacos quimioterápicos es combinar un mecanismo de citotoxicidad con un mecanismo de selectividad por las células tumorales altamente proliferantes con respecto a las células del huésped. Sin embargo, es poco frecuente que los fármacos quimioterápicos posean dicha selectividad. La citotoxicidad de los agentes quimioterápicos limita las dosis que pueden administrarse, afecta a los ciclos de tratamiento y pone en peligro gravemente la calidad de vida del paciente oncológico.
Aunque otros tejidos normales también puedan verse afectados de manera adversa, la médula ósea es particularmente sensible a los tratamientos específicos de proliferación tales como la quimioterapia o la terapia de radiación. La toxicidad aguda y crónica en la médula ósea es un efecto secundario común de las terapias contra el cáncer que conduce a una disminución en el recuento de células sanguíneas y a anemia, leucopenia, neutropenia, agranulocitosis y trombocitopenia. Una causa de tales efectos es una disminución en el número de células hematopoyéticas (p. ej., células madre pluripotentes y otras células progenitoras) provocada tanto por un efecto letal de los agentes citotóxicos o la radiación sobre estas células como por la diferenciación de las células madre provocada mediante un mecanismo de retroalimentación inducido por el agotamiento de los compartimentos más maduros de la médula. La segunda causa es una reducción de la capacidad de autorrenovación de las células madre, que también está relacionada tanto con efectos directos (mutaciones) como indirectos (envejecimiento de la población de células madre) [Tubiana, M., et al., Radiotherapy and Oncology 29:1-17 (1993) ]. Por tanto, el tratamiento del cáncer frecuentemente produce una disminución de los neutrófilos polimorfonucleares (PMN) o neutropenia. Los PMN son la primera línea de defensa contra los patógenos invasores y desempeñan un papel central durante la inflamación aguda, siendo su función primaria fagocitar y destruir los agentes infecciosos. Para cumplir con este papel, los PMN dejan la circulación en respuesta a factores quimiotácticos y penetran en las zonas afectadas para ejercer sus funciones biológicas. En individuos con recuentos normales de células sanguíneas, los neutrófilos comprenden aproximadamente el 60% de los leucocitos totales. [SI Units Conversion Guide, 66-67 (1992) , New England Journal of Medical Books]. Sin embargo, hasta uno de cada tres pacientes que reciben tratamiento de quimioterapia contra el cáncer puede padecer neutropenia. Los recuentos de neutrófilos normales medios para adultos humanos sanos son del orden de 4400 células/!l, con un intervalo de 1800-7700 células/!l. Un recuento de 1.000 a 500 células/!l es una neutropenia moderada y un recuento de 500 células/!l o inferior es una neutropenia grave. Los pacientes en estados de mielosupresión están predispuestos a las infecciones y frecuentemente padecen trastornos de la coagulación sanguínea, requiriendo hospitalización. La falta de neutrófilos y plaquetas es la causa principal de morbimortalidad tras tratamientos contra el cáncer y contribuye al alto coste de la terapia contra el cáncer. En estos estados mencionados anteriormente, el uso de cualquier agente capaz de inhibir la apoptosis de los neutrófilos o de estimular la activación y movilización de los neutrófilos puede tener valor terapéutico. Los esfuerzos para restablecer el sistema inmunitario del paciente después de la quimioterapia implican el uso de factores de crecimiento hematopoyéticos para estimular la proliferación y diferenciación de las células madre restantes en células maduras que luchan contra las infecciones.
En el trasplante de médula ósea, también se ha aprovechado un fenómeno conocido como “movilización”, para recoger un número superior de células madre/progenitoras de sangre periférica. Este método se utiliza actualmente en los trasplantes de médula ósea autólogos o alogénicos. Se usan factores de crecimiento para aumentar el número de células madre progenitoras periféricas que van a recogerse antes de la terapia mieloablativa y la infusión de células madre progenitoras.
El trasplante de médula ósea después de la terapia también puede contrarrestar la neutropenia, pero necesita 10-15
días de tratamiento, que dejan al paciente vulnerable a las infecciones. Los agentes capaces de estimular las células madre de la médula ósea pueden facilitar y acelerar el injerto de las células madre, acortando así la ventana neutropénica después del trasplante de médula ósea.
Aunque los factores de crecimiento hematopoyético tales como el factor estimulante de colonias de granulocitosmacrófagos (GM-CSF) y el factor estimulante de colonias de granulocitos (G-CSF) pueden ejercer tales acciones, su uso es caro debido a que han de producirse mediante tecnología recombinante. Tales tratamientos de mejora posterapéuticos son innecesarios si los pacientes están “quimioprotegidos” frente a la supresión inmunitaria.
Los triglicéridos de cadena media (también denominados en el presente documento como “MCT”) consisten en glicerol esterificado con ácidos grasos con longitudes de cadena de carbono de 8 (8C, ácido octanoico o ácido caprílico) y 10 (C10, ácido decanoico o ácido cáprico) . Los MCT contienen habitualmente una mezcla de ésteres de glicerol de ácidos grasos C8 y C10. Sin embargo, los MCT también pueden contener pequeñas cantidades (2±1% cada uno) de ésteres de glicerol de C6 (ácido hexanoico o ácido caproico) y C12 (ácido dodecanoico o ácido láurico) . CROMADOLTM es un MCT disponible comercialmente de Croda Ltd., Toronto (Canadá) . Tal como se muestra en el ejemplo 1, CROMADOLTM es un MCT que contiene triésteres de glicerol de ácidos grasos C8 y C10 presentes en proporciones variables. Sin embargo, CROMADOLTM no contiene ningún éster de ácido graso C6 o C12.
Los triglicéridos de cadena larga (también denominados en el presente documento “LCT”) consisten en glicerol
esterificado con ácidos grasos con longitudes de cadena superiores a 12. Los ácidos grasos típicos presentes en LCT incluyen ácidos palmítico (C16) y esteárico (C18) . A diferencia de los MCT, los LCT son el componente principal de las grasas alimenticias. De hecho, los MCT y LCT tienen propiedades biológicas significativamente diferentes. Algunas de las diferencias fisiológicas entre MCT y LCT se describen en Harrison’s Principles of Internal Medicine, 8ª edición, 1520-1521 (1977) , McGraw Hill Book Company o 15ª edición, 1668-1669 (2001) . Por ejemplo, los MCT, al contrario que los LCT, no requieren hidrólisis mediante la lipasa pancreática, puesto que pueden absorberse por las células epiteliales intestinales.
D. Waitzberg... [Seguir leyendo]
Reivindicaciones:
1. Compuesto de fórmula I
en la que: A y B son iguales o diferentes y son cada uno H o R1CO, 10 R1 es alquilo C7 o C9, Y es O o NH; 15 para uso en el trasplante de médula ósea o para uso en el tratamiento de un estado seleccionado de neutropenia, heridas y mielosupresión originada por quimioterapia o radioterapia.
2. Compuesto según la reivindicación 1 para uso de acuerdo con la reivindicación 1, en el que el estado es mielosupresión originada por quimioterapia. 20
3. Compuesto según la reivindicación 1 para uso de acuerdo con la reivindicación 1, en el que el estado es mielosupresión originada por radioterapia.
4. Compuesto según la reivindicación 1 para uso de acuerdo con la reivindicación 1, en el que el estado es 25 neutropenia crónica.
5. Compuesto según la reivindicación 1 para uso de acuerdo con la reivindicación 1, en el que el estado es una neutropenia transitoria.
6. Compuesto según la reivindicación 1 para uso de acuerdo con la reivindicación 1, en el que el estado es neutropenia originada por una enfermedad hematológica.
7. Compuesto según la reivindicación 1 para uso de acuerdo con la reivindicación 1, en el que el estado es neutropenia inducida por fármacos. 35
8. Compuesto según la reivindicación 1 para uso de acuerdo con la reivindicación 1, en el que el estado es neutropenia originada por una deficiencia nutricional.
9. Compuesto según la reivindicación 1 para uso de acuerdo con la reivindicación 1, en el que el estado es 40 neutropenia originada por una infección.
10. Compuesto según la reivindicación 1 para uso de acuerdo con la reivindicación 1, en el que el estado es neutropenia originada por radioterapia.
11. Compuesto según la reivindicación 1 para uso de acuerdo con la reivindicación 1, en el que el estado es una herida.
12. Compuesto según la reivindicación 1 para uso de acuerdo con la reivindicación 1, para el trasplante de médula ósea. 50
13. Compuesto según la reivindicación 1 para uso de acuerdo con cualquier reivindicación anterior, que es triglicérido de ácido caprílico.
14. Compuesto según la reivindicación 1 para uso de acuerdo con cualquiera de las reivindicaciones 1 a 12, que es 55 triglicérido de ácido cáprico.
15. Mezcla de dos compuestos según la reivindicación 1 para uso de acuerdo con cualquiera de las reivindicaciones 1 a 12, en la que A = B =R1CO y R1 es alquilo C7 y C9, respectivamente.
16. Mezcla según la reivindicación 15 para uso de acuerdo con la reivindicación 15, en la que R1 es CH3 (CH2) 6- y CH3 (CH2) 8- respectivamente.
17. Mezcla de compuestos para uso de acuerdo con cualquiera de las reivindicaciones 1 a 12, que comprende cuatro isómeros geométricos de triglicéridos de ácidos grasos C8 y C10 descritos en la siguiente fórmula:
18. Compuesto según una cualquiera de las reivindicaciones 1 a 14 o mezcla según cualquiera de las reivindicaciones 15 a 17 para uso de acuerdo con cualquiera de las reivindicaciones 1 a 17, en el que el sujeto de la administración está sometiéndose a administración separada o simultánea de un factor estimulante de colonias humano.
19. Compuesto según una cualquiera de las reivindicaciones 1 a 14 o mezcla según una cualquiera de las reivindicaciones 15 a 17 para uso de acuerdo con la reivindicación 18, en el que el factor estimulante de colonias es G-CSF o GM-CSF.
20. Compuesto según una cualquiera de las reivindicaciones 1 a 14 o mezcla según una cualquiera de las reivindicaciones 15 a 17 para uso de acuerdo con cualquiera de las reivindicaciones 1 a 17, en el que el sujeto de la administración está sometiéndose a administración simultánea de una citocina humana.
21. Compuesto según una cualquiera de las reivindicaciones 1 a 14 o mezcla según una cualquiera de las reivindicaciones 15 a 17 para uso de acuerdo con la reivindicación 20, en el que la citocina es interleucina 2 o 25 interleucina 15.
Patentes similares o relacionadas:
Composición farmacéutica basada en nanoestructura de grafeno para prevenir o tratar enfermedades neurodegenerativas, del 22 de Julio de 2020, de Seoul National University R & DB Foundation: Una composición farmacéutica para su uso en la prevención o el tratamiento de enfermedades neurodegenerativas, que comprende puntos cuánticos de grafeno como […]
Sales de butirato para uso en enfermedades inflamatorias, del 17 de Junio de 2020, de Birrbeheer B.V: Una preparación que comprende una sal de butirato para uso en el tratamiento de un sujeto que padece una enfermedad que está asociada con inflamación sistémica, […]
Derivados de celastrol para el tratamiento de la obesidad, del 3 de Junio de 2020, de THE CHILDREN'S MEDICAL CENTER CORPORATION: Una formulación farmacéutica para su uso en inducir pérdida de peso o reducir la grasa corporal, o una combinación de las mismas, en un paciente pre-obeso, obeso […]
Polimerosomas de gradiente de pH transmembrana y su uso en la eliminación del amoníaco y sus análogos metilados, del 27 de Mayo de 2020, de ETH ZURICH: Un polimerosoma que comprende (a) una membrana, que comprende un copolimero en bloque de poli(estireno) (PS) y poli(oxido de etileno) (PEO), en […]
Composiciones y métodos para tratar afecciones de la piel con luz y ácidos policarboxílicos, del 25 de Marzo de 2020, de JOHNSON & JOHNSON CONSUMER INC: Un kit que comprende: (a) una composición tópica que comprende hasta aproximadamente 5 por ciento en peso de al menos un ácido policarboxílico C2 a […]
Composición como medio auxiliar para medicación oral, del 18 de Marzo de 2020, de Paxtree Ltd: Una composición en forma de gelatina, que comprende carragenina iota, ácido cítrico y maltodextrina, en la que la cantidad de maltodextrina en la composición está en el intervalo […]
Un envase para un concentrado de fluido de diálisis ácido que contiene citrato y glucosa, del 18 de Marzo de 2020, de GAMBRO LUNDIA AB: Un envase que incluye un concentrado que contiene citrato ácido que comprende una concentración total de citrato de 28-45 mM; ácido […]
Un procedimiento para la preparación de una formulación de polvo seco que comprende un anticolinérgico, un corticoesteroide y un beta-adrenérgico, del 4 de Marzo de 2020, de CHIESI FARMACEUTICI S.P.A.: Un procedimiento de preparación de una formulación de polvo para inhalación para su uso en un inhalador de polvo seco, comprendiendo dicha formulación […]