Sales de profármaco de compuestos de 2,4-pirimidindiamina y sus usos.
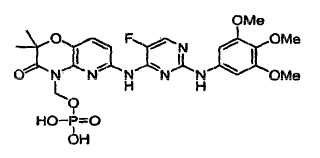
Un cristal que comprende un hidrato de sal de profármaco que tiene la estructura:
**Fórmula**
teniendo dicho cristal picos de difracción de rayos X en polvo característicos a valores de dos theta de 3,4º ± 0,1º, 6,6º ± 0,1º, 9,9º ± 0,1º, 13,2º ± 0,1º, 17,2º ± 0,1º, 19,7º ± 0,1º, 21,2 º ± 0,1º y 21,8º ± 0,1º cuando se usa una longitud de onda de radiación de 1,54059 Å.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2007/085313.
Solicitante: RIGEL PHARMACEUTICALS, INC..
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 1180 VETERANS BOULEVARD SOUTH SAN FRANCISCO, CA 94080 ESTADOS UNIDOS DE AMERICA.
Inventor/es: SINGH, RAJINDER, BHAMIDIPATI,SOMASEKHAR, MASUDA,ESTEBAN, SUN,THOMAS.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/5383 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › condensadas en orto o en peri con sistemas heterocíclicos.
- A61K31/675 A61K 31/00 […] › que tienen el nitrógeno como heteroátomo de un ciclo, p. ej. fosfato de piridoxal.
- A61P37/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Medicamentos para el tratamiento de problemas inmunológicos o alérgicos.
- C07D498/04 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 498/00 Compuestos heterocíclicos que contienen en el sistema condensado al menos un heterociclo que tienen átomos de nitrógeno y oxígeno como únicos heteroátomos del ciclo (4-oxa-1-azabiciclo [3.2.0] heptanos, p. ej. oxapenicilinas C07D 503/00; 5-oxa-1-azabiciclo [4.2.0] octanos, p. ej. oxacefalosporinas C07D 505/00; aquéllos de sus análogos que tienen el átomo de oxígeno del ciclo en otra posición C07D 507/00). › Sistemas orto-condensados.
- C07F9/6561 C07 […] › C07F COMPUESTOS ACICLICOS, CARBOCICLICOS O HETEROCICLICOS QUE CONTIENEN ELEMENTOS DISTINTOS DEL CARBONO, HIDROGENO, HALOGENOS, OXIGENO, NITROGENO, AZUFRE, SELENIO O TELURO (porfirinas que contienen metal C07D 487/22; compuestos macromoleculares C08). › C07F 9/00 Compuestos que contienen elementos de los grupos 5 o 15 del sistema periódico. › que contienen sistemas de dos o más heterociclos determinantes condensados entre ellos ó condensados con un carbociclo o un sistema carbocíclico común, con o sin otros heterociclos no condensados.
PDF original: ES-2380551_T3.pdf
Fragmento de la descripción:
Sales de profármaco de compuestos de 2, 4-pirimidindiamina y sus usos
5 Referencia a solicitudes de patente relacionadas
Antecedentes de la invención
1. Campo de la invención La presente divulgación se refiere a profármacos de compuestos de 2, 4-pirimidindiamina biológicamente activos, composiciones farmacéuticas que comprenden los profármacos, intermedios y métodos de síntesis de preparación de los profármacos y métodos de uso de los profármacos y composiciones en una variedad de contextos, tales como en el tratamiento o prevención de diversas enfermedades.
2. Descripción de la técnica relacionada La reticulación de receptores de Fc, tales como el receptor de alta afinidad para IgE (FcεRI) y/o el receptor de alta afinidad para IgG (FcγRI) , activa una cascada de señalización en mastocitos, basófilos y otras células inmunitarias 20 que da lugar a la liberación de mediadores químicos responsables de numerosos acontecimientos adversos. Por ejemplo, dicha reticulación conduce a la liberación de mediadores preformados de de reacciones de hipersensibilidad anafiláctica de tipo I (inmediata) , tales como la histamina, desde los sitios de almacenamiento en gránulos mediante desgranulación. También conduce a la síntesis y liberación de otros mediadores, incluidos leucotrienos, prostaglandinas y factores activadores plaquetarios (PAF) , que desempeñan papeles importantes en reacciones inflamatorias. Los mediadores adicionales que se sintetizan y se liberan tras la reticulación de receptores de Fc incluyen citocinas y el óxido nítrico.
La (s) cascada (s) de señalización activada (s) por la reticulación de receptores de Fc, tales como FcεRI y/o FcγRI, comprende (n) un conjunto de proteínas celulares. Entre los propagadores de señal intracelular más importantes se encuentran las tirosina cinasas. Y una importante tirosina cinasa implicada en las rutas de transducción de señal asociadas con la reticulación de los receptores FcεRI y/o FcγRI, así como en otras cascadas de transducción de señales, es la cinasa Syk (véase Valent et al., 2002, Intl. J. Hematol. 75 (4) : 257-362 para revisión) .
Los mediadores liberados como resultado de la reticulación de receptores FcεRI y FcγRI son responsables de, o desempeñan papeles importantes en, la manifestación de numerosos acontecimientos adversos. Recientemente, se han descubierto diversas clases de compuestos de 2, 4-pirimidindiamina que inhiben las cascadas de señalización de FcεRI y/o FcγRI y que tiene innumerables aplicaciones terapéuticas. Véanse, por ejemplo, la solicitud de EE.UU. con nº de serie 10/355.543 presentada el 31 de enero de 2003 (documento US 2004/0029902) , la solicitud internacional con nº de serie PCT/US03/03022 presentada el 31 de enero de 2003 (documento WO 03/063794) , la solicitud de EE.UU. nº 10/631.029 presentada el 29 de julio de 2003 (documento US 2005/0028212) , la solicitud internacional con nº de serie PCT/US03/24087 (documento WO 2004/014382) , la solicitud de EE.UU. nº 10/903.263 presentada el 30 de julio de 2004 (documento US2005/0234049) , y la solicitud internacional con nº de serie PCT/US2004/24716 (documento WO 2005/016893) . Aunque muchos de estos compuestos muestran buenas propiedades de biodisponibilidad, en algunos casos, puede ser deseable adaptar su solubilidad u otras propiedades, 45 de manera que su biodisponibilidad se optimice a través de rutas de administración específicas. El documento WO 2006/078846 se refiere a profármacos de compuestos de 2, 4-pirimidindiamina biológicamente activos y sus usos.
Sumario de la invención
50 La presente divulgación proporciona un cristal que comprende una sal de hidrato de profármaco de un compuesto de 2, 4-pirimidindiamina que tiene innumerables actividades biológicas y, por tanto, usos terapéuticos, composiciones que comprenden el hidrato de sal de profármaco, métodos para preparar el hidrato de sal de profármaco y la forma cristalina del mismo y usos del hidrato de sal de profármaco en una variedad de contextos in vitro e in vivo, incluyendo en el tratamiento y/o prevención de enfermedades mediadas, al menos en parte, por la activación de 55 cascadas de señalización de receptores de Fc.
Se ha descubierto que la solubilidad en agua y la biodisponibilidad oral de un compuesto de 2, 4-pirimidindiamina biológicamente activo en particular, que se ilustra a continuación (compuesto 1) , incrementó considerablemente cuando se formula para que incluya un progrupo Rp de fórmula -CH2-O-P (O) (OH) 2 en el átomo de nitrógeno de anillo 60 con el asterisco (compuesto 4) :
Compuesto 1 Compuesto 4
De forma significativa, mientras que la solubilidad en agua del fármaco activo (compuesto 1) está en el intervalo de aproximadamente <1 μg/ml en tampón acuoso en condiciones fisiológicas, la solubilidad del profármaco de fosfato correspondiente (compuesto 4) es mayor de 5 mg/ml en las mismas condiciones, o aproximadamente 2000 veces mayor. Esta solubilidad en agua incrementada permite una mejor disolución en el intestino, facilitando de este modo la administración oral.
La presente invención proporciona un cristal que comprende un hidrato de sal del compuesto 4 de profármaco de fosfato mostrado anteriormente.
En consecuencia, la invención proporciona un cristal que comprende un hidrato de sal de profármaco con la estructura:
teniendo dicho cristal picos de difracción de rayos X en polvo característicos a valores de dos theta de 3, 4º ± 0, 1º , 6, 6º ± 0, 1º , 9, 9º ± 0, 1º , 13, 2º ± 0, 1º , 17, 2º ± 0, 1º , 19, 7º ± 0, 1º , 21, 2 º ± 0, 1º y 21, 8º ± 0, 1º cuando se usa una longitud de onda de radiación de 1, 54059 Ã.
En otro aspecto, la invención proporciona un cristal que comprende un hidrato de sal de profármaco con la estructura:
teniendo dicho cristal simetría espacial de grupo P21/c y parámetros de celda unitaria característicos de a = 27, 73 Ã; b = 7, 98 Ã; c = 15, 17 º C; Ã= 90º ; alfa, beta = 103, 2º ; y gamma = 90º .
En otro aspecto, la presente invención proporciona una composición farmacéutica que comprende el hidrato de sal de profármaco definido anteriormente y un vehículo, excipiente y/o diluyente farmacéuticamente aceptable. La naturaleza exacta del vehículo, excipiente o diluyente dependerá del uso deseado para la composición y puede variar desde ser adecuado o aceptable para usos veterinarios a ser adecuado o aceptable para uso humano. Opcionalmente, la composición puede incluir uno o más compuestos adicionales.
El profármaco definido anteriormente se metaboliza para proporcionar un compuesto de 2, 4-pirimidindiamina que es un potente inhibidor de la desgranulación de células inmunitarias, tales como mastocitos, basófilos, neutrófilos y/o eosinófilos.
Así, en otro aspecto más, la presente invención proporciona un cristal de la invención como se define anteriormente o una composición farmacéutica de la invención como se define anteriormente, para su uso en un método de inhibición de la desgranulación de células en un sujeto. En general, el método implica poner en contacto una célula que se desgranula con una cantidad de la composición o el hidrato de sal de profármaco, eficaz para inhibir la desgranulación de la célula. El método puede ponerse en práctica en contextos in vivo como un enfoque terapéutico para el tratamiento o prevención de enfermedades caracterizadas por, causadas por, o asociadas a, la desgranulación celular.
Sin pretender vincularse a ninguna teoría de funcionamiento, los datos bioquímicos confirman que muchos de estos compuestos de 2, 4-pirimidindiamina activos ejercen su efecto inhibidor de la desgranulación, al menos en parte, bloqueando o inhibiendo la (s) cascada (s) de transducción de señales iniciada por la reticulación de los receptores de Fc de alta afinidad para IgE ("FcεRI") y/o IgG ("FcγRI") (véanse, por ejemplo, la solicitud de EE.UU. con nº de serie 10/631.029 presentada el 29 de julio de 2003 (documento US 2005/0028212) , la solicitud internacional con nº de serie PCT/US03/24087 (documento WO2004/014382) , la solicitud de EE.UU. con nº de serie 10/903.263 presentada el 25 de julio de 2004 (documento US2005/0234049) y la solicitud internacional con nº de serie PCT/US2004/24716 (documento WO 2005/016893) , cuyas divulgaciones se incorporan en el presente documento por referencia) . De hecho, estos compuestos de 2, 4-pirimidindiamina... [Seguir leyendo]
Reivindicaciones:
1. Un cristal que comprende un hidrato de sal de profármaco que tiene la estructura:
teniendo dicho cristal picos de difracción de rayos X en polvo característicos a valores de dos theta de 3, 4º ± 0, 1º , 6, 6º ± 0, 1º , 9, 9º ± 0, 1º , 13, 2º ± 0, 1º , 17, 2º ± 0, 1º , 19, 7º ± 0, 1º , 21, 2 º ± 0, 1º y 21, 8º ± 0, 1º cuando se usa una longitud de onda de radiación de 1, 54059 Ã.
2. Un cristal que comprende un hidrato de sal de profármaco que tiene la estructura:
teniendo dicho cristal simetría espacial de grupo P21/c y parámetros de celda unitaria característicos de a = 27, 73 Ã; b = 7, 98 Ã; c = 15, 17 Ã; alfa = 90º ; beta = 103, 2º ; y gamma = 90º .
3. Una composición farmacéutica que comprende el hidrato de sal de profármaco de acuerdo con la reivindicación 1
ó 2 y un vehículo, excipiente y/o diluyente farmacéuticamente aceptable. 20
4. Un cristal de acuerdo con la reivindicación 1 ó 2, o una composición farmacéutica de acuerdo con la reivindicación 3, para su uso en un método de inhibición de la desgranulación de células en un sujeto.
5. El cristal o la composición farmacéutica de acuerdo con la reivindicación 4, en el que la desgranulación de células
se asocia con una enfermedad seleccionada de una enfermedad alérgica, cicatrización de bajo grado, una enfermedad asociada con destrucción de tejidos, una enfermedad asociada con inflamación de tejidos, inflamación y cicatrización.
6. El cristal o la composición farmacéutica de acuerdo con la reivindicación 4, en el que la desgranulación de células 30 se asocia con artritis reumatoide.
7. Un cristal de acuerdo con la reivindicación 1 ó 2, o una composición farmacéutica de acuerdo con la reivindicación 3, para su uso en un método de inhibición de una actividad de una cinasa Syk en un sujeto.
8. Un cristal de acuerdo con la reivindicación 1 ó 2, o una composición farmacéutica de acuerdo con la reivindicación 3, para su uso en un método de inhibición de una cascada de transducción de señales receptor de Fc en un sujeto, opcionalmente en la que el receptor de Fc se selecciona del grupo que consiste en FcαRI, FcγRI, FcγRIII y FcεRI.
9. Un cristal de acuerdo con la reivindicación 1 ó 2, o una composición farmacéutica de acuerdo con la reivindicación 3, para su uso en un método de tratamiento o prevención de una enfermedad autoinmunitaria en un sujeto y/o uno o más síntomas asociados con la misma.
10. El cristal o la composición de la reivindicación 9, en el que la enfermedad autoinmunitaria se selecciona del grupo que consiste en tiroiditis de Hashimoto, anemia hemolítica autoinmunitaria, gastritis atrófica autoinmunitaria de anemia perniciosa, encefalomielitis autoinmunitaria, orquitis autoinmunitaria, enfermedad de Goodpasture, trombocitopenia autoinmunitaria, oftalmia simpática, miastenia gravis, enfermedad de Graves, cirrosis biliar primaria, hepatitis crónica activa, colitis ulcerosa, glomerulopatía membranosa, lupus eritematoso sistémico, artritis reumatoide, síndrome de Sjögren, síndrome de Reiter, polimiositis-dermatomiositis, esclerosis sistémica, poliarteritis nodosa, esclerosis múltiple y penfigoide ampolloso.
11. Un cristal de acuerdo con la reivindicación 1 ó 2, o una composición farmacéutica de acuerdo con la reivindicación 3, para su uso en un método de tratamiento de artritis reumatoide en un sujeto.
12. El cristal o la composición de la reivindicación 11, en el que la cantidad del cristal o de la composición farmacéutica administrada en el método es eficaz para lograr una concentración sérica del fármaco correspondiente con el hidrato de sal de profármaco que sea de o superior a la CI50 de inhibición de Syk del fármaco, medida en un ensayo in vitro.
13. Un método para la preparación del hidrato de sal de profármaco de acuerdo con la reivindicación 1 ó 2, comprendiendo el método:
ajustar el pH de una solución acuosa del profármaco hasta un valor en el intervalo de aproximadamente 8 a aproximadamente 11 con una base que contiene [Na+]; y precipitar el hidrato de sal de profármaco a partir de la solución acuosa.
14. El método de la reivindicación 13, en el que:
(a) el pH se ajusta a un valor en el intervalo de aproximadamente 9 a 11, opcionalmente a un valor en el intervalo de aproximadamente 9, 3 a aproximadamente 10, 5;
(b) la base que contiene [Na+] es NaOH, NaOMe o Na2CO3;
c) la precipitación del hidrato de sal de profármaco de la solución comprende añadir un disolvente miscible con agua a la solución acuosa, opcionalmente (i) en el que el disolvente miscible con agua se selecciona del grupo que consiste en acetonitrilo, acetona, isopropanol, metanol, etanol y mezclas de los mismos; o ii) en el que la solución acuosa se calienta antes de añadir el disolvente miscible con agua, después de añadir el disolvente miscible con agua, o tanto antes como después de añadir el disolvente miscible con agua, después se 40 deja enfriar para que precipite el hidrato de sal de profármaco; o (d) el método comprende además aislar el hidrato de sal de profármaco de la solución acuosa.
15. Un método para la preparación de una forma cristalina del hidrato de sal de profármaco de acuerdo con la 45 reivindicación 1 ó 2, comprendiendo el método:
(a) ajustar el pH de una solución acuosa del profármaco a un valor en el intervalo de aproximadamente 9 a aproximadamente 11 con una base que contiene [Na+]; 5 (b) precipitar una sal de profármaco a partir de la solución acuosa; y (c) exponer la sal de profármaco a la humedad, proporcionando la forma cristalina del hidrato de sal de profármaco, opcionalmente, en el que el método comprende además: 10
(i) antes de (b) , 1) añadir un disolvente miscible con agua a la solución acuosa, y 2) calentar la solución acuosa, antes de añadir el disolvente miscible en agua, después de añadir el disolvente miscible con agua o antes y después de añadir el disolvente miscible con agua;
(ii) realizar (b) mediante el enfriamiento de la solución acuosa; y (iii) antes de (c) , 1) lavar la sal de profármaco con un disolvente de lavado, y 2) retirar, sustancialmente, todo el disolvente de lavado.
Patentes similares o relacionadas:
Método para producir inmunoconjugados de anticuerpo-SN-38 con un enlazador CL2A, del 22 de Julio de 2020, de IMMUNOMEDICS, INC.: Un método para producir un compuesto, CL2A-SN-38, que presenta la estructura, **(Ver fórmula)** que comprende realizar un esquema de reacción como el que se muestra: **(Ver […]
Agente terapéutico para cáncer sólido, del 17 de Junio de 2020, de IDAC Theranostics, Inc: Un agente para uso en el tratamiento de cáncer sólido que comprende como principio activo un anticuerpo anti-CD4 que es un anticuerpo quimérico de tipo humano, un anticuerpo […]
Una terapia de combinación para un injerto estable y a largo plazo usando protocolos específicos para el agotamiento de los linfocitos T/B, del 20 de Mayo de 2020, de YEDA RESEARCH AND DEVELOPMENT CO. LTD.: Una dosis de células hematopoyéticas inmaduras de linfocitos T agotados, en donde dichas células hematopoyéticas inmaduras de linfocitos T agotados comprenden menos de 5 x 105 […]
Profármaco tenofovir éster monobencílico fosfamida, método de preparación y uso del mismo, del 6 de Mayo de 2020, de Jiangsu Tasly Diyi Pharmaceutical Co., Ltd: Un compuesto tenofovir éster monobencílico fosfamida de la fórmula general X, y el hidrato, solvato, sal farmacéuticamente aceptable del mismo o el isómero […]
Agente terapéutico para la disfunción meibomiana, del 6 de Mayo de 2020, de SANTEN PHARMACEUTICAL CO., LTD.: Una composición farmacéutica que comprende sirolimus a una concentración de 0,01 a 0,5% (p/v) como único ingrediente activo para uso en la supresión de la obstrucción de […]
Formulación de doxilamina y piridoxina y/o metabolitos o sales de estas, del 6 de Mayo de 2020, de DUCHESNAY INC.: Una forma de dosificación oral de liberación dual que comprende de 5 mg a 40 mg de doxilamina y/o una sal farmacéuticamente aceptable de esta y de 5 […]
Composición farmacéutica inyectable estable de antagonista del receptor de neuroquinina-1 y procedimiento para su preparación, del 29 de Abril de 2020, de PHARMATHEN S.A.: Una composición farmacéutica de liberación controlada para administración intramuscular o subcutánea que comprende Aprepitant o Fosaprepitant […]
Bisfosfonatos conjugados para el diagnóstico y la terapia de enfermedades óseas, del 22 de Abril de 2020, de SCV GmbH: Compuesto V para la complejación de isótopos metálicos, que comprende un quelante X y uno o varios vectores diana conjugados con el quelante X con la estructura -L1-R1-L2-R2-L3-R3, […]