NUEVOS MÉTODOS PARA CONSTRUIR BIBLIOTECAS QUE COMPRENDEN MIEMBROS PRESENTADOS Y/O EXPRESADOS EN UNA FAMILIA DIVERSA DE PÉPTIDOS, POLIPÉPTIDOS O PROTEÍNAS Y LAS NUEVAS BIBLIOTECAS.
Un método para producir una población o biblioteca de genes de inmunoglobulina que comprende las etapas de:
(i) introducir diversidad sintética en al menos uno de VH CDR1 o VH CDR2 de estos genes; y
(ii) combinar la diversidad de la etapa (i) con diversidad en VH CDR3 capturada de células B.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2002/012405.
Solicitante: DYAX CORP..
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 300 TECHNOLOGY SQUARE 8TH FLOOR CAMBRIDGE, MA 02139 ESTADOS UNIDOS DE AMERICA.
Inventor/es: LADNER, ROBERT, C., HOOGENBOOM, HENDRICUS, R., J., M., COHEN,Edward H, NASTRI,Horacio G, ROOKEY,Kristin L, HOET,René.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C12N15/00 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K).
- C12N15/09 C12N […] › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Tecnología del ADN recombinante.
- C12N15/63 C12N 15/00 […] › Introducción de material genético extraño utilizando vectores; Vectores; Utilización de huéspedes para ello; Regulación de la expresión.
- C12N15/70 C12N 15/00 […] › Vectores o sistemas de expresión especialmente adaptados a E. coli.
- C12N15/74 C12N 15/00 […] › Vectores o sistemas de expresión especialmente adaptados a huéspedes procariotas distintos a E. coli, p. ej. Lactobacillus, Micromonospora.
- C12P21/04 C12 […] › C12P PROCESOS DE FERMENTACION O PROCESOS QUE UTILIZAN ENZIMAS PARA LA SINTESIS DE UN COMPUESTO QUIMICO DADO O DE UNA COMPOSICION DADA, O PARA LA SEPARACION DE ISOMEROS OPTICOS A PARTIR DE UNA MEZCLA RACEMICA. › C12P 21/00 Preparación de péptidos o de proteínas (proteína monocelular C12N 1/00). › Péptidos o polipéptidos cíclicos o puenteados, p. ej. bacitracina.
- C12P21/06 C12P 21/00 […] › preparados por hidrólisis de un enlace peptídico, p. ej. hidrolizados.
- C12Q1/70 C12 […] › C12Q PROCESOS DE MEDIDA, INVESTIGACION O ANALISIS EN LOS QUE INTERVIENEN ENZIMAS, ÁCIDOS NUCLEICOS O MICROORGANISMOS (ensayos inmunológicos G01N 33/53 ); COMPOSICIONES O PAPELES REACTIVOS PARA ESTE FIN; PROCESOS PARA PREPARAR ESTAS COMPOSICIONES; PROCESOS DE CONTROL SENSIBLES A LAS CONDICIONES DEL MEDIO EN LOS PROCESOS MICROBIOLOGICOS O ENZIMOLOGICOS. › C12Q 1/00 Procesos de medida, investigación o análisis en los que intervienen enzimas, ácidos nucleicos o microorganismos (aparatos de medida, investigación o análisis con medios de medida o detección de las condiciones del medio, p. ej. contadores de colonias, C12M 1/34 ); Composiciones para este fin; Procesos para preparar estas composiciones. › en los que intervienen virus o bacteriófagos.
- C12Q3/00 C12Q […] › Procesos de control sensibles a las condiciones del medio (equipo para este fin C12M 1/36).
- G01N33/53 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › Ensayos inmunológicos; Ensayos en los que interviene la formación de uniones bioespecíficas; Materiales a este efecto.
PDF original: ES-2375952_T3.pdf
Fragmento de la descripción:
Nuevos métodos para construir bibliotecas que comprenden miembros presentados y/o expresados de una familia diversa de péptidos, polipéptidos o proteínas y las nuevas bibliotecas Esta solicitud es una continuación en parte de la solicitud provisional de los Estados Unidos 60/198, 069, presentada el 17 de abril, 2000, una continuación en parte de la solicitud de patente de los Estados Unidos 09/837, 306, presentada el 17 de abril, 2001, una continuación en parte de la solicitud PCT PCT/US01/12454, presentada el 17 de abril, 2001, una continuación en parte de la solicitud de los Estados Unidos 10/000, 516, presentada el 24 de octubre, 2001 y una continuación en parte de la solicitud de los Estados Unidos 10/045, 674, presentada el 25 de octubre, 2001.
La presente invención se refiere a las realizaciones caracterizadas en las reivindicaciones.
Así, se refiere a un método para producir una población o biblioteca de genes de inmunoglobulina que comprende las etapas de:
(i) introducir diversidad sintética en al menos uno de VH CDR1 o VH CDR2 de estos genes; y
(ii) combinar la diversidad de la etapa (i) con diversidad en VH CDR3 capturada de células B.
La presente invención también se refiere a una biblioteca que comprende una colección de paquetes genéticos que presentan un miembro de una familia diversa de péptidos, polipéptidos o proteínas y que presentan colectivamente al menos una parte de la familia, estando codificados los péptidos, polipéptidos o proteínas presentados por secuencias de ADN que comprenden secuencias que codifican
(a) una VH CDR1 que tiene una secuencia de aminoácidos según la fórmula -X1-Y-X2-M-X3-, en la que X1, X2, y X3 se seleccionan independientemente del grupo que consiste en A, D, E, F, G, H, I, K, L, M, N, P, Q, R, S, T, V, W, e Y;
(b) una VH CDR2 que tiene una secuencia de aminoácidos según la fórmula X4-I-X5-X6-S-G-G-X7-T-X8-Y-AD-S-V-K-G-, en la que X4 y X5 se seleccionan independientemente del grupo que consiste en Y, R, W, V, G, y S, X6 se selecciona del grupo que consiste en P y S, y X7 y X8 se seleccionan independientemente del grupo que consiste en A, D, E, F, G, H, I, K, L, M, N, P, Q, R, S, T, V, W, e Y; y
(c) una secuencia que codifica una VH CDR3, en la que dicha VH CDR3 es una VH CDR3 capturada de la región VH CDR3 de un gen de inmunoglobulina de una célula B.
En una realización preferida, los paquetes genéticos son fagos filamentosos o fagémidos.
La presente descripción se refiere además a vectores para presentar y/o expresar una familia diversa de péptidos, polipéptidos o proteínas.
La presente descripción se refiere además a métodos de cribado de las bibliotecas de la invención y a los péptidos, polipéptidos y proteínas identificados por dicho cribado.
ANTECEDENTES DE LA INVENCIÓN
Actualmente es una práctica común en la técnica preparar bibliotecas de paquetes genéticos que presentan, expresan o comprenden un miembro de una familia diversa de péptidos, polipéptidos o proteínas y que presentan, expresan o comprenden colectivamente al menos una parte de la diversidad de la familia. En muchas bibliotecas comunes, los péptidos, polipéptidos o proteínas están relacionados con anticuerpos. Frecuentemente, son Fabs o anticuerpos de cadena única.
En general, los ADN que codifican los miembros de las familias que se van a presentar y/o expresar deben amplificarse antes de que sean clonados y usados para presentar y/o expresar el miembro deseado. Dicha amplificación usa típicamente cebadores directos e inversos.
Dichos cebadores pueden ser complementarios a secuencias nativas del ADN que se va a amplificar o complementarios a oligonucleótidos unidos a los extremos 5' ó 3' de ese ADN. Los cebadores que son complementarios a secuencias nativas del ADN que se va a amplificar presentan desventajas porque sesgan los miembros de las familias que se van a presentar. Sólo se amplificarán aquellos miembros que contienen una secuencia en el ADN nativo que es sustancialmente complementaria al cebador. Aquellos que no la tengan estarán ausentes de la familia. Para aquellos miembros que se amplifican, se suprimirá cualquier diversidad en la región del cebador.
Por ejemplo, en la patente Europea 368, 684 B1, el cebador que se usa está en el extremo 5' de la región VH de un gen de anticuerpo. Hibrida con una región de secuencia en el ADN nativo que se dice que está "suficientemente bien conservada" en una única especie. Dicho cebador sesgará los miembros amplificados favoreciendo a aquellos que tienen esta región "conservada". Se suprime cualquier diversidad en esta región.
Se admite generalmente que los genes de los anticuerpos humanos surgen mediante un proceso que implica una selección combinatoria de V y J o V, D, y J seguido de mutaciones somáticas. Aunque la mayor parte de la diversidad se produce en las Regiones Determinantes de la Complementariedad (CDR) , la diversidad también se produce en las regiones más conservadas, Regiones Marco (FR) y al menos parte de esta diversidad confiere o incrementa la unión específica a antígenos (Ag) . Consecuentemente, las bibliotecas deberían contener tanta diversidad en CDR y FR como fuera posible.
Para clonar los ADN amplificados de los péptidos, polipéptidos o proteínas que codifican para presentación en un paquete genético y/o para expresión, los ADN deben escindirse para producir extremos apropiados para ligación en un vector. Dicha escisión se efectúa generalmente usando sitios de reconocimiento de endonucleasas de restricción portados por los cebadores. Cuando los cebadores están en el extremo 5' del ADN producido por transcripción inversa de ARN, dicha restricción deja regiones no traducidas 5' perjudiciales en el ADN amplificado. Estas regiones interfieren con la expresión de los genes clonados y así la presentación de los péptidos, polipéptidos y proteínas codificados por éstos.
RESUMEN DE LA INVENCIÓN
Es un objeto de esta invención proporcionar un método para producir una población o biblioteca de genes de inmunoglobulina que comprende las etapas de:
(i) introducir diversidad sintética en al menos uno de VH CDR1 o VH CDR2 de estos genes; y
(ii) combinar la diversidad de la etapa (i) con diversidad en VH CDR3 capturada de células B.
Estos métodos no están sesgados a favor de los ADN que contienen secuencias nativas que son complementarias a los cebadores usados para la amplificación. También permiten eliminar cualquier secuencia del ADN amplificado que puede ser perjudicial para la expresión antes de la clonación y presentación y/o expresión.
Los objetos adicionales de la invención están reflejados en las reivindicaciones 3 a 14. Cada una de estas reivindicaciones está incorporada específicamente por referencia en esta especificación.
DESCRIPCIÓN BREVE DE LOS DIBUJOS
La FIG. 1 es un esquema de los diferentes métodos que pueden emplearse para amplificar genes VH sin el uso de cebadores específicos para secuencias VH. La FIG. 2 es un esquema de los diferentes métodos que pueden emplearse para amplificar genes VL sin el uso de cebadores específicos para secuencias VL.
La FIG. 3 es un esquema de amplificación RACE de las cadenas pesadas y ligeras de anticuerpo.
La FIG. 4 muestra el análisis por gel de los productos de amplificación obtenidos después de la reacción de PCR primaria de 4 muestras de pacientes diferentes. La FIG. 5 muestra el análisis por gel del ADN kappa escindido del Ejemplo 2. La FIG. 6 muestra el análisis por gel del extensor-ADN kappa escindido del Ejemplo 2. La FIG. 7 muestra el análisis por gel del producto de PCR de la amplificación extensor-kappa del Ejemplo 2. La FIG. 8 muestra el análisis por gel del producto de PCR purificado de la amplificación extensor-kappa del Ejemplo 2. La FIG. 9 muestra el análisis por gel de las cadenas ligeras kappa escindidas y ligadas del Ejemplo 2. La FIG. 10 es un esquema del diseño para la diversidad sintética de CDR1 y CDR2. La FIG. 11 es un esquema del programa de clonación para la construcción del repertorio de cadena pesada. La FIG. 12 es un esquema de la escisión y ligación de la cadena ligera de anticuerpo. La FIG. 13 muestra el análisis por gel de las cadenas ligeras lambda escindidas y ligadas del Ejemplo 4. La FIG. 14 es un esquema de la escisión y ligación de la cadena pesada de anticuerpo. La FIG. 15 muestra el análisis por gel de las cadenas ligeras lambda escindidas y ligadas del Ejemplo 5. La FIG. 16 es un esquema de un vector... [Seguir leyendo]
Reivindicaciones:
1. Un método para producir una población o biblioteca de genes de inmunoglobulina que comprende las etapas de:
(i) introducir diversidad sintética en al menos uno de VH CDR1 o VH CDR2 de estos genes; y
(ii) combinar la diversidad de la etapa (i) con diversidad en VH CDR3 capturada de células B.
2. El método según la reivindicación 1, en el que la diversidad sintética se introduce tanto en VH CDR1 como en VH CDR2.
3. El método según la reivindicación 2, en el que la diversidad sintética comprende:
(a) una VH CDR1 que tiene una secuencia de aminoácidos según la fórmula -X1-Y-X2-M-X3-, en la que X1, X2, y X3 se seleccionan independientemente del grupo que consiste en A, D, E, F, G, H, I, K, L, M, N, P, Q, R, S, T, V, W, e Y; y
(b) una VH CDR2 que tiene una secuencia de aminoácidos según la fórmula X4-I-X5-X6-S-G-G-X7-T-X8-Y-A-D-S-V-KG-, en la que X4 y X5 se seleccionan independientemente del grupo que consiste en Y, R, W, V, G, y S, X6 se selecciona del grupo que consiste en P y S, y X7 y X8 se seleccionan independientemente del grupo que consiste en A, D, E, F, G, H, I, K, L, M, N, P, Q, R, S, T, V, W, e Y.
4. Una biblioteca que comprende una colección de paquetes genéticos que presentan un miembro de una familia diversa de péptidos, polipéptidos o proteínas y que presentan colectivamente al menos una parte de la familia, estando codificados los péptidos, polipéptidos o proteínas presentados por secuencias de ADN que comprenden secuencias que codifican
(a) una VH CDR1 que tiene una secuencia de aminoácidos según la fórmula -X1-Y-X2-M-X3-, en la que X1, X2, y X3 se seleccionan independientemente del grupo que consiste en A, D, E, F, G, H, I, K, L, M, N, P, Q, R, S, T, V, W, e Y;
(b) una VH CDR2 que tiene una secuencia de aminoácidos según la fórmula X4-I-X5-X6-S-G-G-X7-T-X8-Y-A-D-S-V-KG-, en la que X4 y X5 se seleccionan independientemente del grupo que consiste en Y, R, W, V, G, y S, X6 se selecciona del grupo que consiste en P y S, y X7 y X8 se seleccionan independientemente del grupo que consiste en A, D, E, F, G, H, I, K, L, M, N, P, Q, R, S, T, V, W, e Y; y
(c) una secuencia que codifica una VH CDR3, en la que dicha VH CDR3 es una VH CDR3 capturada de la región VH CDR3 de un gen de inmunoglobulina de una célula B.
5. La biblioteca según la reivindicación 4, en la que dichas secuencias de ADN comprenden además una secuencia que codifica una cadena ligera de inmunoglobulina.
6. La biblioteca según la reivindicación 5, en la que dicha secuencia que codifica una cadena ligera de inmunoglobulina se captura de una célula B.
7. La biblioteca según la reivindicación 6, en la que dicha célula B se aísla de una muestra de sangre de un paciente autoinmune.
8. La biblioteca según la reivindicación 7, en la que el paciente autoinmune está diagnosticado con un trastorno seleccionado del grupo que consiste en lupus eritematoso sistémico, esclerosis sistémica, artritis reumatoide, síndrome antifosfolípido y vasculitis.
9. La biblioteca según cualquiera de las reivindicaciones 4 ó 5 a 8, en la que dichas secuencias de ADN comprenden además secuencias que codifican regiones marco VH 3-23.
10. La biblioteca según cualquiera de las reivindicaciones 4 ó 5 a 8, en la que dichos paquetes genéticos son fagos M13.
11. La biblioteca según la reivindicación 10, en la que dichas secuencias de ADN están en un vector fago.
12. La biblioteca según la reivindicación 10 u 11, en la que dicho fago comprende un gen iii de tipo salvaje y un gen iii truncado para la presentación de péptidos, polipéptidos o proteínas.
13. La biblioteca según cualquiera de las reivindicaciones 4 ó 5 a 8, en la que dichas secuencias de ADN están en un vector fagémido.
14. La biblioteca según cualquiera de las reivindicaciones 10 a 13, en la que dichos péptidos, polipéptidos o proteínas presentados se presentan mediante un conector corto a la parte final del gen III de M13.
Patentes similares o relacionadas:
Composiciones farmacéuticas que contienen una leucocidina E mutada, del 22 de Julio de 2020, de NEW YORK UNIVERSITY: Una composición que comprende: una proteína Leucocidina E (LukE) aislada que comprende la secuencia de aminoácidos de la SEQ ID NO: 4, o un polipéptido […]
Composiciones y métodos para inmunomodulación en un organismo, del 19 de Febrero de 2020, de UNIVERSITY OF CONNECTICUT: Una composicion para su uso en un metodo de (i) tratamiento de cancer en un ser humano; (ii) mejora de la vacunacion en un ser humano; (iii) aumento de las respuestas […]
CD33 soluble para tratar síndromes mielodisplásicos (MDS), del 8 de Enero de 2020, de H. Lee Moffitt Cancer Center And Research Institute, Inc: Una proteína de fusión recombinante quimérica, que comprende: (a) una combinación de al menos dos fracciones de unión a S100A9 seleccionados de entre el grupo que […]
Métodos para la diferenciación y transducción in vitro de células b de memoria con vectores virales pseudotipados vsv-g, del 1 de Enero de 2020, de Immusoft Corporation: Un método in vitro para expresar un ácido nucleico de interés en una célula B, que comprende (a) poner en contacto células B de memoria con una composición que comprende […]
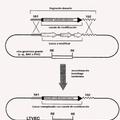 Producción de anticuerpos híbridos que contienen regiones variables humanas y regiones constantes de roedor, del 26 de Junio de 2019, de REGENERON PHARMACEUTICALS, INC.: Un procedimiento para modificar genéticamente un locus génico endógeno de la región variable de cadena pesada de inmunoglobulina en una célula madre embrionaria (ES) de […]
Producción de anticuerpos híbridos que contienen regiones variables humanas y regiones constantes de roedor, del 26 de Junio de 2019, de REGENERON PHARMACEUTICALS, INC.: Un procedimiento para modificar genéticamente un locus génico endógeno de la región variable de cadena pesada de inmunoglobulina en una célula madre embrionaria (ES) de […]
Intercambio de casetes de la región variable de la inmunoglobulina, del 12 de Junio de 2019, de Humanigen, Inc: Un método de modificación genética de un anticuerpo que retiene la especificidad de unión de un anticuerpo de referencia con un antígeno diana, comprendiendo el método: […]
Procedimiento de modificar células eucariotas, del 3 de Abril de 2019, de REGENERON PHARMACEUTICALS, INC.: Un procedimiento de reemplazar in situ, en parte, en una célula madre embrionaria (ES) de ratón, un locus génico endógeno de región variable de […]
Diacuerpos covalentes y usos de los mismos, del 2 de Abril de 2019, de MACROGENICS, INC: Una molécula de diacuerpo que comprende una primera cadena polipeptídica y una segunda cadena polipeptídica, en la que: (a) dicha primera cadena […]