Método para preparar lipopéptidos purificados.
Un método de purificación de daptomicina, el método comprende a.
mezclar la daptomicina en una solución que contenga una sal que contenga un catión divalente de calcio e isopropanol a un pH de 5, 9 a 6, 3 a una temperatura d.
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E07124028.
Solicitante: CUBIST PHARMACEUTICALS, INC..
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 65 HAYDEN AVENUE LEXINGTON, MA 02421 ESTADOS UNIDOS DE AMERICA.
Inventor/es: KEITH, DENNIS, LAI,JAN-JI, Govardhan,Chandrika, Khalaf,Nazer.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K38/00 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00).
- A61K38/10 A61K […] › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Péptidos que tienen de 12 a 20 aminoácidos.
- A61K8/00 A61K […] › Cosméticos o preparaciones similares para el aseo.
- A61K8/64 A61K […] › A61K 8/00 Cosméticos o preparaciones similares para el aseo. › Proteínas; Péptidos; Sus derivados o sus productos de degradación.
- A61K9/12 A61K […] › A61K 9/00 Preparaciones medicinales caracterizadas por un aspecto particular. › Aerosoles; Espumas.
- A61K9/14 A61K 9/00 […] › en estado especial, p. ej. polvos (microcápsulas A61K 9/50).
- A61P31/04 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 31/00 Antiinfecciosos, es decir antibióticos, antisépticos, quimioterápicos. › Agentes antibacterianos.
- A61Q15/00 A61 […] › A61Q USO ESPECIFICO DE COSMETICOS O DE PREPARACIONES SIMILARES PARA EL ASEO. › Anti-transpirantes o desodorantes corporales (desodorización del aire A61L 9/00).
- A61Q19/10 A61Q […] › A61Q 19/00 Preparaciones para el cuidado de la piel. › Preparaciones para la limpieza o el baño.
- A61Q5/02 A61Q […] › A61Q 5/00 Preparaciones para el cuidado del cabello. › Preparaciones para la limpieza del cabello.
- C07K1/14 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 1/00 Procedimientos generales de preparación de péptidos. › Extracción; Separación; Purificación.
- C07K14/36 C07K […] › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › de Actinomyces; de Streptomyces (G).
- C07K7/08 C07K […] › C07K 7/00 Péptidos con 5 a 20 aminoácidos en una secuencia totalmente determinada; Sus derivados. › con 12 a 20 aminoácidos.
- C07K7/54 C07K 7/00 […] › conteniendo al menos un enlace peptídico anormal en el ciclo.
- C12P21/04 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12P PROCESOS DE FERMENTACION O PROCESOS QUE UTILIZAN ENZIMAS PARA LA SINTESIS DE UN COMPUESTO QUIMICO DADO O DE UNA COMPOSICION DADA, O PARA LA SEPARACION DE ISOMEROS OPTICOS A PARTIR DE UNA MEZCLA RACEMICA. › C12P 21/00 Preparación de péptidos o de proteínas (proteína monocelular C12N 1/00). › Péptidos o polipéptidos cíclicos o puenteados, p. ej. bacitracina.
PDF original: ES-2377931_T3.pdf
Fragmento de la descripción:
ÍMBITO TÉCNICO DE LA INVENCIÓN
La presente invención se refiere a métodos de purificación de daptomicina.
ANTECEDENTES DE LA INVENCIÓN
El rápido aumento del índice de infecciones Gram positivas, incluyendo aquellas causadas por bacterias resistentes a antibióticos, ha suscitado un nuevo interés en el desarrollo de novedosas clases de antibióticos. Una de estas clases son los antibióticos lipopéptidos, que incluyen daptomicina. La daptomicina tiene una potente actividad bactericida in vitro contra las bacterias Gram positivas clínicamente relevantes que causan enfermedades graves y potencialmente mortales. Estas bacterias incluyen, sin carácter limitativo, patógenos resistentes, como los enterococos resistentes a la vancomicina (ERV) , Staphylococcus aureus resistente a la meticilina (SARM) , Staphylococcus aureus susceptible a escala intermedia al glicopéptido (GISA) , estafilococos coagulasa negativos (ECN) , Streptococcus pneumoniae resistente a la penicilina (PRSP, por sus siglas en inglés) , para los cuales hay alternativas terapéuticas muy escasas. Véase, por ejemplo, Tally at al., 1999, Exp, Opin. Invest, Drugs 8: 1223-1238. El efecto inhibitorio de la daptomicina es un efecto bactericida rápido in vitro y in vivo que depende de la concentración, y un efecto postantibiótico in vivo que depende de la concentración relativamente prolongado.
La daptomicina ha sido descrita por Blatz en Biotechnology of Antibiotics, 2nd Ed., ed. W.R. Strohl (New York Marcel Dekker, Inc.) , 1997, páginas 415-435. La daptomicina, también conocida como LY 146032, es un antibiótico lipopéptido cíclico que puede ser obtenido a partir de la fermentación de Streptomyces roseosporus. La daptomicina es un miembro de los antibióticos de tipo factor A-21978 C0 de S. roseosporus y está compuesta por una cadena lateral de decanoilo unida al triptófano N-terminal de un péptido cíclico de 13 aminoácidos (Figura 1) . La daptomicina tiene un excelente perfil de actividad porque es altamente eficaz contra la mayoría de las bacterias Gram positivas; es altamente bactericida y de acción rápida; tiene una baja tasa de resistencia y es electivo frente a los organismos resistentes a los antibióticos. El compuesto está siendo desarrollado actualmente en una variedad de formulaciones para tratar infecciones graves causadas por bacterias, incluyendo, pero sin carácter limitativo, Staphylococcus aureus resistente a la meticilina (SARM) y enterococos resistentes a la vancomicina (ERV) .
Diversas patentes estadounidenses describen los antibióticos A-21978C0 y los lipopéptidos relacionados con la daptomicina incluyendo la daptomicina (LY 146032) . Estas patentes describen también los métodos de producción y aislamiento de los antibióticos A-21978C0 y lipopéptidos relacionados con la daptomicina.
[0005] Las patentes estadounidenses RE32.333, RE32.455, 4.800.157, 4.874.843 y 4.885.243 describen métodos para sintetizar y aislar daptomicina a partir de cultivos de fermentación de Streptomyces roseosporus. Las patentes estadounidenses RE32.310, RE32.311, 4.537.717, 4.482.487 y 4.524.135 describen antibióticos A-21978C0 y métodos de desacilación del antibiótico A-21978C0 y reacilación de los núcleos de los péptidos y derivados antibióticos realizados mediante este proceso. La patente estadounidense 5.912.226 (en lo sucesivo patente ‘226) describe la identificación y el aislamiento de dos impurezas producidas durante la producción de daptomicina, anhidro-daptomicina y la forma de isómero º de daptomicina. Ninguna de estas patentes estadounidenses revela un método para precipitar o cristalizar un lipopéptido de tal forma que aumente la pureza del lipopéptido.
La patente estadounidense 4.439.425 (en lo sucesivo patente ‘425) revela un lipopéptido cristalino y un método para cristalizar el lipopéptido. El lipopéptido revelado en la patente ‘425 es estructuralmente diferente a la daptomicina y los lipopéptidos relacionados con la daptomicina. La patente estadounidense 5.336.756 (en lo sucesivo patente ‘756) también revela un lipopéptido cíclico cristalino compuesto por un hexapéptido. El lipopéptido cíclico cristalino revelado en la patene ‘756 es también estructuralmente diferente a la daptomicina y los lipopéptidos relacionados con la daptomicina. La patente ‘756 revela que el lipopéptido, un compuesto de tipo equinocandina, puede obtenerse al utilizar n-propanol acuoso como disolvente cristalizador. Véase, por ejemplo, cols. 1 y 2 de la patente ‘756. Ni la patente ‘425 ni la patente ‘756 revelan métodos de cristalización o precipitación de daptomicina o lipopéptidos relacionados con la daptomicina. Tampoco revelan métodos de cristalización o precipitación de lipopéptidos producidos por Streptomyces.
Jancarik + Kim, J. Appl. Cr y st. (1991) 24: 409-411, describe un conjunto generalizado de condiciones de cristalización que puede ser utilizado para la cristalización de proteínas.
Sería beneficioso desarrollar un método de cristalización o precipitación de daptomicina y lipopéptidos relacionados con la daptomicina para lograr un método de purificación mejorada para estos lipopéptidos. Además, se utilizaría una forma precipitada altamente purificada o cristalina de daptomicina u otro lipopéptido relacionado con la daptomicina al formular composiciones farmacéuticas para tratar infecciones bacterianas. Además, una forma precipitada altamente purificada o cristalina de daptomicina o lipopéptidos relacionados con la daptomicina resultaría útil en un método para fabricar un producto estéril, especialmente productos estériles en grandes cantidades. Por consiguiente, hay una necesidad de métodos para producir daptomicina precipitada o cristalina y lipopéptidos relacionados con la daptomicina y las formas precipitadas y cristalinas de los lipopéptidos así producidos. Sin embargo, no ha habido un método sólido y simple que haya sido efectivo cristalizando o precipitando daptomicina o lipopéptidos relacionados con la daptomicina y que se obtenga un lipopéptido que sea más puro tras la cristalización o precipitación que antes.
RESUMEN DE LA INVENCIÓN
La presente invención proporciona un método de purificación de daptomicina, de acuerdo con la reivindicación 1. Se describen otras características de la invención en las reivindicaciones dependientes.
BREVE DESCRIPCIÓN DE LOS DIBUJOS
[0010]
La Fig. 1 muestra la estructura de la daptomicina.
La Fig. 2 muestra una fotomicrografía de cristales en forma de erizo o partículas de daptomicina similares al cristal producidos por el método descrito en el Ejemplo 12.
La Fig. 3 muestra una fotomicrografía de cristales de daptomicina en forma de aguja.
La Fig. 4 muestra una fotomicrografía de cristales de daptomicina en forma de barra.
La Fig. 5 muestra fotomicrografías de muestras de daptomicina con un aumento de 100x. Se muestran fotomicrografías de daptomicina amoría utilizando luz transmitida plana (A) y luz polarizada cruzada (B) . Se muestran fotomicrografías de cristales de daptomicina utilizando luz transmitida plana (C y B) y luz polarizada cruzada (D y F) . Los cristales de daptomicina fueron producidos mediante el protocolo descrito en el Ejemplo 7.
La Fig. 6 muestra un patrón de difracción de rayos X de polvo para la daptomicina amoría.
La Fig. 7 muestra un patrón de difracción de rayos X de polvo para un cristal de daptomicina producido mediante el protocolo descrito en el Ejemplo 7.
La Fig. 8 muestra un patrón de difracción de rayos X de polvo para una segunda muestra de cristal de daptomicina producido mediante el protocolo descrito en el Ejemplo 7.
La Fig. 9 muestra la birrefringencia de una partícula de daptomicina similar al cristal al exponerla a luz polarizada. La partícula similar al cristal fue producida mediante el método descrito en el Ejemplo 12.
La Fig. 10 muestra un diagrama de un método ejemplar de cristalización.
La Fig. 11 muestra un diagrama de método de producción ejemplar que no utiliza cristalización o precipitación. El método de producción utiliza fermentación bacteriana para producir un cultivo de fermentación que contiene daptomicina, y después la purificación de daptomicina utilizando microfiltración, cromatografía de intercambio aniónico, ultrafiltración por exclusión de tamaño, cromatografía de interacción hidrofóbica,... [Seguir leyendo]
Reivindicaciones:
1. Un método de purificación de daptomicina, el método comprende a. mezclar la daptomicina en una solución que contenga una sal que contenga un catión divalente de calcio e isopropanol a un pH de 5, 9 a 6, 3 a una temperatura d.
2. 30 grados C para obtener daptomicina cristalina o 5 similar al cristal; y b. recolectar la daptomicina cristalina o similar al cristal.
2. El método de la reivindicación 1, en el que la solución contiene acetato de calcio a un pH de 6, 1.
3. El método de cualquiera de las reivindicaciones 1-2, en el que la temperatura de la solución es de 27 grados C.
4. El método de cualquiera de las reivindicaciones 1-3, en el que la solución se guarda durante un periodo de 3 a 24 10 horas antes de recolectar la daptomicina cristalina o similar al cristal.
5. El método de cualquiera de las reivindicaciones 1-4, en el que la sal que contiene un catión divalente de calcio es acetato de calcio o cloruro de calcio.
6. El método de cualquiera de las reivindicaciones 1-5, en el que la solución contiene de 80 a 85% de isopropanol, 0, 01-0, 03 M de sal, y 0, 01-0, 03 M de agente regulador del pH.
7. El método de cualquiera de las reivindicaciones 1-6, en el que el método además comprende someter la daptomicina a una o más fases de purificación seleccionados mediante cromatografía de interacción hidrofóbica (HIC) , cromatografía de intercambio aniónico y filtración previas a la fase de cristalización de la reivindicación 1.
8. El método de cualquiera de las reivindicaciones 1-7, en el que, antes de la fase de cristalización de la reivindicación 1a, a. el pH, la temperatura y/o la concentración de sal de la daptomicina son alterados de forma que la daptomicina forme micelas; y b. las micelas son filtradas para retener las micelas mientras que las impurezas más pequeñas pasan a través del filtro.
Dibujos
Figura 1
Patentes similares o relacionadas:
Composiciones farmacéuticas que contienen una leucocidina E mutada, del 22 de Julio de 2020, de NEW YORK UNIVERSITY: Una composición que comprende: una proteína Leucocidina E (LukE) aislada que comprende la secuencia de aminoácidos de la SEQ ID NO: 4, o un polipéptido […]
Composiciones y métodos para inmunomodulación en un organismo, del 19 de Febrero de 2020, de UNIVERSITY OF CONNECTICUT: Una composicion para su uso en un metodo de (i) tratamiento de cancer en un ser humano; (ii) mejora de la vacunacion en un ser humano; (iii) aumento de las respuestas […]
CD33 soluble para tratar síndromes mielodisplásicos (MDS), del 8 de Enero de 2020, de H. Lee Moffitt Cancer Center And Research Institute, Inc: Una proteína de fusión recombinante quimérica, que comprende: (a) una combinación de al menos dos fracciones de unión a S100A9 seleccionados de entre el grupo que […]
Métodos para la diferenciación y transducción in vitro de células b de memoria con vectores virales pseudotipados vsv-g, del 1 de Enero de 2020, de Immusoft Corporation: Un método in vitro para expresar un ácido nucleico de interés en una célula B, que comprende (a) poner en contacto células B de memoria con una composición que comprende […]
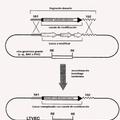 Producción de anticuerpos híbridos que contienen regiones variables humanas y regiones constantes de roedor, del 26 de Junio de 2019, de REGENERON PHARMACEUTICALS, INC.: Un procedimiento para modificar genéticamente un locus génico endógeno de la región variable de cadena pesada de inmunoglobulina en una célula madre embrionaria (ES) de […]
Producción de anticuerpos híbridos que contienen regiones variables humanas y regiones constantes de roedor, del 26 de Junio de 2019, de REGENERON PHARMACEUTICALS, INC.: Un procedimiento para modificar genéticamente un locus génico endógeno de la región variable de cadena pesada de inmunoglobulina en una célula madre embrionaria (ES) de […]
Intercambio de casetes de la región variable de la inmunoglobulina, del 12 de Junio de 2019, de Humanigen, Inc: Un método de modificación genética de un anticuerpo que retiene la especificidad de unión de un anticuerpo de referencia con un antígeno diana, comprendiendo el método: […]
Procedimiento de modificar células eucariotas, del 3 de Abril de 2019, de REGENERON PHARMACEUTICALS, INC.: Un procedimiento de reemplazar in situ, en parte, en una célula madre embrionaria (ES) de ratón, un locus génico endógeno de región variable de […]
Diacuerpos covalentes y usos de los mismos, del 2 de Abril de 2019, de MACROGENICS, INC: Una molécula de diacuerpo que comprende una primera cadena polipeptídica y una segunda cadena polipeptídica, en la que: (a) dicha primera cadena […]