Procedimiento de ligación de aceptores de péptidos.
Un procedimiento para fijar un aceptor de péptidos a una molécula de ARN,
que comprende:
(a) proporcionar una molécula de ARN; y
(b) ligar químicamente dicho aceptor de péptidos a dicha molécula de ARN para formar un enlace covalente.
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E07005917.
Solicitante: BRISTOL-MYERS SQUIBB COMPANY.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: ROUTE 206 AND PROVINCE LINE ROAD PRINCETON NJ 08543-4000 ESTADOS UNIDOS DE AMERICA.
Inventor/es: WAGNER, RICHARD, LOHSE,PETER, KURZ,MARKUS.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07K1/107 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 1/00 Procedimientos generales de preparación de péptidos. › por modificación química de los péptidos precursores.
- C07K1/22 C07K 1/00 […] › Cromatografía de afinidad o técnicas análogas basadas en procesos de absorción selectiva.
- C07K14/00 C07K […] › Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados.
- C07K17/02 C07K […] › C07K 17/00 Péptidos fijados sobre un soporte o inmovilizados; Su preparación. › Péptidos inmovilizados, o en, un soporte orgánico.
- C12N15/09 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Tecnología del ADN recombinante.
- C12N15/10 C12N 15/00 […] › Procedimientos para el aislamiento, la preparación o la purificación de ADN o ARN (preparación química de ADN o ARN C07H 21/00; preparación de polinucleótidos no estructurales a partir de microorganismos o con la ayuda de enzimas C12P 19/34).
- C12N15/11 C12N 15/00 […] › Fragmentos de ADN o de ARN; sus formas modificadas (ADN o ARN no empleado en tecnología de recombinación C07H 21/00).
- C12P19/34 C12 […] › C12P PROCESOS DE FERMENTACION O PROCESOS QUE UTILIZAN ENZIMAS PARA LA SINTESIS DE UN COMPUESTO QUIMICO DADO O DE UNA COMPOSICION DADA, O PARA LA SEPARACION DE ISOMEROS OPTICOS A PARTIR DE UNA MEZCLA RACEMICA. › C12P 19/00 Preparación de compuestos que contienen radicales sacárido (ácido cetoaldónico C12P 7/58). › Polinucleótidos, p. ej. ácidos nucleicos, oligorribonucleótidos.
PDF original: ES-2383332_T3.pdf
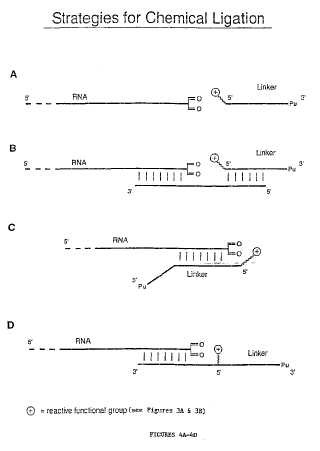
Fragmento de la descripción:
Procedimientos de ligación de aceptores de péptidos Antecedentes de la invención En general, la presente invención se refiere a procedimientos de ligación, en particular, para unir aceptores de péptidos a ácidos nucleicos.
Actualmente existen procedimientos para la preparación de fusiones de ARN-proteína. Una fusión de ARN-proteína se crea uniendo un aceptor de péptidos al extremo 3' de una molécula de ARN, seguido de la traducción in vitro o in situ del ARN. El producto es un péptido unido al extremo 3' del ARN que lo codifica. La generación de estas fusiones de ARN-proteína facilita el aislamiento de proteínas con propiedades deseadas a partir de grandes conjuntos de secuencias de aminoácidos parcial o completamente aleatorias, y resuelve el problema de recuperar y amplificar la información de la secuencia de la proteína por unión covalente de la secuencia codificante de ARN a su molécula de proteína correspondiente.
En el documento WO98/31700 se describe el uso de la ADN ligasa de T4 para unir el aceptor de péptidos puromicina a ARN por medio de un "puente" de ADN. El documento WO98/31700 también describe la preparación de moldes de traducción mínimos que contienen puromicina 3' por unión de nucleótidos individuales a puromicina inmovilizada usando una síntesis de oligonucleótidos convencional basada en fosforamidato.
Roberts y Szostak (PNAS 94:12297-12302, 1997) informan sobre la preparación de ARN sintéticos con puromicina 3' usando puromicina inmovilizada como soporte para la síntesis convencional de un engarce oligonucleotídico, y ligando la molécula de engarce de puromicina resultante a un ARN que codifica un polipéptido en tampón de ADN ligasa de T4.
En el documento WO98/155636 se describe un procedimiento para la preparación de productos de ligación quiméricos de ARN-ADN que comprenden puromicina 3' usando ARN ligasa de T4.
Tuniskaya y col. (FEBS Letters 442: 20-24, 1999) informan sobre estudios de interacción de proteína-ácido nucleico usando oligonucleótidos que contienen 2'-O-β-ribofuranosil-citidina que se oxidaron con IO4- para producir los dialdehídos correspondientes que permitían la unión covalente a la proteína investigada.
Pieles y col. (Nucleic Acids Research 17 (22) , 8967-77, 1989) describen la formación de enlaces covalentes entre un oligonucleótido que lleva psoraleno y la cadena de matriz complementaria por fotorreacción.
Misiura y col. (Nucleic Acids Res. 18 (15) : 4345-54, 1990) han descrito unidades de engarce de fosforamidita no nucleosídicas para la incorporación directa de grupos indicadores durante la síntesis de oligonucleótidos.
Sumario de la invención La presente invención se refiere a procedimientos para la unión de un aceptor de péptidos a una molécula de ARN, así como a los productos de ARN-aceptor de péptidos. Estos procedimientos facilitan la producción de fusiones de ARN-proteína que pueden usarse, por ejemplo, para el aislamiento de proteínas o ácidos nucleicos con propiedades deseadas a partir de grandes conjuntos de secuencias de ácido nucleico o de aminoácidos parcial o completamente aleatorias. Este procedimiento de la invención puede realizarse por una diversidad de estrategias para fijar un aceptor de péptidos a una molécula de ácido nucleico. Estos diversos enfoques difieren entre sí en los tipos de enlaces formados por la unión del péptido al ácido nucleico, y en los reactivos usados para conseguir la unión.
En el presente documento se describe un procedimiento para fijar un aceptor de péptidos a una molécula de ARN que implica proporcionar una molécula de ARN que tiene una secuencia 3' que forma una estructura de horquilla, proporcionar un aceptor de péptidos unido covalentemente a una molécula de engarce de ácido nucleico, e hibridar la molécula de ARN con la molécula de engarce de ácido nucleico en condiciones que permiten que se produzca la formación de enlaces covalentes entre el aceptor de péptidos y la molécula de ARN.
También se describe en el presente documento un procedimiento para fijar un aceptor de péptidos a una molécula de ARN que implica proporcionar un aceptor de péptidos que tiene un engarce con una secuencia 5' que forma una horquilla, hibridar el aceptor de péptidos con la molécula de ARN, y unir covalentemente el aceptor de péptidos al ARN.
En un primer aspecto, la invención se refiere a un procedimiento para fijar un aceptor de péptidos a una molécula de ARN ligando químicamente la molécula de ARN al aceptor de péptidos.
En una realización de este aspecto, el aceptor de péptidos está unido a un resto de psoraleno y forma enlaces cruzados con la molécula de ARN a través del resto de psoraleno. El resto de psoraleno puede estar unido al extremo 5' o 3' de una molécula de engarce que se une por sí misma al aceptor de péptidos, o el resto de psoraleno puede estar situado en una posición interna de la molécula de engarce. De acuerdo con esta técnica, el aceptor de péptidos forma enlaces cruzados con la molécula de ARN usando irradiación UV. En realizaciones adicionales de este aspecto particular, el psoraleno está unido al aceptor de péptidos a través de una cadena alquilo C6 y/o la molécula de ARN contiene un codón de terminación colocado cerca de su extremo 3'. Preferentemente, el engarce tiene una longitud comprendida entre 25 y 40 unidades nucleotídicas. Además, antes del entrecruzamiento del aceptor de péptidos a la molécula de ARN, el ARN puede hibridar con un engarce que incluye además un resto fotoescindible. El ARN hibridado después puede inmovilizarse en un soporte sólido a través del resto fotoescindible. Preferentemente, el resto fotoescindible es biotina.
En otra realización del primer aspecto de la invención, la molécula de ARN está funcionalizada y se une a un péptido que se ha modificado de manera adecuada para permitir la formación de enlaces químicos entre el aceptor de péptidos y la molécula de ARN. Preferentemente, la molécula de ARN se funcionaliza mediante oxidación con IO4-. El aceptor de péptidos puede funcionalizarse por unión al aceptor de péptidos de una molécula elegida entre el grupo que consiste en aminas, hidrazinas, (tio) hidrazidas y (tio) semicarbazonas.
En otra realización más del primer aspecto de la invención, la ligación química se realiza en ausencia de un molde externo. Como alternativa, la reacción de ligación química puede realizarse en presencia de un molde externo. Este segundo procedimiento implica alinear la molécula de ARN y la parte de engarce de un aceptor de péptidos usando un molde, de tal forma que el extremo 5' del molde hibride con la parte de engarce del aceptor de péptidos y el extremo 3' del molde hibride con la molécula de ARN. La ligación química de una molécula de ARN a un aceptor de péptidos también puede realizarse en ausencia de un molde externo por hibridación de la propia molécula de engarce, que está unida covalentemente al aceptor de péptidos, a la molécula de ARN. Esta hibridación aproxima el aceptor de péptidos y la molécula de ARN para la ligación. Preferentemente, el grupo funcional está en el extremo 5' de la región de engarce del aceptor de péptidos, o está flanqueado por un dominio de hibridación por un lado y por el aceptor de péptidos por el otro lado.
En una realización adicional del primer aspecto de la invención, la ligación química del aceptor de péptidos a la molécula de ARN implica la unión de un grupo funcional a la molécula de ARN por medio de aminación reductora del ARN, seguida de la modificación del aceptor de péptidos para reaccionar con la molécula de ARN. Las dos moléculas después se unen mediante la formación de un enlace covalente. Preferentemente, el grupo funcional unido a la molécula de ARN es un tiol, maleimida o amina.
En otros aspectos, la invención se refiere a moléculas de ARN ligadas químicamente a aceptores de péptidos así como a las fusiones de ácido nucleico-proteína generadas por transcripción y traducción (y, si se desea, transcripción inversa y/o amplificación) de estas moléculas de ARN. En una realización, el aceptor de péptidos está ligado al extremo 3' de la molécula de ARN.
También se describen procedimientos para la selección de una proteína o ácido nucleico deseado usando las moléculas de ARN-aceptor de péptidos de la invención. Las técnicas de selección usan las moléculas de la presente invención para la formación de fusiones de ARN-proteína, y la posterior selección de proteínas... [Seguir leyendo]
Reivindicaciones:
1. Un procedimiento para fijar un aceptor de péptidos a una molécula de ARN, que comprende:
(a) proporcionar una molécula de ARN; y
(b) ligar químicamente dicho aceptor de péptidos a dicha molécula de ARN para formar un enlace covalente.
2. El procedimiento de la reivindicación 1, en el que dicho aceptor de péptidos se une a un resto de psoraleno y dicha etapa de ligación química comprende entrecruzar dicho aceptor de péptidos, a través de dicho resto de psoraleno, con dicha molécula de ARN.
3. El procedimiento de la reivindicación 2, en el que dicho resto de psoraleno se une a dicho aceptor de péptidos a través de un engarce.
4. El procedimiento de la reivindicación 3, en el que dicho resto de psoraleno se sitúa en el extremo 5' de dicho engarce.
5. El procedimiento de la reivindicación 3, en el que dicho resto de psoraleno se sitúa en el extremo 3' de dicho engarce.
6. El procedimiento de la reivindicación 3, en el que dicho resto de psoraleno se sitúa dentro de dicho engarce.
7. El procedimiento de la reivindicación 3, en el que dicho engarce comprende una cadena alquilo C6.
8. El procedimiento de la reivindicación 3, en el que dicha molécula de ARN contiene un codón de terminación colocado cerca de su extremo 3'.
9. El procedimiento de la reivindicación 3, en el que dicho engarce tiene una longitud comprendida entre 25 y 40 unidades nucleotídicas.
10. El procedimiento de la reivindicación 2, en el que dicho entrecruzamiento se consigue por irradiación de luz UV.
11. El procedimiento de la reivindicación 3, en el que, antes de dicho entrecruzamiento, dicho ARN se hibrida con dicho engarce que comprende además un resto fotoescindible, y dicho ARN hibridado se inmoviliza en un soporte sólido a través de dicho resto fotoescindible.
12. El procedimiento de la reivindicación 11, en el que dicho resto fotoescindible es biotina.
13. El procedimiento de la reivindicación 1, en el que dicha molécula de ARN se funcionaliza, y en el que se une un grupo funcional a dicho aceptor de péptidos.
14. El procedimiento de la reivindicación 13, en el que dicha molécula de ARN se funcionaliza por oxidación con IO4.
15. El procedimiento de la reivindicación 13, en el que dicha ligación química se realiza en ausencia de un molde externo.
16. El procedimiento de la reivindicación 13, en el que dicho aceptor de péptidos está unido covalentemente a una molécula de engarce y, antes de dicha etapa de ligación química, dicha molécula de ARN y dicho aceptor de péptidos se alinean usando un molde externo, hibridando dicho molde externo con el extremo 3' de dicha molécula de ARN y con el extremo 5' de dicha molécula de engarce.
17. El procedimiento de la reivindicación 13, en el que dicho aceptor de péptidos se une covalentemente a una molécula de engarce y, antes de dicha etapa de ligación química, dicha molécula de ARN y dicho aceptor de péptidos se alinean por hibridación de dicha molécula de engarce al extremo 3' de dicho ARN.
18. El procedimiento de la reivindicación 17, en el que dicho grupo funcional de dicho aceptor de péptidos se localiza en el extremo 5' de dicha molécula de engarce.
19. El procedimiento de la reivindicación 17, en el que dicho grupo funcional de dicho aceptor de péptidos está flanqueado por una región que hibrida con dicha molécula de ARN por un lado y por dicho aceptor de péptidos por el otro lado.
20. El procedimiento de la reivindicación 13, en el que dicho grupo funcional de aceptor de péptidos se selecciona entre el grupo que consiste en una amina, hidrazina, (tio) hidrazida y (tio) semicarbazona.
21. El procedimiento de la reivindicación 1, en el que dicha etapa de ligación química comprende:
(a) unir un grupo funcional a dicha molécula de ARN mediante aminación reductora;
(b) modificar un aceptor de péptidos para que reaccione con dicho grupo funcional de dicha molécula de ARN; y
(c) poner en contacto dicho aceptor de péptidos con dicha molécula de ARN en condiciones que permiten la formación de enlaces covalentes.
22. El procedimiento de la reivindicación 21, en el que dicho grupo funcional es un tiol, una maleimida o una amina.
23. El procedimiento de la reivindicación 1 o 22, en el que dicha molécula de ARN comprende una secuencia de inicio de la traducción y un codón de iniciación unido operativamente a una secuencia codificante de proteína.
24. El procedimiento de la reivindicación 1 o 22, en el que dicho aceptor de péptidos es puromicina.
25. El procedimiento de la reivindicación 1 o 22, en el que dicho aceptor de péptidos está unido covalentemente a una molécula de engarce no nucleotídica.
26. El procedimiento de la reivindicación 3, en el que dicho engarce comprende espaciadores de trietilenglicol.
27. El procedimiento de la reivindicación 3, en el que dicho engarce comprende 2'-OMe-ARN fosforamiditas.
28. El procedimiento de la reivindicación 1, 3 o 22, en el que dicho ARN o dicho engarce contienen una secuencia de purificación de afinidad y dicho procedimiento comprende además purificar dicho ARN.
29. El procedimiento de la reivindicación 28, en el que dicha secuencia de purificación de afinidad comprende una secuencia de poli (A) .
30. Una molécula de ARN entrecruzada con un aceptor de péptidos a través de un resto de psoraleno.
31. La molécula de ARN de la reivindicación 30, en la que dicho ARN contiene un codón de terminación colocado en su sitio diana de fotoentrecruzamiento.
32. La molécula de ARN de la reivindicación 30, en la que dicho aceptor de péptidos está ligado al extremo 3' de dicha molécula de ARN.
33. La molécula de ARN de la reivindicación 30, en la que dicha molécula de ARN comprende una secuencia de inicio de la traducción y un codón de iniciación unido operativamente a una secuencia codificante de proteína.
34. La molécula de ARN de la reivindicación 30, en la que dicho aceptor de péptidos es puromicina.
35. La molécula de ARN de la reivindicación 30, en la que dicho resto de psoraleno está unido a dicho aceptor de péptidos a través de un engarce.
36. Un procedimiento para generar una fusión de ARN-proteína, comprendiendo dicho procedimiento:
(a) proporcionar una molécula de ARN hibridada con un engarce, comprendiendo dicho engarce un resto fotoescindible, un resto de psoraleno y un aceptor de péptidos;
(b) inmovilizar dicho ARN en un soporte sólido en condiciones en las que el ARN no inmovilizado se retira sustancialmente del soporte;
(c) entrecruzar dicho aceptor de péptidos con dicho ARN, a través de dicho resto de psoraleno, con lo que dicho entrecruzamiento libera simultáneamente dicho ARN entrecruzado de dicho soporte sólido; y
(d) traducir el ARN entrecruzado formado en la etapa (c) para formar una proteína de fusión de ARN.
Patentes similares o relacionadas:
Polipéptidos de unión específica novedosos y usos de los mismos, del 15 de Julio de 2020, de Pieris Pharmaceuticals GmbH: Muteína de lipocalina lagrimal humana que tiene especificidad de unión para IL-17A, en la que la muteína se une a IL-17A con una KD de aproximadamente 1 nM o menos, en la que […]
Formulaciones liofilizadas para antídoto del factor Xa, del 1 de Julio de 2020, de PORTOLA PHARMACEUTICALS, INC.: Una formulación acuosa, que comprende de 10 mM a 55 mM de arginina, de 1% a 3% de sacarosa (p/v), de 2% a 8% de manitol (p/v), y al menos 5 mg/ml de un polipéptido […]
Péptidos de unión beta amiloide y sus usos para el tratamiento y el diagnóstico de la demencia de Alzheimer, del 17 de Junio de 2020, de Priavoid GmbH: Péptido que contiene al menos una secuencia de aminoácidos que se une a especies beta amiloides y en el que la carga negativa del grupo carboxilo presente […]
Arginina desiminasa con reactividad cruzada reducida hacia anticuerpos para ADI - PEG 20 para el tratamiento del cáncer, del 6 de Mayo de 2020, de TDW Group: Una composición terapéutica que comprende una arginina desiminasa (ADI) aislada y un vehículo farmacéuticamente aceptable, en donde la ADI aislada comprende la secuencia de […]
Composiciones y métodos utilizando andamios de lisofosfatidilcolina, del 6 de Mayo de 2020, de NATIONAL UNIVERSITY OF SINGAPORE: Un método para seleccionar uno o más compuestos o ácidos grasos para determinar el transporte mediado por lisofosfatidilcolina (LPC) del uno o más compuestos o ácidos […]
Péptidos antimicrobianos y composiciones de los mismos, del 29 de Abril de 2020, de REVANCE THERAPEUTICS, INC: Composición farmacéutica o cosmética que comprende un péptido, en donde dicho péptido consiste en la secuencia de aminoácidos SEQ ID NO: 3 correspondiente […]
COMPOSICIÓN PARA LA ESTIMULACIÓN DEL SISTEMA INMUNE EN PECES QUE CONTIENE PÉPTIDOS RECOMBINANTES, PÉPTIDOS RECOMBINANTES INMUNOESTIMULANTES Y SECUENCIAS NUCLEOTÍDICAS QUE LOS CODIFICAN, del 23 de Abril de 2020, de UNIVERSIDAD DE CONCEPCION: La presente invención se refiere a una composición, una micropartícula y una formulación alimenticia que comprende péptidos recombinantes que estimulan el sistema inmune […]
Nuevo péptido con cuatro epítopos CTL unidos, del 15 de Abril de 2020, de TAIHO PHARMACEUTICAL CO., LTD.: Un péptido que consiste en 4 epítopos unidos, en el que los 4 péptidos de epítopo se seleccionan del grupo que consiste en los péptidos de epítopo CTL: el péptido como […]