Análogos azetidina de inhibidores de nucleosidasa y fosforilasa.
Un compuesto de fórmula (I):
donde:
cada uno de W y X se selecciona independientemente entre hidrógeno,
CH2OH, CH2OQ y CH2SQ;
cada uno de Y y Z se selecciona independientemente entre hidrógeno, halógeno, CH2OH, CH2OQ, CH2SQ, SQ,OQ y Q;
Q es un grupo alquilo, aralquilo o arilo, pudiendo estar cada uno de los mismos opcionalmente sustituido con unoo más sustituyentes seleccionados entre hidroxi, halógeno, metoxi, amino o carboxi;
R1 es un radical de la fórmula (II)
o R1 es un radical de la fórmula (III)
A se selecciona entre N, CH y CR2, donde R2 se selecciona entre halógeno, alquilo, aralquilo, arilo, OH, NH2,NHR3, NR3R4 y SR5, donde cada R3, R4 y R5 es un grupo alquilo, aralquilo o arilo, opcionalmente sustituido conhidroxi o halógeno, y donde R2 está opcionalmente sustituido con hidroxi o halógeno cuando R2 es alquilo,aralquilo o arilo;
B se selecciona entre hidroxi, NH2, NHR6, SH, hidrógeno y halógeno, donde R6 es un grupo alquilo, aralquilo oarilo opcionalmente sustituido con hidroxi o halógeno;
D se selecciona entre hidroxi, NH2, NHR7, hidrógeno, halógeno y SCH3, donde R7 es un grupo alquilo, aralquilo oarilo opcionalmente sustituido con hidroxi o halógeno;
E se selecciona entre N y CH;
G es un grupo alquilo C1-4 saturado o insaturado opcionalmente sustituido con hidroxi o halógeno;
o un tautómero del mismo, o una sal farmacéuticamente aceptable del mismo, o un éster del mismo.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/NZ2007/000387.
Solicitante: INDUSTRIAL RESEARCH LIMITED.
Nacionalidad solicitante: Nueva Zelanda.
Dirección: GRACEFIELD RESEARCH CENTRE 69 GRACEFIELD ROAD LOWER HUTT NUEVA ZELANDA.
Inventor/es: FURNEAUX, RICHARD HUBERT, TYLER, PETER CHARLES, SCHRAMM, VERN, L., EVANS,GARY BRIAN, GREATREX,Ben William.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07D401/02 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 401/00 Compuestos heterocíclicos que contienen dos o más heterociclos, que tienen átomos de nitrógeno como únicos heteroátomos del ciclo, siendo al menos un ciclo de seis miembros con solamente un átomo de nitrógeno. › que contienen dos heterociclos.
- C07D401/04 C07D 401/00 […] › directamente unidos por un enlace entre dos miembros cíclicos.
- C07D401/06 C07D 401/00 […] › unidos por una cadena de carbono que contiene solamente átomos de carbono alifáticos.
- C07D403/14 C07D […] › C07D 403/00 Compuestos heterocíclicos que contienen dos o más heterociclos, que tienen átomos de nitrógeno como únicos heteroátomos del ciclo, no previstos por el grupo C07D 401/00. › que contiene tres o más heterociclos.
- C07D405/14 C07D […] › C07D 405/00 Compuestos heterocíclicos que contienen a la vez uno o más heterociclos que tienen átomos de oxígeno como únicos heteroátomos del ciclo y uno o más heterociclos que tienen átomos de nitrógeno como único heteroátomo del ciclo. › que contienen tres o más heterociclos.
PDF original: ES-2385759_T3.pdf
Fragmento de la descripción:
Análogos azetidina de inhibidores de nucleosidasa y fosforilasa
5 Campo de la técnica
La presente invención se refiere a determinados análogos azetidina de inhibidores de nucleosidasa y nucleósido fosforilasa, al uso de estos compuestos como productos farmacéuticos, a composiciones farmacéuticas que contienen los compuestos, a compuestos para el tratamiento de determinadas enfermedades, a procesos para preparar los compuestos y a productos intermedios útiles en la preparación de los compuestos
Antecedentes
Recientes investigaciones en el área de inhibidores de purina nucleósido fosforilasa (PNP) , metiltioadenosin fosforilasa (MTAP) , 5’-metiltioadenosin nucleosidasa (MTAN) y nucleósido hidrolasa han dado como resultado el diseño de una clase de compuestos conocidos como Inmucilinas, algunas de las cuales son fuertes inhibidores de una o más de las enzimas anteriores. Las Inmucilinas son análogos de nucleósidos donde la parte “azúcar” de la molécula se ha sustituido con un resto “imino azúcar”.
La PNP cataliza la escisión fosforolítica de los ribo- y desoxirrbonucleósidos de guanina e hipoxantina para dar el correspondiente azúcar-1-fosfato y guanina, hipoxantina u otras bases de purina.
Los seres humanos con déficit de PNP padecen una inmunodeficiencia específica de células T debido a una acumulación de dGTP que impide la estimulación de linfocitos T. Por lo tanto los inhibidores de PNP son inmunosupresores y son activos contra tumores malignos de células T y trastornos proliferativos de células T.
Los documentos US 5.985.848, US 6.066.722 y US 6.228.741 describen compuestos conocidos como Inmucilinas que son inhibidores de PNP y de purina fosforibosiltransferasas (PPRT) . Estas Inmucilinas son útiles para el tratamiento de infecciones parasitarias, tumores malignos de células T, enfermedades autoinmunes y trastornos inflamatorios. También son útiles para inmunosupresión en transplante de órganos.
Los documentos US 6.693.193 y US 7.022.852 describen un proceso para preparar determinados compuestos de Inmucilina, proporcionando otra vía útil para la síntesis de esta clase de compuestos. El documento US 7.109.331 describe otras Inmucilinas que son inhibidores de PNP y PPRT.
La parte imino azúcar de una molécula de Inmucilina tiene el átomo de nitrógeno localizado entre el C-1 y el C-4 para formar un compuesto 1, 4-didesoxi-1, 4-imino-D-ribitol. La localización del átomo de nitrógeno en el anillo ribitol puede ser importante para la unión a enzimas. Además, la localización de la unión entre el resto imino azúcar y el análogo base nucleósido puede ser crítica para la actividad inhibidora enzimática. Los compuestos descritos anteriormente tienen esta unión en el C-1 del anillo imino azúcar.
Se ha desarrollado otra clase relacionada de compuestos inhibidores de nucleósido fosforilasa y nucleosidasa, conocidas como DAD-Me-Inmucilinas. La localización del átomo de nitrógeno en el anillo imino azúcar de esta clase de compuestos varía y/o el resto imino azúcar está unido al análogo base nucleósido mediante un 45 puente metileno. En el documento US 10/524.995 se describen DAD-Me-Inmucilinas.
También se han identificado algunas de las Inmucilinas como fuertes inhibidores de MTAP y MTAN. Estas son el objeto del documento US 10/395.636. La MTAP y la MTAN funcionan en la ruta de biosíntesis de poliaminas, en la recuperación de purina en mamíferos y en las rutas de percepción de quórum en bacterias. La MTAP cataliza la fosforolisis reversible de la MTA a adenina y a 5-metiltio-!-D-ribosa-1-fosfato (MTR-1P) . La MTAN cataliza la hidrólisis reversible de la MTA a adenina y 5-metiltio-!-D-ribosa, y la hidrólisis reversible de S-adenosil-Lhomocisteína (SAH) a adenina y S-ribosil-homocisteína (SRH) . La adenina formada se recicla posteriormente y se convierte en nucleótidos. La única fuente de adenina libre en la célula humana es el resultado de la acción de estas enzimas. La MTR-1P se convierte posteriormente en metionina mediante acciones enzimáticas sucesivas.
55 [0010] La MTA es un subproducto de la reacción que implica la transferencia de un grupo aminopropilo de la Sadenosilmetionina descarboxilada a putrescina durante la formación de espermidina. La reacción la cataliza la espermidina sintasa. Así mismo, la espermina sintasa cataliza la conversión de espermidina a espermina, con producción concomitante de MTA como un subproducto. La espermidina sintasa es muy sensible a la inhibición de productos por acumulación de MTA. Por lo tanto, la inhibición de MTAP o MTAN limita gravemente la biosíntesis de poliamina y la ruta de recuperación para adenina en las células.
La MTA también es el subproducto de la síntesis bacteriana de homoserina lactonas aciladas a partir de Sadenosilmetiltionina (SAM) y proteínas acil-acil transportadoras en la que la lactonización posterior produce la 65 liberación de MTA y la homoserina lactona acilada. La homoserina lactona acilada es una molécula de percepción de quórum bacteriana en bacterias que está implicada en la virulencia bacteriana contra tejidos humanos. La ruta de homoserina lactona sufrirá inhibición de retroalimentación por la acumulación de MTA.
La deficiencia de MTAP, debida a deleción genética, se ha descrito con muchos tumores malignos. Se sabe que la pérdida de función enzimática de la MTAP en estas células se debe a deleciones homocigotas en el cromosoma 9 del gen supresor tumoral p16/MTS1 y MTAP estrechamente unido. Como la ausencia de p16/MTS1 es probablemente responsable de tumores, la ausencia de actividad de MTAP es una consecuencia de la deleción genética y no es causante del cáncer. Sin embargo, la ausencia de MTAP altera el metabolismo de purina en estas células de manera que estas dependen principalmente de la ruta de novo para su aporte de purinas.
También se espera que los inhibidores de MTAP sean muy eficaces contra infecciones parasitarias, tales como malaria, que infectan glóbulos rojos (RBS, de las siglas Red Blood Cells en inglés) , porque dichas infecciones carecen de la ruta de novo para la biosíntesis de purina. Los parásitos protozoarios dependen completamente de las purinas producidas por la ruta de recuperación para su crecimiento y propagación. Los inhibidores de MTAP por lo tanto destruirán estos parásitos sin tener ningún efecto negativo sobre los RBC hospedadores, porque los RBS son células terminalmente diferenciadas y no sintetizan purinas, producen poliaminas o se multiplican.
Se ha observado que la MTA induce apóptosis en la división de células cancerosas, pero tienen el efecto opuesto, anti-apoptótico, sobre la división de células normales tales como hepatocitos (E. Ansorena et al., Hepatology, 2002, 35: 274-280) . La administración de MTA en circunstancias donde su degradación por MTAP está inhibida por un inhibidor de MTAP conducirá a mayores niveles de MTA en circulación y tejidos y por consiguiente a un efecto potenciado en el tratamiento del cáncer.
Por lo tanto, pueden usarse inhibidores de MTAP y MTAN en el tratamiento de enfermedades tales como cáncer, infecciones bacterianas o infecciones parasitarias protozoarias, donde es deseable inhibir MTAP o MTAN. Tales tratamientos se describen en los documentos US 10/395.636 y US 10/524.995.
Las Inmucilinas y las DAD-Me-Inmucilinas también son útiles como inhibidores de nucleósido hidrolasas. Estas enzimas catalizan la hidrólisis de nucleósidos. No se encuentran en mamíferos, pero se requieren para la recuperación de nucleósidos en algunos parásitos protozoarios. Algunos parásitos protozoarios usan nucleósido fosforilasas en lugar de, o además de, nucleósido hidrolasas para este propósito. Puede esperarse que inhibidores de nucleósido hidrolasas y fosforilasas interfieran con el metabolismo de los parásitos y por lo tanto se empleen útilmente contra parásitos protozoarios.
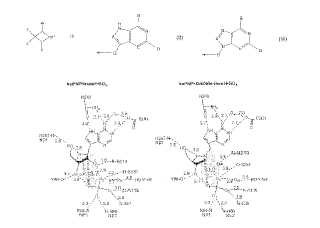
[0017] Se ha descrito la estructura cristalina de rayos X de uno de los compuestos inhibidores (DAD-MeInmucilina-H) unido a la PNP de Mycobacterium tuberculosis (A. Lewandowicz, W. Shi, G.B. Evans, P.C. Tyler, R.H. Furneaux, L.A. Basso, D.S. Santos, S.C. Almo y V.L. Schramm, Biochemistr y , 42 (2003) 6057-6066.) . El complejo de este inhibidor con PNP tiene enlaces de hidrógeno favorables con casi todos los sitios donante-aceptor de enlaces de hidrógeno en el complejo. Incluso un ligero cambio estructural puede interrumpir este patrón de unión de hidrógeno favorable, como se demuestra... [Seguir leyendo]
Reivindicaciones:
1. Un compuesto de fórmula (I) :
donde:
cada uno de W y X se selecciona independientemente entre hidrógeno, CH2OH, CH2OQ y CH2SQ; cada uno de Y y Z se selecciona independientemente entre hidrógeno, halógeno, CH2OH, CH2OQ, CH2SQ, SQ, OQ y Q; Q es un grupo alquilo, aralquilo o arilo, pudiendo estar cada uno de los mismos opcionalmente sustituido con uno o más sustituyentes seleccionados entre hidroxi, halógeno, metoxi, amino o carboxi; R1 es un radical de la fórmula (II)
o R1 es un radical de la fórmula (III)
A se selecciona entre N, CH y CR2, donde R2 se selecciona entre halógeno, alquilo, aralquilo, arilo, OH, NH2, NHR3, NR3R4 y SR5, donde cada R3, R4 y R5 es un grupo alquilo, aralquilo o arilo, opcionalmente sustituido con hidroxi o halógeno, y donde R2 está opcionalmente sustituido con hidroxi o halógeno cuando R2 es alquilo, aralquilo o arilo; B se selecciona entre hidroxi, NH2, NHR6, SH, hidrógeno y halógeno, donde R6 es un grupo alquilo, aralquilo o arilo opcionalmente sustituido con hidroxi o halógeno; D se selecciona entre hidroxi, NH2, NHR7, hidrógeno, halógeno y SCH3, donde R7 es un grupo alquilo, aralquilo o arilo opcionalmente sustituido con hidroxi o halógeno; E se selecciona entre N y CH; G es un grupo alquilo C1-4 saturado o insaturado opcionalmente sustituido con hidroxi o halógeno;
o un tautómero del mismo, o una sal farmacéuticamente aceptable del mismo, o un éster del mismo.
2. Un compuesto de acuerdo con la reivindicación 1, donde W es CH2OH o CH2SQ.
3. Un compuesto de acuerdo con la reivindicación 2, donde X es CH2OH o CH2SQ.
4. Un compuesto de acuerdo con cualquiera de las reivindicaciones 1 a 3, donde Z se selecciona entre hidrógeno, halógeno, CH2OH, CH2OQ y CH2SQ.
5. Un compuesto de acuerdo con la reivindicación 4, donde Y o Z es CH2OH, CH2SQ o CH2OQ.
6. Un compuesto de acuerdo con la reivindicación 4, donde Y, Z o los dos son Q o CH2OH.
7. Un compuesto de acuerdo con la reivindicación 1, donde W y X son los dos hidrógeno.
8. Un compuesto de acuerdo con la reivindicación 7, donde Y, Z o los dos son CH2OH o CH2SQ. 15
9. Un compuesto de acuerdo con la reivindicación 1, donde Y y Z son los dos hidrógeno o donde Y, Z o los dos son CH2OH.
10. Un compuesto de acuerdo con cualquiera de las reivindicaciones 1 a 9, donde G es CH2.
11. Un compuesto de acuerdo con cualquiera de las reivindicaciones anteriores, donde R1 es un radical de la fórmula (II) .
12. Un compuesto de acuerdo con cualquiera de las reivindicaciones 1 a 11, donde E es N y B es hidroxi o NH2. 25
13. Un compuesto de acuerdo con cualquiera de las reivindicaciones 1 a 12, donde E es N y A es CH o N.
14. Un compuesto de acuerdo con cualquiera de las reivindicaciones 1 a 13, donde E es N y D es H o NH2.
15. Un compuesto de acuerdo con cualquiera de las reivindicaciones 1 a 14, donde, cuando cualquiera de Y, Z, B y D es halógeno, cada halógeno es independientemente cloro o flúor.
16. Un compuesto de acuerdo con la reivindicación 1 que es:
i. meso-7- ( (2, 4-cis-2, 4-bis (hidroximetil) azetidin-1-il) metil) -3H-pirroIo[3, 2-d]pirimidin-4 (5H) -ona;
ii. (±) 7- ( (2, 4-trans-2, 4-bis (hidroximetil) azetidin-1-il) metil) -3H-pirroIo[3, 2-d]pirimidin-4 (5H) -ona;
iii. (+) 7- ( (2, 4-trans-2, 4-bis (hidroximetil) azetidin-1-il) metil) -3H-pirroIo[3, 2-d]pirimidin-4 (5H) -ona;
iv. (-) 7- ( (2, 4-trans-2, 4-bis (hidroximetil) azetidin-1-il) metil) -3H-pirroIo[3, 2-d]pirimidin-4 (5H) -ona;
v. 7- ( (3, 3-bis (hidroximetil) azetidin-1-il) metil) -3H-pirroIo[3, 2-d]pirimidin-4 (5H) -ona;
vi. (±) 7- ( (2- (hidroximetil) azetidin-1-il) metil) -3H-pirroIo[3, 2-d]pirimidin-4 (5H) -ona;
vii. 7- ( ( (2R) -2- (hidroximetil) azetidin-1-il) metil) -3H-pirroIo[3, 2-d]pirimidin-4 (5H) -ona;
viii. 7- ( ( (2S) -2- (hidroximetil) azetidin-1-il) metil) -3H-pirroIo[3, 2-d]pirimidin-4 (5H) -ona;
ix. 7- ( (3- (hidroximetil) azetidin-1-il) metil) -3H-pirroIo[3, 2-d]pirimidin-4 (5H) -ona;
x. 7- ( (3-hidroxi-3- (hidroximetil) azetidin-1-il) metil) -3H-pirroIo[3, 2-d]pirimidin-4 (5H) -ona; 45 xi. (±) 7- ( (2, 3-cis-3-hidroxi-2- (hidroximetil) azetidin-1-il) metil) -3H-pirroIo[3, 2-d]pirimidin-4 (5H) -ona;
xii. (+) 7- ( (2, 3-cis-3-hidroxi-2- (hidroximetil) azetidin-1-il) metil) -3H-pirroIo[3, 2-d]pirimidin-4 (5H) -ona;
xiii. (-) 7- ( (2, 3-cis-3-hidroxi-2- (hidroximetil) azetidin-1-il) metil) -3H-pirroIo[3, 2-djpirimidin-4 (5H) -ona;
xiv. (±) 7- ( (2, 3-trans-3-hidroxi-2- (hidroximetil) azetidin-1-il) metil) -3H-pirroIo[3, 2-d]pirimidin-4 (5H) -ona;
xv. (+) 7- ( (2, 3-trans-3-hidroxi-2- (hidroximetil) azetidin-1-il) metil) -3H-pirroIo[3, 2-d]pirimidin-4 (5H) -ona;
xvi. (-) 7- ( (2, 3-trans-3-hidroxi-2- (hidroximetil) azetidin-1-il) metil) -3H-pirroIo[3, 2-d]pirimidin-4 (5H) -ona;
xvii. meso-2-amino-7- ( (2, 4-cis-2, 4-bis (hidroximetil) azetidin-1-il) metil) -3H-pirroIo[3, 2-d]pirimidin-4 (5H) -ona;
xviii. (±) 2-amino-7- ( (2, 4-trans-2, 4-bis (hidroximetil) azetidin-1-il) metil) -3H-pirroIo[3, 2-d]pirimidin-4 (5H) -ona;
xix. (+) 2-amino-7- ( (2, 4-trans-2, 4-bis (hidroximetil) azetidin-1-il) metil) -3H-pirroIo[3, 2-d]pirimidin-4 (5H) -ona;
xx. (-) 2-amino-7- ( (2, 4-trans-2, 4-bis (hidroximetil) azetidin-I-il) metil) -3H-pirroIo[3, 2-d]pirimidin-4 (5H) -ona; 55 xxi. 2-amino-7- ( (3, 3-bis (hidroximetil) azetidin-1-il) metil) -3H-pirroIo[3, 2-d]pirimidin-4 (5H) -ona;
xxii. (±) 2-amino-7- ( (2- (hidroximetil) azetidin-1-il) metil) -3H-pirroIo[3, 2-d]pirimidin-4 (5H) -ona;
xxiii. 2-amino-7- ( ( (2R) -2- (hidroximetil) azetidin-1-il) metil) -3H-pirroIo[3, 2-d]pirimidin-4 (5H) -ona;
xxiv. 2-amino-7- ( ( (2S) -2- (hidroximetil) azetidin-1-il) metil) -3H-pirroIo[3, 2-d]pirimidin-4 (5H) -ona;
xxv. 2-amino-7- ( (3- (hidroximetil) azetidin-1-il) metil) -3H-pirroIo[3, 2-d]pirimidin-4 (5H) -ona;
xxvi. 2-amino-7- ( (3-hidroxi-3- (hidroximetil) azetidin-1-il) metil) -3H-pirroIo[3, 2-d]pirimidin-4 (5H) -ona;
xxvii. (±) 2-amino-7- ( (2, 3-trans-3-hidroxi-2- (hidroximetil) azetidin-1-il) metil) -3H-pirroIo[3, 2-d]pirimidin-4 (5H) -ona;
xxviii. (-) 2-amino-7- ( (2, 3-trans-3-hidroxi-2- (hidroximetil) azetidin-1-il) metil) -3H-pirroIo[3, 2-d]pirimidin-4 (5H) -ona;
xxix. (+) 2-amino-7- ( (2, 3-trans-3-hidroxi-2- (hidroximetil) azetidin-1-il) metil) -3H-pirroIo[3, 2-d]pirimidin-4 (5H) -ona;
xxx. (±) 2-amino-7- ( (2, 3-cis-3-hidroxi-2- (hidroximetil) azetidin-1-il) metil) -3H-pirroIo[3, 2-d]pirimidin-4 (5H) -ona; 65 xxxi. (+) 2-amino-7- ( (2, 3-cis-3-hidroxi-2- (hidroximetil) azetidin-1-il) metil) -3H-pirroIo[3, 2-d]pirimidin-4 (5H) -ona;
xxxii. (-) 2-amino-7- ( (2, 3-cis-3-hidroxi-2- (hidroximetil) azetidin-1-il) metil) -3H-pirroIo[3, 2-d]pirimidin-4 (5H) -ona;
xxxiii. (1- ( (4-amino-5H-pirroIo[3, 2-d]pirimidin-7-il) metil) -3- (metiltiometil) azetidin-3-il) metanoI;
xxxiv. 1- ( (4-amino-5H-pirroIo[3, 2-d]pirimidin-7-il) metil) -3- (metiltiometil) azetidin-3-oI;
xxxv. (±) - (2, 4-trans-1- ( (4-amino-5H-pirroIo[3, 2-d]pirimidin-7-il) metil) -4- (metiltiometil) azetidin-2-il) metanol; 5 xxxvi. (+) - (2, 4-trans-1- ( (4-amino-5H-pirrolo[3, 2-d]pirimidin-7-il) metil) -4- (metiltiometil) azetidin-2-il) metanol;
xxxvii. (-) - (2, 4-trans-1- ( (4-amino-5H-pirrolo[3, 2-d]pirimidin-7-il) metil) -4- (metiltiometil) azetidin-2-il) metanol;
xxxviii. meso- (2, 4-cis-1- ( (4-amino-5H-pirrolo[3, 2-d]pirimidin-7-il) metil) -4- (metiltiometil) azetidin-2-il) metanol;
xxxix. 7- ( ( (2RS) -2- (metiltiometil) azetidin-1-il) metil) -5H-pirrolo[3, 2-d]pirimidin-4-amina;
xl. 7- ( ( (2R) -2- (metiltiometil) azetidin-1-il) metil) -5H-pirrolo[3, 2-d]pirimidin-4-amina; 10 xli. 7- ( ( (2S) -2- (metiltiometil) azetidin-1-il) metil) -5H-pirrolo[3, 2-d]pirimidin-4-amina;
xlii. 7- ( (3- (metiltiometil) azetidin-1-il) metil) -5H-pirrolo[3, 2-d]pirimidin-4-amina; y xliii. (±) 2, 3-trans-1- ( (4-amino-5H-pirrolo[3, 2-d]pirimidin-7-il) metil) -2- (metiltiometil) azetidin-3-ol.
xliv. (+) 2, 3-trans-1- ( (4-amino-5H-pirrolo[3, 2-d]pirimidin-7-il) metil) -2- (metiltiometil) azetidin-3-ol.
xlv. (-) 2, 3-trans-1- ( (4-amino-5H-pirrolo[3, 2-d]pirimidin-7-il) metil) -2- (metiltiometil) azetidin-3-ol. 15 xlvi. (±) 2, 3-cis-1- ( (4-amino-5H-pirrolo[3, 2-d]pirimidin-7-il) metil) -2- (metiltiometil) azetidin-3-ol.
xlvii. (+) 2, 3-cis-1- ( (4-amino-5H-pirrol) o[3, 2-d]pirimidin-7-il) metil) -2- (metiltiometil) azetidin-3-ol.
xlviii. (-) 2, 3-cis-1- ( (4-amino-5H-pirrolo[3, 2-d]pirimidin-7-il) metil) -2- (metiltiometil) azetidin-3-ol.
17. Una composición farmacéutica que comprende un compuesto de cualquiera de las reivindicaciones 1 a 16 y un 20 excipiente, diluyente o portador farmacéuticamente efectivo.
18. Un compuesto de cualquiera de las reivindicaciones 1 a 16 para su uso como medicamento.
19. Un compuesto de cualquiera de las reivindicaciones 1 a 16 para tratar, prevenir o reducir el riesgo de una 25 enfermedad o afección en la que es deseable inhibir PNP, MTAP o MTAN.
20. El uso de un compuesto de cualquiera de las reivindicaciones 1 a 16 en la fabricación de un medicamento para tratar, prevenir o reducir el riesgo de una enfermedad o afección en la que es deseable inhibir PNP, MTAP o MTAN.
21. El compuesto o el uso, como se reivindica en la reivindicación 19 o en la reivindicación 20, donde la enfermedad o afección es cáncer, infección bacteriana, infección parasitaria o una enfermedad mediada por células T.
REFERENCIAS CITADAS EN LA DESCRIPCIÓN
Esta lista de referencias citadas por el solicitante es únicamente para la comodidad del lector. No forma parte del documento de la patente europea. A pesar del cuidado tenido en la recopilación de las referencias, no se pueden 5 excluir errores u omisiones y la EPO niega toda responsabilidad en este sentido.
Documentos de patentes citados en la descripción
Literatura diferente de patentes citadas en la descripción
Patentes similares o relacionadas:
Derivados de piperidina 1,4 sustituidos, del 29 de Julio de 2020, de 89Bio Ltd: Un compuesto de acuerdo con la Fórmula I: **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en donde: A se selecciona de […]
Compuestos y procedimientos de uso, del 29 de Julio de 2020, de Medivation Technologies LLC: Un compuesto de fórmula (Aa-1): **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en la que: A representa H, halógeno, amino, […]
Ureas asimétricas p-sustituidas y usos médicos de las mismas, del 22 de Julio de 2020, de Helsinn Healthcare SA: Un compuesto de Fórmula I: **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en donde: una línea discontinua indica un enlace opcional; X es CH; […]
Derivados de bencimidazol como inhibidores Nav 1.7 (subunidad alfa del canal de sodio, dependiente del voltaje, tipo IX (SCN9A)) para tratar el dolor, la disuria y la esclerosis múltiple, del 22 de Julio de 2020, de Sumitomo Dainippon Pharma Co., Ltd: Un compuesto de fórmula (I): **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, donde R1a, R1b, R1c, y R1d son independientemente hidrógeno, […]
N-acil-N''-(piridin-2-il) ureas y análogos que presentan actividades anticancerosas y antiproliferativas, del 24 de Junio de 2020, de Deciphera Pharmaceuticals, LLC: Un compuesto de fórmula I, **(Ver fórmula)** o una sal, un enantiómero, un estereoisómero o un tautómero farmacéuticamente aceptables del mismo, en donde […]
Derivados de lactama, urea cíclica y carbamato y de triazolona como inhibidores potentes y selectivos de ROCK, del 24 de Junio de 2020, de BRISTOL-MYERS SQUIBB COMPANY: Un compuesto de Fórmula (I): **(Ver fórmula)** o un estereoisómero, un tautómero, una sal farmacéuticamente aceptable del mismo, en donde: […]
Nuevos derivados de dihidroisoquinolin-1-ona bicíclicos, del 17 de Junio de 2020, de F. HOFFMANN-LA ROCHE AG: Un compuesto seleccionado de 6-cloro-2-piridin-3-il-3,4-dihidro-2H-isoquinolin-1-ona; 5-(6-cloro-1-oxo-3,4-dihidro-1H-isoquinolin-2-il)-nicotinonitrilo; […]
Compuestos de diaminopirimidilo sustituidos, composiciones de los mismos y procedimientos de tratamiento con ellos, del 17 de Junio de 2020, de SIGNAL PHARMACEUTICALS LLC: Un compuesto de fórmula (I): **(Ver fórmula)** o una sal, un tautómero, un isotopólogo o un estereoisómero farmacéuticamente aceptable […]