PROTEÍNA FRPB MUTANTE Y PROCEDIMIENTO DE REPLEGAMIENTO.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2003/009634.
Solicitante: GLAXOSMITHKLINE BIOLOGICALS S.A.
UTRECHT UNIVERSITY
TECHNOLOGY FOUNDATION (STICHTING VOOR DE TECHNISCHE WETENSCHAPPEN).
Nacionalidad solicitante: Bélgica.
Dirección: RUE DE L'INSTITUT 89 1330 RIXENSART BELGICA.
Inventor/es: DENOEL, PHILIPPE, POOLMAN, JAN, FERON,CHRISTIANE, WEYNANTS,VINCENT, BIEMANS,RALPH, TOMMASSEN,JAN, GORAJ,CARINE, KORTEKAAS,JEROEN.
Fecha de Publicación: .
Fecha Solicitud PCT: 28 de Agosto de 2003.
Fecha Concesión Europea: 22 de Septiembre de 2010.
Clasificación Internacional de Patentes:
- A61K39/095 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 39/00 Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53). › Neisseria.
- A61K39/102 A61K 39/00 […] › Pasteurella; Haemophilus.
- A61K39/104M
- C07K14/22 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › de Neisseriaceae (F), p. ej. Acinetobacter.
Clasificación PCT:
- A61K39/095 A61K 39/00 […] › Neisseria.
- C07K14/22 C07K 14/00 […] › de Neisseriaceae (F), p. ej. Acinetobacter.
- C07K16/12 C07K […] › C07K 16/00 Inmunoglobulinas, p. ej. anticuerpos mono o policlonales. › contra materiales bacterianos.
- G01N33/48 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › Material biológico, p. ej. sangre, orina (G01N 33/02, G01N 33/26, G01N 33/44, G01N 33/46 tienen prioridad ); Hemocitómetros (cómputo de glóbulos repartidos sobre una superficie por barrido óptico de la superficie G06M 11/02).
Clasificación antigua:
- C07K14/00 C07K […] › Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia, Ex República Yugoslava de Macedonia, Albania.
Fragmento de la descripción:
Campo de la invención
La presente invención se refiere a mutantes de FrpB -una proteína de membrana externa de organismos de Neisseria meningitidis, a un procedimiento de replegamiento de proteínas FrpB, a tales proteínas replegadas, a composiciones farmacéuticas que comprenden proteínas FrpB y a su uso en el tratamiento, la prevención y el diagnóstico de infecciones bacterianas tales como infecciones por Neisseria y particularmente, pero no exclusivamente, a Neisseria meningitidis y/o Neisseria gonorrhoeae. Antecedentes de la invención
Las cepas de Neisseria de bacterias son los agentes causales de varias patologías humanas contra las que existe la necesidad de desarrollar vacunas eficaces. En particular, Neisseria gonorrhoeae y Neisseria meningitidis producen patologías que podrían tratarse mediante vacunación.
La Neisseria gonorrhoeae es el agente etiológico de la gonorrea, una de las enfermedades de transmisión sexual más frecuentemente informadas en el mundo con una incidencia anual estimada de 62 millones de casos (Gerbase y col. 1998 Lancet 351; (Suppl 3) 2-4). Las manifestaciones clínicas de la gonorrea incluyen inflamación de las membranas mucosas del tracto urogenital, garganta o recto e infecciones oculares neonatales. Las infecciones gonocócicas ascendentes en mujeres pueden conducir a infertilidad, embarazo ectópico, enfermedad inflamatoria pélvica crónica y a la formación de abscesos tubo-ováricos. La septicemia, artritis, endocarditis y meningitis están asociadas a gonorrea complicada.
El alto número de cepas gonocócicas con resistencia a antibióticos contribuye a un aumento de la morbilidad y a complicaciones asociadas a gonorrea. Una alternativa atractiva al tratamiento de gonorrea con antibióticos sería su prevención usando vacunación. Actualmente no existe vacuna para infecciones por N. gonorrhoeae.
La Neisseria meningitidis (meningococo) es una bacteria Gram-negativa aislada frecuentemente del tracto respiratorio superior humano. Ocasionalmente produce enfermedades bacterianas invasivas tales como bacteremia y meningitis. La mayoría de los casos de enfermedad son en bebés o niños pequeños. La incidencia de la enfermedad meningocócica muestra diferencias estacionales y anuales geográficas (Schwartz, B., Moore, P.S., Broome, C.V.; Clin. Microbiol. Rev. 2 (suplemento), pág. 18-S24, 1989). La mayor parte de la enfermedad en países templados es debida a cepas del serogrupo B y varía en incidencia de 1-10/100.000/año de población total, alcanzando algunas veces valores mayores (Kaczmarski, E.B. (1997), Commun. Dis. Rep. Rev. 7: R55-9, 1995; Scholten, R.J.P.M., Bijlmer, H.A., Poolman, J.T. y col. Clin. Infect. Dis. 16: 237-246, 1993; Cruz, C., Pavez, G.,
Aguilar, E., y col. Epidemiol. Infect. 105: 119-126, 1990).
Las epidemias dominadas por los meningococos del serogrupo A, la mayoría en África central, se encuentran algunas veces alcanzando niveles de hasta 1000/100.000/año (Schwartz, B., Moore, P.S., Broome, C.V. Clin. Microbiol. Rev. 2 (suplemento), pág. 18-S24, 1989). Casi todos los casos de manera global de enfermedad meningocócica son producidos por los meningococos del serogrupo A, B, C, W-135 y Y y está disponible una vacuna de polisacárido A, C, W-135, Y tetravalente (Armand, J., Arminjon, F., Mynard, M.C., Lafaix, C., J. Biol. Stand. 10: 335-339, 1982).
La frecuencia de infecciones por Neisseria meningitidis ha aumentado espectacularmente en las últimas décadas. Esto se ha atribuido a la aparición de cepas multirresistentes a antibióticos y a un aumento de la población de personas con sistemas inmunitarios debilitados. Ya no es raro aislar cepas de Neisseria meningitidis que son resistentes a algunos o todos los antibióticos convencionales. Este fenómeno ha creado una necesidad médica sin resolver y demanda nuevos agentes antimicrobianos, vacunas, procedimientos de cribado de fármacos y pruebas de diagnóstico para este organismo.
Van der Ley y col. (1996) Microbiology 142:3269-3274 informan que actualmente no hay ninguna vacuna disponible contra organismos del grupo B, que son la causa predominante de enfermedad meningocócica. El uso del polisacárido capsular del grupo B como vacuna se ha dificultado por la presencia de estructuras idénticas sobre moléculas de adhesión a células neurales en el huésped humano, aumentando la posibilidad de inducir patología autoinmunitaria con una vacuna tal. Se ha propuesto usar vacunas basándose en proteínas de membrana externa meningocócicas. Sin embargo, se ha encontrado que una gran proporción de los anticuerpos protectores inducidos son específicos de cepa. Además, no todos los componentes de la membrana externa contribuyen a la inducción de anticuerpos bactericidas. La proteína FrpB de Neisseria es una proteína de membrana externa regulada por hierro que muestra las características de un receptor de la membrana externa dependiente de TonB. Tiene un peso molecular de aproximadamente 77kDa; aunque éste puede variar entre cepas. Se ha pensado que la proteína FrpB puede ser un buen candidato para la producción de anticuerpos bactericidas. Sin embargo, Ala'Aldeen y col. (1994) Vaccine 12:535 encontraron que se encontró que los anticuerpos monoclonales (mAb) aislados contra la FrpB natural eran específicos de cepa.
También se ha previsto que la FrpB recombinante expresada en células podría producirse para uso en tales nuevos agentes antimicrobianos, vacunas, procedimientos de cribado de fármacos y pruebas de diagnóstico. Sin embargo, una de las mayores limitaciones a la expresión de proteínas es la incapacidad de muchas proteínas recombinantes de plegarse en sus conformaciones biológicamente activas. Frecuentemente sólo se obtienen bajos rendimientos de la proteína recombinante debido a la agregación y el plegamiento inadecuado de las especies sin plegar. De hecho, el replegamiento de proteínas, en el que la proteína adquiere su estructura nativa y activa, es uno de los mayores retos en la biología molecular. El replegamiento de PorA de N. meningitidis se trata en Jansen y col. 2000 Biochimica et Biophysica Acta. Biomembranes, Ámsterdam, NL, vol. 1464, nº 2, página 284-298.
Claramente, por tanto, queda la necesidad de proporcionar una vacuna contra enfermedad por Neisseria que comprende proteínas de membrana externa protectoras purificadas que incluyen proteínas mutantes en una conformación replegada adecuada para provocar una respuesta inmunitaria eficaz, preferentemente una respuesta protectora cruzada. Resumen de la invención
La presente invención proporciona proteínas FrpB mutantes de deleción de bucles que pueden inducir anticuerpos bactericidas de amplio espectro.
La presente invención también proporciona un procedimiento para el replegamiento de la proteína FrpB.
La presente invención también se refiere a tales proteínas FrpB replegadas.
La presente invención también proporciona procedimientos para usar las proteínas de la presente invención que incluyen su uso en la prevención y el tratamiento de enfermedades microbianas, entre otras, en, por ejemplo, vacunas de subunidades y de vesículas de membrana externa. En otro aspecto, la invención se refiere a ensayos de diagnóstico para detectar enfermedades asociadas a infecciones microbianas y afecciones asociadas a tales infecciones. Exposiciones de la invención
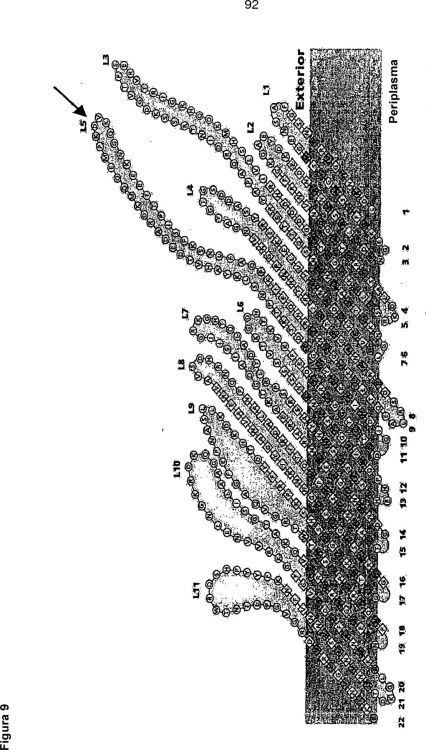
Según un aspecto de la presente invención se proporciona una proteína FrpB de Neisseria que tiene una o más deleciones de aminoácidos no conservados del bucle 7 y el bucle 5, según la numeración de bucles de la Figura 6, en comparación con una proteína FrpB de Neisseria natural correspondiente. Estas proteínas de la presente invención se denominan generalmente proteínas "mutantes". El término "deleción" como se usa en este documento incluye la sustitución, reemplazo o mutación de uno o más de los aminoácidos no conservados. La secuencia sustituida puede o puede no tener el mismo tamaño que la secuencia que reemplaza. Por aminoácidos "no conservados" los inventores incluyen aminoácidos presentes en una proteína FrpB natural de una primera cepa, pero que pueden no estar presentes en una proteína FrpB natural de una segunda cepa. Las proteínas de la presente invención son proteínas aisladas. Por "aisladas" los inventores incluyen proteínas que han sido sacadas de su estado natural o sometidas de otro modo a intervención humana. Preferentemente, la proteína también se ha purificado hasta un nivel superior al...
Reivindicaciones:
1. Una proteína FrpB de Neisseria que tiene una o más deleciones de aminoácidos no conservados del bucle 7 y el bucle 5 según la numeración de bucles de la Figura 6 en comparación con una proteína FrpB natural correspondiente de Neisseria.
2. La proteína según la reivindicación 1 que es de protección cruzada.
3. La proteína según cualquiera reivindicación precedente en la que se han delecionado uno o más aminoácidos de uno cualquiera o más de bucles 1, 2, 3, 4, 6, 8, 9, 10, 11, 12 y 13.
4. La proteína según cualquiera reivindicación precedente en la que se han delecionado 11 a 33 aminoácidos del bucle 7.
5. La proteína según cualquiera reivindicación precedente en la que se han delecionado 23-33 aminoácidos del bucle 7.
6. La proteína según cualquiera reivindicación precedente en la que se han delecionado 28 aminoácidos del bucle 7.
7. La proteína según cualquiera reivindicación precedente en la que se han delecionado 18-29 aminoácidos del bucle 5.
8. La proteína según cualquiera reivindicación precedente en la que se han delecionado 19-29 aminoácidos del bucle 5.
9. La proteína según cualquiera reivindicación precedente en la que se han delecionado 24 aminoácidos del bucle 5.
10. La proteína según cualquiera reivindicación precedente en la que, con referencia a la cepa de FrpB H44/76, la deleción de aminoácidos se hace en el intervalo de los aminoácidos 376-413, o se hace una deleción correspondiente, del bucle 7.
11. La proteína según cualquiera reivindicación precedente en la que, con referencia a la cepa de FrpB H44/76, la deleción de aminoácidos se hace en el intervalo de los aminoácidos 381-408, o se hace una deleción correspondiente, del bucle 7.
12. La proteína según cualquiera reivindicación precedente en la que, con referencia a la cepa de FrpB H44/76, se deleciona una secuencia de aminoácidos que comprende TTEEKNGQKVDKPMEQQMKDRADEDTVH, o se hace una deleción correspondiente, del bucle 7.
13. La proteína según cualquiera reivindicación precedente en la que, con referencia a la cepa de FrpB H44/76, la deleción de aminoácidos se hace en el intervalo de los aminoácidos 247-280, o se hace una deleción correspondiente, del bucle 5.
14. La proteína según cualquiera reivindicación precedente en la que, con referencia a la cepa de FrpB H44/76, la deleción de aminoácidos se hace en el intervalo de los aminoácidos 252-275, o se hace una deleción correspondiente, del bucle 5.
15. La proteína según cualquiera reivindicación precedente en la que, con referencia a la cepa de FrpB H44/76, se deleciona una secuencia de aminoácidos que comprende QHRGIRTVREEFTVGDKSSRINID, o se hace una deleción correspondiente, del bucle 5.
16. La proteína de cualquier reivindicación precedente en la que la secuencia delecionada es sustituida por otra secuencia de aminoácidos.
17. La proteína de la reivindicación 16 en que la secuencia se deleciona por mutagénesis.
18. Un polinucleótido que codifica la proteína de cualquier reivindicación precedente.
19. Un vector de expresión que comprende el polinucleótido de la reivindicación 18
20. Una célula huésped que comprende el vector de expresión de la reivindicación 19.
21. Un procedimiento para producir la proteína de una cualquiera de las reivindicaciones 1
a 17 que comprende: cultivar la célula huésped de la reivindicación 20 y recuperar la proteína expresada.
22. Un procedimiento para replegar una proteína FrpB que comprende poner en contacto la proteína FrpB con un tampón de replegamiento alcalino que comprende propanosulfonato de 3-dimetildodecilamonio (Zwittergent 3-12 o SB-12), en el que la proteína es una proteína según
una cualquiera de las reivindicaciones 1 a 17.
23. Un procedimiento según la reivindicación 22, en el que el tampón de replegamiento comprende etanolamina y SB-12.
24. Un procedimiento según la reivindicación 23, en el que la etanolamina es etanolamina 20 mM.
25. Un procedimiento según una cualquiera de las reivindicaciones 22 a 24, en el que el tampón de replegamiento tiene pH 11.
26. Un procedimiento según una cualquiera de las reivindicaciones 22 a 25, en el que el SB-12 es SB-12 al 0,2%.
27. Un procedimiento según una cualquiera de las reivindicaciones 22 a 25, en el que el SB-12 es SB-12 al 0,5%.
28. Un procedimiento según una cualquiera de las reivindicaciones 22 a 27, en el que el tampón de replegamiento comprende además cloruro de guanidinio, NaCl y/o urea.
29. Un procedimiento según la reivindicación 28, en el que el tampón de replegamiento comprende además cloruro de guanidinio.
30. Un procedimiento según la reivindicación 29, en el que el tampón de replegamiento comprende además cloruro de guanidinio 0,4 M.
31. Un procedimiento de una cualquiera de las reivindicaciones 22 a 30 que comprende las siguientes etapas:
a. expresar una proteína FrpB en una célula huésped; romper la célula huésped para obtener un cuerpo de inclusión que comprende la proteína FrpB; lavar el cuerpo de inclusión;
b. solubilizar al menos parte del cuerpo de inclusión y la proteína FrpB con clorhidrato de guanidinio;
c. poner en contacto la proteína FrpB solubilizada con el tampón de replegamiento; y
d. eliminar o cambiar el tampón de replegamiento de la proteína FrpB.
32. Un tampón de replegamiento que comprende etanolamina, SB-12 y cloruro de guanidinio para uso en el procedimiento de una cualquiera de las reivindicaciones 22 a 31.
33. Una proteína FrpB replegada aislada de las reivindicaciones 1-17 obtenida o que puede obtenerse mediante el procedimiento de una cualquiera de las reivindicaciones 22 a 31.
34. Una composición farmacéutica que comprende al menos una proteína FrpB de una cualquiera de las reivindicaciones 1 a 17 y 33, y un vehículo farmacéuticamente aceptable.
35. Una composición farmacéutica según la reivindicación 34, en el que al menos el 30%, 50%, 70% o el 90% de la proteína FrpB presente en la composición está replegada.
36. Una composición farmacéutica según la reivindicación 34 ó 35 en forma de una vacuna.
37. La composición farmacéutica de una cualquiera de las reivindicaciones 34 a 36 que comprende una proteína FrpB derivada de Neisseria meningitidis.
38. La composición farmacéutica de una cualquiera de las reivindicaciones 34 a 37 que comprende una proteína FrpB derivada de Neisseria gonorrhoeae.
39. La composición farmacéutica según una cualquiera de las reivindicaciones 34 a 38, en la que dicha composición comprende al menos otro antígeno de Neisseria.
40. La composición farmacéutica de la reivindicación 39 que comprende al menos otro antígeno de Neisseria derivado de Neisseria gonorrhoeae.
41. La composición farmacéutica de la reivindicación 39 ó 40 que comprende al menos otro antígeno de Neisseria derivado de Neisseria meningitidis.
42. La composición farmacéutica de una cualquiera de las reivindicaciones 34 a 41 en forma de una composición de subunidades.
43. La composición farmacéutica de una cualquiera de las reivindicaciones 34 a 41 en forma de una preparación de vesículas de membrana externa, o una subunidad más la preparación de vesículas de membrana externa mezcladas.
44. Una composición farmacéutica según una cualquiera de las reivindicaciones 34 a 43 que comprende además al menos otro antígeno de Neisseria seleccionado de una o más de las siguientes clases:
a. al menos una adhesina de Neisseria seleccionada del grupo que está constituido por FhaB, NspA, Hsf, NadA, PilC, Hap, MafA, MafB, Omp26, NMB0315, NMB0995 y NMB1119;
b. al menos un autotransportador de Neisseria seleccionado del grupo que está constituido por Hsf, Hap, proteasa de IgA, AspA y NadA;
c. al menos una toxina de Neisseria seleccionada del grupo que está constituido por FrpA, FrpC, FrpA/C, VapD, NM-ADPRT y uno cualquiera o ambos de inmunotipo L2 de LPS e inmunotipo L3 de LPS;
d. al menos una proteína de adquisición de Fe de Neisseria seleccionada del grupo que está constituido por TbpA alto, TbpA bajo, TbpB alto, TbpB bajo, LbpA, LbpB, P2086, HpuA, HpuB, Lipo28, Sibp, FbpA, BfrA, BfrB, Bcp, NMB0964 y NMB0293; y
e. al menos una proteína asociada a la membrana de Neisseria, preferentemente proteína de membrana externa, seleccionada del grupo que está constituido por PldA, NspA, TspA, FhaC, NspA, TbpA (alto), TbpA (bajo), LbpA, HpuB, TdfH, PorB, HimD, HisD, GNA1870, OstA, HlpA, mltA, NMB 1124, NMB 1162, NMB 1220, NMB 1313, NMB 1953, HtrA, TspB, PilQ y OMP85.
45. La composición farmacéutica de una cualquiera de las reivindicaciones 34 a 44 que comprende además uno o más polisacáridos u oligosacáridos capsulares bacterianos.
46. La composición farmacéutica de la reivindicación 45, en la que el uno o más polisacáridos u oligosacáridos capsulares se derivan de bacterias seleccionadas del grupo que está constituido por serogrupo A, C, Y y/o W-135 de Neisseria meningitidis, Haemophilus influenzae b, Streptococcus pneumoniae, estreptococos del grupo A, estreptococos del grupo B, Staphylococcus aureus y Staphylococcus epidermidis, y están conjugadas con una fuente de epítopes de células T auxiliares.
47. Uso de una proteína FrpB de una cualquiera de las reivindicaciones 1 a 17 y 33 (o una composición farmacéutica de las reivindicaciones 34 a 46) en la preparación de un medicamento para el tratamiento o la prevención de infección por Neisseria.
48. El uso de la reivindicación 47 en el que se previene o se trata infección por Neisseria
49. El uso de las reivindicaciones 47 ó 48 en el que se previene o se trata infección por Neisseria gonorrhoeae.
50. Un anticuerpo inmunoespecífico para la proteína FrpB según una cualquiera de las reivindicaciones 1 a 17 y 33.
51. Una composición farmacéutica útil en el tratamiento de seres humanos con una enfermedad por Neisseria que comprende al menos un anticuerpo según la reivindicación 50 y un vehículo farmacéutico adecuado.
52. Uso del anticuerpo de la reivindicación 50 (o una composición de la reivindicación 51) en la preparación de un medicamento para el tratamiento o la prevención de enfermedad por Neisseria.
53. El uso de la reivindicación 52 en el que se previene o se trata infección por Neisseria meningitidis.
54. El uso de la reivindicación 52 ó 53 en el que se previene o se trata infección por Neisseria gonorrhoeae.
55. Un procedimiento de diagnóstico de una infección por Neisseria que comprende las etapas de identificar una proteína FrpB, o un anticuerpo para la misma, dentro de una muestra biológica de un animal que se sospecha tiene una infección tal usando una proteína FrpB según una cualquiera de las reivindicaciones 1 a 17 y 33, o un anticuerpo según la reivindicación 50.
56. El procedimiento de la reivindicación 55 en el que se diagnostica infección por Neisseria meningitidis.
57. El procedimiento de la reivindicación 55 ó 56 en el que se diagnostica infección por Neisseria gonorrhoeae.
Patentes similares o relacionadas:
Vacuna de ADN contra pseudotuberculosis en peces marinos, del 1 de Julio de 2020, de NATIONAL UNIVERSITY CORPORATION TOKYO UNIVERSITY OF MARINE SCIENCE AND TECHNOLOGY: Una vacuna de ADN para peces, caracterizada por: - impartir inmunidad contra la pseudotuberculosis causada por Photobacterium damselae subsp. piscicida - que comprende, […]
Proteína de fusión de Haemophilus influenzae y método de construcción y uso de la misma, del 12 de Febrero de 2020, de Cansino Biologics Inc: Proteína de fusión de Haemophilus influenzae Hin47-Ligador-HiD, en la que la secuencia de aminoácidos de Hin47 es la secuencia mostrada en SEQ ID NO.1, y la secuencia […]
Vacuna para proteger a un rumiante contra la neumonía causada por Mannheimia haemolytica, del 11 de Diciembre de 2019, de INTERVET INTERNATIONAL B.V: Vacuna para su uso en un método para proteger a un rumiante contra la neumonía causada por la bacteria Mannheimia haemolytica, comprendiendo la vacuna […]
Composiciones y métodos para mejorar la inmunogenicidad de los conjugados de polisacárido-proteína, del 23 de Octubre de 2019, de Kanvax Biopharmaceuticals Ltd: Un conjugado de polisacárido-proteína que comprende una proteína transportadora quimérica y un antígeno polisacárido, en donde la proteína […]
Composiciones y métodos para la retirada de biopelículas, del 14 de Agosto de 2019, de UNIVERSITY OF SOUTHERN CALIFORNIA: Un agente interferente que inhibe, compite o valora la unión de una proteína o polipéptido DNABII a un ADN microbiano para su uso en un método de inhibición, prevención […]
Composición de vacuna que comprende polisacáridos capsulares naturales conjugados de N. Meningitidis, del 24 de Julio de 2019, de GLAXOSMITHKLINE BIOLOGICALS SA: Una composición inmunogénica que comprende polisacáridos capsulares de N. meningitidis de los serogrupos A, C, W135 e Y, en donde cada polisacárido […]
Composición inmunógena, del 24 de Julio de 2019, de GLAXOSMITHKLINE BIOLOGICALS S.A.: Una composición inmunógena que comprende sacárido capsular del serogrupo A de N. meningitidis (MenA), sacárido capsular del serogrupo C de […]
Composición inmunogénica, del 12 de Junio de 2019, de GLAXOSMITHKLINE BIOLOGICALS S.A.: Una composición inmunogénica que no usa ningún adyuvante de sal de aluminio o no usa ningún adyuvante, comprendiendo la composición polisacáridos capsulares […]