POLIPÉPTIDOS Y RUTAS BIOSINTÉTICAS.
Procedimiento de producción de monatina, que comprende convertir el triptófano y/o el ácido indol-3láctico en monatina,
en el que el procedimiento comprende: (a) poner en contacto el triptófano o el ácido indol-3-láctico con un primer polipéptido, en el que, cuando el triptófano está en contacto con el primer polipéptido, el primer polipéptido se selecciona de entre triptófano aminotransferasa (CE 2.6.1.27), triptófano deshidrogenasa (CE 1.4.1.19), tirosina aminotransferasa (aromática) (CE 2.6.1.5), triptofan-fenilpiruvato transaminasa (CE 2.6.1.28), sustrato múltiple aminotransferasa (CE 2.6.1.-), aspartato aminotransferasa (CE 2.6.1.1), triptófano oxidasa, L-aminoácido oxidasa (CE 1.4.3.2), D-aminoácido deshidrogenasa (CE 1.4.99.1), D-aminoácido oxidasa (CE 1.4.3.3), D- triptófano aminotransferasa, D-alanina aminotransferasa (CE 2.6.1.21), glutamato deshidrogenasa (CE 1.4.1.2-4), fenilalanina deshidrogenasa (CE 1.4.1.20), o una combinación de las mismas, en el que, cuando el ácido indol-3-láctico se pone en contacto con el primer polipéptido, el primer polipéptido se selecciona de entre indol-lactato deshidrogenasa (CE 1.1.1.110), R-4 hidroxifenil-lactato deshidrogenasa (CE 1.1.1.222), 3-(4)-hidroxifenilpiruvato reductasa (CE 1.1.1.237), lactato deshidrogenasa (CE 1.1.1.27, 1.1.1.28, 1.1.2.3), (3-imidazol-5-il) lactato deshidrogenasa (CE 1.1.1.111), y lactato oxidasa (CE 1.1.3.-), o una combinación de las mismas, en el que el primer polipéptido convierte el triptófano o el ácido indol-3láctico en indol-3-piruvato; (b) poner en contacto el indol-3-piruvato con un segundo polipéptido y una fuente de carbono C3, en el que el segundo polipéptido es una enzima CE 4.1.2 o CE 4.1.3., en el que el segundo polipéptido convierte el indol-3-piruvato y la fuente de carbono C3 en 2-hidroxiácido 2-(indol-3-ilmetil)-4-cetoglutárico; y (c) poner en contacto el 2-hidroxiácido 2-(indol-3-ilmetil)-4-cetoglutárico con un tercer polipéptido, en el que el tercer polipéptido se selecciona de entre tirosina aminotransferasa (aromática) (CE 2.6.1.5), triptófano deshidrogenasa (CE 1.4.1.19), triptófano-fenilpiruvato transaminasa (CE 2.6.1.28), triptófano aminotransferasa (CE 2.6.1.27), aspartato aminotransferasa (CE 2.6.1.1), D-alanina aminotransferasa (CE 2.6.1.21), D-triptófano aminotransferasa, glutamato deshidrogenasa (CE 1.4.1.2-4), fenilalanina deshidrogenasa (CE 1.4.1.20), sustrato múltiple aminotransferasa (CE 2.6.1.-), D-aminoácido deshidrogenasa (CE 1.4.99.1), una lisina épsilon aminotransferasa, o una combinación de las mismas, en el que el tercer polipéptido convierte el 2-hidroxiácido 2-(indol-3ilmetil)-4-cetoglutárico en monatina
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2003/012588.
Solicitante: CARGILL INCORPORATED.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: P.O. BOX 5624 MINNEAPOLIS, MN 55440-5624 ESTADOS UNIDOS DE AMERICA.
Inventor/es: HICKS,PAULA,M, ABRAHAM,TIMOTHY W, CAMERON,DOUGLAS C, MCFARLAN,SARA C, ROSAZZA,JOHN, ZHAO,LISHAN, WEINER,DAVID P, DALLUGE,Joseph, HOBSON,Russell,J, MILLIS,Jim.
Fecha de Publicación: .
Fecha Solicitud PCT: 23 de Abril de 2003.
Clasificación Internacional de Patentes:
- C12N9/10F
- C12P17/10 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12P PROCESOS DE FERMENTACION O PROCESOS QUE UTILIZAN ENZIMAS PARA LA SINTESIS DE UN COMPUESTO QUIMICO DADO O DE UNA COMPOSICION DADA, O PARA LA SEPARACION DE ISOMEROS OPTICOS A PARTIR DE UNA MEZCLA RACEMICA. › C12P 17/00 Preparación de compuestos heterocíclicos que contienen O, N, S, Se o Te como únicos heteroátomos del ciclo (C12P 13/04 - C12P 13/24 tienen prioridad). › nitrógeno como único heteroátomo del ciclo.
Clasificación PCT:
- C12P17/10 C12P 17/00 […] › nitrógeno como único heteroátomo del ciclo.
Clasificación antigua:
- C07D209/18 C […] › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 209/00 Compuestos heterocíclicos que contienen ciclos de cinco miembros, condensados con otros ciclos, con solamente un átomo de nitrógeno como heteroátomo. › Radicales sustituidos por átomos de carbono que tienen tres enlaces a heteroátomos con a lo sumo un enlace a halógeno, p.ej. radicales éster o nitrilo.
- C12P17/10 C12P 17/00 […] › nitrógeno como único heteroátomo del ciclo.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia, Ex República Yugoslava de Macedonia, Albania.
PDF original: ES-2356132_T3.pdf


Fragmento de la descripción:
CAMPO DE LA INVENCIÓN
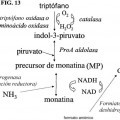
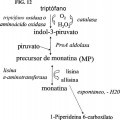
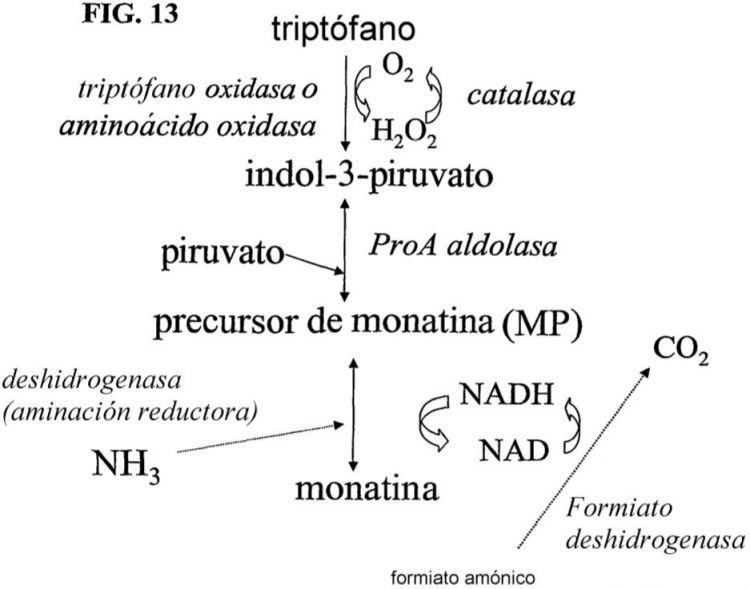
La presente invención proporciona polipéptidos y rutas biosintéticas que son útiles en la producción de 5 indol-3-piruvato, 2-hidroxiácido 2-(indol-3-ilmetil)-4-cetoglutárico (PM) y/o monatina.
ANTECEDENTES
Indol piruvato 10
El indol-3-piruvato es un potente antioxidante que se cree que contrarresta el estrés oxidativo en tejidos con altas concentraciones de oxígeno (Politi et al., "Recent advances in Tryptophan Research", editado por G. A. Filippini et al., Plenum Press, Nueva York, 1996, págs. 291-8). El indol piruvato además es un compuesto intermedio en una serie de reacciones para producir ácido indol-acético (IAA), la hormona auxina del crecimiento 15 vegetal primario (factor activador de crecimiento difusible). El IAA es activo en cantidades inferiores al microgramo en una gama de procesos fisiológicos que incluyen la dominancia apical, tropismos, alargamiento del brote, inducción de la división de las células del cambium e iniciación de la raíz. Las auxinas sintéticas se utilizan en horticultura para provocar enraizamiento y para favorecer el cuajado y el desarrollo del fruto. A altas concentraciones las auxinas sintéticas son herbicidas eficaces contra las plantas de hoja ancha. Las auxinas 20 naturales producidas por fermentación pueden considerarse más adecuadas desde un punto de vista ambiental que los herbicidas producidos químicamente. Los reguladores del crecimiento se vendieron en todo el mundo en 1999 por valor de 0,4 miles de millones de libras (1,4 miles de millones de dólares US).
Algunos ejemplos de patentes sobre el ácido indolacético y de derivados del mismo incluyen: la patente US 25 nº 5.843.782 Micropropagation of rose plants, auxina utilizada en el medio de cultivo y la patente US nº 5.952.231 Micropropagation of rose plants.
Además de las utilidades relacionadas con las plantas, el ácido indolacético es útil en aplicaciones farmacéuticas, por ejemplo, la patente US nº 5.173.497 "Method of preparing alpha-oxopyrrolo[2,3-B]indole acetic 30 acids and derivatives” propone la utilización de estos compuestos en el tratamiento del deterioro de la memoria tal como el asociado a la enfermedad de Alzheimer y a la demencia senil. El mecanismo propuesto en la patente US nº 5.173.497 es que estos compuestos inhiben la polipéptido acetilcolinestarasa y aumentan las concentraciones de acetilcolina en el cerebro.
35
El indol-3-carbinol se produce a partir del indol-3-acético por oxidación catalizada por peroxidasa, y puede convertirse fácilmente en diindolilmetano. Se informa de que ambos compuestos eliminan toxinas y favorecen la producción de hormonas beneficiosas para la salud de las mujeres.
Derivados de triptófano 40
El D-triptófano clorado se ha identificado como un edulcorante no nutritivo, y existe un interés creciente en dedicarse también a otros derivados. La monatina es un edulcorante natural que es similar en composición al aminoácido triptófano. Puede extraerse de la corteza de las raíces del arbusto sudafricano, Sclerochiton ilicifolius, y es prometedor en la industria alimenticia y de bebidas como edulcorante de gran intensidad. Algunos ejemplos de 45 patentes sobre monatina incluyen: la patente US nº 5.994.559 Synthesis of monatin-A high intensity natural sweetener, la patente US nº 5.975.298 3-(1-amino-1,3-dicarboxy-3-hydroxy-but-4-yl)-indole compouds, la patente US nº 5.128.164 Composition for human consumption containing 3-(1-amino-1,3-dicarboxy-3-hydroxy-but-4-yl)-indole compounds; y la patente US nº 5.128.482 Process for the production of 3-1(1-amino-1,3-dicarboxy-3-hydroxy-but-4-yl) indole. 50
Algunos de los precursores de monatina descritos en la presente memoria pueden ser también útiles como edulcorantes sintéticos o como productos intermedios en la síntesis de derivados de monatina.
Anteriormente, fueron descritos procedimientos para producir monatina (Nakamura et al., Organic Letters, 55 2, 19: 2967-2970, 2000). Además, una cepa de E. coli que sobreexpresa un gen para aldolasa (Patil et al., J. Bacteriol., 171, 1: 1402-107, 1992), se han descrito células de E. coli que expresan aminoácido deshidrogenasas o aminoácido transferasas heterólogas (Galkin et al., Applied and Environmental Microbiology, 63, 12:4651-4656, 1997) y las células de levadura que expresan glutamato deshidrogenasas (Deluna et al., J. Biol. Chem., 274, 47:43775-43783, 2001). Además, la patente EP 1 445 323 describe la producción biosíntética de monatina a partir 60 de triptófano con indol-3-piruvato y 2-hidroxiácido 2(indol-3-il-metil)-4-cetoglutárico como productos intermedios.
SUMARIO
La presente invención se refiere a las formas de realización caracterizadas en las reivindicaciones. Por lo 65 tanto se refiere a un procedimiento de producción de monatina, que comprende convertir el triptófano y/o el ácido
indol-3-láctico en monatina, en el que el procedimiento comprende:
(a) poner en contacto el triptófano o el ácido indol-3-láctico con un polipéptido, en el que, cuando el triptófano está en contacto con el primer polipéptido, el primer polipéptido se selecciona de entre triptófano aminotransferasa (CE 2.6.1.27), triptófano deshidrogenasa (CE 1.4.1.19), tirosina aminotransferasa 5 (aromática)(CE 2.6.1.5), triptofan-fenilpiruvato transaminasa (CE 2.6.1.28), sustrato múltiple aminotransferasa (CE 2.6.1. ), aspartato aminotransferasa (CE 2.6.1.1), triptófano oxidasa, L-aminoácido oxidasa (CE 1.4.3.2), D-amino-ácido deshidrogenasa (CE 1.4.99.1), D-aminoácido oxidasa (CE 1.4.3.3), D-triptófano aminotransferasa, D-alanina aminotransferasa (CE 2.6.1.21), glutamato deshidrogenasa (CE 1.4.1.2-4), fenilalanina deshidrogenasa (CE 1.4.1.20), o una combinación de las mismas, en la que, cuando 10 el ácido indol-3-láctico se pone en contacto con el primer polipéptido, el primer polipéptido se selecciona de entre indol-lactato deshidrogenasa (CE 1.1.1.110), R-4 hidroxifenil-lactato deshidrogenasa (CE 1.1.1.222), 3-(4)-hidroxifenilpiruvato reductasa (CE 1.1.1.237), lactato deshidrogenasa (CE 1.1.1.27, 1.1.1.28, 1.1.2.3),(3-imidazol-5-il) lactato deshidrogenasa (CE 1.1.1.111), y lactato oxidasa (CE 1.1.3. ), o una combinación de las mismas, en la que el primer polipéptido convierte el triptófano o el ácido indol-3-15 láctico en indol-3-piruvato;
(b) poner en contacto el indol-3-piruvato con un segundo polipéptido y una fuente de carbono C3, en el que el segundo polipéptido es una enzima CE 4.1.2 o CE 4.1.3., en la que el segundo polipéptido convierte el indol-3-piruvato y la fuente de carbono C3 en 2-hidroxiácido 2-(indol-3-ilmetil)-4-cetoglutárico; y 20
(c) poner en contacto el 2-hidroxiácido 2-(indol-3-ilmetil)-4-cetoglutárico con un tercer polipéptido, en el que el tercer polipéptido se selecciona de entre tirosina aminotransferasa (aromático) (CE 2.6.1.5), triptófano deshidrogenasa (CE 1.4.1.19), triptófano-fenilpiruvato transaminasa (CE 2.6.1.28), triptófano aminotransferasa (CE 2.6.1.27), aspartato aminotransferasa (CE 2.6.1.1), D-alanina aminotransferasa (CE 25 2.6.1.21), D-triptófano aminotransferasa, glutamato deshidrogenasa (CE 1.4.1.2-4), fenilalanina deshidrogenasa (CE 1.4.1.20), sustrato múltiple aminotransferasa (CE 2.6.1. ), D-aminoácido deshidrogenasa (CE 1.4.99.1), una lisina épsilon aminotransferasa, o una combinación de las mismas, en la que el tercer polipéptido convierte el 2-hidroxiácido 2-(indol-3ilmetil)-4-cetoglutárico en monatina.
30
La presente invención se refiere además, al procedimiento de producción de monatina, en el que, cuando el primer polipéptido que convierte triptófano en indol-3-piruvato es una aminoácido oxidasa (CE 1.4.3. ), se utiliza además una catalasa (CE 1.11.1.6).
La presente invención se refiere además, al procedimiento de producción de monatina, en el que, cuando 35 el primer polipéptido que convierte triptófano en indol-3-piruvato es una aminoácido oxidasa (CE 1.4.3. ), se utiliza además una catalasa (CE 1.11.1.6) en el que la aminoácido oxidasa es una triptófano oxidasa..
La presente... [Seguir leyendo]
Reivindicaciones:
1. Procedimiento de producción de monatina, que comprende convertir el triptófano y/o el ácido indol-3-láctico en monatina, en el que el procedimiento comprende:
(a) poner en contacto el triptófano o el ácido indol-3-láctico con un primer polipéptido, en el que, cuando el 5 triptófano está en contacto con el primer polipéptido, el primer polipéptido se selecciona de entre triptófano aminotransferasa (CE 2.6.1.27), triptófano deshidrogenasa (CE 1.4.1.19), tirosina aminotransferasa (aromática) (CE 2.6.1.5), triptofan-fenilpiruvato transaminasa (CE 2.6.1.28), sustrato múltiple aminotransferasa (CE 2.6.1. ), aspartato aminotransferasa (CE 2.6.1.1), triptófano oxidasa, L-aminoácido oxidasa (CE 1.4.3.2), D-aminoácido deshidrogenasa (CE 1.4.99.1), D-aminoácido oxidasa (CE 1.4.3.3), D-10 triptófano aminotransferasa, D-alanina aminotransferasa (CE 2.6.1.21), glutamato deshidrogenasa (CE 1.4.1.2-4), fenilalanina deshidrogenasa (CE 1.4.1.20), o una combinación de las mismas, en el que, cuando el ácido indol-3-láctico se pone en contacto con el primer polipéptido, el primer polipéptido se selecciona de entre indol-lactato deshidrogenasa (CE 1.1.1.110), R-4 hidroxifenil-lactato deshidrogenasa (CE 1.1.1.222), 3-(4)-hidroxifenilpiruvato reductasa (CE 1.1.1.237), lactato deshidrogenasa (CE 1.1.1.27, 15 1.1.1.28, 1.1.2.3), (3-imidazol-5-il) lactato deshidrogenasa (CE 1.1.1.111), y lactato oxidasa (CE 1.1.3. ), o una combinación de las mismas, en el que el primer polipéptido convierte el triptófano o el ácido indol-3-láctico en indol-3-piruvato;
(b) poner en contacto el indol-3-piruvato con un segundo polipéptido y una fuente de carbono C3, en el que el 20 segundo polipéptido es una enzima CE 4.1.2 o CE 4.1.3., en el que el segundo polipéptido convierte el indol-3-piruvato y la fuente de carbono C3 en 2-hidroxiácido 2-(indol-3-ilmetil)-4-cetoglutárico; y
(c) poner en contacto el 2-hidroxiácido 2-(indol-3-ilmetil)-4-cetoglutárico con un tercer polipéptido, en el que el tercer polipéptido se selecciona de entre tirosina aminotransferasa (aromática) (CE 2.6.1.5), triptófano 25 deshidrogenasa (CE 1.4.1.19), triptófano-fenilpiruvato transaminasa (CE 2.6.1.28), triptófano aminotransferasa (CE 2.6.1.27), aspartato aminotransferasa (CE 2.6.1.1), D-alanina aminotransferasa (CE 2.6.1.21), D-triptófano aminotransferasa, glutamato deshidrogenasa (CE 1.4.1.2-4), fenilalanina deshidrogenasa (CE 1.4.1.20), sustrato múltiple aminotransferasa (CE 2.6.1. ), D-aminoácido deshidrogenasa (CE 1.4.99.1), una lisina épsilon aminotransferasa, o una combinación de las mismas, en 30 el que el tercer polipéptido convierte el 2-hidroxiácido 2-(indol-3ilmetil)-4-cetoglutárico en monatina.
2. Procedimiento según la reivindicación 1, en el que, cuando el primer polipéptido que convierte el triptófano en indol-3-piruvato es una aminoácido oxidasa (CE 1.4.3. ), se utiliza además una catalasa (CE 1.11.1.6).
35
3. Procedimiento según la reivindicación 2, en el que la aminoácido oxidasa es una triptófano oxidasa.
4. Procedimiento según la reivindicación 1, en el que la enzima CE 4.1.3 es la 4-hidroxi-2-oxoglutarato glioxilato-liasa (CE 4.1.3.16), la 4-hidroxi-4-metil-2-oxoglutarato piruvato-liasa (CE 4.1.3.17) o una combinación de las mismas. 40
5. Procedimiento según la reivindicación 1, en el que el segundo polipéptido es una secuencia de aminoácidos seleccionada de entre el grupo constituido por:
(a) SEC. ID. nº 66, nº de registro en Genbank: CAC46344, nº de registro en Genbank: CAB 14127.1, nº de 45 registro en Genbank: AAC74920.1 o nº de registro en Genbank: CAC47463.1;
(b) una secuencia de aminoácidos que comprende por lo menos 90% de identidad de la secuencia con la SEC. ID. nº 66, nº de registro en Genbank: CAC46344, nº de registro en Genbank: CAB14127.1, nº de registro en Genbank: AAC74920.1 o nº de registro en Genbank: CAC47463.1; y 50
(c) secuencias de aminoácidos que se diferencian de la SEC. ID. nº 66, nº de registro en Genbank: CAC46344, nº de registro en Genbank: CAB 14127.1, nº de registro en Genbank: AAC74920.1 o nº de registro en Genbank: CAC47463.1 en menos de 50 sustituciones de aminoácidos conservadoras, en el que la secuencia de aminoácidos convierte el indol-3-piruvato y el piruvato en 2-hidroxiácido 2-(indol-3-ilmetil)-55 4-cetoglutárico.
6. Procedimiento según la reivindicación 1, en el que cuando el tercer polipéptido es una aspartato aminotransferasa, el 2-hidroxiácido 2-(indol-3-ilmetil)-4-cetoglutárico se pone en contacto con el aspartato para producir oxaloacetato y monatina. 60
7. Procedimiento según la reivindicación 6, que comprende además poner en contacto oxaloacetato con una descarboxilasa.
8. Procedimiento según la reivindicación 1, en el que cuando el tercer polipéptido es una lisina épsilon 65 aminotransferasa, el 2-hidroxiácido 2-(indol-3ilmetil)-cetoglutárico se pone en contacto además con la lisina.
9. Procedimiento según la reivindicación 1, en el que el primer y/o el tercer polipéptido son seleccionados de entre el grupo constituido por:
(a) una secuencia de aminoácidos represenada en las SEC. ID. nº: 2, 4, 6, 8, 10, 12, 14, 32, nº de registro en Genbank: NP_388848.1, nº de registro en Genbank: ZP00005082.1 o nº de registro en Genbank: 5 ACC74014.1;
(b) una secuencia de aminoácidos que comprende por lo menos 90% de identidad de secuencia con la secuencia representada en las SEC. ID. nº 2, 4, 6, 8, 10, 12, 14, 32, nº de registro en Genbank: NP_388848.1, nº de registro en Genbank: ZP00005082.1 o nº de registro en Genbank: ACC74014.1; y 10
(c) secuencias de aminoácidos que se diferencian de las SEC. ID. nº 2, 4, 6, 8, 10, 12, 14, 32, nº de registro en Genbank: NP_388848.1, nº de registro en Genbank: ZP00005082.1 o nº de registro en Genbank: ACC74014.1 en menos de 50 sustituciones de aminoácidos conservadoras, en el que la secuencia de aminoácidos convierte el triptófano en indol-3-piruvato. 15
10. Procedimiento según la reivindicación 1, en el que el triptófano es producido a partir de indol utilizando el polipéptido de CE 4.1.99.1.
11. Procedimiento según la reivindicación 1, en el que la fuente de carbono C3 se selecciona de entre 20 piruvato, fosfoenolpiruvato, alanina, serina, cisteína o una combinación de los mismos.
12. Procedimiento según la reivindicación 11, en el que el piruvato es producido por:
(a) la alanina y un polipéptido que puede realizar la transaminación de la alanina; 25
(b) la serina y un polipéptido que puede realizar la beta-eliminación de la serina;
(c) la cisteína y un polipéptido que puede realizar la beta-eliminación de la cisteína;
30
(d) el aspartato y un polipéptido que puede realizar las reacciones de beta-liasa con un aminoácido dicarboxílico;
(e) el lactato y la lactato-oxidasa (CE 1.1.3. ) o una lactato-deshidrogenasa (CE 1.1.1.27, 1.1.1.28, 1.1.1.2.3); o
35
(f) una combinación de los mismos.
13. Procedimiento según la reivindicación 1, en el que el procedimiento comprende además reducir una cantidad de peróxido de hidrógeno producido cuando el triptófano se convierte en indol-3-piruvato poniendo en contacto el peróxido de hidrógeno con una catalasa. 40
14. Procedimiento según la reivindicación 1, en el que se produce por lo menos 10 g/l de monatina.
15. Procedimiento según la reivindicación 1, en el que el procedimiento comprende además la detección del 2-hidroxiácido 2-(indol-3-ilmetil)-4-cetoglutárico por espectrometría de masas. 45
16. Procedimiento de producción de monatina, que comprende convertir el indol-3-piruvato en monatina en presencia de piruvato y un primer y un segundo polipéptidos, en el que el primer polipéptido es una aldolasa, y en el que el segundo polipéptido se selecciona de entre tirosina aminotransferasa (aromática) (CE 2.6.1.5), triptófano deshidrogenasa (CE 1.4.1.19), triptófano-fenilpiruvato transaminasa (CE 2.6.1.28), triptófano amino-50 transferasa (CE 2.6.1.27), aspartato aminotransferasa (CE 2.6.1.1), D-alanina aminotransferasa (CE 2.6.1.21), D-triptófano aminotransferasa, glutamato deshidrogenasa (CE 1.4.1.2-4), fenilalanina deshidrogenasa (CE 1.4.1.20), sustrato múltiple aminotransferasa (CE 2.6.1. ), D-aminoácido deshidrogenasa (CE 1.4.99.1) o una combinación de las mismas.
Patentes similares o relacionadas:
Procedimiento para la hidrólisis de material lignocelulósico, en el que el hidrolizado se usa para la producción de hidrolasa microbiana, del 6 de Mayo de 2020, de CLARIANT INTERNATIONAL LTD.: Un procedimiento para la hidrólisis enzimática autosuficiente de material que contiene lignocelulosa, que comprende las etapas de: (a) someter un material que contiene lignocelulosa […]
Método para la síntesis de pentostatina, del 4 de Septiembre de 2019, de Synbias Pharma AG: Método para la síntesis estéreo-selectiva de pentostatina, que comprende: (i) hacer reaccionar 6,7-dihidroimidazo-[4,5-d]-[1,3]diazepin-8(3H)-ona […]
Microorganismos y métodos para la biosíntesis de adipato, hexametilendiamina y ácido 6-aminocaproico, del 17 de Julio de 2019, de Genomatica, Inc: Un organismo microbiano de origen no natural con una vía de hexametilendiamina que comprende al menos un ácido nucleico exógeno que codifica […]
Procesos químicos para preparar espiroindolonas y compuestos intermedios correspondientes, del 3 de Julio de 2019, de NOVARTIS AG: Un proceso para preparar un compuesto de fórmula (II) o una de sus sales o solvatos o hidratos,**Fórmula** que comprende transaminar enzimáticamente un compuesto de fórmula […]
Productores microbianos de ácido succínico novedosos y purificación del ácido succínico, del 7 de Junio de 2019, de BASF SE: Un procedimiento para la producción fermentativa de ácido succínico o una sal o derivado de este, procedimiento que comprende las etapas de: a. incubar […]
Microorganismo recombinante que produce ácido quinolínico y procedimiento de producción de ácido quinolínico mediante su uso, del 22 de Noviembre de 2017, de CJ CHEILJEDANG CORPORATION: Un microorganismo recombinante que produce ácido quinolínico, que expresa una proteína de fusión de Laspartato oxidasa y quinolinato sintasa unidas […]
Proceso para la preparación de aminopirrolidinas quirales ópticamente activas (3-AP, B3-AP), del 1 de Marzo de 2017, de LONZA AG: Un proceso para la preparación de una 3-aminopirrolidina (3-AP) quiral ópticamente activa o una N-1-boc-3- aminopirrolidina (B3-AP) quiral ópticamente activa que […]
Polipéptidos y rutas biosintéticas para la producción de estereoisómeros de monatina y sus precursores, del 25 de Mayo de 2016, de CARGILL INCORPORATED: Procedimiento para producir R,R-monatina o una sal de la misma, que comprende hacer reaccionar un precursor de la monatina y una o más D-aminotransferasas seleccionadas de […]