PÉPTIDOS INMUNOGÉNICOS Y MÉTODOS DE USO.
Un polipéptido aislado que comprende como mucho diez aminoácidos consecutivos de la secuencia de aminoácidos expuesta como MSARVRSRSRGRGDGX1X2APDVVAFVAPGESQQEEPPTDNQDIEPGQEREGTPPIEERKX3X4GDCQEMDX5EKTR SERGDGSDVKEX6X7PPNPKHX8KTKEAGDGQP (SEC ID Nº 1) y comprendiendo el polipéptido uno de (a) los aminoácidos 16 a 25 de la SEC ID Nº 1 donde el aminoácido 1 (X1) es una glutamina y el aminoácido 2 (X2) es una leucina;
(b) los aminoácidos 16 a 25 de la SEC ID Nº 1 donde el aminoácido 1 (X1) es una tirosina y el aminoácido 2 (X2) es una leucina; (c) los aminoácidos 59 a 68 de la SEC ID Nº 1 donde el aminoácido 1 (X3) es una valina y el aminoácido 2 (X4) es una leucina; (d) los aminoácidos 59 a 68 de la SEC ID Nº 1 donde el aminoácido 1 (X3) es una tirosina, el aminoácido 2 (X4) es una leucina, y el aminoácido 3 (X5) es una valina, o (e) los aminoácidos 84 a 92 de la SEC ID Nº 1 donde el aminoácido 1 (X6) es una tirosina, el aminoácido 2 (X7) es una leucina y el aminoácido 9 (X8) es una valina
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2007/004603.
Solicitante: THE GOVERNMENT OF THE UNITED STATES OF AMERICA AS REPRESENTED BY THE SECRETARY OF THE DEPARTMENT OF HEALTH AND HUMAN SERVICES.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: NATIONAL INSTITUTES OF HEALTH OFFICE OF TECHNOLOGY TRANSFER 60011 EXECUTIVE BOULEVARD SUITE 323 ROCKVILLE, MD 20852-3804 ESTADOS UNIDOS DE AMERICA.
Inventor/es: SCHLOM, JEFFREY, TSANG, KWONG-YOK, PASTAN, IRA, H..
Fecha de Publicación: .
Fecha Solicitud PCT: 21 de Febrero de 2007.
Clasificación Internacional de Patentes:
- C07K14/47A34
- C07K14/82 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › Productos de traducción de oncogenes.
Clasificación PCT:
- A61K38/17 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › que provienen de animales; que provienen de humanos.
- A61K39/00 A61K […] › Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53).
- C07K14/47 C07K 14/00 […] › de mamíferos.
- C12N15/12 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Genes que codifican proteínas animales.
- C12N15/86 C12N 15/00 […] › Vectores virales.
- G01N33/569 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › para microorganismos, p. ej. protozoarios, bacterias, virus.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia, Ex República Yugoslava de Macedonia, Albania.
PDF original: ES-2356574_T3.pdf




Fragmento de la descripción:
CAMPO
Esta solicitud se refiere al campo de agentes terapéuticos contra el cáncer, específicamente a péptidos inmunogénicos y su uso en el tratamiento de cáncer de próstata, cervical, uterino y testicular. 5
ANTECEDENTES
El cáncer de próstata es el cáncer más habitualmente diagnosticado en los hombres y es la segunda causa más común de muerte por cáncer (Carter y Coffey, Prostate 16:39-48, 1990; Armbruster et al., Clinical Chemistry 39:181, 1993). Si se detecta en una fase temprana, el cáncer de próstata es potencialmente curable. Sin embargo, la mayoría de los casos se diagnostican en fase tardías cuando ya ha sucedido la metástasis del tumor primario (Wang 10 et al., Meth. Cancer Res. 19:179, 1982). Incluso el diagnóstico temprano es problemático porque no todos los individuos que dan positivo en el positivo en estas exploraciones desarrollan cáncer.
El tratamiento actual para el cáncer de próstata incluye prostatectomía radical, radioterapia, o terapia hormonal. Con intervención quirúrgica, no siempre se consigue la erradicación completa del tumor y la re-aparición observada del cáncer (12-68%) depende de la fase del tumor clínico inicial (Zietman et al., Cancer 71:959, 1993). 15 Por tanto, son deseables métodos alternativos de tratamiento incluyendo profilaxis o prevención.
Los cánceres de próstata, testicular, y uterino, habitualmente se tratan, en parte, por la eliminación quirúrgica del órgano afectado. Hasta el 30% de los pacientes de los Estados Unidos con cáncer en fase temprana potencialmente curable, tal como cáncer de próstata, fallarán en cirugía convencional o radioterapia en 2004. Además, los pacientes con cáncer de próstata metastático disfrutan de un beneficio limitado de la quimioterapia 20 convencional y las terapias basadas en hormonas. Las metástasis, sin embargo, pueden no ser susceptibles a eliminación quirúrgica, o pueden ser demasiado pequeñas para detectarse fácilmente. La potenciación de la respuesta inmune del paciente contra el cáncer; y particularmente la potenciación de la respuesta de linfocitos T citotóxicos ("CTL") contra el cáncer, pueden ayudar en la ralentización o detención del progreso de la enfermedad.
La inmunoterapia puede tener gran potencial para mejorar estos resultados, combinado la especificidad de 25 tumor de la inmunidad mediada por células con la libertada de las quimioterapias tóxicas.
La inmunoterapia implica provocar una respuesta inmune contra las células cancerosas en base a su producción de antígeno diana. La inmunoterapia basada en respuestas inmunes mediadas por células implica generar una respuesta inmune mediada por células contra células que producen determinantes antigénicos particulares, mientras que la inmunoterapia basada en respuestas inmunes humorales implica generar anticuerpos 30 específicos contra células que producen determinantes antigénicos particulares.
Estudios recientes muestran que la inmunoterapia de pacientes con cáncer puede mejorarse drásticamente por el hallazgo de que las CTL CD8+ reconocen y eliminan las células tumorales que presentan péptidos de antígenos asociados con tumores dentro de las moléculas MHC de clase I. En estudios clínicos se ha descubierto que las células T CD8+ efectoras desempeñan una tarea principal en la regresión tumoral. Se han identificado varios 35 antígenos tumorales en modelos de cáncer de próstata y se han identificado los péptidos específicos de alelo HLA a partir de esos antígenos asociados con cáncer de próstata como epítopos de células T CD8+. Por ejemplo, se describieron péptidos de unión a HLA-A2.1 que se obtuvieron del antígeno específico de próstata (PSA) (Correale et al., J Immunol 161:3186, 1998), el antígeno de membrana específico de próstata (PSMA) (Tjoa et al., Prostate 28:65, 1996), el antígeno de células madre prostáticas (PSCA) (Kiessling et al., Int J Cancer 102:390, 2002), y la fosfatasa 40 ácida de próstata (Peshwa et al., Prostate 36:129, 1998). Para PSA, están en progreso ensayos clínicos que usan diferentes estrategias de vacuna. Sin embargo, hay claramente una necesidad de identificar antígenos adicionales para ayudar en el diagnóstico de un cáncer de un órgano reproductor, y para su uso como agentes terapéuticos adicionales.
El documento WO 00/12706 describe PAGE-4 y usos 45
SUMARIO
La invención se define en las reivindicaciones.
El gen PAGE4 se expresa en tejidos reproductores, y se expresa en cánceres reproductores, tales como cáncer de próstata, cáncer uterino, cáncer cervical y cáncer testicular. En este documento se describen polipéptidos PAGE4 inmunogénicos. Estos polipéptidos pueden usarse en ensayos de diagnóstico para la expresión de PAGE4, 50 así como para inducir una respuesta inmune contra PAGE4.En este documento se proporcionan polinucleótidos que codifican los polipéptidos PAGE4 inmunogénicos, vectores que incluyen estos polipéptidos, células hospedadoras transformadas con estos vectores, y métodos para usar estos polipéptidos, polinucleótidos, vectores, y células hospedadoras.
Se describen polipéptidos PAGE4 inmunogénicos, tales como un polipéptido aislado que incluye como 55 mucho diez aminoácidos consecutivos de la secuencia de aminoácidos expuesta como
MSARVRSRSRGRGDGX1X2APDVVAFVAPGESQQEEPPTDNQDIEPGQEREGTPPIEERKX3X4GDCQEMDX5EKTRSERGDGSDVKEX6X7PPNPKHX8KTKEAGDGQP (SEC ID Nº 1, PAGE4 CONSENSO QUE MUESTRA SUSTITUCIONES)
donde X1 es Q o Y, X2 es E o L, X3 es V o Y, X4 es E o L, X5 es V o L, X6 es K o Y, X7 es T o L, y X8 es A o 60
V. El polipéptido incluye uno de (a) los aminoácidos 16 a 25 de la SEC ID Nº 1, (b) los aminoácidos 59 a 68 de la SEC ID Nº 1, o (c) los aminoácidos 84 a 92 de la SEC ID Nº 1.
Se proporcionan moléculas de ácido nucleico aisladas que codifican los polipéptidos PAGE4 inmunogénicos, así como vectores de expresión que incluyen estos ácidos nucleicos. Estos vectores incluyen vectores virales, tales como, aunque sin limitación, vectores poxvirales. También se proporcionan células 5 hospedadoras transformadas con estos vectores. En una realización, se describe una composición que incluye un primer virus recombinante que ha incorporado en un genoma viral o parte infectable del mismo un ácido nucleico que codifica el polipéptido PAGE4 inmunogénico y un segundo virus recombinante que ha incorporado en un genoma viral o parte infectable del mismo uno o más genes o secuencias de ADN que codifican B7-1, B7-2, o B7-1 y B7-2, donde la composición es capaz de co-infectar una célula hospedadora provocando la co-expresión del 10 polipéptido y los genes o secuencias de ADN que codifican B7-1, B7-2, o B7-1 y B7-2.
También se proporcionan métodos para diagnostica un cáncer de expresión de PAGE4, tal como un cáncer reproductor, que incluyen el uso de los polipéptidos PAGE4 inmunogénicos descritos o los ácidos nucleicos que codifican estos polipéptidos. Los cánceres ejemplares incluyen cáncer de próstata, uterino, o testicular.
También se describen métodos para inducir una respuesta inmune contra PAGE4. Los métodos incluyen el 15 uso de los polipéptidos PAGE4 inmunogénicos descritos en este documento, los ácidos nucleicos que codifican estos polipéptidos, y/o vectores virales que codifican un polipéptido PAGE4 inmunogénico, solo o junto con otros agentes, tales como B7-1, B7-2, y/o una citoquina y/o con terapias tradicionales contra el cáncer, tales como cirugía, radioterapia y/o quimioterapia. También se describen métodos para tratar a un sujeto con un tumor, tal como cánceres reproductores, por ejemplo, cáncer de próstata, uterino, o testicular. 20
Las características y ventajas anteriores y otras llegarán a ser más evidentes a partir de la siguiente descripción detallada de varias realizaciones, que procede con referencia a las figuras adjuntas.
BREVE DESCRIPCIÓN DE LAS FIGURAS
Las FIG. 1A y 1B son gráficos lineales que muestran la unión de péptidos PAGE4 nativos y sus péptidos agonistas a moléculas HLA-A2. Los péptidos se analizaron para la unión a la línea celular T2 como se describe en el 25 Ejemplo 1. Para los resultados presentados en la FIG. 1A, los péptidos se usaron a concentraciones de 0 a 25 g/ml. Péptido P16 (○), P16-1 (●), P16-2 (▲), P84 (□) y P84-1 (■),control positivo (péptido MUC-1) (+) y control negativo (péptido de unión a HLA-A3) (X). Los... [Seguir leyendo]
Reivindicaciones:
1. Un polipéptido aislado que comprende como mucho diez aminoácidos consecutivos de la secuencia de aminoácidos expuesta como
MSARVRSRSRGRGDGX1X2APDVVAFVAPGESQQEEPPTDNQDIEPGQEREGTPPIEERKX3X4GDCQEMDX5EKTRSERGDGSDVKEX6X7PPNPKHX8KTKEAGDGQP (SEC ID Nº 1) 5
y comprendiendo el polipéptido uno de
(a) los aminoácidos 16 a 25 de la SEC ID Nº 1 donde el aminoácido 1 (X1) es una glutamina y el aminoácido 2 (X2) es una leucina;
(b) los aminoácidos 16 a 25 de la SEC ID Nº 1 donde el aminoácido 1 (X1) es una tirosina y el aminoácido 2 (X2) es una leucina; 10
(c) los aminoácidos 59 a 68 de la SEC ID Nº 1 donde el aminoácido 1 (X3) es una valina y el aminoácido 2 (X4) es una leucina;
(d) los aminoácidos 59 a 68 de la SEC ID Nº 1 donde el aminoácido 1 (X3) es una tirosina, el aminoácido 2 (X4) es una leucina, y el aminoácido 3 (X5) es una valina, o
(e) los aminoácidos 84 a 92 de la SEC ID Nº 1 donde el aminoácido 1 (X6) es una tirosina, el aminoácido 2 15 (X7) es una leucina y el aminoácido 9 (X8) es una valina.
2. Un polinucleótido aislado que comprende una secuencia de ácido nucleico que codifica el polipéptido de la reivindicación 1, unido preferiblemente de forma funcional a un promotor.
3. Un vector que comprende el polinucleótido de la reivindicación 2.
4. Un vector de acuerdo con la reivindicación 3, siendo el vector un vector plasmídico o un vector viral. 20
5. Un vector de acuerdo con la reivindicación 4, siendo el vector un vector plasmídico que se expresa en Salmonella o un vector plasmídico que se expresa en levaduras.
6. Un vector de acuerdo con la reivindicación 4, siendo el vector un vector viral.
7. Un vector de acuerdo con la reivindicación 6, siendo el vector viral un vector de retrovirus, orthopoxvirus, avipoxvirus, fowlpoxvirus, capripoxvirus, suipoxvirus, adenovirus, herpesvirus, alfavirus, baculovirus, virus Sindbis, 25 virus vaccinia o poliovirus.
8. Una composición que comprende un primer virus recombinante que tiene incorporado en un genoma viral o parte infectable del mismo un ácido nucleico que codifica el polipéptido aislado de la reivindicación 1 y un segundo virus recombinante que tiene incorporado en un genoma viral o parte infectable del mismo uno o más genes o secuencias de ADN que codifican una molécula co-estimuladora, siendo capaz la composición de co-infectar una 30 célula hospedadora provocando la co-expresión del polipéptido y los genes codificantes o las secuencias de ADN que codifican la molécula co-estimuladora.
9. Una composición de acuerdo con la reivindicación 8, en la que la molécula co-estimuladora uno o más de B7-1, B7-2, LFA o ICAM-1.
10. Una composición de acuerdo con la reivindicación 8 ó 9, en la que el segundo virus recombinante 35 comprende adicionalmente una o más secuencias de ADN exógenas que codifican una o más moléculas inmunoestimuladoras, en la que la molécula inmunoestimuladora se selecciona entre el grupo compuesto por IL-2, ICAM-1, LFA-3, CD72, GM-CSF, TNF-, IFN-, IL-12, e IL-6.
11. Una composición de acuerdo con la reivindicación 8, 9 ó 10, comprendiendo adicionalmente la composición una cantidad eficaz para la inmunomodulación de al menos uno de una molécula inmunoestimuladora exógena 40 seleccionada entre el grupo compuesto por IL-2, GM-CSF, TNF-, IL-12, e IL-6.
12. La composición de una cualquiera de las reivindicaciones 8 a 11, que comprende el primer y segundo virus en cantidades eficaces para mejorar una enfermedad en un mamífero, siendo la enfermedad un cáncer.
13. La composición de la reivindicación 12, en la que el cáncer es cáncer uterino, cervical, de próstata o testicular. 45
14. La composición de una cualquiera de las reivindicaciones 8 a 13, en la que el primer virus recombinante, el segundo virus recombinante, o el primer y segundo virus recombinantes se seleccionan entre el grupo compuesto por vectores de retrovirus, vectores de orthopoxvirus, vectores de avipoxvirus, vectores de fowlpoxvirus, vectores de capripoxvirus, vectores de suipoxvirus, vectores adenovirus, vectores de herpesvirus, vectores de alfavirus, vectores de baculovirus, vectores de virus Sindbis, vectores de virus vaccinia y vectores de poliovirus, preferiblemente virus 50 vaccinia o fowlpoxvirus.
15. Una célula hospedadora transformada con el vector de una cualquiera de las reivindicaciones 3 a 7.
16. Una célula hospedadora de acuerdo con la reivindicación 15, siendo la célula hospedadora una célula dendrítica o una célula tumoral.
17. Una composición farmacéutica que comprende la composición de una cualquiera de las reivindicaciones 8 a 14 y un vehículo farmacéuticamente aceptable.
18. Una composición farmacéutica que comprende una cantidad terapéuticamente eficaz de la célula hospedadora de la reivindicación 15 ó 16 en un vehículo farmacéuticamente aceptable.
19. Una composición farmacéutica que comprende una cantidad terapéuticamente eficaz del polipéptido de la 5 reivindicación 1 en un vehículo farmacéuticamente aceptable.
20. Una composición farmacéutica que comprende una cantidad terapéuticamente eficaz del polinucleótido de la reivindicación 2 en un vehículo farmacéuticamente aceptable.
21. El polipéptido de la reivindicación 1 para su uso en un método para provocar una respuesta inmune en un sujeto, que comprende administrar a un sujeto una cantidad terapéuticamente eficaz del polipéptido, preferiblemente 10 con un adyuvante, produciendo de este modo una respuesta inmune en el sujeto.
22. La composición de una cualquiera de las reivindicaciones 8 a 14 para su uso en un método para potenciar una respuesta inmune contra células que expresan PAGE4 en un mamífero, que comprende infectar las células in vitro con una cantidad terapéuticamente eficaz de la composición, para producir que las células infectadas expresen un polipéptido PAGE4 inmunogénico y administrar una cantidad de células infectadas a un mamífero afectado con 15 células que expresan la proteína PAGE4, potenciado de este modo la respuesta inmune.
23. La composición de la reivindicación 22, siendo la composición administrable con un adyuvante.
24. La composición de la reivindicación 22 ó 23, en la que las células son células dendríticas o células tumorales.
25. El polinucleótido de la reivindicación 2 para su uso en un método para provocar una respuesta inmune en 20 un sujeto, que comprende administrar a un sujeto una cantidad terapéuticamente eficaz del polinucleótido, produciendo de este modo una respuesta inmune en el sujeto.
26. El polinucleótido de la reivindicación 25, en el que la composición es administrable con un adyuvante.
27. El vector de una cualquiera de las reivindicaciones 3 a 7 para su uso en un método para tratar a un sujeto con cáncer, comprendiendo el método administrar al sujeto una cantidad terapéuticamente eficaz del vector, 25 tratando de este modo al sujeto.
28. El vector de la reivindicación 27, siendo el vector un vector viral recombinante.
29. El vector de la reivindicación 28, comprendiendo adicionalmente el vector viral recombinante un ácido nucleico que codifica una molécula co-estimuladora, preferiblemente siendo la molécula co-estimuladora B7-1, B7-2, B7-1 B7-2, LFA e ICAM-1. 30
30. El polipéptido, polinucleótido o vector de una cualquiera de las reivindicaciones 21 a 29, comprendiendo adicionalmente el método administrar al sujeto una cantidad terapéuticamente eficaz de IL-2, RANTES, GM-CSF, TNF-, IFN-, IL-15, IFN-, G-CSF, o una combinación de los mismos.
31. El polipéptido, polinucleótido o vector de una cualquiera de las reivindicaciones 21 a 29, comprendiendo adicionalmente el método administrar al sujeto un ácido nucleico que codifica uno o más de IL-2, RANTES, GM-CSF, 35 TNF-, IFN-, IFN-, IL-15, G-CSF, LFA-3, CD72, B7-1, B7-2, OX-40L, 41 BBL e ICAM-1.
32. El polipéptido, composición, polinucleótido o vector de una cualquiera de las reivindicaciones 21 a 31, comprendiendo la respuesta inmune una respuesta de células T.
33. El polipéptido, composición, polinucleótido o vector de la reivindicación 32, comprendiendo la respuesta inmune inducir células T citotóxicas que inducen la lisis de células que expresan la SEC ID Nº 1. 40
34. El polipéptido, composición, polinucleótido o vector de la reivindicación 33, teniendo el sujeto cáncer, siendo el cáncer más particularmente cáncer uterino, cervical, de próstata o testicular.
35. El polipéptido, composición, polinucleótido o vector de la reivindicación 34, disminuyendo la respuesta inmune el crecimiento del cáncer.
36. El polipéptido, composición, polinucleótido o vector de una cualquiera de las reivindicaciones 21 a 35, 45 comprendiendo adicionalmente el método administrar una cantidad terapéuticamente eficaz de un agente quimioterapéutico al sujeto.
37. El vector de la reivindicación 27, 28 ó 29, siendo el vector administrable como parte de una composición de una cualquiera de las reivindicaciones 8 a 14.
38. El polipéptido de la reivindicación 1 para su uso en un método para inhibir el crecimiento de una célula 50 cancerosa de próstata, comprendiendo el método,
(i) cultivar linfocitos T citotóxicos (CTL) o células precursoras CTL con el polipéptido y una célula presentadora de antígeno para producir CTL activados o CTL madurados a partir de los precursores CTL que reconocen las células cancerosas de próstata, y
(ii) poner en contacto la célula de cáncer de mama o de cáncer de próstata con los CTL activados o CTL madurados a partir de los precursores CTL,
inhibiendo de este modo el crecimiento de la célula cancerosa de próstata.
39. El polipéptido de la reivindicación 38, en el que la célula cancerosa está en un sujeto, y el método comprende administrar los linfocitos T citotóxicos al sujeto. 5
40. El polipéptido de la reivindicación 1 o el polinucleótido de la reivindicación 2, para su uso en un método para inhibir el crecimiento de una célula cancerosa reproductora en un sujeto, comprendiendo el método,
poner en contacto una célula dendrítica con el polipéptido, o expresar el polinucleótido en las células dendríticas, preparando de este modo una célula presentadora de antígeno específica, y
administrar la célula presentadora de antígeno al sujeto, induciendo de este modo una respuesta inmune e 10 inhibiendo el crecimiento de la célula cancerosa reproductora.
41. El polipéptido de la reivindicación 1 o el polinucleótido de la reivindicación 2, para su uso en un método para inhibir el crecimiento de una célula cancerosa reproductora en un sujeto, comprendiendo el método,
poner en contacto una célula dendrítica con el polipéptido, o expresar el polinucleótido en las células dendríticas, preparando de este modo una célula presentadora de antígeno específica, y 15
poner en contacto la célula presentadora de antígeno con una población de células T citotóxicas, produciendo de este modo células T citotóxicas activadas; y administrar las células T citotóxicas activadas al sujeto.
42. El polipéptido o polinucleótido de la reivindicación 41, siendo el cáncer reproductor un cáncer de próstata, de cuello del útero, testicular, o uterino.
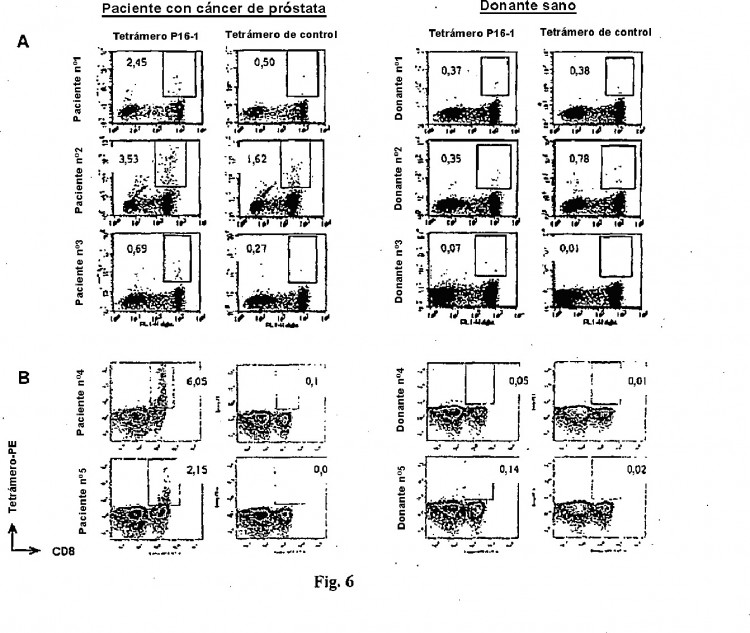
43. Un método para detectar células T que expresan CD8 que reconocen específicamente la SEC ID Nº 1 en 20 un sujeto, que comprende
poner en contacto células mononucleares de sangre periférica aisladas del sujeto con el reactivo que comprende el polipéptido de la reivindicación 1;
detectar la presencia del reactivo unido a las células mononucleares de sangre periférica, detectando de este modo las células T que expresan CD8 que se unen específicamente a la SEC ID Nº 1. 25
Patentes similares o relacionadas:
Nuevo péptido con cuatro epítopos CTL unidos, del 15 de Abril de 2020, de TAIHO PHARMACEUTICAL CO., LTD.: Un péptido que consiste en 4 epítopos unidos, en el que los 4 péptidos de epítopo se seleccionan del grupo que consiste en los péptidos de epítopo CTL: el péptido como […]
Receptores de células T anti-KRAS mutado, del 8 de Enero de 2020, de The United States Of America, As Represented By The Secretary, Department Of Health And Human Services (100.0%): Receptor de células T (TCR) aislado que tiene especificidad antigénica para un epítopo mutado presentado en el contexto de una molécula de HLA-A11, consistiendo […]
Vacuna peptídica que comprende péptido ras mutante y agente quimioterapéutico, del 18 de Junio de 2019, de TARGOVAX ASA: Al menos un péptido, adecuado para provocar una respuesta inmunitaria, en el que el o cada péptido corresponde a un fragmento de una proteína RAS de tipo silvestre pero tiene […]
Proteína Brachyury, vectores adenovirales que codifican proteína Brachyury y su uso, del 5 de Junio de 2019, de The U.S.A. as represented by the Secretary, Department of Health and Human Services: Una cantidad eficaz de un vector adenoviral que codifica (a) una proteína que comprende una secuencia de aminoácidos idéntica al menos en un 90 % a […]
Nuevo antígeno de cáncer EEF2, del 17 de Abril de 2019, de INTERNATIONAL INSTITUTE OF CANCER IMMUNOLOGY, INC.: Una composición farmacéutica para su uso en el tratamiento o prevención de cánceres en un sujeto positivo para HLA-A*2402, en donde dicha composición farmacéutica […]
Moléculas de fusión KIF5B-RET y usos de las mismas, del 14 de Marzo de 2019, de Foundation Medicine, Inc: Un agente anticáncer para su uso en un procedimiento de tratamiento a un sujeto que tiene un cáncer colorrectal con una fusión del miembro de la […]
Polipéptidos y polinucleótidos, y usos de los mismos como una diana farmacológica para producir fármacos y agentes biológicos, del 9 de Enero de 2019, de COMPUGEN LTD: Un anticuerpo monoclonal o policlonal o un fragmento de unión a antígeno del mismo que se une al ectodominio de C1ORF32 o porciones o variantes del mismo y bloquea la interacción […]
Una mezcla de péptidos, del 18 de Septiembre de 2018, de TARGOVAX ASA: Una mezcla de péptidos adecuada para desencadenar una respuesta inmunitaria que comprende un primer, segundo, tercer, cuarto, quinto, sexto, séptimo y octavo péptido, cada […]